血红蛋白和其他许多功能蛋白质一样,其分子结构可划分为一、二、三级或四级。如前所述,人血红蛋白是由4个亚单位组成的,每个亚单位含有一个亚铁血红素和一条多肽链。组成Hb的多肽链分为两大类:①α类链:ζ、α和θ链;②非α类链:ε、γ、β、δ链。α链由141个氨基酸组成,其N-末端为缬氨酸(Val),C-端为精氨酸(Arg)。ε、γ、β、δ链由146个氨基酸组成,除γ链N-末端氨基酸为甘氨酸(Gly)外,β、δ链的N-末端为Val,β、δ、γ链C-末端均为组氨酸(His)。
所谓Hb的一级结构(化学结构)是指氨基酸残基在珠蛋白肽链上的线性排列顺序,两个相邻氨基酸之间以肽键(—CONH—)相连。一级结构对Hb的立体结构起决定性作用,对于了解血红蛋白病的分子病理学是很重要的。珠蛋白肽链氨基酸顺序测定是Ingram(1958)指纹技术和通过Edman逐步降解技术测定各个酶解肽段的顺序而完成的。从氨基端排起,下图中已指出全链α和β链的一级结构,上一篇图表中有列出各功能珠蛋白链的氨基酸排列顺序。
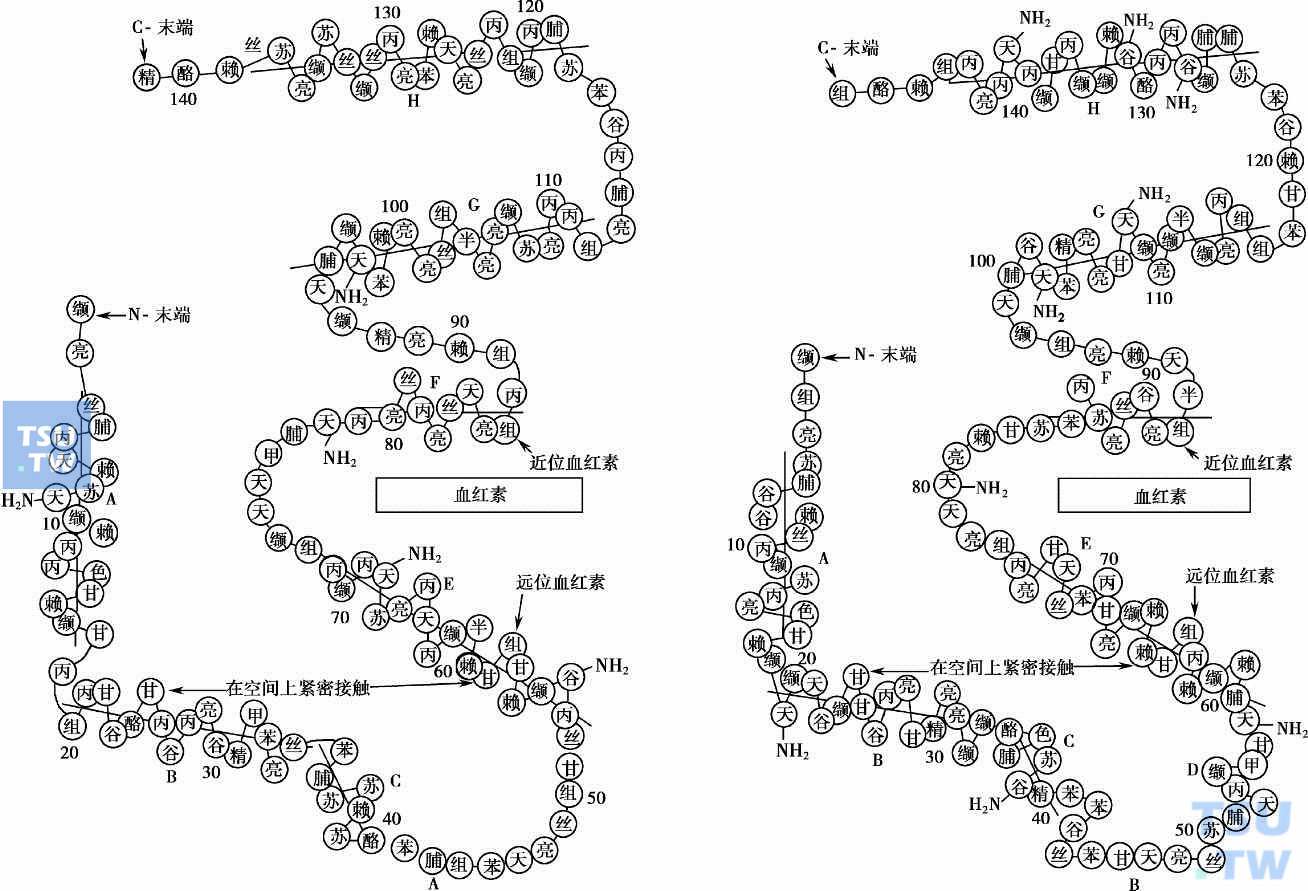
血红蛋白α链和β链 的一级结构和二级结构:A.α链;B.β链
血红蛋白的二级结构:指多肽链主链骨架中若干肽段在一个方向上按一定规律盘绕成α螺旋结构(称为二级结构)。α螺旋结构是链内肽链间氢键使肽链中有些段落以3. 6个氨基酸残基为一周,盘成一个右手螺旋。珠蛋白肽链的70%以上氨基酸处于螺旋形位置,组成7或8个节段,称为螺旋段(下图),每两个节段之间为少数处于非螺旋形结构的氨基酸。α链有7个螺旋段,分别用A,B,C,E,F,G,H来表示;β链有8个螺旋段,分别用A,B, C,D,E,F,G,H来表示。非螺旋段位于其间,分别用CD,EF等来表示。每个氨基酸残基的位置可以用从N端开始的序号表示,也可以用在区段的序号表示。比较已知20多个物种,(从鳗鱼到人)的血红蛋白的一级结构,发现有9个位置在所有或几乎所有已被研究的物种中含有相同的氨基酸。这些保守的位置对血红蛋白分子的功能至关重要,有一些直接参与血红素与氧的结合过程,而CH2位的酪氨酸残基的羟基与FG5位缬氨酸残基形成氢键加强了分子的稳定性。β6甘氨酸残基体积最小,使螺旋区B和螺旋区E得以充分靠近,另外C2脯氨酸的存在使螺旋区终结。
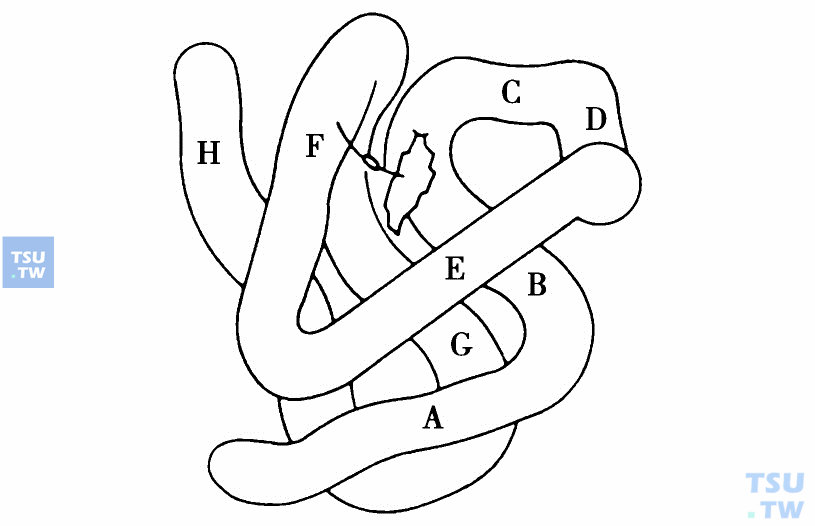
β-珠蛋白链的螺旋节段示意图
血红蛋白中的保守氨基酸残基
血红蛋白的三级结构:指在二级结构的基础上,珠蛋白肽链借助于次级键(主要是疏水键),又可按一定方式再盘曲折叠,使其本来较长的肽链,在空间上形成较紧密的球状三维构象(下图),其内部多为疏水性氨基酸,为血红素提供了必要的疏水环境,而外部多为极性氨基酸,是Hb分子高度可溶、具有稳定的立体结构。血红素位于E,F螺旋段和CD非螺旋段组成的疏水性“口袋”中(称为“血红素袋”),通过次级键固定在一定的位置上。分析可见,血红素与珠蛋白链相结合,主要有以下三种方式:①血红素中的Fe2+与F8组氨酸(近位组氨酸)咪唑基的N原子之间的配位键;②卟啉环上一个丙酸侧链与FG2组氨酸及H5谷氨酰胺形成氢链,另一个丙酸侧链与CD3精氨酸形成氢键;③珠蛋白与血红素之间还有很多非极性相互作用,“血红素袋”周围多为疏水性氨基酸,在使血红素-珠蛋白复合物稳定中,疏水基团起着重要作用。血红素中Fe2+与O2相连是在卟啉环平面的另一侧。具体说,在血红素的两侧各有一个组氨酸残基(F8和E7),其中F8的位置距血红素很近,称为近位组氨酸,E7组氨酸距血红素很远,称为远位组氨酸,与血红素没有直接联系,但起着“血红素袋”门户作用。
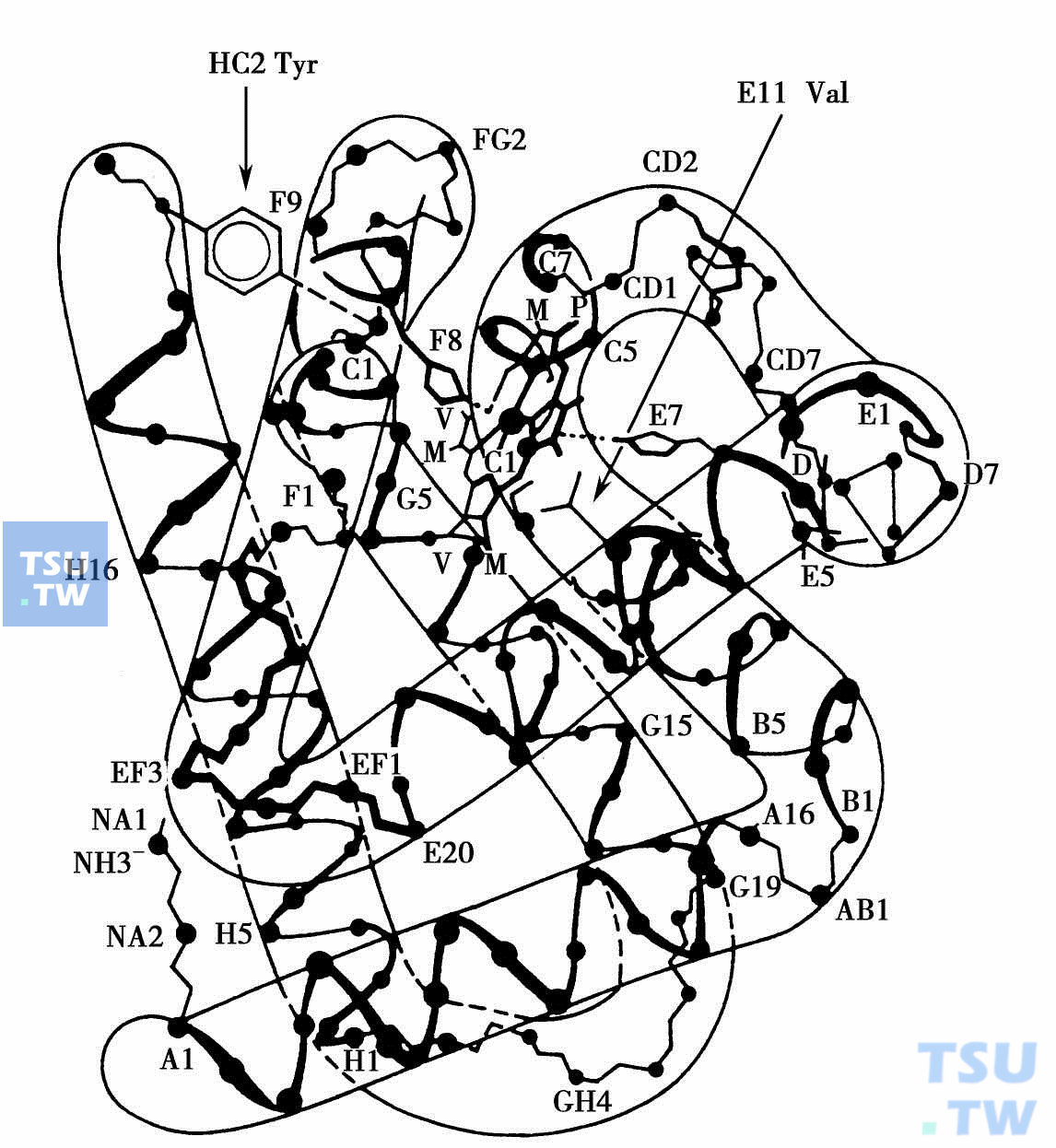
血红蛋白的三级结构
血红蛋白的四级结构:组成血红蛋白的四条肽链(亚基)在三级结构的基础上,借助亚基间的次级键,按一定空间关系相互组成一个完整的、呈椭圆形的四聚体——有功能的血红蛋白分子,其大小约为6. 4nm×5. 5nm×5. 0nm。Monod等人指出,每个血红蛋白分子以两种不同的物理形式存在,也就是采取两种不同的四级结构,一种是易和氧结合、高亲和力的R型(松弛态),另一种形式是易于放氧、低亲和力的T型(紧张态)。T型构象血红蛋白分子(脱氧Hb)中,其四条多肽链之间由8对盐键相连而成为受约束的强制状态,其中包括末端氨基和末端羧基之间、末端羧基和46位赖氨酸残基的侧链之间、141位精氨酸残基的侧链和94位天冬氨酸残基的侧链之间,以及146位组氨酸残基和94位天冬氨酸残基之间形成的盐键。当血红蛋白氧合后转为R型构象,上述盐键全部破坏,使肽链的羧基端完全自由。在血红蛋白分子之中,四个亚基对称排列形成α1β1 和α2β2两个重要接触面(下图)。这两种接触面的划分,主要是根据Hb分子氧合和脱氧是二者的移动情况,在氧合和脱氧过程中移动较小的(约1Å),称为α1β1接触面或α2β2接触面;在氧合和脱氧过程中移动较大(约7Å),则称为α1β2接触面或α2β1接触面。α1β1接触面相对较大较长(包括34个残基和110个原子),对Hb分子的稳定性很重要,α1β1接触面相对较小较短(包括19个残基和80个原子),在结合配体(O2)时发生T→R构象跃进中可产生7Å左右的滑动,因此α1β1接触面对Hb分子对氧的亲和力很重要。一切在接触面中突变都会减小血红素-血红素之间的相互作用,从而影响血红蛋白分子的氧亲和性,而α1β1接触面中的突变一般并不这样。
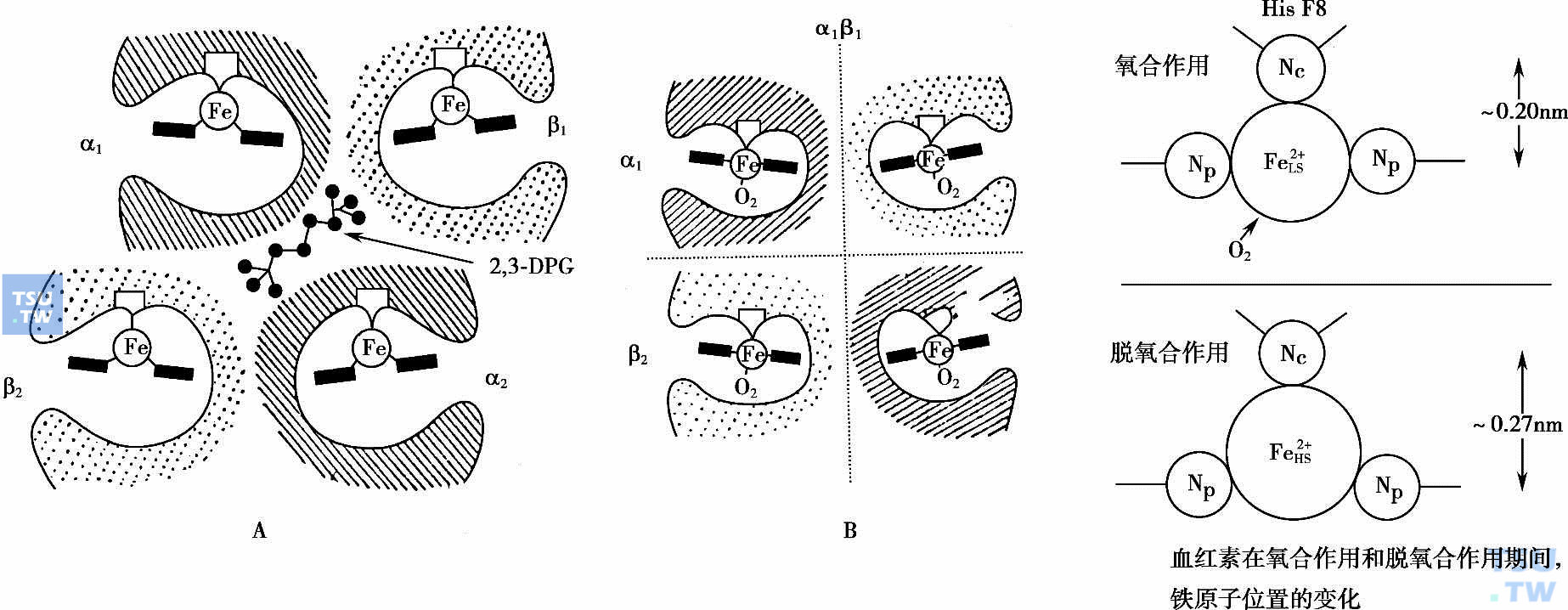
血红蛋白与氧结合前后的构象变化:A.脱氧血红蛋白(T-构象);B.氧合血红蛋白(IR-构象)
血红蛋白的X射线晶体衍射分析始于1936年,化学家佩鲁茨(Max Perutz)及其同事应用X线衍射技术,费时20余年,才确定了血红蛋白分子中数万个原子坐标,完成了脱氧和氧合血红蛋白的三维结构分析,终于从立体化学上揭开了分子呼吸(Hb分子摄氧和释氧)的奥秘,并建立了描述Hb变构效应的模型。后来,他们又从立体化学角度阐述氧亲和性改变的异常Hb病的发病机制。由于这项杰出工作,Perutz和研究肌红蛋白的Kendrew分享1962年诺贝尔化学奖。
