Perutz及其同事构建了血红蛋白分子的三维结构模型,使人们可以观察到氨基酸取代作用对分子功能的影响。Perutz的模式表明,通过范德华型非极性相互作用,无水的分子核心是稳定的。带极性侧链的氨基酸由内部完全地被赶出来,且仅发现于分子表面,与水相互作用,表现出该分子是可溶性的。共价结合血红素(heme)于P8的组氨酸,而且在血红素裂隙中与非极性氨基酸也形成约60个接触面,因而有助于四级结构的稳定。在该非极性环境中使血红素铁有可能与氧结合,而又无显著高铁血红蛋白(methemoglobin)形成。由此模型,也评估了每个Hb分子中四条肽链之间的接触;鉴定出两类接触:较大的称为α1β1接触,是由34个氨基酸中非极性相互作用形成;较小的称为α1β2接触,只涉及19个氨基酸。氧合作用时,αβ接触有显著的变化,约有0. 7nm(7Å)的移动或产生所谓血红素-血红素或亚单位间相互作用。
珠蛋白链的C-末端对氧结合也是重要的。当氧被加到分子上时,改变了铁旋转的状态,接着分子变化导致在F及H螺旋之间从其口袋第二位酪氨酸残基被逐出。Perutz讨论了与氧结合相关的这些及其他立体化学变化。
在此总的背景基础上,使人了解到在某一分子位置上的取代作用的影响,可以按功能对异常血红蛋白进行分类(下表)。
异常血红蛋白的功能分类
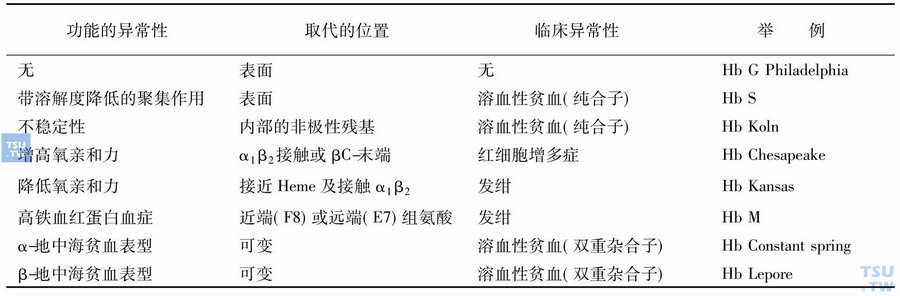
发生在分子表面的替代突变作用,一般来说是无害的,因它们不会影响到四级结构,血红素功能或亚单位之间的相互作用。实际上,多数功能正常的变异血红蛋白替代突变都是发生在分子表面,多数是由于替代突变改变了分子的净电荷而在人群筛选中经Hb电泳检测发现的。某些分子表面的替代突变作用导致多聚合化或聚集作用。某些突变作用似乎在分子表面创建了一个位点,它能和相邻分子上的代偿位置相互作用。这些分子相互间作用的实质尚不知晓,但有的学者提出过一些假想。聚集了的血红蛋白如HbS,趋向于细胞内结晶或多聚化,同时伴有细胞形状的变形,细胞的可变形性降低,溶血并损伤微血管循环。
有些血红蛋白变异物显示出结构的不稳定性,这些血红蛋白具有在细胞内沉淀、形成包涵体并引起细胞生存期缩短倾向。很多不稳定性血红蛋白是中性的(电荷未变化)氨基酸取代作用的结果,其影响内部非极性残基,这些取代中许多会影响接触血红素的残基接触。因而减低了血红素-珠蛋白结合,水可以接近血红素口袋,且血红素可能从分子中脱离。无血红素的正常珠蛋白及部分无血红素的血红蛋白(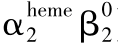 )自身是不稳定的。有些不稳定性血红蛋白,其整个分子的构象有明显的变化,特别是带有丢失的血红蛋白(如HbGun Hill),以及那些脯氨酸插进螺旋段的血红蛋白,使螺旋发生断裂和弯曲(如Hb Bibba,α136[H19]Leu→Pro)。由于分子空间大小会影响结构稳定性所依赖的范德华力,因此被取代氨基酸改变的空间大小具有广泛的作用。一个带电荷的氨基酸插进非极性核心,似乎对稳定性起着破坏作用,除非该电荷被分子内部形成的盐键稳定,如Hb Wien;或者电荷被容纳于分子表面,如Hb Sogn、Riverdale-Bronx、Shepherds Bush及Ann Arbor。
)自身是不稳定的。有些不稳定性血红蛋白,其整个分子的构象有明显的变化,特别是带有丢失的血红蛋白(如HbGun Hill),以及那些脯氨酸插进螺旋段的血红蛋白,使螺旋发生断裂和弯曲(如Hb Bibba,α136[H19]Leu→Pro)。由于分子空间大小会影响结构稳定性所依赖的范德华力,因此被取代氨基酸改变的空间大小具有广泛的作用。一个带电荷的氨基酸插进非极性核心,似乎对稳定性起着破坏作用,除非该电荷被分子内部形成的盐键稳定,如Hb Wien;或者电荷被容纳于分子表面,如Hb Sogn、Riverdale-Bronx、Shepherds Bush及Ann Arbor。
许多血红蛋白显示氧亲和力增高,它足以引发红细胞增多症(erythrocytosis)。产生这种异常性的大多数取代发生于α1β2接触点,在此它们损害了亚单位(血红素-血红素)相互间的作用,某些则靠近β链的C末端,在此它们干扰碱性波尔效应(alkaline Bohr effect)、2,3-二磷酸甘油酸的结合或盐桥的形成作用。这些作用能够在低氧亲和力(T)状态下稳定血红蛋白。
已叙述过氧亲和力降低的变异物,其中有一些具不稳定性。例如Hb Kansas,其严重性足以使其发生发绀。许多其他的变异物,仅是在实验室中检测出异常性。在Hb Kansas中(β102[G4]Asn→Thr)替代突变作用发生于一能形成α1β2接触部分并能接触到血红素基的残基上。该β102Asn残基在正常时与α94 Asp于血红蛋白氧合时形成氢键,该键能够稳定高亲和力(R)型血红蛋白。其他带有相同位置的取代的血红蛋白,如Hb Beth Israel(β102 [G4]Asn→Ser),也具有Hb Kansas的许多特征。
由酪氨酸去取代近处(F8:α87,β92)或远处(E:α58,β63)的组氨酸残基,引起了高铁血红蛋白的形成。这些取代能在血红素铁与酪氨酸的酚基氧之间形成一离子键,从而使铁固定于无功能的高铁状态。HbM Milwaukee(β67[E11]Val→Glu),因其谷氨酸残基中有羧基,能形成类似的离子键,但该血红素基不能结合氧,患者出现高铁血红蛋白血症及发绀。
有些不稳定性血红蛋白也有形成高铁血红蛋白的倾向,但是尚缺乏临床、电泳及其他HbM的分光光谱特性,这些Hb包括St. Louis,Freiburg及 I-Toulouse。
有几种不同的机制限制了异常结构珠蛋白链的合成,从而产生了地中海贫血表型。杂交珠蛋白链的合成,约是正常β-及δ-链(如Hb-Lepore)或β-及γ-链之间的中间物(如Hb Kenya)。经链终末端突变所产生的mRNA比正常mRNA缺少稳定性,加之打破了α-及-β间珠蛋白合成平衡,因此有些含延长的α-链的血红蛋白(Hb constant spring,Hb Icaria,Hb Seal Rock及Hb Koya Dora)具α-地中海贫血表型特性。突变作用激活了隐形的剪切位点,经与正常剪切点的竞争,限制了正常mRNA的合成。此突变作用解释了β-地中海贫血表型并发HbE及Hb Knossos。最后,地中海贫血表型可能是由珠蛋白链变异物的不稳定性引起,例如Hb Indianapolis的β-链、Hb Quong Sze、Hb Suan-Dok及Hb Petah Tikva的α-链。
