造血干细胞移植,特别是自体造血干细胞移植(ASCT)在淋巴瘤的治疗中已较为成熟。虽然目前的常规化放疗可以使相当部分的淋巴瘤获得治愈,但是原发耐药和复发患者的预后依然很不理想,对于这些患者,高剂量治疗(HCT)联合造血干细胞移植是重要的选择之一。1978年Appelbaum等最先报道应用高剂量化疗联合自体骨髓移植治疗复发NHL,可以使患者获得较常规化疗更长的DFS。此后的随机临床研究证实,ASCT治疗敏感复发的NHL,与常规化疗相比,无论在OS和DFS上均有提高。由此ASCT在恶性淋巴瘤患者中的应用得到了广泛的接受,并开展了大量的临床研究,使得ASCT的适应证更加明确,安全性和疗效不断提高。
ASCT治疗滤泡淋巴瘤
ASCT在FL中的治疗作用仍不明确。目前没有证据表明化疗可以治愈此类肿瘤,同样也没有证据显示ASCT可以治愈FL。大部分研究的生存曲线未能出现平台期,提示患者仍不能被治愈。对于有选择的患者,可以进行异基因造血干细胞移植,有研究显示异基因造血干细胞移植可以治愈部分FL,尽管非清髓性或清髓性异基因移植的治疗相关死亡率很高,分别为10%~25%和40%。
对于利妥昔单抗耐药的患者,如果解救治疗后肿瘤缓解,ASCT可作为选择之一。一项研究采用含全身照射的预处理方案治疗二次以上复发的患者,结果48%的患者在随访12年后,仍处于持续缓解状态。
Coiffier等分析了GELF- 86和GELF- 94两个回顾性临床研究,其目的是评价利妥昔单抗、ASCT以及利妥昔单抗联合ASCT治疗首次复发的滤泡淋巴瘤的疗效。研究共分析了254例接受CHVP(环磷酰胺,多柔比星,替尼泊苷,泼尼松)序贯干扰素治疗后复发或病情进展的患者。其中98例接受了ASCT治疗,包括33例应用了含有利妥昔单抗的解救方案;69例仅应用利妥昔单药或与化疗联合,未接受ASCT。两项研究的中位随访时间分别为12. 75年和7. 6年。结果显示,ASCT治疗可以提高复发患者的EFS和OS,但利妥昔单抗治疗在EFS和OS上的获益优于ASCT。当采用利妥昔单抗联合ASCT治疗时,患者的5年复发后生存率可达90%。
自体造血干细胞移植治疗侵袭性NHL
ASCT治疗敏感复发的侵袭性NHL
1995 年Philip等报告了前瞻性大样本随机对照的Parma研究结果。研究比较了常规化疗与ASCT对敏感复发的侵袭性NHL的疗效。109例2周期DHAP(顺铂、高剂量阿糖胞苷和泼尼松)化疗后达到或接近CR的患者被随机分组,一组接受ASCT,另一组继续4周期DHAP方案化疗。结果ASCT和常规化疗组8年DFS率分别为36%和11%(P<0. 002),OS率分别为47%和27%(P = 0. 042)。因Parma的研究结果,ASCT被认可为年龄小于60岁敏感复发的侵袭性NHL患者的标准治疗。
ASCT一线治疗高危侵袭性NHL
几项随机临床研究,探讨了ASCT在高危侵袭型NHL中的意义,但各研究中患者的入组条件、移植前诱导化疗方案、试验分组设计各不相同,研究结论并不一致,因此ASCT作为一线治疗的价值尚存争议。下表列举了几项HDT/ASCT一线治疗伴有不良预后因素的侵袭性NHL的随机对照临床研究的结果。
HDT/ASCT一线治疗伴有不良预后因素的侵袭性NHL随机对照研究结果
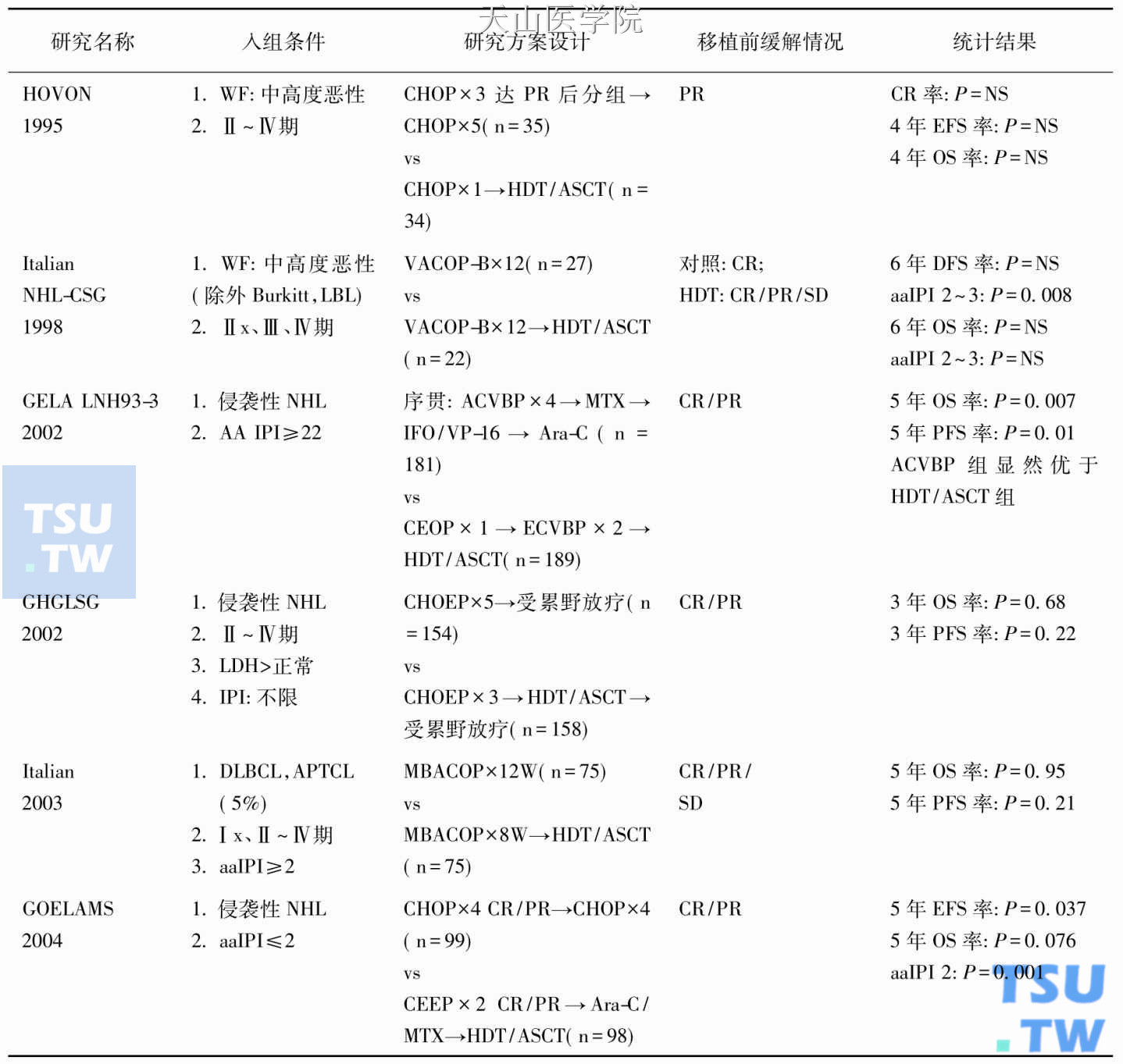
WF:工作分类;aaIPI:年龄调整的IPI预后指数;LBL:淋巴母细胞淋巴瘤
2003年Strehl等发表了一项高危患者一线应用ASCT的Meta分析研究结果。该研究收集了1995~2003年发表的11项前瞻性随机对照研究的结果,共纳入2228例患者。但研究的结论是因各试验设计的差别显著,不具有可比性,很难进行有效的比较。各项研究在设计上的主要区别包括:①化疗方案各不相同;②ASCT治疗前的化疗周期数不同;③ASCT治疗前患者的缓解状态不同;④入组患者的病理类型组成不同。
2004年发表了一项Ⅲ期临床研究的结果,为了避免可能的影响因素对结果的干扰,对入组条件包括病理类型、诱导化疗的敏感性及IPI评分等作了明确的限定。共随机入组了197例患者,结果5年EFS率在ASCT和常规治疗组分别为55%和37%(P =0. 037),但OS率没有显著性差异,分别为71%和56%(P= 0. 076)。然而在IPI = 2的患者中,5年的OS在ASCT组显著高于常规化疗组,分别为74%和44%(P=0. 001)。
多项临床研究探讨了ASCT前最佳的诱导化疗方案及治疗周期数的问题。移植前的诱导化疗设计主要包括三种类型:①标准方案和治疗周期数的诱导化疗;②标准方案但治疗周期数减少的诱导化疗;③剂量强度增加,治疗周期数进一步减少的诱导化疗。多数研究认为ASCT前应有足够的标准化疗周期,无论是减少标准化疗周期数还是在强化基础上减少化疗周期数的诱导方案,疗效均不理想。
高度侵袭性NHL包括淋巴母细胞型淋巴瘤、Burkitt淋巴瘤和Burkitt样淋巴瘤。因高度侵袭型NHL多有骨髓受侵且发病率低,ASCT治疗的临床研究比较少,且样本量小,治疗结论不明确。目前唯一一项随机对照研究是ASCT作为一线巩固治疗LBL。化疗敏感的65例成人LBL随机分组,接受诱导化疗后ASCT巩固治疗或2年的维持和强化治疗。中位随访37个月时,3年EFS率和OS率在ASCT组分别为55%和56%,维持治疗组分别为24%和45%,ASCT较常规治疗可以减少45%的复发危险性(P=0. 065)。
Smeland等报道了49例15~70岁成人Burkitt/ Burkitt样NHL采用不同治疗方案的随访结果。研究对比了MmCHOP(MTX静脉+鞘注给药+CHOP)、MmCHOP联合ASCT和BFM治疗Burkitt淋巴瘤方案的治疗结果。其中MmCHOP(n= 13)、MmCHOP+ HDT(n=17)和BFM(n = 19)三组的5年PFS率分别为30. 8%、70. 6%和73. 7%。作者认为,MmCHOP +ASCT和BFM方案较常规CHOP方案的疗效更优。
异基因造血干细胞移植
异基因造血干细胞移植(Allo- SCT)较ASCT的优势有两点:一是避免了回输的造血干细胞被肿瘤细胞污染;二是移植物抗肿瘤(GvHT)作用可以清除宿主体内残存的肿瘤细胞。Allo- SCT在淋巴瘤中的应用远不及ASCT广泛,因为早期报道未显示其在生存上的优势。虽然Allo- SCT的复发率低于ASCT,但有高达30%的移植相关死亡率。
20世纪50年代后开始出现低剂量强度的非清髓性Allo- SCT,这使得居高不下的Allo- SCT相关死亡率有所下降,并使得Allo- SCT在淋巴瘤治疗中的应用逐渐增多。
目前认为Allo- SCT低复发率的原因主要与GvHT作用相关。GvHT在增殖较慢的淋巴瘤,如慢性淋巴细胞白血病、惰性淋巴瘤和某些T细胞淋巴瘤的作用较为明显,这可能与异体的T淋巴细胞更能有效攻击增殖较慢的肿瘤细胞有关。但对侵袭性淋巴瘤的作用不如前者,需要在充分降低肿瘤负荷的情况下才可能获得较好的疗效。虽然降低剂量强度的预处理方案多可以降低移植相关死亡率,但是对于侵袭性淋巴瘤及多程治疗后的患者,死亡率依然很高。现有的临床研究尚不足以证实Allo- SCT在淋巴瘤治疗中的作用,其治疗作用还需大样本前瞻性临床的研究证实。
ASCT治疗NHL的新进展
自体造血干细胞净化
目前认为ASCT后复发的主要原因之一是采集的造血干细胞中存在肿瘤细胞污染。为了减少回输干细胞中肿瘤细胞的污染,可以采用体外和体内净化方法。
体外净化是对采集的造血干细胞进行净化,方式包括使用化疗药物或单克隆抗体联合补体在体外杀伤移植物中的肿瘤细胞,或通过CD34抗体对移植物进行阳性筛选纯化,或应用抗肿瘤细胞单抗筛选排除肿瘤细胞。体外净化可以使采集的造血干细胞中肿瘤细胞减少2~3个对数级。体外净化对于患者预后的影响尚存争议。到目前为止,尚无完整的直接比较体外净化ASCT和非净化ASCT疗效差异的前瞻性随机对照研究。
由于体外净化的方法烦琐昂贵,对采集的干细胞有损耗,并且不能保证完全清除采集物中的肿瘤细胞,人们开始探索体内净化的方法。利妥昔单抗的出现使体内净化成为可能。已证实利妥西单抗对自体造血干细胞的动员、采集和移植后造血功能的重建无任何不良影响。
含放射性同位素标记的单抗作为预处理方案
放射性同位素标记的抗CD20单克隆抗体90Y-ibritumomab和131I- tositumomab可以单药或与化疗药物联合的方式组成新的预处理方案。有研究显示,含有放射免疫药物的预处理方案较传统的含全身照射或单纯化疗的预处理方案更加安全,对于多次复发耐药患者的疗效可能优于传统的预处理方案。
(石远凯 孙燕 秦燕)
