20世纪60年代前列腺素的分离提纯和对APUD系统的深入了解、80年代心血管内分泌功能的发现和近年对细胞因子功能的深入认识,使人们清楚地看到,在经典的内分泌系统外还存在着一个广阔的领域——弥散性激素分泌系统和器官激素分泌系统,这些系统所分泌的肽类、胺类物质,通过旁分泌、自分泌甚至内分泌方式,维持机体内环境稳定,给内分泌腺某些激素的作用提供了精细调节的网络系统。有的在发挥自身作用时则需要特定的内分泌激素作为介导,有的则与内分泌激素一道发挥“双效应”;反之,如果它们失调同样也导致功能障碍和疾病。
(本图片来自网络)
【肺脏激素调节系统】肺脏是唯一汇合体循环和肺循环的器官,肺脏毛细血管表面积达70m2,是体表面积的40多倍,占人体毛细血管床的60%以上,它不仅是呼吸的重要器官,而且还含有许多激素分泌功能细胞,其分泌的激素调节着机体的代谢与内分泌功能。
肺脏分泌旁分泌激素/细胞因子/免疫因子
Ⅱ型肺泡上皮细胞
又称肺泡立方上皮细胞、大肺泡细胞、角细胞及壁龛细胞等。Ⅱ型肺泡上皮细胞位于肺泡壁上,为立方形,占肺实质细胞的15%~16%,覆盖肺泡表面积的10%。此类细胞含有较多的细胞器如高尔基复合体、粗面内质网,核糖体、多囊泡体及线粒体,细胞有嗜银板层体,主要分泌并合成肺泡表面活性物质。
肺血管内皮细胞
肺血管内皮细胞(endothelium cell,EC)覆盖血管腔表面,并与血液成分直接接触,且有独特的结构-细胞膜返折而形成大小不等的小囊泡(caveolar),其开口处由一极薄的隔膜(diaphragm)遮盖,使其形成血细胞不能进入而血液循环物质可透过的微循环“室”,EC的腔壁表面存在各种酶及受体,能迅速进行生物化学反应,释放或代谢灭活各种生物活性物质。加上EC表面的指状突起(figer-like projection),使EC接触表面明显增加,有助于加速代谢。EC分泌前列腺素I(PGI)、内皮舒张因子(endothelial relaxing factor)、内皮收缩因子(endothelial constricting factor)、血管紧张素-2(angiotensin-2,AT-2),维持血管的渗透性和舒缩功能,并能清除组胺、5-羟色胺、二磷酸腺苷等物质。
肥大细胞
肥大细胞(mast cell)位于肺小血管周围、肺泡间质和支气管壁,细胞中充满嗜碱颗粒,当受到刺激脱颗粒时释放出组胺及其他生物活性物质,如某些肽类酶、肝素等,引起支气管哮喘。
神经分泌细胞
神经分泌细胞(Kulchitsky cell)起源于胚胎神经嵴,属于APUD细胞的一种,其主要作用是合成和分泌生物胺和多肽类激素。
肺泡巨噬细胞
肺泡巨噬细胞(alveolar phagocyte)含有丰富的蛋白水解酶,肺泡巨噬细胞能产生多种细胞因子,它们在肺防御、肺组织重建和纤维化过程中起着重要作用。内毒素(endotoxin)是体外促肺泡巨噬细胞产生细胞因子的主要刺激物,使其产生大量的IL-6和TNF及少量IL-1β,防止日常吸入的微粒引发肺炎。轻度或中度入侵,可能不致引起炎症反应。肺巨噬细胞还能产生IL-8、TGF-β、PDGF样肽、TGF-α、IGF-1和IFN-γ。巨噬细胞产生的细胞因子中,IL-1β和TNF对IL-8的生成有诱导作用,提示IL-8产生是通过自分泌和旁分泌方式调节的。肺泡巨噬细胞分泌的IL-8使中性粒细胞汇集入肺,PDGF样肽、TGF-α、IGF-1、TGF-β、 IFN-γ、IL-1和TNF相互作用,对细胞和纤维化反应也有调节作用。
表面活性物质防止肺萎陷和肺水肿
肺表面活性物质及其生理作用
肺表面活性物质(pulmonary surfactant,PS)在肺泡Ⅱ型上皮细胞板层体内合成,与载体蛋白结合成脂蛋白后,分泌到肺泡腔内形成薄层,构成气液界面,其主要功能是:①降低气液面的表面张力,防止肺泡萎陷;②保持适当的肺顺应性,减少呼吸功;③防止肺微血管内成分渗入肺泡,防止肺水肿;④增强肺防御能力。包裹细菌或微粒,促进肺泡巨噬细胞的吞噬消化功能;保护巨噬细胞及肺未分化细胞;肺表面活性物质含有IgG、IgA、转铁蛋白、补体成分等;在免疫反应抑制巨噬细胞氧化应激,防止大量氧自由基的产生。
肺泡表面活性物为磷脂蛋白复合物,磷脂约占总重量的90%。磷脂中含非饱和和(或)饱和脂肪酸。磷脂酸与胆碱结合成磷脂酸胆碱(卵磷脂);它的两个分子的脂肪酸为棕榈酸二棕榈酰卵磷脂(DPPC)是PS的主要成分,约占总磷脂的54%~81%,其中双饱和DPPC降低表面张力作用很强,也是细胞膜的主要成分,不溶于水,但以微泡(micelle)形式分散存在,并呈双饱和卵磷脂,具有降低表面张力的物理特性。但单独DPPC并不能在肺泡表面降低表面张力的表层,只有DPPC以磷脂-蛋白复合物形式存在,并有其他成分参加时,才能发挥降低表面张力作用。不饱和卵磷脂在PS中的作用目前尚不清楚。
肺表面活性物质与肺脏疾病
Ⅱ型细胞分化延迟或合成不足可导致肺表面活性物质缺乏,产生肺部透明膜病变,导致婴幼儿、新生儿呼吸窘迫综合征;其特征是肺不张和肺水肿。临床表现为进行性呼吸困难、青紫及呼吸衰竭。氧中毒、缺氧、吸入有害气体、呼吸道烧伤、休克、感染、成人呼吸窘迫综合征、糖尿病血管病变、血黏度增高、肺栓塞和肺组织缺血均可减少表面活性物质的合成和分泌,进而导致肺不张和免疫功能下降。
血管活性物质调节肺功能
肾素-血管紧张素-醛固酮系统
肾素-血管紧张素-醛固酮(RAA)系统不仅存在血液循环中,肺脏也是RAA合成与代谢的主要器官,肺血管内皮细胞含有丰富的血管紧张素转换酶(angiotensin converting enzyme,ACE),是循环血中AT-1转变为AT-2的主要场所,AT-2在ACE的作用下代谢为无活性的血管紧张素-3(AT-3),进一步代谢为无活性肽,AT-2刺激醛固酮的合成分泌,影响水盐代谢。急性缺氧时,ACE活性下降。由于ACE是一种激肽酶(kininase),激活舒张血管的缓激肽酶,因此ACE活性下降可减弱缺氧的加压反应。一些影响肺部通气功能障碍的疾病(如阻塞性肺气肿、肺结节病)ACE活性升高,当治疗好转时下降,因此ACE的活性可作为疾病进展或追踪疗效的有用指标。
激活肺循环和肺实质局部RAA,能通过增加血管渗透性、血管紧张度和成纤维细胞活性等多种机制造成肺损伤,运用ACE抑制剂(ACEI)和AT-2受体拮抗剂(ARB)可使实验性肺损伤减轻,提示RAA系统激活在其发病过程中的作用及此类药物在弥漫性肺部疾病中的治疗意义。
前列腺素系统
主要在组织器官局部起调节作用。天然前列腺素(prostaglandin,PG)有20多种,按5碳环结构分为A、B、C、D、E、F等9类(下表)。
肺内主要的前列腺素及其作用
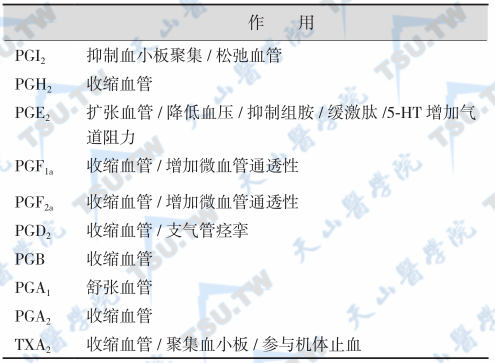
IgE介导的Ⅰ型变态反应使肺泡缺氧,各种因素引起的肺栓塞均可激活细胞膜磷脂酶A2(phospholipase A2),使细胞膜磷脂裂解,形成PG的前体花生四烯酸(arachidonic acid,AA)。AA在环氧酶作用下形成极不稳定的中间产物——内过氧化物(PGG和PGH),继而转化为各种前列腺素。除PGI 和PGA外,其他PG在肺脏被15-羟-PG脱氢酶灭活。
PG主要作用是:①调节肺血容量:低氧性肺动脉高压时有PGF2a样物质的释放,静注PGI,或雾化吸入均可使肺血管阻力降低。采用血栓素合酶抑制剂与硝苯地平(心痛定)联合治疗,可使肺和肺血管阻力明显下降。应用PGI可预防或治疗内毒素所致的肺损伤。②血栓素A2(thromboxane A2,TXA2)是引起支气管哮喘的重要介质之一,组胺和白三烯引起TXA2释放,加重支气管哮喘。哮喘发作时,PGF2a的释放增加,哮喘患者雾化吸入PGF2a时支气管收缩反应的敏感性比正常人高8000倍,提示支气管哮喘对PG有特异性反应。β受体兴奋剂可阻止白三烯和组胺引起的TXA2释放而起治疗作用,吸入PGI能防止运动和其他刺激诱发的哮喘发作,用PG辅以β受体兴奋剂喷雾可治疗支气管哮喘。③改善心、脑、肾动脉硬化,糖尿病的神经血管等病变。因它能使小血管平滑肌扩张,可改善因动脉硬化引起的心脑供血不足,增加微循环的灌注。
内皮素-一氧化氮系统
在肺部,一氧化氮合酶(nitric-oxide synthase,NOS)不仅存在于血管内皮细胞,亦广泛存在于支气管树的自主神经纤维,其中与气道平滑肌舒张有关的非胆碱能、非肾上腺能神经末梢释放的主要递质是一氧化氮(nitric oxide,NO)。
一、NO
是内皮细胞源性舒张因子(endothelium derived relaxing factor,EDRF)的重要成分,它是由L-精氨酸在NOS作用下生成的。生理情况下,当血管内皮细胞受到剪切力等作用时,可持续产生少量NO,在维持血管基础张力,抑制血小板聚集,抑制组织增殖,神经传递及免疫学方面有重要作用。NO既有血管内皮舒张作用,又有氧自由基性质。在慢性缺氧时大量产生的NO与氧自由基反应生成大量含氮氧自由基,这不仅减弱了NO的血管舒张作用,并与缺氧引起的血管内皮收缩因子协同作用,导致肺血管收缩及平滑肌增生。肺内产生的NO参与通气/血流比值的调节。NO通道支配肺动脉神经末梢释放兴奋性神经递质,肺动脉内存在着NO的基础释放,可能是维持肺循环低张、低压状态的一个重要因素。
二、内皮素(endothelin,ET)
主要是以ET-1和巨-ET两种形式存在,还有少量的ET-3。ET通过肺血管内皮细胞的ET-B受体促进EDRF和PGI2的释放,引起肺血管的舒张。气管上皮含有巨-ET转换酶(ECE),可促使巨-ET转变为ET-1。体内ET约有30%是由肺清除的,有一种中性内肽酶,可水解ET分子的两个肽键,使其失活。同时,肺组织中分布有密集的ET受体。因此,肺不仅是ET合成、分泌代谢的主要场所,还是ET的靶器官。气管、支气管有较多对ET-1具有高度亲和力的特异性结合位点。ET是较强的气管平滑肌收缩剂,致支气管痉挛作用比白三烯D4强4倍。呼吸道给药或静脉给药,ET均可致气管、支气管和细支气管持续性强烈收缩。ET-1的收缩效应强度最高,诱发支气管收缩反应起效缓慢,持续时间长。ET的收缩作用通过ETA受体起作用,特异性ETA受体拮抗剂BQ123可抑制ET-1收缩气管的作用。ET-1能刺激培养的动物气管上皮细胞和肺泡巨噬细胞合成花生四烯酸及其代谢产物,如PGE2、PGF2、PGD2。这些代谢产物有使气管收缩作用,ET还能刺激血小板活化因子(PAF)、白三烯、组胺及氧自由基的生成和释放,参与支气管收缩,血小板活化因子受体拮抗剂,白三烯D4受体阻滞剂、吲哚美辛、TXA2受体阻滞剂等对ET的收缩支气管作用有不同程度的抑制效应,但不被肾上腺素、异丙肾上腺素和阿托品阻滞,也不受地塞米松的影响。一般认为,ET致气管平滑肌收缩的机制,也是由于通过激活L型Ca2+通道使细胞外液Ca2+内流以及ET与受体结合后产生磷酸肌酸而使细胞储存Ca2+释放的结果。此外,ET还诱导支气管黏膜下腺体分泌,增加血管通透性,导致黏膜水肿。
其他血管活性物质
肺脏分泌的血管活性物质还有组胺、心钠素、白三烯、肿瘤坏死因子等。
一、组胺
组胺的主要作用是引起支气管平滑肌收缩,使血管通透性增加,黏膜水肿、黏液分泌增加、肺血管收缩及肺内血小板聚集,引起其他血管活性物质如PG、血小板激活因子(PAF)及白三烯释放。体内组胺有两种受体即H1和H2,H1受体与血管通透性和肺血管平滑肌及气道平滑肌收缩有关,H1受体效应可被组胺H1受体拮抗剂苯海拉明、氯苯那敏(扑尔敏)等阻断。H2受体效应与胃酸分泌和子宫松弛有关,不被H1受体拮抗剂所阻断。
二、心钠素(ANP)
除心脏外,肺也是分泌ANP的重要器官之一。肺脏ANP作用:①利钠利尿作用,肺分泌的ANP和心房分泌的ANP一样促使机体利尿和排钠。②扩张肺动脉和支气管,并能拮抗组胺或去甲肾上腺素引起的肺动脉和支气管痉挛。③静脉注射ANP可使肺表面活性物质含量增加。
呼吸窘迫综合征(respiratory distress syndrome)患儿血中ANP含量明显升高;机械通气患者由于肺受牵张,ANP含量明显升高;呼吸衰竭时ANP含量上升,其浓度与右心房压及肺动脉楔压呈正相关。慢性肺心病患者血中ANP升高,急性发作期上升更明显。先天性支气管肺发育不良患者血中ANP高于正常人10倍以上,说明ANP升高可以降低肺血容量和肺动脉高压。胸腔积液时胸水中ANP含量升高,其机制可能是从肺小静脉和毛细血管渗入胸腔积液中或者是直接分泌于积液中。实验性肺水肿ANP含量上升,但预先注射ANP可以防止或减轻肺水肿的产生,同时可见肺表面活性物质含量上升。临床上尝试用ANP注射治疗肺动脉高压,但作用维持时间短暂。
三、白三烯
白三烯与PG均系细胞膜磷脂,在磷脂酶A2催化下,由花生四烯酸裂解而来,是AA经脂氧化酶途径生成的产物。白三烯的主要生物作用是引起气道黏膜肿胀,腺体分泌增加,炎症加重,引起平滑肌收缩。
四、肿瘤坏死因子
能使肺血管通透性增高,并促使中性粒细胞在肺中聚集。体外试验注射肿瘤坏死因子(TNF)能使肉瘤组织产生出血坏死,在肿瘤免疫和抗感染中有重要作用。
