红斑狼疮是一种常见于15~40岁女性、临床上有多种表现、可累及全身任何脏器的自身免疫性疾病。红斑狼疮是一个病谱性疾病,病谱的一端为盘状红斑狼疮(discoid lupus erythematosus,DLE),病变主要限于皮肤,另一端为有内脏多系统累及并常有皮肤损害的系统性红斑狼疮(systemic lupus erythematosus,SLE)。中间有很多亚型,如播散性盘状红斑狼疮、深在性红斑狼疮、亚急性皮肤型红斑狼疮和抗核抗体阴性的系统性红斑狼疮等。
JN.Gilliam最早将LE的皮肤表现分为LE特异性皮损和非LE特异性皮损(下表)。皮肤红斑狼疮常与LE特异性皮损同义,包括了三类主要的LE特异性皮肤表现:急性皮肤红斑狼疮(acute cutaneous lupus erythematosus,ACLE)、亚急性皮肤红斑狼疮(subacute cuataneous lupus erythematosus,SCLE)和慢性皮肤红斑狼疮(chronic cuataneous lupus erythematosus,CCLE)。
LE相关皮损的Gilliam分类


目前,许多人认为DLE与SLE是红斑狼疮的两个异型,因为两个病有许多相同的临床表现,只是DLE的系统性损害发生率较低。下表为一组DLE与SLE临床资料的比较。15%的SLE病人可有临床和组织学上典型的盘状红斑,大多数先有DLE的SLE患者病程较良性,某些SLE患者在病情缓解时可出现典型的DLE皮损,DLE病人也偶可转变为SLE,其转变率是很低的,文献报道从1.3%~5%,发生的时间可从2年到29年不等。南京医科大学皮肤科的临床资料为2%~10%。一般认为有血液学和(或)血清学异常的DLE病人(约占DLE病人的55%)转变为SLE的危险为6.5%,有作者认为播散性DLE的病人转变为SLE的危险性更高,可达22%,而局限性DLE的病人(皮损只出现在头、颈部)只有1.2%。
DLE与SLE临床资料比较
DLE病人转变为SLE的危险因素包括:散在的非瘢痕性秃发;播散性淋巴结病;甲周毛细血管扩张;雷诺现象;SCLE/ACLE皮损;LE非特异性皮损如血管炎;不明原因的贫血;明显白细胞减少;梅毒血清学试验假阳性;持续高滴度ANA;抗单链DNA抗体;高丙球蛋白血症;血沉增快(>50mm/h);非皮损、非曝光部位狼疮带试验阳性;可溶性IL-2受体水平升高。
大致有1/4的SLE病人在病程中出现DLE皮损,这些病人的SLE病情往往不太严重。各型LE特异性皮损并发或进展出现系统性损害的相关危险性见下图。
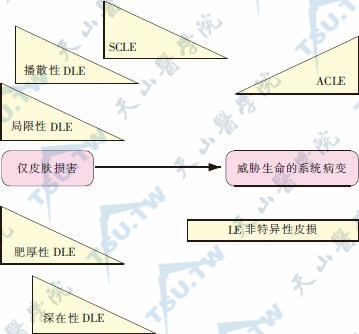
LE特异性皮损并发或进展出现系统性病变的相关危险
病因及发病机制
病因
红斑狼疮的病因尚不清楚,现在发现与本病发病有关的因素有:
一、遗传因素
有不少证据表明遗传因素在红斑狼疮发病中起一定的作用。在同卵双生儿中均发病的可达65%,二人发病的间隔时间一般在2年以内,且临床表现颇为相似。患者家族成员中高γ球蛋白血症、类风湿因子、抗核抗体阳性发生率较高,在直系亲属中的发病率可达5%~12%,发病间隔时间在9年以内,父母或祖父母中有LE的发病的间隔约20年。
近年来组织相容性抗原(HLA)的研究进一步支持了本病的遗传易感性,发现SLE患者中表达率明显高于正常人的有HLA-B8、HLA-DR2、HLA-DR3、DQw1等。在女性DLE病人中HLA-B1阳性的转为SLE的要比其他病人高2.15倍。而药物引起的红斑狼疮综合征与DRw4相关。
研究还发现SLE病人常有与遗传有关的补体缺陷,如C2(主要是C2d),C4(特别是C4a、C4d),Gm和水低平的CR1有关。还有人发现SLE病人的一些自身抗体的产生与HLA也有一定的关系,如抗Sm抗体与DR7,DR4相关。抗SSB抗体与DR3和Dw2、Dw3有关,抗SSA抗体与DR2、DR3、DQ1/DQ2和补体C2D缺陷有关。
目前认为影响SLE发病的是多个独立的分隔基因,这些基因可影响到病人的免疫调节、免疫反应、单核吞噬细胞系统、免疫球蛋白和性激素等。这些都说明SLE发病与遗传因素有一定关联。
二、病毒
有人认为SLE发病与感染有关。在SLE病人的受累和非受累的真皮浸润细胞中和真皮乳头下血管网中的毛细血管、静脉和动脉的内皮细胞中可发现黏病毒样管状结构,在肾脏累及的SLE病人的肾小球内皮细胞中也发现有一样的黏病毒样管状结构,但尚不能肯定这些结构源于病毒,认为可能是对病毒的免疫反应,也可能是内皮细胞吞噬的成分。如果这些结构真是病毒颗粒,它们可能是易感者的激发因素。
在SLE病人中抗逆转录病毒双链RNA抗体的阳性率可达70%,在病人中对麻疹病毒和风疹病毒的抗体滴度也常升高,表明SLE发病与病毒感染有关。
在对新西兰鼠模型(NZB、NZB/NZW杂种鼠)的研究中,实验NZB小鼠及其杂交后代可发生一种很像SLE的自身免疫病。已有研究发现NZB小鼠血液和组织中有一种C型RNA病毒的包膜糖蛋白gp70,它与相应抗体形成免疫复合物沉积于NZB小鼠肾小球内。有人用C型RNA病毒结构中蛋白P30的抗血清检测,发现SLE患者肾中存在P30相关抗原。还有人从人胚肺细胞内分离出一种C型病毒(HEL12),这些事实提示SLE的发病似与C型RNA病毒有密切关系。
此外,在患者肾小球内皮细胞胞质、血管内皮细胞、皮肤损害中都可发现类似包涵体的物质。同时患者血清中往往有几种抗病毒抗体,包括抗麻疹病毒,副流感病毒Ⅰ、Ⅱ型,EB病毒,风疹病毒和黏病毒等抗体。患者血清中尚有抗dsRNA、dsDNA和RNA-DNA抗体。前者通常只在具有病毒感染的组织中才能找到。
根据上述发现,认为SLE的发病与某些病毒(特别是慢病毒)持续而缓慢的感染有关。
三、药物
药物引起SLE已有很多报道。这些病人与自发性的SLE有一定的区别。有作者报道1193例SLE,药物引起或导致病情活动的占3%~12%。一方面药物引起的SLE病人中HLA-DR4表达明显增多,表明这些病人有遗传易感性;另一方面在药物中又以抗高血压药肼屈嗪为代表的一组药物易引起药物性SLE。在这组药物中还有普鲁卡因胺、左旋多巴、甲基多巴、盐酸安他唑啉(心得宁)、利血平、抗癫痫药(苯妥英、扑米酮、乙琥胺、苯琥胺)、抗生素类(青霉素、灰黄霉素)、磺胺类药,其他如异烟肼、氯丙嗪、口服避孕药、青霉胺、布他酮、奎尼丁。有报道,长期接受普鲁卡因胺治疗者,可能有50%以上出现LE临床或实验室表现。接受肼屈嗪治疗者,8%~13%引起LE。值得注意的是,药物引起的SLE除病人的易感性外,还有一定的剂量依赖关系。以肼屈嗪为例,50mg/d无SLE发生;100mg/d发生率为5.4%;200mg/d为10.4%。
药物引起的SLE与特发性的SLE不同还在于:药物性的SLE多见于年龄较大的病人中,临床上主要的系统表现为多发性关节炎、浆膜炎、肝大、淋巴结肿大及肺部浸润,肾和中枢神经系统累及较少发生。皮损主要表现为血管炎、大疱、多形红斑样皮损或与坏疽性脓皮病相似。实验室检查除了有高γ球蛋白血症、白细胞减少、抗核抗体及LE细胞阳性外,抗组蛋白抗体阳性常在临床表现前检出,且阳性率可高达82%。但病人血清中抗双链DNA抗体常常阴性,血清补体也正常。病人的症状、体征在停药后会消退。
药物引起LE的机制目前不清楚,有以下几种可能性:
患者有潜在的LE,药物使之激化。动物实验显示,肼屈嗪、普鲁卡因酰胺和甲基多巴等药喂饲小白鼠8个月,许多小白鼠出现和人LE相似的综合征,20%~40%小白鼠血清中检出DNA的自身抗体。几种纯系小鼠比较实验结果证明某些鼠系发病率高、某些鼠系发病率低,似与遗传有关。药物引起人LE者过去病史及家族史中也发现有遗传倾向。
药物增加了免疫原性作用。如肼屈嗪能与脱氧核糖核蛋白形成药物核蛋白复合物,比核蛋白稳定并具有免疫原性,肼屈嗪联结于载体蛋白,反复免疫动物,肼屈嗪联结于载体蛋白,反复免疫动物,能产生抗单链DNA抗体,最后产生抗双链DNA抗体,这种抗体与DNA及肼屈嗪之间有交叉反应。肼屈嗪引起的LE者有抗重氮化肼屈嗪抗体,在此药存在情况下可使淋巴细胞转化。又如普鲁卡因酰胺在试管内能与DNA形成复合体,具有免疫原性,能产生高滴度的抗体,这种抗体能与天然DNA或光氧化DNA发生反应。
肼屈嗪已知可以抑制补体C4的结合,这个作用使补体激活失控,而引起药物性狼疮。
四、物理因素
在SLE病人的病程中日晒可以激发或加重病情的可达60%。病人对中波紫外线(UVB)和长波紫外线(UVA)的最小红斑剂量也降低。有人在实验中发现经紫外线照射后,DNA的抗原性加强,在实验动物中引起抗DNA抗体,在它的再刺激下可发生肾炎。有人发现紫外线辐射可诱导培养的角质形成细胞Ro抗原的表达,而Ro抗原常常被认为是一种与光敏感有关的抗体。但Ro抗体的滴度与SLE病人病情活动并无相关性。种种证据表明,紫外线辐射在SLE发病中有一定的作用,但其确切的机制仍不清楚。
五、性激素
鉴于本病在育龄妇女发生率明显高于男性,故认为雌激素与本病发生有关。已发现SLE患者性激素的异常在于患者,特别是女性患者产生较强而持久雌激素效应和较弱的雄激素效应。在动物模型中也发现雌性NZB/NZW杂种鼠发病早、且症状重,雄性阉割鼠死亡率较雌性鼠明显增高,给雌激素的雄鼠比给雄激素的雄鼠死亡率高等,实验结果均说明本病发病与性激素有密切关系。
六、其他:细菌的感染、精神忧郁、人种、地区、妊娠及环境污染等其他环境因素等对本病发病均有关系。
发病机制
本病发病机制尚未完全阐明。大量的研究证明本病是一种自身免疫性疾病,正常情况下机体对自身组织不能发生免疫反应。正常机体内有完整的免疫系统,存在复杂的免疫调节功能,调节各种免疫活性细胞活动,控制免疫活性细胞突变和防止禁株免疫活性细胞复活,以阻止发生自身免疫,其中T抑制细胞在免疫调节功能上起重要作用。如在正常人中有对自身抗原受体的B淋巴细胞,血循环中亦有微量的DNA、甲状腺球蛋白等自身抗原,并有识别这些自身抗原及与之起反应的淋巴细胞,机体之所以不发生自身免疫病,是因为T抑制细胞有识别和抑制具有与自身抗原结合的B淋巴细胞的作用,使这种自身免疫细胞群保持在最少,只产生相当少量的自身抗体而不发病,称为自身耐受性。本病可能是遗传、病毒感染、某些环境和激素等因素的相互作用使自身组织细胞结构改变,或免疫活性细胞发生突变,从而失去自身耐受性,造成的机体免疫调节失常的结果。
近年来在NZB小鼠,特别是NZB/NZW小鼠的自身免疫病研究中证明,发病原因之一是T抑制细胞减少,其减少在生后数周即可见到。发现这些小鼠生后早期的血流中有特异性抗胸腺细胞抗体,随着年龄增长逐渐增加,这种抗体是自然发生的抗体,称为自然胸腺细胞毒性自身抗体(natural thymocytotoxic autoantibody,简称NTA)。此后证明小鼠生后NTA逐渐增加,同时发生T抑制细胞逐渐减少,使免疫反应的抑制功能障碍,从而产生自身免疫病。人类SLE中一般可见外周血淋巴细胞抗体,这种抗体也具有低温反应性,属IgM,对T抑制细胞本身的感受性最高。此外,SLE亦可能有淋巴细胞本身异常,在体外加胸腺素后T细胞的抑制功能即可恢复正常。
在SLE病人中的免疫失常也主要表现在淋巴细胞减少,特别是某些亚群如CD4+(辅助/诱导),或CD8+(细胞毒/抑制)淋巴细胞有所减少。特别是抑制性T细胞功能的异常出现较早,IL-2的产生也随之增加,使B细胞多克隆激活,引起自身抗体的大量产生,其中最重要的是抗核抗体、抗DNA抗体和针对各种细胞成分的其他抗体如抗白细胞、抗血小板、抗淋巴细胞或抗非特异性的细胞膜结构如抗磷脂抗体的产生。这些自身抗体可能作为免疫复合物成分与它们的相应抗原结合参与SLE的发病。免疫复合物沉积于关节、小血管内膜或肾小球基膜等,激活补体引起炎症与坏死,临床上表现为血管炎、肾小球肾炎等Ⅲ型变态反应。有些自身抗体也可与器官或细胞的某些抗原直接相互作用,表现为Ⅱ型变态反应,如红细胞与血小板的特异抗原与自身抗体结合后引起溶血性贫血或血小板减少症。另外,Ⅳ型变态反应(细胞免疫)造成的组织损伤对本病的慢性病程可能起重要作用。最近有人认为自身抗体可通过与淋巴细胞的相互作用及补体的参与或通过Fc受体或抗体依赖的细胞毒性的间接作用引起参与免疫调节的淋巴细胞减少,也可以通过肝脏和其他单核吞噬细胞系统清除淋巴细胞,从而引起免疫调节的紊乱,使机体对自身组织产生免疫反应(包括体液免疫和细胞免疫),正常组织和功能被自身免疫细胞或自身抗体破坏而发病。
症状表现
皮肤红斑狼疮
皮肤红斑狼疮的临床表现多种多样。
一、急性皮肤红斑狼疮(ACLE)
即系统性红斑狼疮(SLE)病人的皮损,包括面部蝶形红斑、伴有或不伴有水肿的泛发性红斑。
局限性ACLE主要表现为面颊部蝶形红斑,为对称分布于面颊和鼻梁部的融合的水肿性红斑,可累及前额、下颏、颈部和前胸V字区,并可伴有明显的面部肿胀。
泛发性ACLE通常表现为广泛分布的麻疹样或发疹样红斑,好发于上肢伸侧及手背,虽然也可有甲周红斑和毛细血管扩张,但在皮肌炎中更常见也更典型。
大疱性皮损是本型皮肤LE的一种新亚型,又称大疱性红斑狼疮(bullous lupus erythematosus)。皮损为单个或成簇的水疱或大疱,常广泛分布,好发在曝光部位,瘙痒常不明显。皮肤组织病理为含有中性粒细胞的表皮下水疱。免疫电镜示,在致密板有颗粒状IgG、IgM或IgA沉积。多数病人为HLA-DR2阳性。病人对氨苯砜治疗十分敏感,以此可与获得性大疱表皮松解坏死症鉴别。
大疱性红斑狼疮 鲜红色斑,水肿性,在此损害上出现水疱或血疱
ACLE日晒后常加重,皮损消退后可有色素沉着,如无继发细菌感染,一般不留瘢痕。偶见ACLE并发DLE,但ACLE和DLE同时发生罕见。无论局限性还是泛发性ACLE,其皮损加重或减轻往往与潜在的SLE(包括狼疮肾炎)病情平行。
二、亚急性皮肤红斑狼疮(SCLE)
1979年Sontheimer等首先报道了27例SCLE的临床和实验室特征,近半数(48%)患者符合美国风湿病协会SLE的诊断标准,而系统性损害轻,因此认为这是一种以皮肤症状为主的LE特殊亚型,属DLE和SLE的中间型,过去曾称为对称性离心性红斑(1925年Brocq)、自身免疫性环状红斑、亚急性播散性LE、浅表性播散性LE和银屑病样LE等。
本病女性多见,患者以中青年为主。在所有LE病例中占10%~15%。皮肤表现主要有二型:
- 环状/多环型,损害初起为水肿性红斑和(或)斑块,逐渐向外围扩大成环形或弧形,可与邻近的皮损融合成多环形或脑回形,边缘红色、隆起,内侧缘覆细小鳞屑,中央消退后留浅灰色色素沉着和毛细血管扩张。或呈离心性环,环中央消退处又起新环。
- 丘疹鳞屑型(银屑病型),初起为红色丘疹,逐渐扩大成大小不等形状不规则斑丘疹,上覆菲薄鳞屑,呈银屑病样或糠疹样,没有毛囊性栓塞和黏着性鳞屑。以上2种皮损中,通常只出现一种类型皮损,偶有二型同时存在。约20%病例伴DLE损害。皮损持续数周或数月消退,可在原处或它处复发,消退后不留瘢痕。皮损好发于曝光部位,主要分布于面、颈、躯干上部、上肢伸侧及手足、指(趾)背,硬腭累及可达40%,唇和颊黏膜偶可累及。
额、鼻及两颊部红斑,边缘炎症明显,部分稍隆起,鼻背至颊部呈蝶形分布
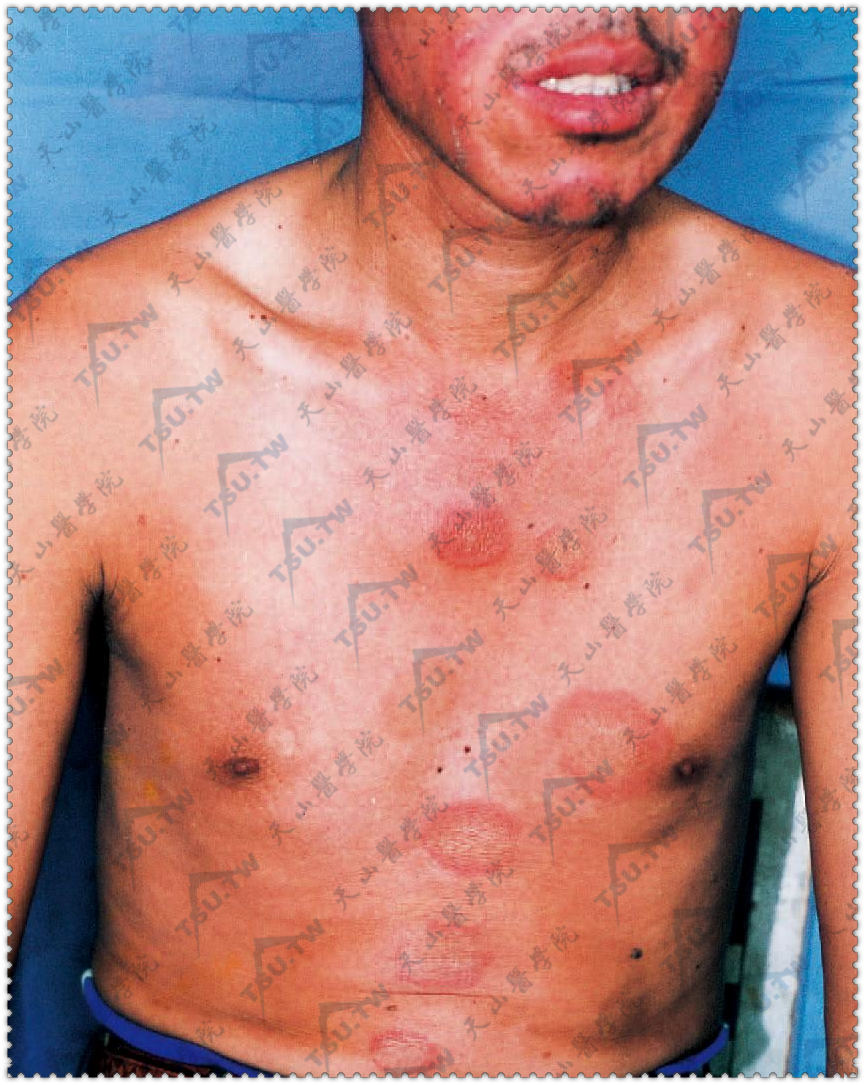
躯干环形红斑,边缘水肿,稍隆起,中央有轻度色素沉着
此外,还可有光敏、脱发、雷诺现象、网状青斑和甲周毛细血管扩张等。
除皮损外可合并有关节痛或关节炎,其次为发热、肌痛、浆膜炎。肾损害及中枢神经系统病损发生率低、病情轻。
实验室检查:可有贫血、白细胞降低、血小板减少、血沉快。LE细胞阳性(10%~55%),ANA(+)(80%)。63%患者抗Ro/SSA抗体阳性,50%~70%抗La/SSB抗体阳性,此两抗体测定的高阳性率为本病的免疫学特征。47%有Ro/SSA、La/SSB两种抗体,也可有抗dsDNA抗体(10%~30%)、抗RNA抗体(8%~19%)和抗Sm抗体(4%~13%)阳性。此外有循环免疫复合物(CIC)升高和补体降低。直接免疫荧光检测皮损,约60%患者真皮表皮交界处有IgG沉积,呈连续性、不规则颗粒型,无皮损处检测约30%(+)。HLA表型以A1、B8、DR3多见。
在亚急性皮肤红斑狼疮中还有以下两种特殊类型:
(1)新生儿红斑狼疮(neonatal lupus erythematosus,NLE):本病是由母亲体内的Ro/SSA抗体经胎盘转移给婴儿,使其发生皮肤损害或心脏传导阻滞的独特疾病。临床上多见于女性(约占75%),发生于出生后头几周的新生儿。
皮损为SCLE样的环状鳞屑性红斑,主要见于头、颈、眼眶周围曝光部位,非曝光部位也可受累。
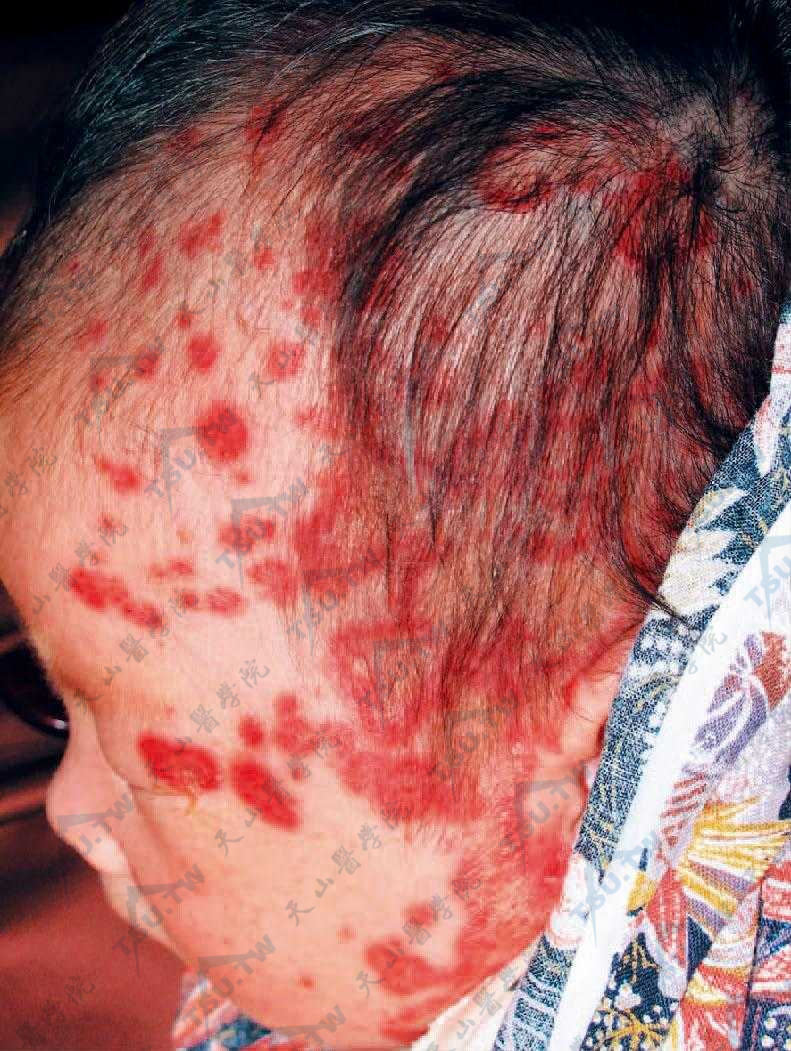
面部多数鲜红色斑,呈环状
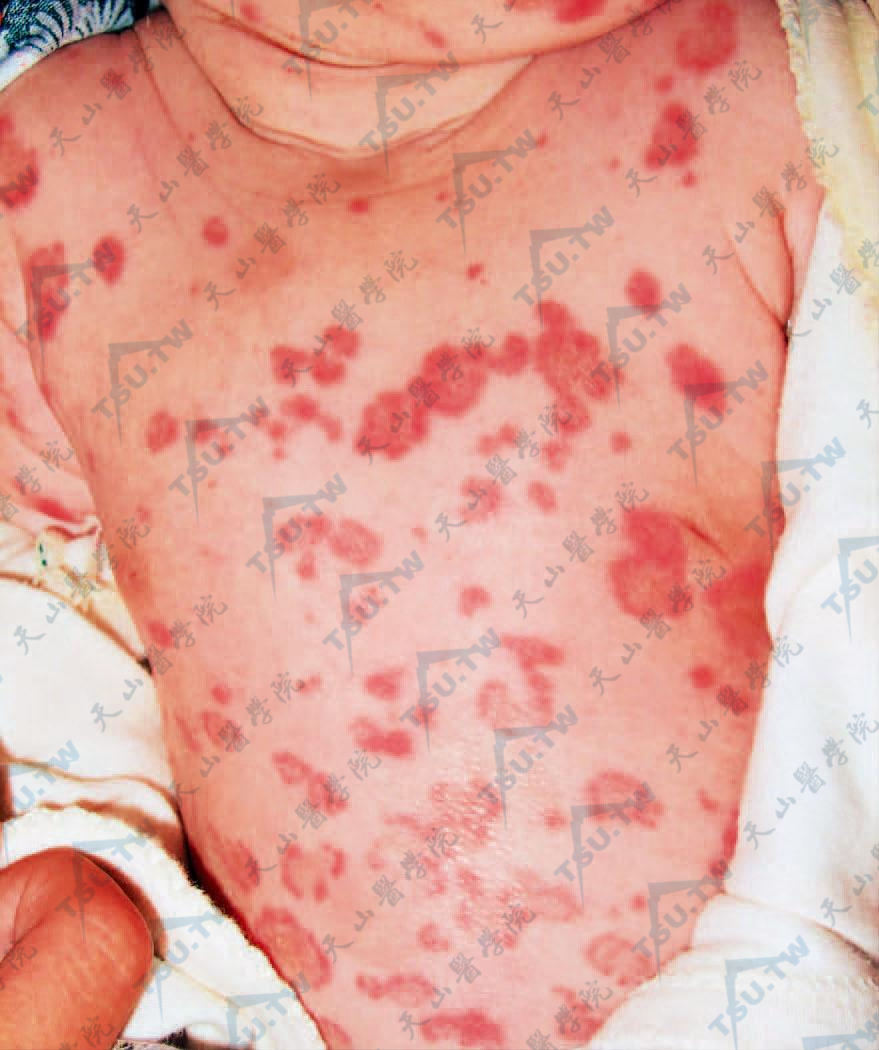
躯干部多数大小不等环状红斑,有少许鳞屑
完全性或不完全性先天性心脏房室传导阻滞(CHB)是NLE的常见临床症状,通常为三度,并是终身性的,可伴有或不伴有皮肤病变。患儿有时也可有血小板减少、溶血性贫血、白细胞减少和肝炎等系统症状。
Ro/SSA抗体为本病的血清学标志,母、婴血中均可有。患儿偶可发现有U1RNP抗体阳性。
患儿的皮损通常在6个月内自动消失,皮损消退后不留瘢痕。少数患者可发展成活动性SLE。同时有皮损和CHB者预后较差。
皮损的组织病理和免疫病理具LE的特征。
患儿母亲可以是SLE患者,也可以是其他风湿病患者,多数临床上无症状。HLA-DR3频率较高。由于本病多发生先天性CHB,因此,具有Ro/SSA抗体阳性的妊娠妇女要严密观察胎儿的心脏变化。
(2)补体缺陷综合征(complement deficiency syndrome):许多补体成分的缺陷可伴有LE样的表现,特别是C2和C4的缺陷。此临床亚型病人的共同特点为环状的SCLE样皮损、光敏感和Ro/SSA抗体的阳性。
三、慢性皮肤红斑狼疮(CCLE)
(1)盘状红斑狼疮(discoid lupus erythematosus,DLE):早期的DLE皮损为钱币大小红斑,境界清楚,上覆黏着性鳞屑,鳞屑下方有毛囊角栓,剥离鳞屑,可见扩张的毛囊口。在发展过程中,红斑扩大,有周围色素沉着,而损害中心逐渐出现萎缩,微凹,色素减退。
皮损局限者称为局限性DLE,好发于面部,特别是两颊和鼻背,呈蝶形分布(图3-12-7);其次发生于口唇、耳廓、头皮等处。在唇及口腔黏膜的DLE损害呈灰白色斑块,可形成糜烂及浅溃疡,最后出现萎缩。60%的DLE累及头皮,有1/3可导致永久性秃发。
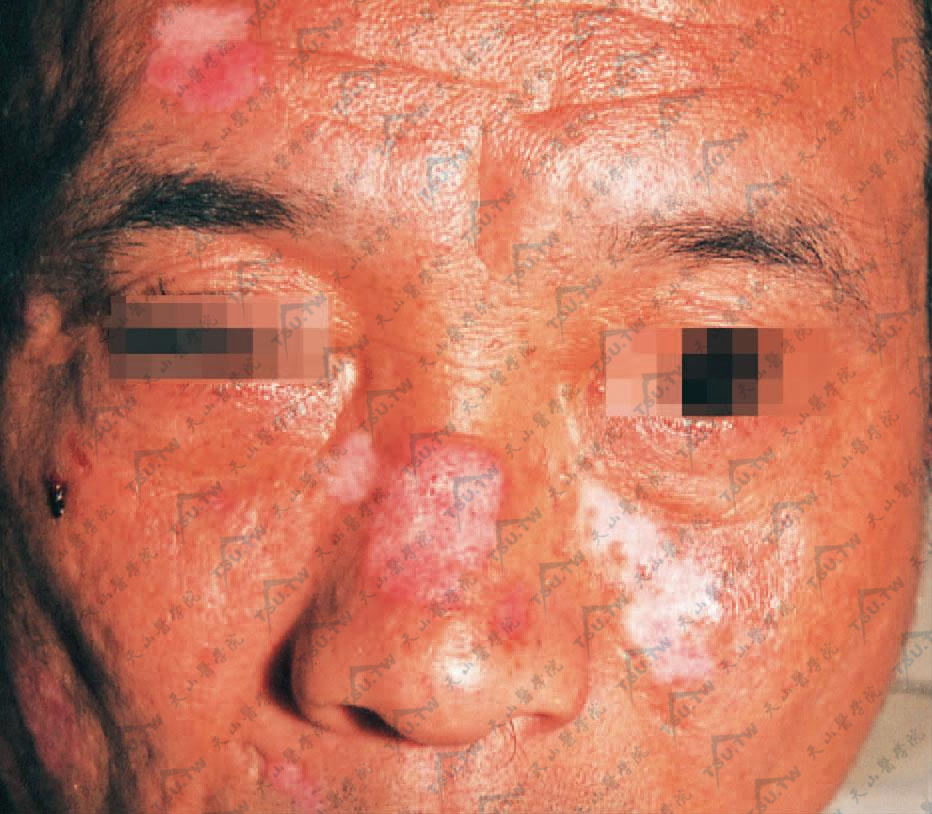
DLE 两颊和鼻背,见持久性盘状红斑,境界清楚,表面毛细血管扩张并有黏着性鳞屑,剥离鳞屑可见其下的毛囊口。损害中心逐渐萎缩、微凹、色素减退
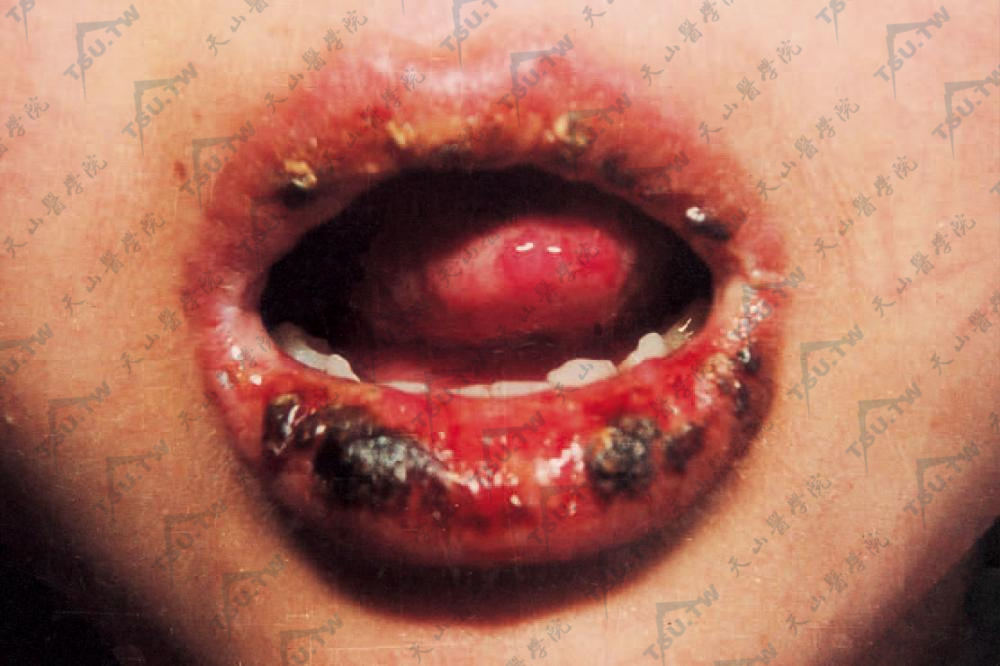
唇红部糜烂及浅溃疡,表面有结痂及血痂,下唇较明显
DLE皮损也可广泛地发生于四肢、手背、手指、躯干,称播散性盘状红斑狼疮(disseminated discoid lupus erythematosus)。此外,DLE尚可有第二种类型损害,为紫红色荨麻疹样斑块,不发生萎缩和鳞屑,一般在面部,可不对称,或呈蝶形分布。DLE病程呈慢性,少数病例皮损可自行消退。一般愈后留下色素减退的萎缩性瘢痕,严重的瘢痕可引起毁形,头皮则形成萎缩性脱发区。容易复发。有时在日晒或过度劳累后加剧。少数经久不愈的陈旧损害因局部用药不当或长期慢性刺激可发展为鳞状细胞癌。
(2)疣状(肥厚性)狼疮(verrucous/hypertrophic lupus erythematosus):皮损好发于面部、上肢伸侧、上背部,为非瘙痒性丘疹结节样损害,皮损显著高出皮面,表面可呈疣状,与角化棘皮瘤和肥厚性扁平苔藓相似。
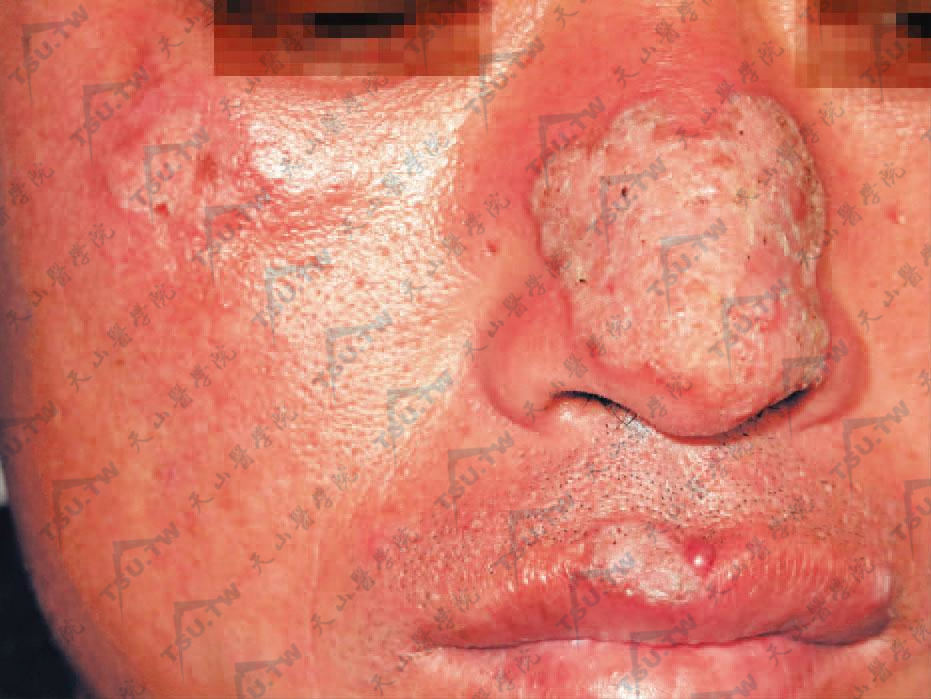
鼻背部、颧及上唇红色斑块,表面疣状,中央有萎缩性瘢痕
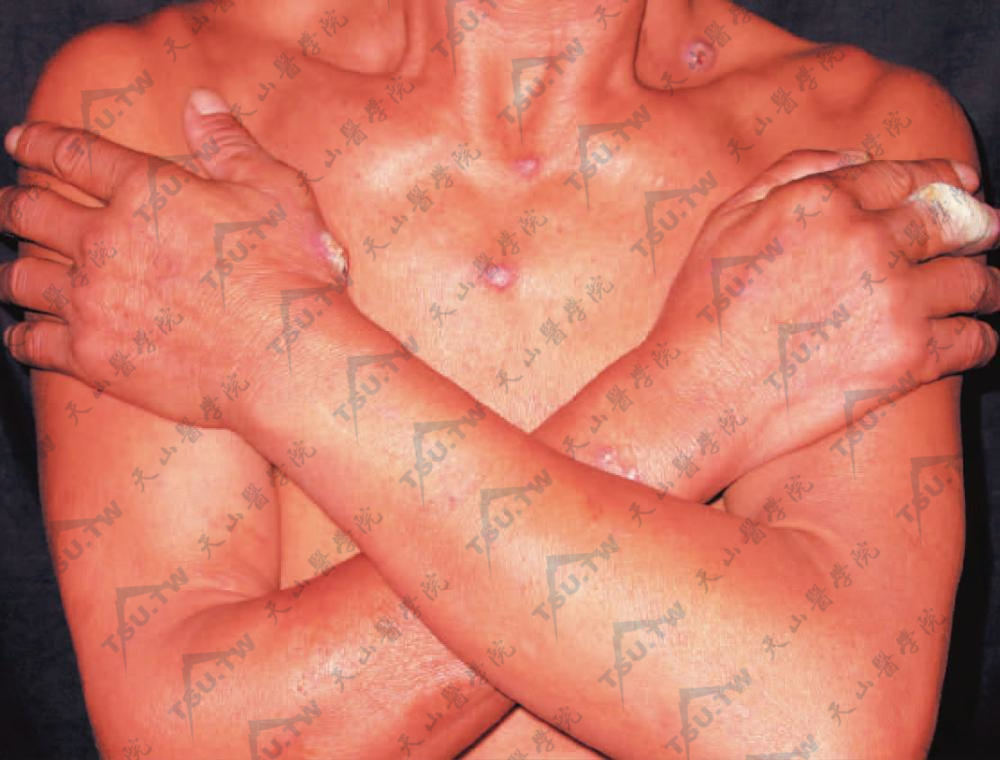
手臂部丘疹结节损害,皮损显著高出皮面,表面呈疣状
(3)狼疮性脂膜炎(lupus panniculitis):又称深在性红斑狼疮(lupus erythematosus profundus,LEP),为介于DLE和SLE间的中间类型。发生率占LE的2%以上。男女都可发生,主要见于女性。大多为中年人(40~50岁),但少数儿童亦发生。皮损表现为深部皮下结节或斑块,一个或多个,坚硬。表面皮肤常为皮色或淡红色,或为典型DLE。有的结节持续不变,而在其他部位发生新损害,有的逐渐扩大或与邻近结节融合成斑块。有的结节可吸收,皮面凹陷或坏死,溃疡,愈合后留萎缩性瘢痕。结节可发生于任何部位,常见于颊、臀、臂,其次为股、胸部。单侧或两侧分布。
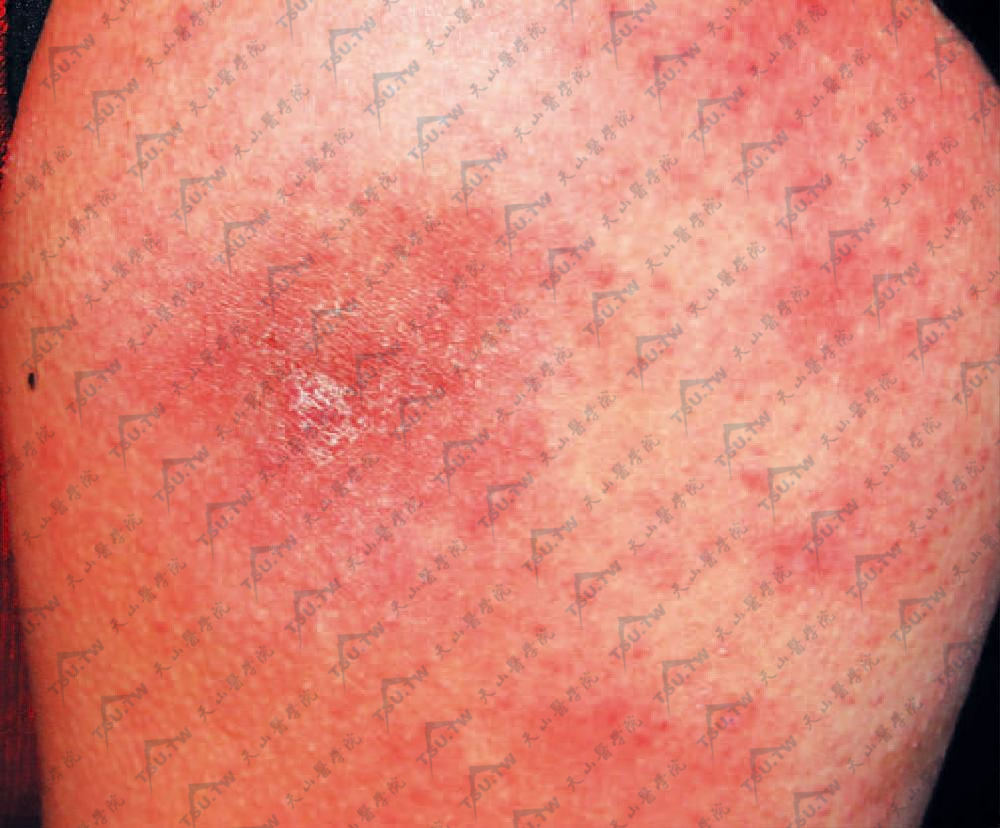
深在性红斑狼疮 皮损为深部皮下结节或斑块,质硬。皮面凹陷萎缩
实验室检查:可有贫血、白细胞减少、血小板减少和血沉增快。30%病例ANA(+),类风湿因子阳性,免疫球蛋白升高。组织病理病变主要在皮下脂肪组织,直接免疫荧光示脂肪小叶间隔内血管壁有免疫球蛋白沉积。
LEP经过慢性,可同时伴SLE或DLE,亦可在LE发病之前或之后发生,或者以结节形式存在而无典型LE皮损。本型不稳定,可向DLE或SLE转变。亦可初为DLE或SLE,以后转为LEP。
(4)肿胀性(瘤样)狼疮(lupus erythematosus tumidus):是CCLE的一种少见亚型,多见于青年男性,皮肤肿胀、发热,类似荨麻疹样斑片,直径数厘米甚至整个面颊或肢体;光敏明显。
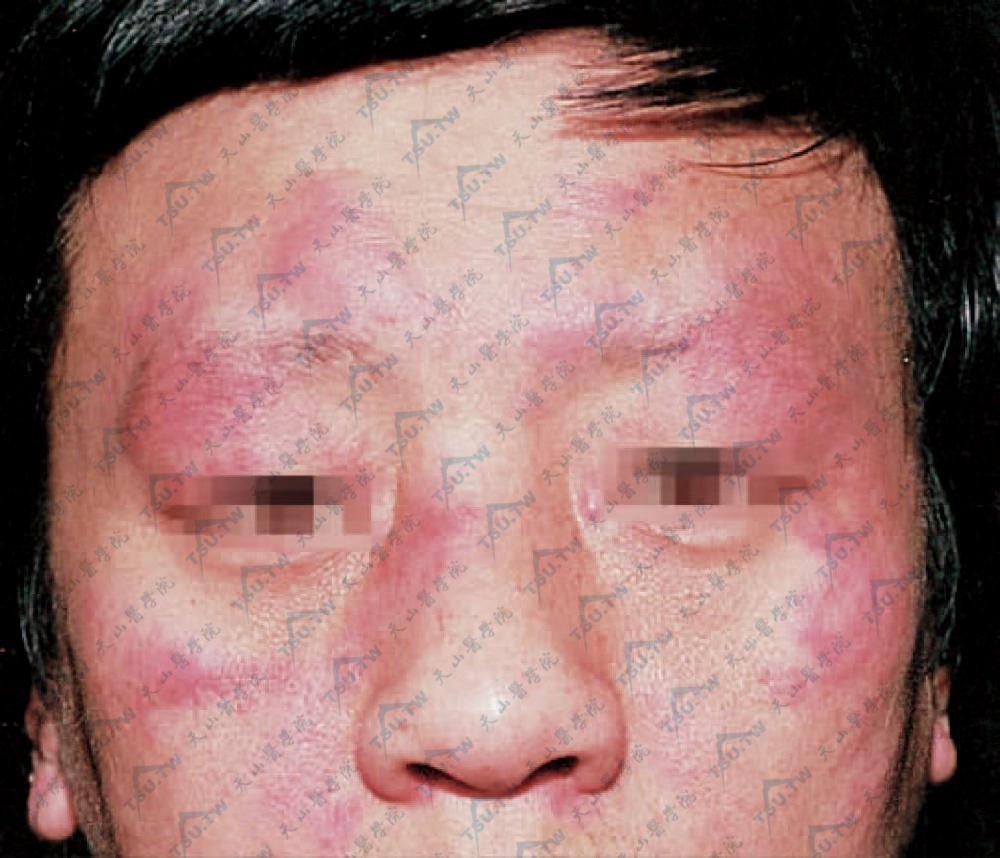
肿胀性红斑狼疮 前额、双上眼睑、颧部、鼻部散在水肿性红斑(北京协和医院皮肤科 曹海鹏提供)
(5)冻疮样狼疮(chilblain lupus erythematosus):是一型分布于肢端的由微血管受到冷创伤引起的慢性红斑狼疮,以指(趾)尖、足跟、小腿后侧、肘、膝、鼻和耳等处的紫红色斑片为特征,多见于女性。常发生在面部的DLE之后,有时可有系统累及。有报道可有抗磷脂抗体阳性。用治疗LE的药物治疗通常无效。
(6)红斑狼疮与扁平苔藓重叠综合征(LE/LP overlap syndrome):近年来有报道,部分患者在皮损的临床、组织病理和免疫荧光检测方面同时显示LE和扁平苔藓(LP)两者的典型表现,这些患者不可能明确诊断两种疾病中的任何一种,称之为LE/LP重叠综合征。
可见三种皮损:LE样损害,苔藓样丘疹及疣状损害。
所有患者都有DLE样损害,为圆形紫红色斑或斑块,境界清楚,轻度浸润,部分皮损表面萎缩,常有毛囊性角化过度和鳞屑,偶有毛细血管扩张小点。也有报道皮损中央有水疱、溃疡者,好发于面部与四肢末端,尤其是手足背、甲皱襞和掌跖。
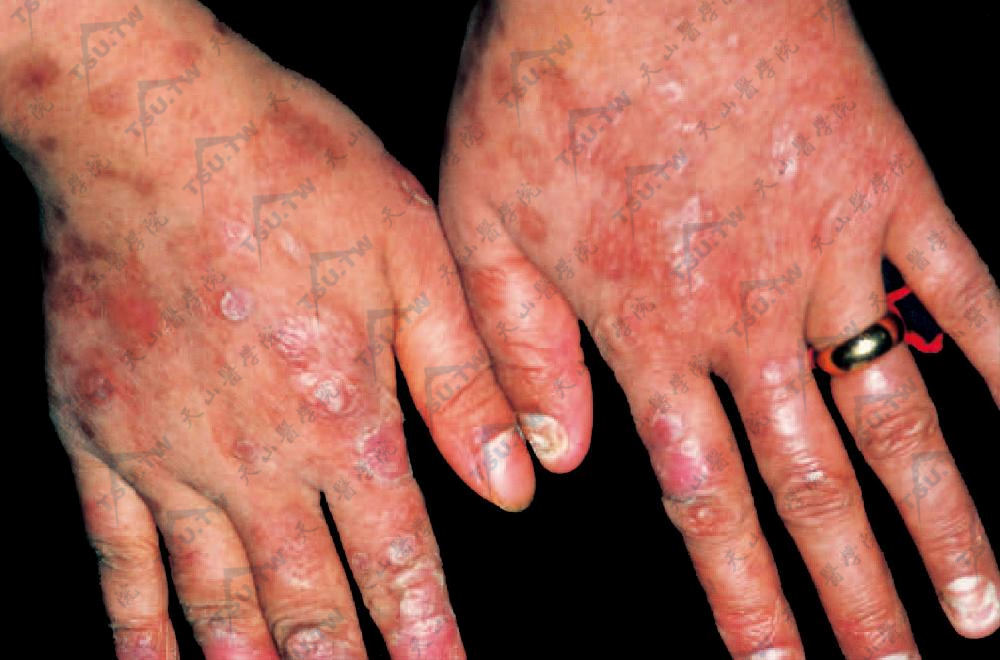
手背部慢性盘状红斑狼疮样损害,圆形或椭圆形紫红色斑块,部分皮损表面萎缩、毛囊角化过度和鳞屑。同时见扁平苔藓样扁平紫红色丘疹
有的患者可见苔藓样扁平紫红色丘疹位于前臂屈侧、腕部、小腿和外生殖器。
疣状损害表现为紫红色硬的丘疹、结节,位于四肢伸侧或掌跖。皮损瘙痒不明显,可有疼痛和触痛。
部分患者口腔黏膜有白色或红色网状斑,偶有糜烂。亦可有甲损害、光敏感、脱发、关节痛等。
实验室检查:可有类风湿因子(+),梅毒血清反应假阳性,ANA(+)低滴度。个别患者抗DNA抗体阳性。
对本病的本质尚有不同看法,有人认为进一步的实验室检查有助于LE/LP重叠综合征区别出是LE或LPL。在LE及LP中均可见胶样小体中有免疫球蛋白及在BMZ中有线状纤维蛋白原沉积,但如在同一标本上可见上述两种表现,则是LP的特征性表现,如BMZ无颗粒免疫球蛋白沉积则更支持为LP。应用组织化学技术,用maleimide衍生的荧光色素测出胶样小体中二硫化物,可将LP从LE中区别出来。1983年Olsen等用自身皮损作底物作间接免疫荧光,可在颗粒层及棘层发现有LP特异性抗原(LPSA),这些方法的应用,将进一步了解本病的本质,而有助于指导对本症的治疗。
系统性红斑狼疮(SLE)
SLE早期表现多种多样。初发时可仅单个器官累及,如皮肤、关节、肾脏,或多系统同时受累。全身症状如发热、乏力、疲倦等,有时可长达数年而查不出原因。关节及皮肤表现为本病最常见的早期症状,其次是发热、光敏感、雷诺现象、肾炎及浆膜炎等。
一、全身症状
SLE发病时常见的全身症状有中等到严重的乏力(75%)、体重减轻(67%)和发热(90%)。这些症状在病情好转时可消失,病情活动时可重现。病人的热型不规则,以低热为多,疾病恶化时常有高热,伴畏寒、头痛等。
二、关节、肌肉和骨骼表现
关节痛、肿胀是临床上最常见的症状,常在多系统累及前出现,几乎所有患者(95%)都有程度不同的关节症状,常在疾病活动期加重。晨僵和关节痛最常见,伴附近肌肉疼痛,但疼痛常与体检发现不一致,好侵犯四肢大小关节。有时出现风湿或类风湿关节炎样症状。关节症状往往是本病的最早表现,甚至在长时间内为惟一的表现。X线检查无关节破坏征象,亦无关节挛缩及强直表现。
肌痛是常有的主诉(约占25%),偶可有近端肌萎缩。
累及骨者罕见,但长期接受糖皮质激素治疗的病人,5%~40%患者可发生无菌性骨坏死。股骨头最常累及,其次为肱骨头、胫骨头等。多数为双侧性,系因局部血管闭塞,供血不足,致骨无菌性坏死。临床表现为骨关节疼痛,可急性发作或缓慢发生,进行性发展,活动时加剧,发生于股骨头者则伴髋关节活动尤其是外旋受限,患者不能下蹲,严重者步行困难。一般于临床症状出现后2~6个月X线方显示典型的早、中、晚三期改变。
三、皮肤黏膜表现
80%~90%SLE患者有皮损。皮疹表现为多形性,可表现为:
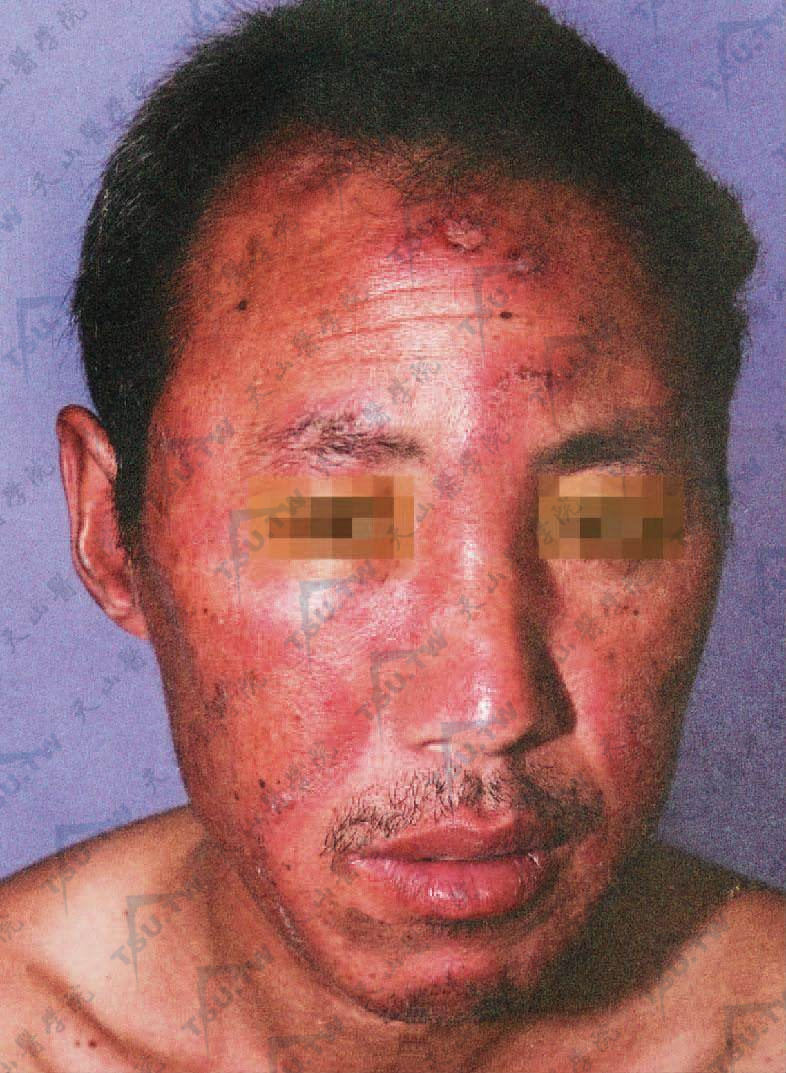
- 面部蝶形红斑:是本病特有的皮肤症状,为略具水肿性的红斑,颜色鲜红或有灰白鳞屑。在渗出性炎症严重时,出现水疱、结痂。好发于鼻颊部,呈对称性蝶形分布(下图:面部蝶形红斑,水肿性,颜色鲜红或紫红,表面光滑或附有灰白色鳞屑)。广泛者可发展至前额、下颌、耳、颈前三角区、四肢。有痒或灼热感。红斑一般在缓解期逐渐消退,遗留棕黑色色素沉着,偶见萎缩。面部红斑常在全身症状之前或在病程中出现,晚期罕见。
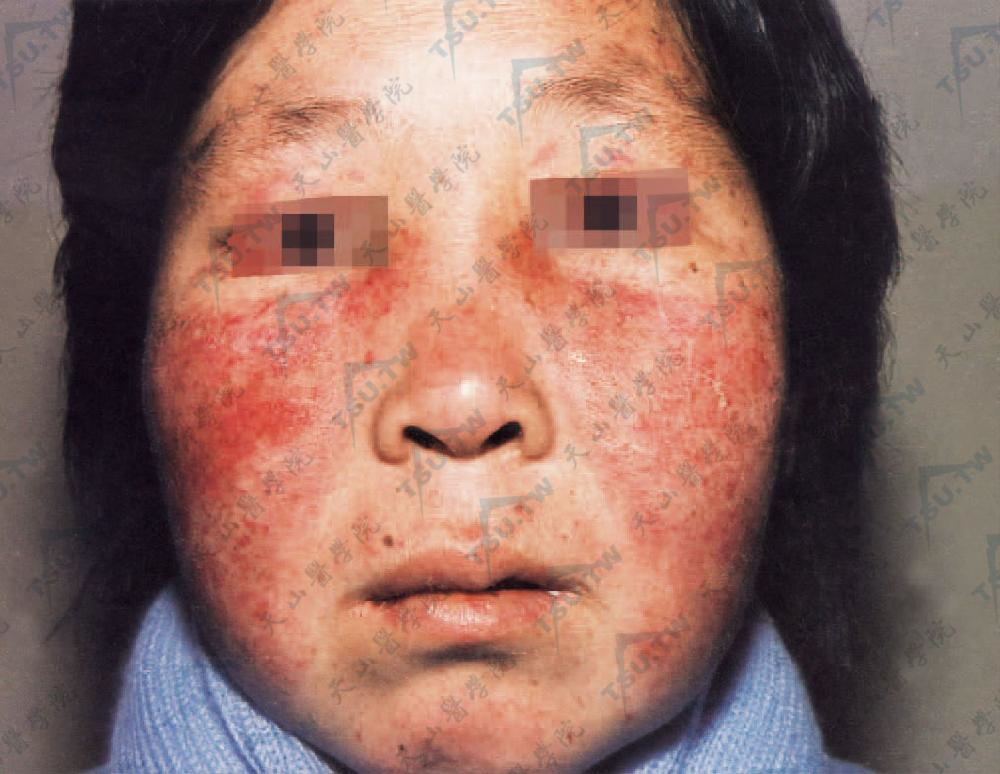
- 慢性盘状狼疮皮损:约见于15%的病人,可发生在多系统损害之前,皮损特点同慢性皮肤红斑狼疮。
- 眶周水肿带紫红色和毛细血管扩张:颈部和胸部V区紫红色斑,虽在皮肌炎中常见,也可见于SLE。
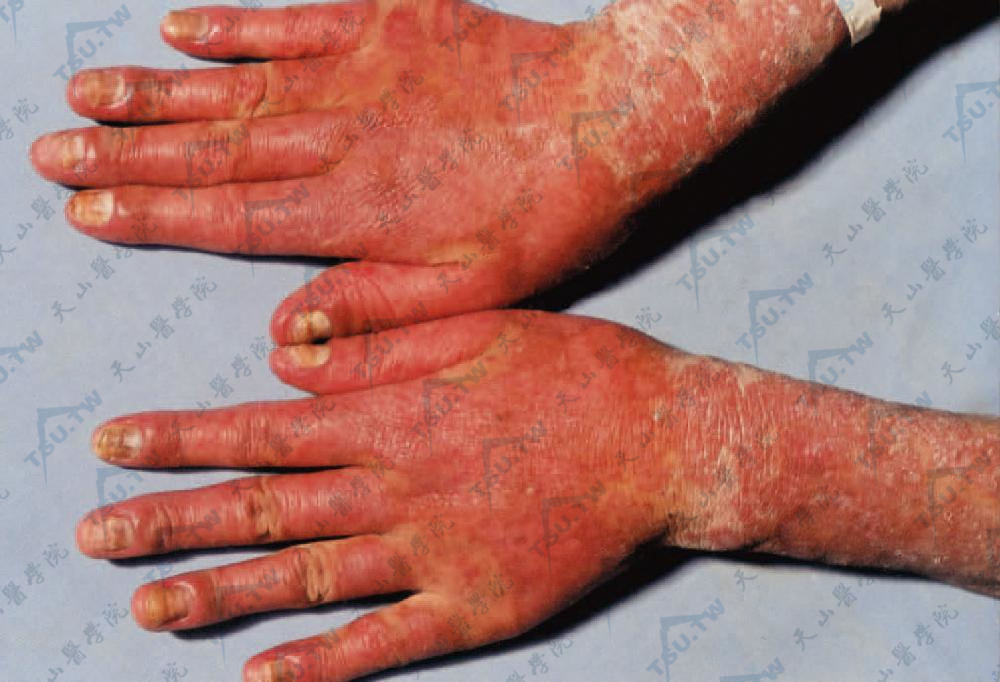
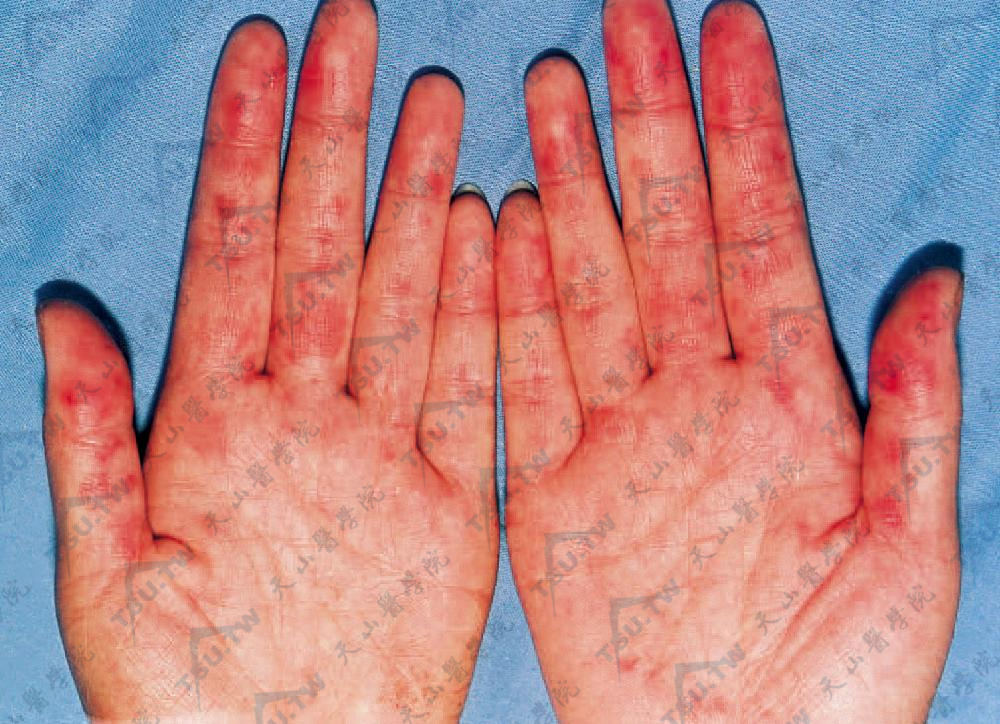
- 手足部皮损:临床上常表现为指(趾)伸屈侧类似面部的渗出性水肿性红斑或多形红斑型冻疮样皮疹。手掌的大小鱼际、指背、足跟侧及趾部可有网状毛细血管扩张性红斑。甲周皮肤、甲后皱襞和邻近护膜有短线状毛细血管扩张。甲周及指(趾)尖部出现鲜红色或紫红色斑点和点状出血,久之局部轻度点状萎缩。掌、指有散在丘疹样毛细血管扩张,此也系SLE的特征性体征(下图:指尖部鲜红色或紫红色斑点和点状出血)。
- 血管炎皮损:SLE血管炎皮损根据其累及的血管(动脉或静脉)的大小和部位不同而表现不同。四肢等部皮肤的真皮和皮下脂肪组织小动脉发生坏死性血管炎,表现为皮下结节,或为水肿、红斑、紫癜、结节、坏死、溃疡等各种皮疹混合存在,此时要注意其他脏器如中枢神经系统、眼、肾、心等也可有血管炎。
- 紫癜:是坏死性血管炎的表现,常表现为紫癜样丘疹,需与血小板减少性紫癜和糖皮质激素性紫癜鉴别。前两者要加大糖皮质激素治疗剂量,后者则相反。
- 网状青斑:由于皮肤小动脉血管痉挛、内腔狭小或闭塞引起小静脉扩张淤血或血黏稠度增加,浅表毛细血管血流缓慢致皮肤出现网状或树枝状青斑。多发生在四肢伸侧、手背等处,好发于小腿,躯干部少见。
- 慢性荨麻疹:7%~22%LE病例有慢性荨麻疹,常与疾病活动性增加有关。也可发生面部和四肢血管神经性水肿。其中大部分损害病理表现有坏死性血管炎变化,在真皮表皮交界部和真皮血管中有Ig和补体沉积,故SLE中的荨麻疹通常是其潜在循环免疫复合物病的皮肤表现,而不是普通的慢性荨麻疹。患者血清中往往存在IgG-抗FcεRIα自身抗体或(和)抗IgE自身抗体,发病以自身免疫机制为基础,该IgG抗体的亚型主要为IgG1和IgG3,有补体激活功能。这类慢性荨麻疹临床上多表现为严重的难治性的慢性荨麻疹,与普通的慢性荨麻疹患者相比,其发作时皮损数量较多,分布范围较广,瘙痒更剧烈,系统症状,尤其是消化道症状和发热亦更常见。
- 雷诺现象:约20%患者有雷诺现象,常见于疾病早期。
- 光感性皮损:约33%患者对日光敏感性增加,日光曝晒后皮损发红,部分病例出现新的皮疹。
- 脱发:是一种很重要的特征,呈局限性或弥漫性。约发生在67%的活动期SLE病人中。局限性脱发者出现单发或多发性脱发斑,境界清楚,具典型的DLE改变。弥漫性脱发可由于患者病情重,引起暂时性脱发,但也见于病情不重的LE患者,头皮外观正常,病情缓解后头发再生。
- 狼疮发(lupus hair):系指前额部发线下降,发变短,长短不齐,干燥,变细变脆,失去光泽,容易拔脱,形成散乱外观。
- 黏膜损害:在红斑狼疮中并不少见,发生于10%~15%的SLE患者,常见于病情加重时,可表现为眼结膜炎,口腔黏膜的损害表现为齿龈红肿、糜烂。口腔黏膜和唇部红斑、淤点、糜烂,伴有红晕的浅溃疡、牙龈炎和鼻咽部溃疡等。红斑、出血和糜烂也可发生在硬腭。
- 其他皮损:SLE活动期尚可出现下列皮疹:
- 荨麻疹样损害上出现水疱或血疱,此是皮损基底细胞层的水肿变性加上真皮上部严重水肿,引起表皮下水疱;
- 紫红色荨麻疹样丘疹或斑块,仅持续几天;
- 多形红斑样皮疹,特别在冷季发生;
- 皮下结节,5%~7%患者有临床和组织学上与类风湿关节炎中的类风湿结节相同的皮下结节,一般非痛性,软骨样硬度。好发于手部小关节周围,使用抗疟药物治疗后可消失。
值得注意的是,少数SLE患者始终无皮疹。故皮疹并非本病诊断之必备条件。皮疹的严重性与本病的预后不完全一致。
四、肾脏损害
狼疮性肾病是SLE最常见和最严重的内脏损害。根据出现蛋白尿估计,发生率约50%,因有些隐匿性狼疮性肾病可无蛋白尿,故实际发生率还要高。肾脏损害出现于本病任何阶段,以第一年较多。临床上,肾外表现与肾脏病变并无明显平行关系,严重和活动性SLE患者可无肾脏损害;但有严重肾脏损害者一般见于活动性SLE,且有肾脏之外的内脏表现。SLE肾脏损害临床表现为肾炎或肾病综合征。肾炎时尿内出现红细胞、蛋白及管型。肾病综合征时,全身水肿,大量蛋白尿,低蛋白血症,血胆固醇正常或增高。早期肾功能正常,后期可出现尿毒症和肾性高血压。
血中免疫复合物与肾脏病变有一定的平行关系,严重的活动性肾脏病变免疫复合物常明显增高,补体成分明显下降,可出现冷球蛋白。但也有例外,血循环中出现DNA抗DNA抗体复合物并不一定提示有活动性肾病,若血清中出现C3降解产物,尿中免疫球蛋白轻链浓度增高,则有活动性肾病可能性较大。
一般应进行肾脏穿刺活检确定狼疮性肾炎病变的类型及其活动性,根据组织上病变广泛程度及病理改变,一般分为四型。各型临床表现、预后和治疗有所不同。
- 轻微性狼疮性肾炎或系膜性狼疮性肾炎:本型病情轻,发生率约10%。肾小球正常或有系膜组织轻度增生和基质轻度增多。大多数病例无肾脏损害的临床症状,少数患者出现轻度蛋白尿,偶有镜下血尿,一般没有高血压,肾功能常正常。小部分患者可转为膜性或弥漫增殖性狼疮性肾炎。
- 局灶增殖性狼疮性肾炎:发生率为15%~30%。病变局限于几个肾小球,呈局灶性和节段性分布,主要是增殖性变化。临床表现一般较轻,为轻度蛋白尿和(或)显微镜下血尿,一般没有高血压,很少发展为肾病综合征及肾衰竭。少数可毫无症状,完全为隐匿性。大多数患者预后好,少数继发肾功能不全。部分患者病变加重则转变为弥漫增殖性狼疮性肾炎。
- 膜性狼疮性肾炎:病情介于局灶增殖性和弥漫增殖性两者之间,约占10%。肾小球基膜高度肥厚,几乎无细胞增殖,临床特征为持续性蛋白尿,一般不伴高血压及肾衰竭。很少转变为其他类型。
- 弥漫增殖性狼疮性肾炎:本型是最常见、最严重的病变类型,占45%~50%。全部或几乎全部肾小球受累,肾小球血管间质及内皮细胞弥漫增殖。特征表现是膜内有沉积物,呈嗜酸性,折光性强,不规则地累及毛细血管袢,使有些毛细血管袢僵硬,呈铁丝圈(wireloop)状。某些活动病例还可见坏死灶及苏木素小体。临床上常有明显蛋白尿、镜下血尿及各种管型。常有高血压,常见肾病综合征及肾衰竭。肾衰竭的严重程度差异很大,病变可为急性、可逆性活动性或慢性硬化性损害。本型如不治疗,肾功能常进行性衰退,活动性损害变为纤维增生而成硬化性损害。
五、心血管系统表现
约见于1/3SLE患者,以心包炎为多,可有心包积液。心肌炎亦常见。可有心内膜炎。心包炎时患者可以无症状,仅在心电图或心超声检查时发现。多数病人感到心前区不适、气急,心前区可听到心包摩擦音。心内膜炎波及瓣膜(多为二尖瓣)时,心前区常听到收缩期杂音。心肌受损时可产生心动过速、奔马律、心脏扩大,最后可导致心力衰竭。心电图有相应改变,如心包膜或心肌受损呈低电压,ST变化,T波倒置,PR间期延长。心肌炎常常与心包炎合并发生,也见于多达25%的病人。对于难以解释的静止期的心动过速,与体温不成比例的心动过速,ECG提示有ST段改变,或X线显示心脏肥大而无心包积液的患者,应怀疑心肌炎。可发生充血性心力衰竭与心律失常,以及心肌酶谱的升高。个别病例出现冠状动脉炎。糖皮质激素应用后疣状心内膜炎已不多见。
六、呼吸系统表现
SLE患者40%~50%的病人出现肺与胸膜受累。胸膜炎或胸腔积液往往为双侧,是最常见的临床表现。也可表现为间质性肺炎,出现咳嗽、多痰、呼吸困难、发绀、胸痛等症状。X线检查可显示肺纹理增强,双肺片状浸润,胸膜增厚或胸腔积液等。可引起肺不张以至呼吸衰竭。少数病人可发生肺栓塞,引起肺梗死,并可导致肺动脉高压。这种肺动脉高压,像原发性肺动脉高压一样,预后极差。它常可伴有抗磷脂抗体阳性。
七、消化系统表现
约见于40%患者,胃肠道任何部位均可受累,系胃肠道血管发生血管炎和栓塞所致。临床症状包括食欲不振、恶心、呕吐、腹痛、腹泻、呕血、便血等。消化道出血系弥漫性肠系膜动脉炎或弥漫性血管凝血引起,重者致死。SLE患者常有肝大,黄疸却很少见,如病人有黄疸,多与溶血性贫血有关。肝酶的升高有多种因素,包括阿司匹林和其他非甾体类抗炎药、硫唑嘌呤以及巨细胞病毒感染等。
胰腺炎可以是少数SLE病人(1%~4%)的最初表现,病人有可放射到背部的上腹部剧痛,伴恶心、呕吐和血清淀粉酶升高。重者可同时有皮下脂肪的坏死。但有时病人的胰腺炎是SLE治疗药物如糖皮质激素和硫唑嘌呤等诱发的。也有部分SLE病人有血清淀粉酶的轻度升高,而临床上无胰腺炎的症状。
八、中枢神经系统表现
神经精神性狼疮(neuropsychiatric systemic lupus erythematousus,NPSLE)近十年来认为SLE者中枢神经系统侵犯较多见,表现为各种各样的神经、精神症状,是SLE病情严重的一种表现,其中精神症状发生率高。早期表现为举止行为模式的细微、难以察觉的改变。Baker(1937年)报道52%SLE患者有精神症状。主要为情绪变化和精神分裂症样。情绪变化轻者为抑郁状态,重者为痴呆。精神症状多变,常为可逆性,经系统治疗能减轻。本病的精神症状必须与应用糖皮质激素后引起的精神症状相鉴别。
神经精神性狼疮系统病理学的异常是多样的,主要表现为缺血、出血、白质损害以及抗体所致的神经细胞损伤。有时临床及解剖学上并无必然的关联,而各不相同的表现可有共同的病因和病理改变。
神经症状主要表现为癫痫样发作,占中枢神经系统SLE的17%~50%,发生在本病活动中或发病前数年。其他表现包括中风、一过性脑缺血。也可表现为脑神经损害,可突然发生,常见为失明、外眼运动异常、视盘变化、单侧眼睑下垂、同侧偏盲等。此外可有偏瘫、痉挛性截瘫、多发性硬化症样临床表现、脊髓炎、脑膜炎等。运动方面的中枢神经损害报道最多的是舞蹈症及小脑共济失调,常见于抗心磷脂抗体阳性的病人;较少见的是周围神经炎。此外,典型偏头痛亦为SLE的症状之一。精神及神经病变可同时存在,其发生可能系脑血管炎所致,已证实有免疫复合物沉积于脑血管。
CT检查发现神经精神性狼疮皮质萎缩发生率为27%~71%。MRI可发现神经精神性狼疮的梗死及灰白质密度增加。PET可发现神经精神性狼疮在氧、葡萄糖摄取和脑血流存在多种局部缺陷。
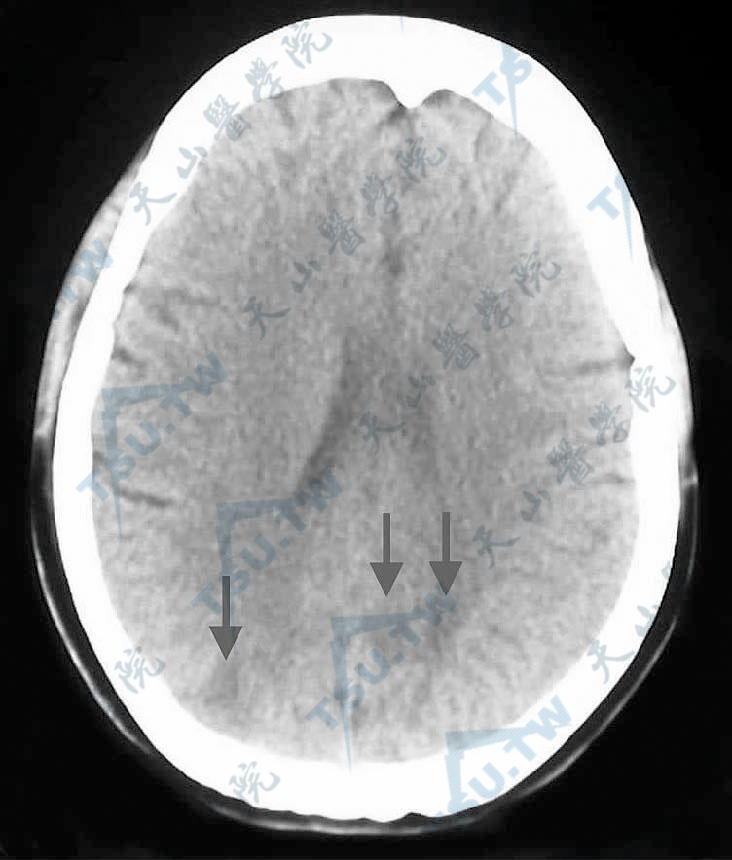
神经精神性狼疮颅脑CT示枕叶皮层及皮层下多发性小片状低密度影(第四军医大学西京医院皮肤科 孙林潮提供)
九、单核巨噬细胞系统表现
约50%SLE患者有局部或全身淋巴结肿大,一般无压痛,质较软。较多见于颈部及腋下。病理检查显示慢性非特异性炎症。脾脏可中等度肿大。
十、眼部病变
约14%SLE患者有视网膜病变。比较具特征性的改变是眼底中心血管附近出现小的、圆或卵圆形白色浑浊物,称丝绵样白斑。此斑不是渗出物,其中可见细胞样体(cytoid body),由肿胀的神经纤维和轴索结构增生及变性所产生。其他有眼底出血、视网膜渗出物、视盘水肿、角膜病变和结膜炎等。
十一、外分泌腺病变
南京医科大学皮肤科统计(1981年)66例LE(55例SLE和11例DLE)有92%发生外分泌腺损害(泪腺、唾液腺损害,发生眼、口干燥症状),病程早期即可检出,部分患者腮腺肿胀、龋齿和口腔干燥三者的变化程度与SLE病情的活动和缓解相一致。
十二、合并症
SLE可与其他自身免疫病或有关病合并,如桥本甲状腺炎、干燥综合征、重症肌无力、原发性胆汁性肝硬化、类天疱疮、疱疹样皮炎、白塞病等。恶性肿瘤发生率亦比正常人高。SLE也可伴发卟啉综合征,现至少已报道24例,原因不明。包括伴发迟发性皮肤卟啉症、急性间歇性卟啉症和变异性卟啉症。SLE与卟啉症同时或相继发病,彼此间隔可长达8年。
十三、实验室检查
(1)贫血:活动性SLE常有正细胞正血色素性贫血,即所谓慢性病贫血。这种贫血在5%的患者可作为首发症状。少数有溶血性贫血,有抗红细胞抗体,约15%患者Coombs直接试验阳性。
(2)白细胞减少:一般低于4×109/L,以淋巴细胞减少为主,在极少的病例白细胞可降至0.5×109/L以下,3/4患者血清中可有补体依赖性抗白细胞抗体,其存在与SLE活动有关,特别是在发热、皮疹、血液系统及中枢神经系统受累时。严重者也可有嗜酸性粒细胞减少或消失等。
(3)血小板减少:可见于25%的患者,可先于SLE表现若干年。也可发生血小板减少性紫癜,有时可检出血小板抗体。
(4)血沉增快:较常见,活动期可明显加快,缓解期恢复正常,但也有临床症状控制后血沉仍不下降者。
(5)血清蛋白:白蛋白降低,球蛋白和总蛋白增加。蛋白电泳显示γ球蛋白明显增高,有时α2球蛋白和纤维蛋白原增多。巨球蛋白亦可增加。约11%的SLE病人可发现有冷凝球蛋白,冷球蛋白血症可比SLE的临床症状早出现许多年。有6%的病人血清中有冷凝集素。约75%患者有高球蛋白血症,IgG及IgM的平均值比正常高而IgA可正常,偶可见IgA减少。有报道患者血中游离免疫球蛋白轻链比正常浓度高,测定尿中游离轻链浓度可判断临床疾病的活动性。约30%患者类风湿因子阳性。约20%患者梅毒血清反应呈假阳性。
(6)抗核抗体:SLE中ANA滴度较高。高滴度ANA(至少>1:64)可以作为诊断SLE的标准之一。随病情稳定、好转而下降,以至阴转,故连续观察滴度变化可作为疗效观察指标之一。临床稳定又出现高滴度ANA时应警惕病情又活动。ANA阴性也不能排除SLE。施守义等(1985年)报道,持续大量蛋白尿病人,血清ANA阳性率显著降低,但可在尿中测出。临床上还有一种抗核抗体阴性的系统性红斑狼疮。有中枢神经系统累及的SLE患者的脑脊液中ANA阳性率可达70%,这有助于SLE与其他脑病的鉴别。
(7)其他自身抗体:SLE相关自身抗体见下表。
SLE相关自身抗体
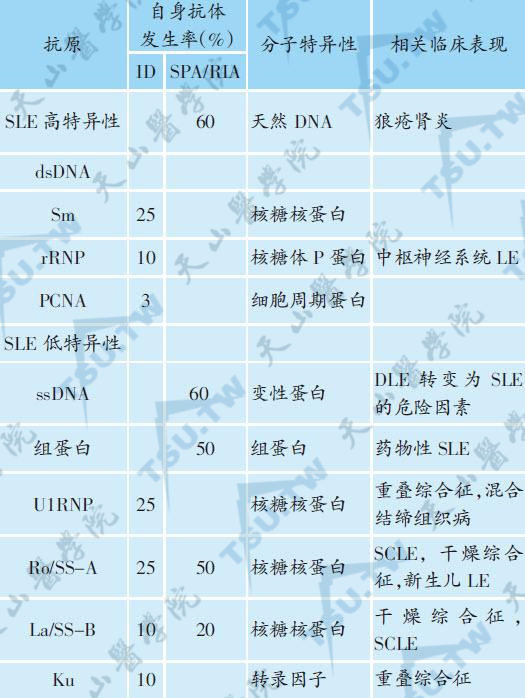
注:ID,免疫扩散;SPA,固相免疫测定(如:ELISA);RIA,放免测定。
抗dsDNA抗体:是SLE特异的自身抗体。活动期病人阳性率高达93%~100%,抗体滴度与疾病活动相关,抗体阳性常伴有肾脏受累。
抗ENA抗体:虽然这类抗原在细胞质内也存在,但仍习惯应用可提取性核抗原(ENA)这个名称。目前用免疫印迹法已可将其分离出20多种不同的抗原成分。对SLE病人主要有:抗Sm抗体,阳性率30%~40%,抗体滴度与疾病活动无关,缓解期病人仍可阳性,有助于SLE回顾性诊断;抗RNP抗体,常与Sm抗体同时存在,阳性率为30%~50%,常伴有雷诺现象;抗Ro/SSA和抗La/SSB抗体,前者阳性率30%~40%,在SCLE和新生儿LE阳性率高,与光敏感有关;后者阳性率10%~20%,与疾病活动无关。
(8)抗心磷脂抗体:SLE病人阳性率30%~44%,该抗体阳性与血小板减少、自发性流产或死胎、血栓形成、血管炎以及神经系统病变有关。
(9)血清补体和循环免疫复合物(CIC)测定:约75%~95%的SLE患者血清总补体值下降。分补体中,C1、C4、C3、C2及C9均下降。下降程度和SLE的活动性一致,特别是狼疮性肾炎患者,因补体参与了抗原抗体复合物反应,在病情急性活动时形成大量可溶性免疫复合物,总补体可明显降低,C3、C4亦降低,尤以C3显著,故测定补体值可作为SLE治疗观察的指标之一。
测定脑脊液中补体有助于判断SLE有无中枢神经系统侵犯。
血清循环免疫复合物测定,活动期增高。
(10)狼疮带试验(lupus band test,LBT):对疑诊LE者进行皮损或“正常”皮肤直接免疫荧光检查称为狼疮带试验。真皮表皮连接处(DEJ)有一局限性免疫球蛋白和补体沉积带,呈黄绿色荧光,则为LBT(+)。皮损处阳性率:SLE92%,DLE为80%~90%。SLE“正常”皮肤阳性率曝光部位为70%,非曝光部位为50%;而DLE“正常”皮肤阴性。较新的红斑水肿性皮损多为颗粒状或细线状,慢性萎缩性或过度角化的皮损呈团块状,而SLE病人“正常”皮肤的LBT则呈点彩状。此免疫荧光带为免疫球蛋白(主要为IgG,亦有IgM、IgA)与补体在真皮表皮连接处沉积所致。
“正常”皮肤LBT假阳性少见。酒渣鼻、药疹、血管炎、多形性日光疹、脂溢性皮炎和面部肉芽肿等的皮损处均可出现假阳性荧光带,多为单一的IgM,荧光一般较弱。活检时,“正常”皮肤曝光部位一般选择前臂伸侧,非曝光部位选择臀部、肩背部或前臂屈侧皮肤。
临床意义:
- LBT特异性高,有助于LE的诊断及鉴别。
- “正常”皮肤LBT(+)高度提示SLE,有助于与DLE鉴别和确诊无皮损的SLE,特别是无肾外症状的LE肾炎。
- “正常”曝光部位皮肤LBT中Ig类别和荧光强度与疾病活动性、肾病的发生和判断预后有关联,例如IgA沉着意味病变活动,单有IgG沉积或合并有任何其他Ig比单有IgM沉积意味疾病活动性明显,肾病更重,死亡率也较高。非曝光部“正常”皮肤LBT(+)显示病情比较严重。
- 有些作者认为LBT与SLE病情变化一致,在治疗中随病情缓解而消失(一般需时6个月),可作为判断疗效的指标之一。
十四、预后
SLE是比较慢性的疾病,经过多变,缓解和活动期往往交替发生。可自然缓解,有时持续10~30年。仅少数暴发性病例迅速致死。近20余年来由于诊断技术的进步,治疗方法的进展,预后大为改善。有作者采用寿命表法研究存活情况:总的预后良好,确诊后,5年生存率为97%,10年为90%,15年为84%。
一般肾和中枢神经系统病变严重时预后差,其次为心脏病变。侵犯单一器官(如关节、肝、肺)者预后较好,某些患者长期未积极治疗,病情也并不严重,而且不丧失劳动力。也有认为有DLE皮损的女性SLE及有雷诺现象的SLE预后比较良好。男性发病率虽低于女性,但男性病人更易发展为肾衰竭,预后比女性病人差。
SLE的死亡原因首先为进行性肾衰竭,其次为中枢神经系统血管炎产生的癫痫、昏迷、精神病及麻痹,其他为心肺功能衰竭、感染、糖皮质激素的副作用等。
十五、妊娠和SLE
多数报道认为活动期患者妊娠、分娩可使症状加剧,应避免妊娠。一般认为无严重心、肾受累的女性患者缓解期泼尼松日量少于15mg时可以妊娠,但早产率比正常人群高2倍,死胎率也增加。LE患者怀孕时约半数病例病情不变、33%缓解、17%恶化。病情加重一般均发生在妊娠后期或产后。SLE患者妊娠对患者本人的影响,一是自发性流产危险性增加,特别是抗心磷脂抗体阳性者,大剂量泼尼松联合小剂量阿司匹林治疗可有效防止流产;二是可能引发病情恶化,应密切观察病情,经常进行临床及实验室指标检查,妊娠期间应停用非甾类抗炎药、抗疟药和免疫抑制剂,分娩期间,应静脉使用糖皮质激素。糖皮质激素治疗对胎儿是安全的。可的松、泼尼松、泼尼松龙、甲泼尼龙、倍他米松、地塞米松均可透过胎盘,糖皮质激素诱发胎儿异常的报道少见,对实验兔、鼠可致腭裂,人类中无报道。偶有报道出生低体重儿,但认为胎儿宫内生长迟缓可能为狼疮本身引起。由于胎盘氧化酶即11-羟基脱氢酶可灭活可的松、泼尼松、泼尼松龙,对倍他米松、地塞米松无作用,泼尼松口服后胎儿脐血中浓度为母体的10%,甲基泼尼松龙为18%~45%,倍他米松为33%,地塞米松为100%。因此治疗母体疾病宜选用泼尼松,治疗胎儿疾病宜选用地塞米松。同时,产后6周内应密切观察,注意疾病暴发。对未经治疗的活动性患者发生妊娠,应该在进行治疗性流产前用大量糖皮质激素控制病情。SLE母亲的ANA可通过胎盘传给胎儿,应注意新生儿红斑狼疮的发生,一般发生在母亲Ro/SSA抗体阳性者,即使母亲没有临床症状也应引起重视。
抗核抗体阴性的系统性红斑狼疮
抗核抗体阴性的系统性红斑狼疮(ANA negative systemic lupus erythematosus)一般认为ANA阳性对诊断SLE具有重要价值,但少部分病人符合SLE的诊断标准,而ANA却持续阴性。这组病人被称为ANA阴性的SLE,为SLE的一个亚型。但是大约60%的此型病人可测出Ro/SSA抗体,因此Ro/SSA抗体是诊断此型SLE的重要依据。本型SLE约占全部SLE患者的2%,女性多见,发病年龄多数为21~40岁。
临床上有明显的皮肤表现,91%有无瘢痕性颧部皮疹,79%有光敏性皮炎,雷诺现象、脱发和口腔溃疡发生率也较高。
其他器官很少受累,或被累及但不严重,多数病人可有非特异性全身症状,如发热、无力、疲劳及关节痛。因皮肤外受累较少,预后较好。
组织病理
不同的LE的组织病理变化不同,SLE与DLE皮损的组织病理改变没有本质的区别,仅仅是数量上或程度上的差异。
DLE的组织病理学变化主要表现为:角化过度,毛囊口及汗孔有角栓,颗粒层增厚,棘层萎缩,表皮突变平,灶性基底细胞液化变性,PAS染色能见基底膜增厚,真皮上部水肿,血管扩张及轻度红细胞外渗,尤以红斑水肿性皮损为明显。由于基底细胞液化变性可见色素失禁。在真皮血管和皮肤附件周围有淋巴细胞为主的灶性浸润。
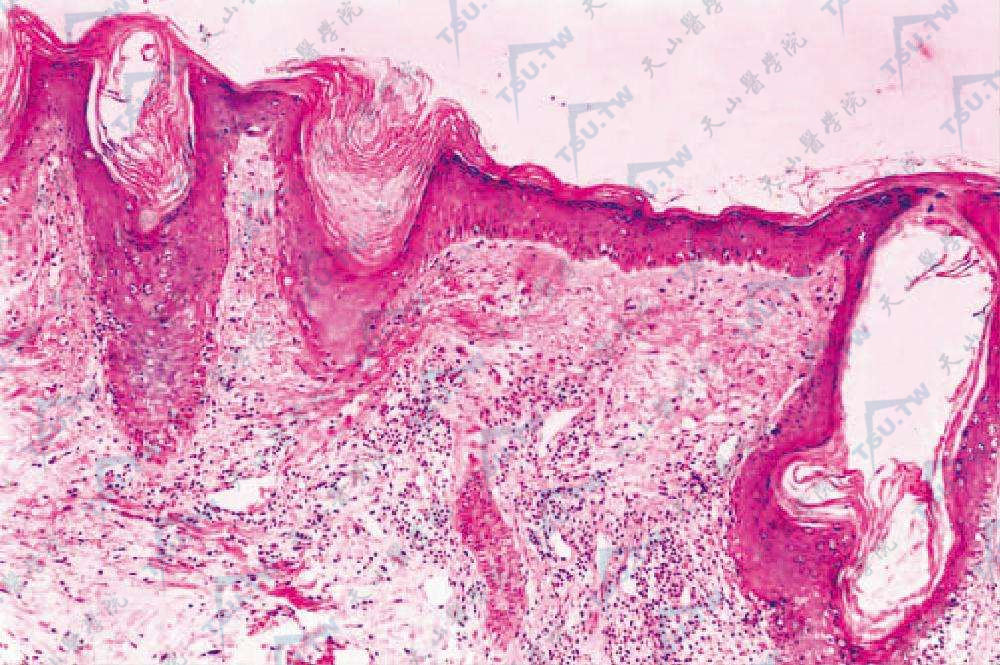
DLE组织病理毛囊角栓,表皮萎缩,血管周围淋巴细胞浸润(HE染色×100)
SCLE的皮肤组织病理与DLE相近,基底细胞层液化变性及真皮和附件周围有淋巴和单核细胞浸润,但炎症浸润比DLE轻。
肿胀性红斑狼疮的组织病理可见真皮处大量黏蛋白沉积,而DLE的组织学改变不明显。
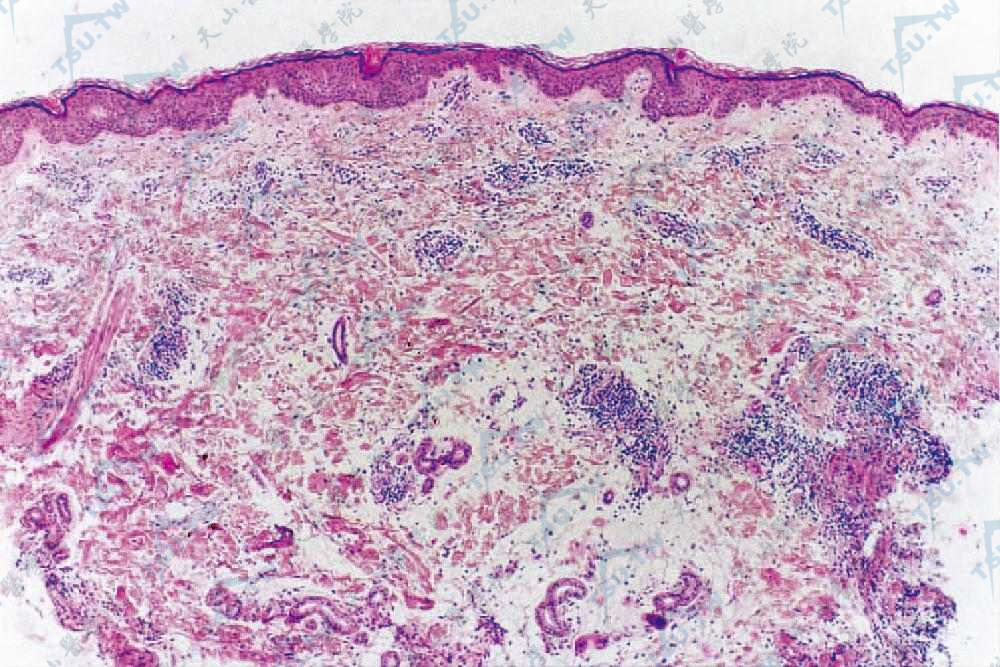
肿胀性红斑狼疮 真皮浅、深层和附属器周围有中等量淋巴细胞、组织细胞浸润(HE染色×40)(北京协和医院 马东来提供)
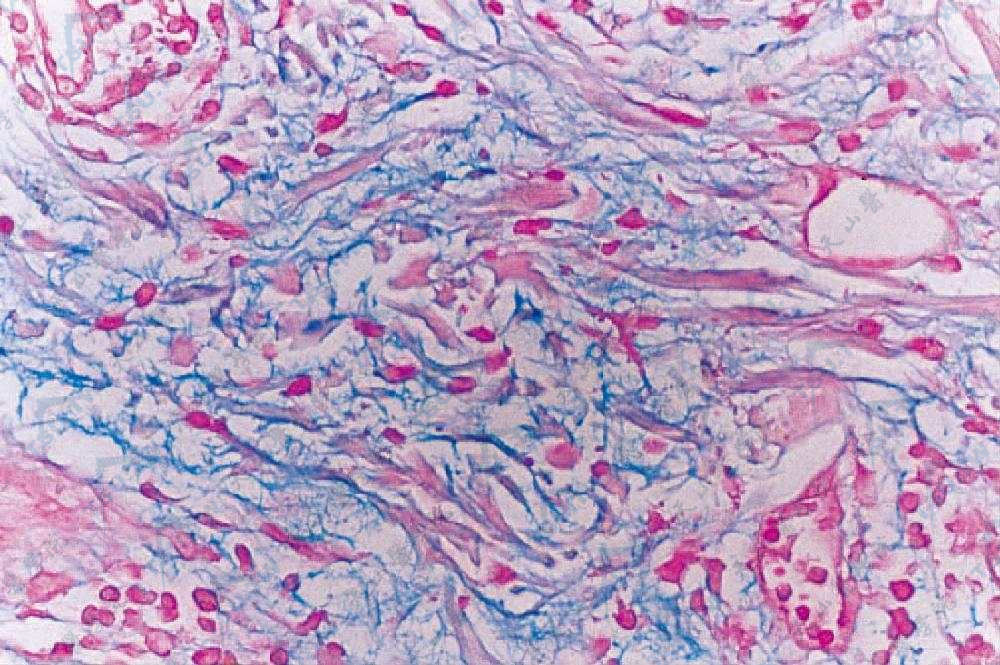
肿胀性红斑狼疮 胶原纤维束间黏蛋白沉积(HE染色×400)(北京协和医院 马东来提供)
SLE早期红斑水肿性皮损组织学变化可以很轻微且不具特征性,有时基底细胞只见空泡变,有时表皮萎缩更明显,有时可见基底细胞液化及真皮乳头层水肿。有时在皮肤结缔组织、真皮毛细血管壁及表皮下基底膜带见纤维蛋白样沉积物,呈深嗜伊红染色。
SLE内脏器官主要病理组织学特征为纤维蛋白样坏死,侵及毛细血管、微小动脉、间质结缔组织及浆膜、关节囊。免疫荧光检查纤维蛋白样坏死处可见大量免疫球蛋白、补体及纤维蛋白原沉着。具诊断意义的另一表现为苏木素小体(haematoxylin body),其变化与LE细胞相似。肾脏损害典型表现为毛细血管袢基膜嗜酸性增厚,即所谓“铁丝圈”变化。
中枢神经系统主要为小血管的破坏或增生和淋巴细胞等浸润,有广泛的微血栓和局限性软化灶等。
心包膜有纤维蛋白样物质沉着。心肌炎时小动脉壁局灶性纤维蛋白样变性。典型的心内膜炎为心瓣膜赘生物,即所谓“Libman Sacks心内膜炎”。
脾脏的特征性变化为小动脉周围纤维化呈洋葱皮样表现。肺部初起为血管炎和血管周围炎,以后波及间质和实质,为间质组织、肺泡壁、毛细血管的纤维蛋白样变性、坏死和透明性变,伴淋巴细胞及浆细胞浸润。
诊断及鉴别
DLE的诊断主要根据皮疹特点及皮肤病理检查。有条件可作免疫荧光带试验以助确诊。
SLE的诊断主要根据病史、临床表现及实验室检查三方面综合确定。目前一般采用美国风湿病学会1982年修订的SLE诊断标准。患者具有11项标准中4项或更多项、相继或同时出现,即可诊断为SLE。但本病需与皮肌炎、硬皮病、风湿热和类风湿关节炎等鉴别。
SLE诊断标准

*此项于1992年修订。
预防及治疗
一般治疗
- 应该树立和疾病作斗争的坚强信心。近年来由于糖皮质激素、免疫抑制剂的应用及中西医结合等治疗成果,SLE预后已有明显改善。
- 避免日晒,对日光敏感者尤应注意。外出应该使用防光剂、撑伞或戴宽边帽,穿浅色长袖上衣和长裤。忌用有光敏作用的药物,如酚噻嗪、氢氯噻嗪、磺胺类药和灰黄霉素等。
- 避免过劳,急性或活动期SLE应卧床休息。避免妊娠,也不宜服用避孕药,有肾功能损害或多系统损害者避孕失败宜早作治疗性流产。
- 避免受凉、感冒或其他感染。
- 增强机体抵抗力,注意营养及维生素补充。
皮肤红斑狼疮的治疗
一、系统治疗
- 抗疟药:如羟氯喹每日0.2~0.4g,病情好转后减为半量。有时每周0.2g即可控制病情,疗程视病人耐受情况和病情而定,一般总疗程为2~3年。由于羟氯喹能缓慢地在体内许多组织积储,特别是视网膜的色素上皮细胞,引起视网膜病,开始用药后6个月应作一次眼底检查,以后每3个月复查一次。
- 沙利度胺(酞咪哌啶酮,反应停):可试用,初量200mg/d,分两次口服。出现疗效后减为每日100mg维持,并继续治疗3~5个月,在大多数患者有效,但停药易复发。
- 氯法齐明(clofazimine):每日100mg。不良反应为皮肤红染。
- 泛发病例可以口服小量糖皮质激素。
二、局部治疗
外用糖皮质激素软膏,每天2次,或封包。或皮损内注射糖皮质激素,如曲安萘德(triamcinolone aeetonide)、醋酸氢化可的松混悬液等,1~2周注射1次。
系统性红斑狼疮的治疗
系统性红斑狼疮(SLE)治疗的个性化十分重要,在SLE病人开始治疗以前,必须对SLE病人病情的活动性进行评估,如抗核抗体、抗DNA抗体和低补体血症,及脏器受损程度,如肾、心、肺病变,皮肤和浆膜炎等作出正确的评价,对于制定适当的治疗方案、观察疗效和随后连续地判断治疗的成败是十分重要的。评估SLE活动性有多种指标,目前多采用“系统性红斑狼疮活动指数”(systemic lupus erythem-atosus disease activity index,SLEDAI),SLEDAI由多伦多大学的临床医师提出,以24种临床表现按其严重性依次排列评分(下表),以病人在评价时10天前的临床表现为评价依据,建议SLEDAI>12分时,可用原双倍的糖皮质激素的剂量治疗,或需住院。
SLEDAI积分表

引自:Bombardier C,Gladman DD,Urowitz MB et al,Derivation of the SLEDAI,A disease activity index for lupus patients.The Committee on Progenosis Studies in SLE.Arthritis Rheum 1992; 35:630-640
一、非甾体类抗炎药
单独用于轻型病例,如仅有皮疹、低热或关节症状者,或与糖皮质激素并用,以尽量减少糖皮质激素的用量。有时能迅速缓解发热及肌肉、关节疼痛等症状,或用于糖皮质激素已经减量,而仍有关节痛等症状,或用于糖皮质激素已经减量,而关节痛加剧时。
一般应用水杨酸盐制剂如阿司匹林每日3g;吲哚美辛25mg,每日3次或布洛芬1片,每日2次口服。因为此类药物对前列腺素的抑制作用,造成血清肌酐清除率减少,使用后可能导致病人血清肌酐升高,应及时减量或停用,对有肾脏累及的病人尤应慎用。注意不宜采用多种非甾体类抗炎药联合治疗。
二、糖皮质激素
是现有治疗SLE最重要的药物,剂量视病情轻重而异。
推荐剂量:轻型病例泼尼松(或相当的药物)每日<0.5mg/kg,一般为20~40mg/d;病情中等者每日1.0mg/kg,一般为每日60~80mg;理想的给药方法是早晨8点一次顿服,这样可以减少对脑垂体肾上腺轴的抑制,病情得不到控制时,可将剂量分为每天2~3次口服。
病情重者用大剂量,必要时用氢化可的松或地塞米松静脉滴注,每日相当泼尼松2~3mg/kg,一般为100~200mg/d;对弥漫增殖性狼疮性肾炎,神经精神性狼疮,重症溶血性贫血以及血小板减少等症状迅速恶化病例可应用大剂量甲泼尼龙静脉冲击疗法,剂量为每天1g(或15mg/kg)琥珀酸钠甲基泼尼松龙静脉注射(应在30分钟内注射完毕),连续使用3天,然后迅速减至常规剂量或用3mg/kg,维持2~3天。糖皮质激素治疗中应注意:
- 治疗原则:早期、足量和持续用药。病情越是危重者,最初用量越要大,以迅速控制病情,抢救生命,避免重要器官受损伤或发生不可逆损害,如不规则服药或突然停药可影响病程和预后。若糖皮质激素初量足够,则在1~2天内退热,关节痛消失及一些急性活动症状得到良好控制,一般情况好转。若2天内上述症状不好转,应立即将原剂量再增加25%~50%。一般经2~3周病情得到最大限度控制后,逐渐减量,开始时每周减泼尼松10mg或相当剂量其他制剂,同时密切注意疾病活动情况,当减至30mg/d时,递减应更缓慢,每周减2.5~5mg。如有活动倾向应立即在先前剂量上增加5~10mg/d。最低维持量病人间差异较大,一般为泼尼松每日7.5~20mg。也有在泼尼松剂量减至30mg/d时,采用每周隔日减少5mg的方法,直到病人每隔一天早晨服泼尼松30mg维持。糖皮质激素治疗后,最快消失的症状是发热、关节痛和浆膜炎等。LE细胞、皮疹消失和心、肾及神经、精神损害恢复较慢。
- 预防和及时处理糖皮质激素的副作用:当患者遇应激情况,如手术、感染、精神创伤时,必须加大剂量,直至应激过去,以免发生急性肾上腺皮质功能不足。对感染应积极控制。
- 观察疗效:糖皮质激素减量指标主要根据临床症状的改善和有关实验室指标。ANA和dsDNA抗体滴度与病情活动常平行,血清补体主要是C3、C4与疾病活动有重要联系。与病情活动有关的实验室指标还有血沉、血清白蛋白、球蛋白和血、尿常规等。
三、抗疟药
氯喹或羟氯喹有抗光敏和稳定溶酶体膜的作用,对控制皮损和轻度关节症状十分有效,用于病情较轻及皮肤损害明显者,糖皮质激素减量过程中也可加用,剂量、疗程和注意事项如前述。
四、免疫抑制剂
具有抗炎和免疫抑制作用,常用硫唑嘌呤和环磷酰胺(CTX)。环磷酰胺可每日1~4mg/kg,分次口服,但采用静脉冲击治疗则副作用更小,目前CTX已常用于中、大剂量糖皮质激素不能控制的狼疮性肾炎和神经精神性狼疮,方法为:每月静脉滴注1次,0.5~0.75g/m2体表面积,要求60分钟内注射完毕,随后24小时内多饮水,诱导迅速利尿。根据病情可重复6次,以后可改为每3个月1次。硫唑嘌呤剂量为每日1~2.5mg/kg。亦可应用苯丁酸氮芥等。上述各种免疫抑制剂主要在下列情况下采用:单独使用糖皮质激素无效者;对长期大剂量糖皮质激素治疗不能耐受者:为了更有效地控制SLE中的某些器官损害;在急性症状得到控制后,为了进一步减少糖皮质激素维持量,或更顺利地逐渐递减糖皮质激素。免疫抑制剂可以与糖皮质激素联合使用。
环孢素A(cyclosporin A,CyA)是一种化学合成的新一代免疫抑制剂,无明显细胞毒性,对吞噬细胞的移动作用无明显影响,故不增加感染的危险性,对Th淋巴细胞有选择性的抑制作用。在SLE治疗中,可作为第二线的免疫抑制药物,一般采用较小剂量,3~5mg/d,使用中注意病人的血清肌酐和血压。如病人的血清肌酐水平较治疗开始前升高50%,则应减量或停药。
吗替麦考酚酯(mycophenolate mofetil)是一种新型的免疫抑制剂也可用于狼疮性肾病的治疗,常用剂量:1.5g/d,分两次空腹服用,3个月后减量至1g/d维持6个月。
来氟米特(leflunomide)是一种具有抗增生活性的异恶唑类抑制剂,其作用机制主要是通过抑制二氢乳清酸脱氢酸及酪氨酸激酶减少嘧啶的形成,致使DNA合成障碍,进而抑制淋巴细胞活化及由此而致的免疫反应。该药主要抑制淋巴细胞的增殖,而对白细胞及血小板的影响较小。与环磷酰胺、环孢素A等免疫抑制剂相比,来氟米特的不良反应较少,且严重不良反应少,一般不出现肺间质纤维化。可用于狼疮性肾病的治疗,常用剂量为20mg/d。
狼疮性肾炎的治疗:轻型或局灶增殖性者,一般仅需要中小剂量糖皮质激素;若病变活动,发展较快,可使用中等到大剂量;对肾功能减退型、膜性和弥漫增殖性以糖皮质激素与免疫抑制剂合用为佳;对高度活动的进展肾炎使用大剂量冲击疗法;此外,弥漫增殖性狼疮性肾炎尚需根据病变属活动阶段或硬化阶段而有所选择,活动阶段早期使用大剂量糖皮质激素,并用免疫抑制剂或氯喹类药物,硬化期患者糖皮质激素和免疫抑制剂一般无效,晚期肾衰竭可作血液透析和肾移植。
五、雷公藤
雷公藤具有较强的抗炎症和免疫抑制等作用,适用于轻、中度病情的SLE病人,疗效确实。秦万章等(1982年)报道治疗103例SLE,有效率达91.2%,临床表现、免疫指标均有改善。南京医科大学皮肤科资料(1984年),雷公藤单独用于轻~中等严重度的SLE,显效、好转、无效病例各占1/3。用量:福建产雷公藤生药(去皮的干根)每日20~40g,煎汁分两次服或制成糖浆等剂型;雷公藤多苷片每日1~1.5mg/kg(一般每日量60mg),分三次食后服。重症病人须合用糖皮质激素治疗。
雷公藤有一定的毒副作用。该药对生殖系统有影响,育龄妇女服用后可出现月经紊乱,甚至闭经;该药可以使男性精子生成受阻,影响精子发育,导致不育,故未生育的患者应慎用。哺乳期妇女服用雷公藤后能通过乳汁影响婴儿,亦应禁忌使用。此外雷公藤的副作用还有刺激胃黏膜引起恶心,呕吐,腹痛,腹泻等胃肠道不良反应;肝损害,血中ALT升高;抑制骨髓造血,使白细胞、血小板减少,使机体易发生感染,严重时可诱发再生障碍性贫血;还可出现心律失常,心电图改变等。约有40%患者服用雷公藤后可有皮肤色素改变,皮疹、疱疹、口腔溃疡等皮肤黏膜反应,停药后可逐渐缓解,故在服药期间要定期查血尿常规,肝肾功能,随时调整用药。
六、免疫调节剂
根据SLE的发病机制与T抑制细胞功能损伤,细胞免疫功能低下有密切关系,近年来也配合采用:胸腺素5~25mg,肌内注射,每日1次,2周后,隔日或每周2次,连用数月;转移因子2mL,上臂内侧皮下注射,每周1~2次,一疗程3个月;中药黄芪等。
七、血浆置换疗法
一般应用于糖皮质激素治疗效果差的进行性多脏器损害者、器质性脑病综合征、全血细胞减少及活动性肾炎等重症病例。
八、静脉注射丙种球蛋白
注射丙种球蛋白制剂保留了IgG分子的完整性,而无抗补体活性,既可增加病人对各种微生物感染的抵抗力,又可直接阻断单核巨噬细胞的Fc受体,作为免疫调节剂有类激素样作用,可用于自身免疫性疾病的治疗。对于有溶血性贫血或血小板减少症的患者及用糖皮质激素治疗疗效不满意的SLE病人可考虑使用。剂量为每日400mg/kg,连用5天,以后每三周用一个单剂。
九、精神症状的对症治疗
除了糖皮质激素和(或)免疫抑制剂外,对症治疗是处理神经精神性狼疮患者的常用措施。精神异常可以单独使用精神药物,如氯丙嗪。认知功能不全可试用去氢表雄酮(DHEA),癫痫发作的病人在抗癫痫疗效欠佳时,可考虑加用激素和(或)免疫抑制剂。舞蹈病可采用甾类药物、氟哌啶醇、抗血小板聚集药、抗凝药或联合治疗。头痛和偏头痛的病人可给予大剂量镇痛剂、三环类抗抑郁药、β受体阻滞剂、钙通道阻滞剂或新型抗惊厥药。有时激素在控制狼疮患者的头痛方面可能比传统的抗偏头痛治疗更有效。
抗凝治疗是神经精神性狼疮治疗措施的一个重要进展。合并抗磷脂综合征、缺血性中风、一过性黑矇和脑静脉血栓、舞蹈病、认知功能不全、头痛、横断脊髓炎和癫痫发作显著相关。阿司匹林70~100mg/d作为首选。发生过血栓事件的患者可用华法林长期抗凝使国际标准化比率(INR)≥3,是抗栓、预防复发最有效的治疗。急性期需要肝素治疗。
中医疗法
慢性盘状红斑狼疮一般多属气滞血淤所致,故治以活血化淤、疏肝理气为主,可用柴胡疏肝饮或通窍活血汤加减。
系统性红斑狼疮在急性发作期,除见红斑、紫癜外,并伴高热、关节疼痛、烦热不眠、舌红或绛、脉数,以清热解毒,凉血养阴为治则,以犀角地黄汤或化斑汤加减;若病情转入缓解,有长期持续低热、面颧潮红、手足心烫、腰膝酸软、口干咽燥等阴虚内热之证者,则予以滋肾养阴、凉血清热,常服知柏地黄丸、六味地黄丸、大补阴丸、二至丸等;待急性症状消退,出现脾肾两虚证者,如面浮肢肿、腰酸背痛、四肢无力、肢端发凉、食纳呆滞等证,则以健脾益肾,济生肾气丸加减。
