-
细菌药敏与临床药效不符的常见原因是什么?
答:主要有如下几个方面:①体外药敏试验和体内药物疗效确实有差异,主要是因为体外和体内的环境不同,有些细菌可以利用体内的一些物质生成抵抗抗菌药的成分,使抗菌药失效,导致出现体
1 -
今后改善真菌药敏试验的方向是什么?
答:①规范操作现有的药敏试验,做好质量控制;②建立对卡泊芬净等新药的体内和体外相关性好的药敏试验方法;③建立不产孢丝状真菌的体外药敏试验的方法;④提高现有真菌药敏试验的可
2 -
为什么真菌药敏试验会出现重复性较差的现象?
答:重复性差常发生在三唑类抗真菌药物,其原因是判断终点会产生拖尾现象,终点的判断可以是被测试真菌完全被抑制,也可以80%被抑制,由此可产生重复性差的现象。
3 -
为什么测定抗真菌药对受试真菌最低抑菌浓度对临床医生的帮助更大?
为什么测定抗真菌药对受试真菌的最低抑菌浓度(MIC)对临床医生的帮助更大?答:文献报道剂量(DOSE)/MIC比值与疗效的关系对临床更有指导价值。当DOS/MIC比值超过25以上时,治疗成功率在
4 -
为什么在真菌治疗中存在“90/60”现象?
答:①真菌药敏试验与疗效的相关性存在难以明确的原因,如体外试验结果存在局限性,耐药株少见,缺少理想的动物模型,缺少记录完整的病例;②抗真菌药物的疗效受多种因素的影响:如不同组
5 -
新型抗真菌药物伏立康唑和卡泊芬净、体外药敏结果与体内疗效一致性如何?
答:新型抗真菌药物伏立康唑参照M27-A的方法作酵母样菌的药敏试验,与临床有较好的相关性,结果可靠,重复性好。但卡泊芬净用M27-A方案测定酵母样菌药敏试验和用M38-A方法做产孢丝
7 -
氟胞嘧啶药敏结果如何应用于临床治疗?
答:氟胞嘧啶治疗念珠菌属主张联合用药,单独用药很快产生耐药性,所以CLSI推荐的判断标准也是针对联合治疗的,如氟胞嘧啶药敏结果为敏感(S)时提示的是其与其他药物联合用药所能获得
8 -
如何评价两性霉素B药敏试验结果和临床疗效的关系?
答:两性霉素B的抗真菌谱可覆盖酵母样真菌、曲霉菌和毛霉菌,虽然CLSI没有明确规定判断标准,但认为当MIC > 2mg/L时应报告耐药。对念珠菌属通常认为MIC >= 0.25即代表是耐药菌株
9 -
伊曲康唑药敏结果对临床治疗的参考价值是什么?
答:当前伊曲康唑药敏判断标准是基于黏膜念珠菌感染制定的,伊曲康唑的血药浓度和组织浓度差异大,各组织间药物能达到的浓度也各不相同,在同样的治疗条件下,脂肪中的药物浓度高于血
10 -
做E-test测定时注意事项有哪些?
答:①注意E-test条必须在有效期范围内;②贴于琼脂表面时,一定要注意有刻度的一面要朝上;③试剂条一旦贴于琼脂表面即不可随意移动,因为E-test条中的抗菌药会在贴于琼脂的瞬间释放
12 -
如何保存E-test条?
答:保存方法与抗菌药纸片相同。未开封的E-test条可长时间保存于−40℃环境中;已开封但尚未用完的E-test条必须密封后保存于−40℃或4℃冰箱中。使用前必须待试剂条
13 -
E-test有哪些优缺点?
答:本法可用于营养要求较高、生长缓慢或需特殊培养条件的病原菌的药敏试验,如流感嗜血杆菌、肺炎链球菌、淋病奈瑟菌、空肠弯曲菌和厌氧菌等,具有操作简单、结果容易判断等特点
14 -
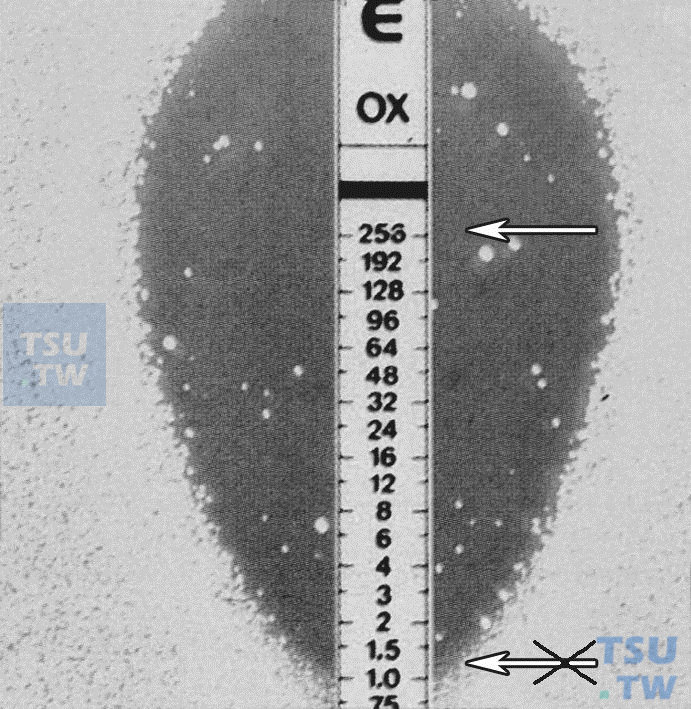
抑菌圈内出现散在菌落时如何阅读结果?
答:抑菌圈内出现散在菌落是由低水平耐药突变引起的,阅读时要注意。如下图所示,其MIC > 256µg/ml。抑菌圈内出现散在菌落时E-test结果的阅读
15 -
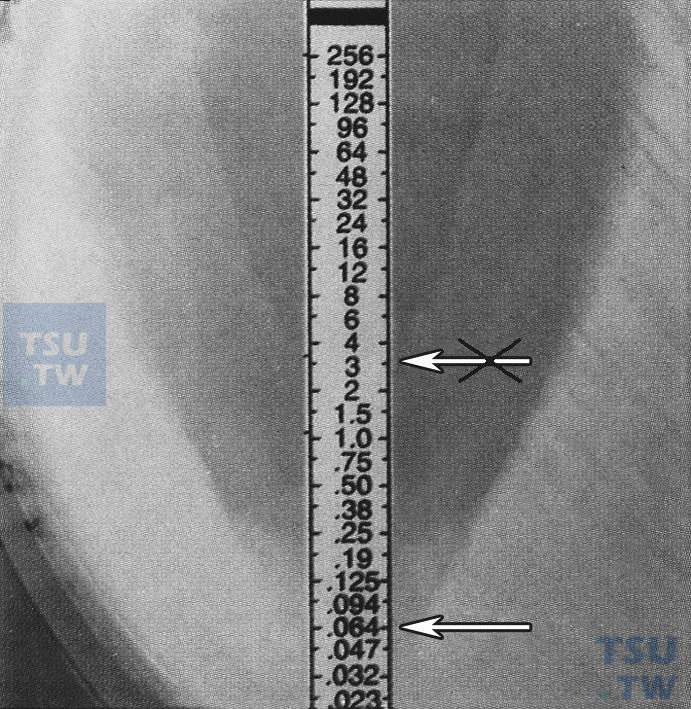
如何正确阅读溶血链球菌的E-test结果?
答:忽略溶血链球菌的溶血圈,读取生长完全被抑制处的MIC值,如下图所示,MIC = 0.032µg/ml。溶血性链球菌E-test结果阅读
17 -
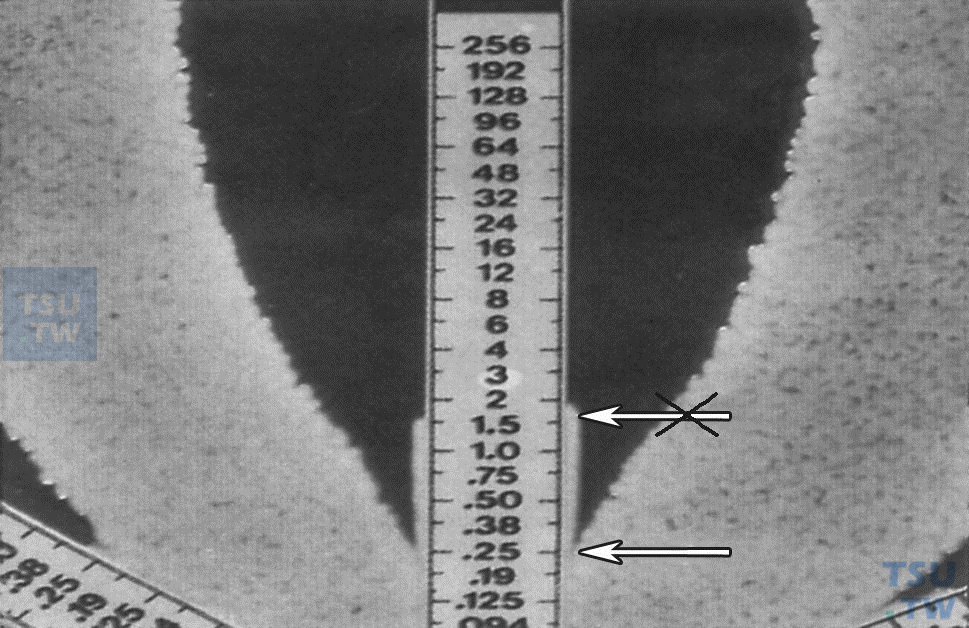
E-test试验结果试剂条边缘有细菌生长时应如何阅读?
答:忽略试剂条周边的薄线生长,它常为细菌沿水渠生长的结果,如下图所示,MIC = 0.25µg/ml。试剂条边缘有细菌生长时E-test结果阅读
18 -
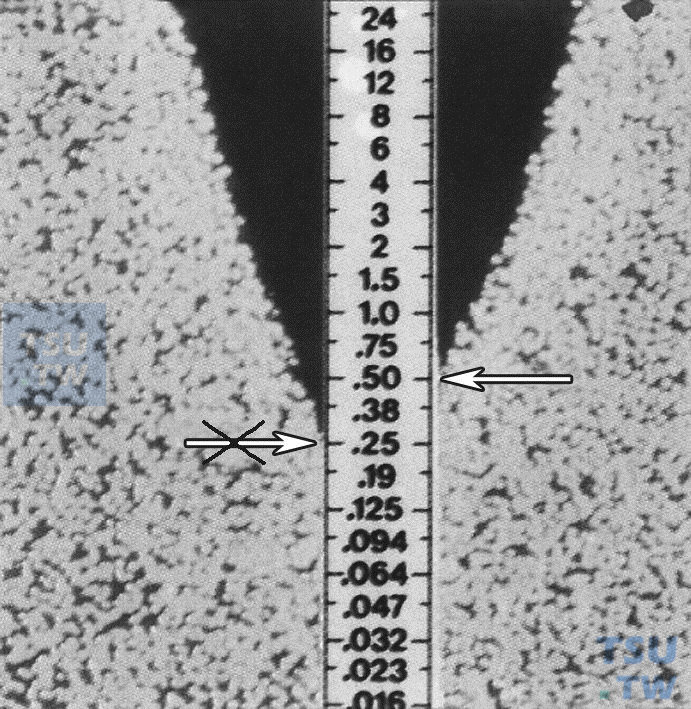
E-test试验结果试剂条两边抑菌圈高度不等时应如何阅读?
答:试剂条两边产生不同的交界点,读取较高数值侧的MIC,下图所示,MIC = 0.5µg/ml。如果两侧差> 1个稀释度,须重复试验。试剂条两边抑菌圈高度不等时E-test结果阅读
19