-
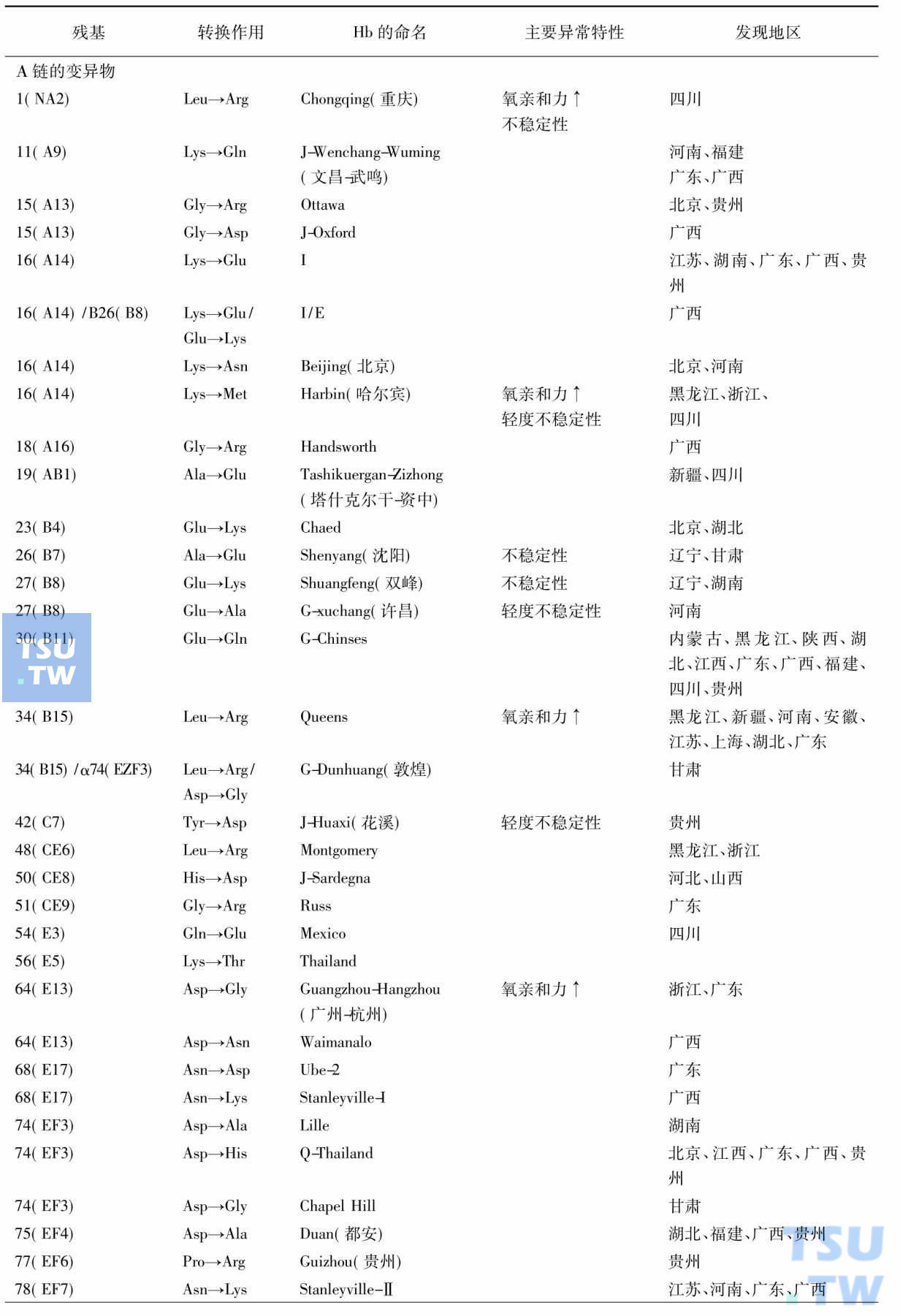
认识异常血红蛋白、血红蛋白
近年对血红蛋白的生物合成,遗传控制,结构与功能关系、珠蛋白基因缺陷与缺失等已有了深刻了解,血红蛋白病(异常Hb病、地中海贫血)导致常见的遗传病。到2001年2月底,全世界已报道的
1 -
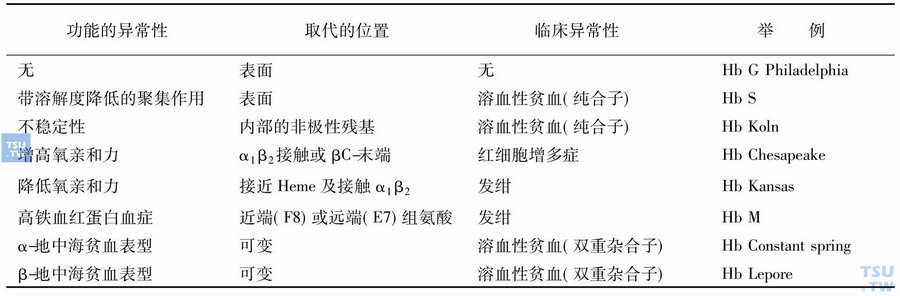
血红蛋白的功能变化
根据Perutz血红蛋白四级结构模型,氨基酸变异发生在不同的部位,对其功能的影响是不相同的。一般来说,如果氨基酸的替代或改变发生在分子的内部,则对血红蛋白的功能影响比较严重,临
3 -
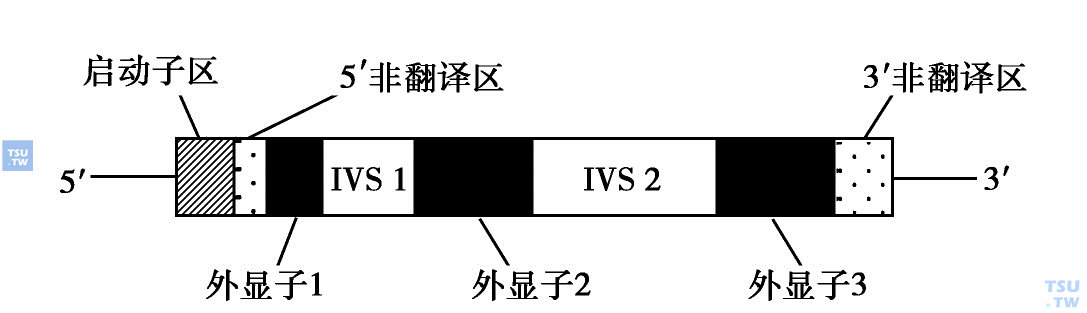
珠蛋白基因的组成与结构
珠蛋白基因呈簇状分布,α-及α-类基因定位于第16号染色体的短臂,而β-及β-类基因定位于第11号染色体的短臂。α-类基因簇总长超过40kb,而β-类基
4 -
异常血红蛋白的遗传基础
点突变点突变(point mutations)。目前发现的异常Hb中绝大多数属于肽链上单个氨基酸替代,其相应密码子发生单个碱基替代。如HbS的β-链第6位谷氨酸被缬氨酸替代。(β6谷&
5 -
血红蛋白的变异:遗传模式
异常β-链变异物的全部基因是等位基因,即占有同一基因座的基因。而且该基因产生β-地中海贫血及遗传性持续性血红蛋白F(hereditary persistence of hemoglobin F)是带
6 -
与不同遗传结合作用相关的血红蛋白型
β-链变异物(beta chian variants)已叙述过的纯合子状态Hbs S、C、D Punjab、E及O Arab及一些变异物,未并发任何临床的与血液学的异常性。这种变异物的Hb中包含主要的血红
7 -
异常血红蛋白的病理生理学
Perutz及其同事构建了血红蛋白分子的三维结构模型,使人们可以观察到氨基酸取代作用对分子功能的影响。Perutz的模式表明,通过范德华型非极性相互作用,无水的分子核心是稳定的。
8 -
异常血红蛋白的实验室诊断方法
电泳(eletrophoresis)血红蛋白电泳是检测和鉴定异常血红蛋白最主要、最常用的实验室方法。由于该方法是按照电荷的多少来分离蛋白质,故其不能鉴别那些未引起电荷变化的氨基酸取
9 -
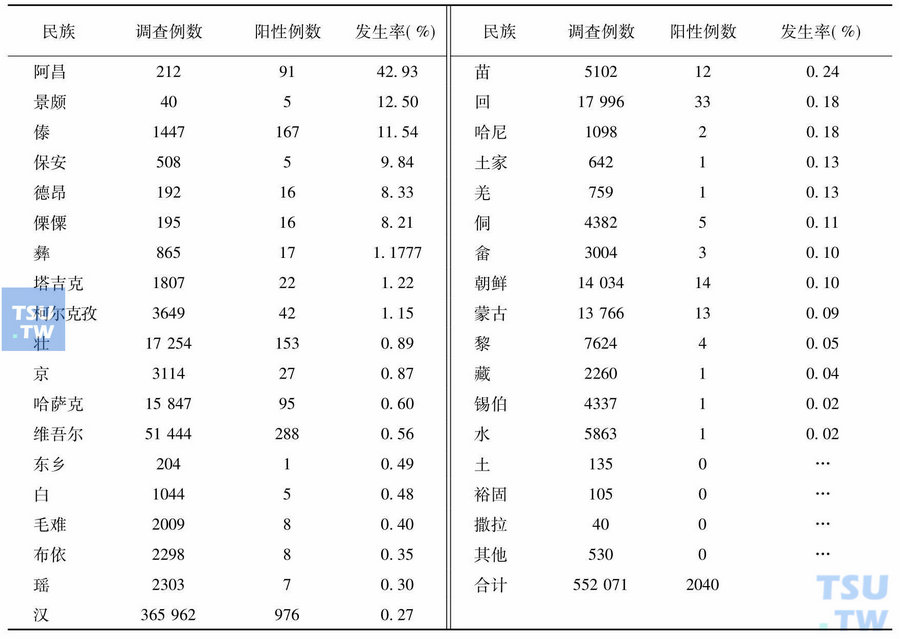
我国异常血红蛋白的研究
在工业化与发展中国家,已经对异常血红蛋白进行了研究。但1983年联合国(WHO)备忘录中,并未包括中国研究出来的有关结果。早在1960年,中国内地就开始了大量的异常Hb普查工作;我国台
10 -
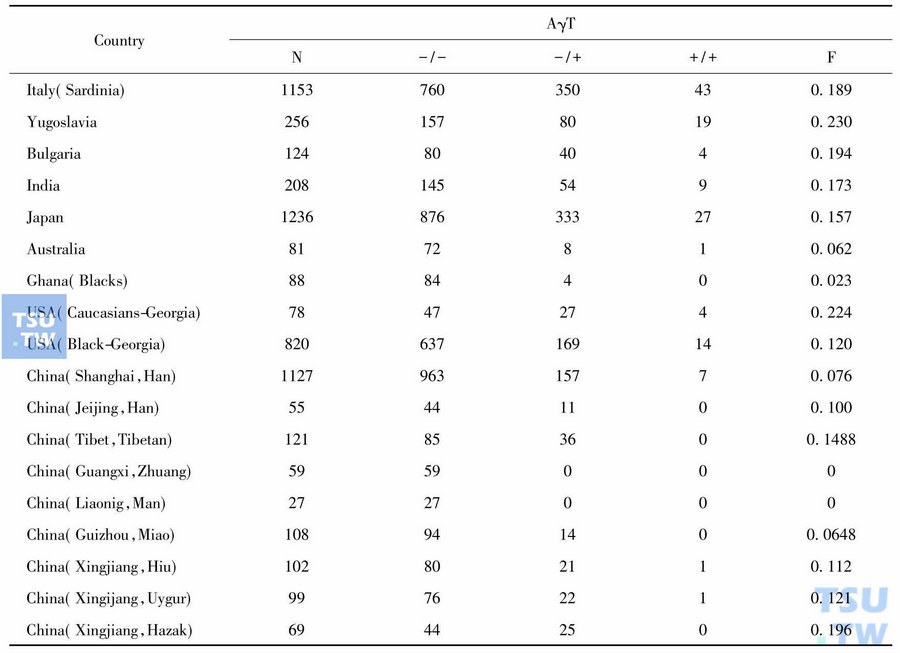
我国胎儿血红蛋白F 的γ珠蛋白链多态性及γ-珠蛋白基因重排
1968年Schroeder等发现人类胎血红蛋白F (HbF)中的γ-珠蛋白链(γ-链)存在两种类型,一种γ链第136位为甘氨酸(Gly),另一种为丙氨酸(Ala),分别称为Gγ和Aγ链,它
11