-
测试酵母样真菌药敏试验判断结果的标准是怎样产生的?
答:1992年,NCCLS起草了《酵母菌的液体稀释法抗真菌药物敏感试验参考方案》,文件名称为M-27P,用于检测引起深部感染的酵母样真菌,包括念珠菌、光滑球似酵母和新生隐球菌等对两性霉
1 -
测试丝孢子真菌的参考标准是如何制定的?
答:初始方案产生于1998年,命名为M-38P,该方案包括微量稀释法和宏量稀释法,对曲霉菌、镰刀菌、波氏假性阿利什霉等丝状真菌有较好的一致性;2003年NCCLS对某些最低抑菌浓度(MIC)判定
2 -
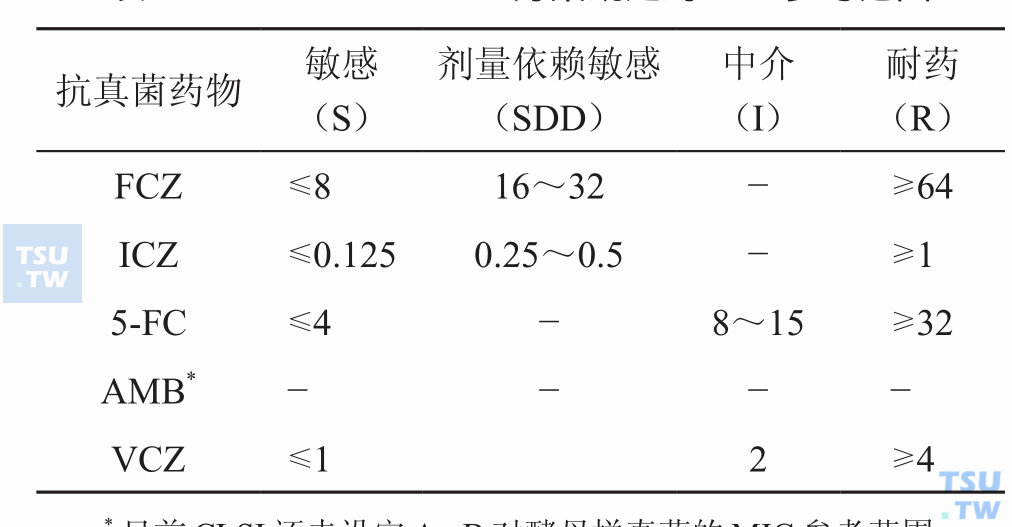
目前哪些抗真菌药物已设定对酵母样真菌的MIC参考范围?
答:主要有5-FC、FCZ、ICZ、AmB和VCZ,见表:CLSI M-27A2方案规定的MIC参考范围*目前CLSI还未设定AmB对酵母样真菌的MIC参考范围
3 -
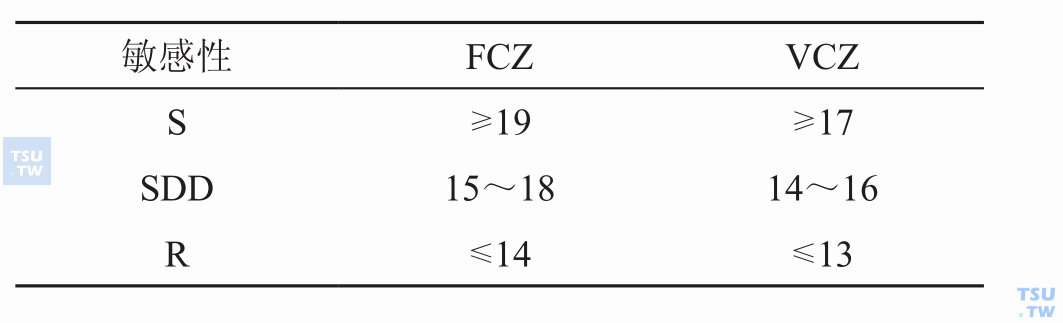
纸片法药敏试验的结果判断标准是如何制定的?
答:CLSI于2003年颁布M44-P对酵母样真菌纸片扩散药敏试验的判断标准,但只提供氟康唑(FCZ)和伏立康唑(VCZ)的标准,见表:CLSI M44-P对纸片扩散法的判断标准(mm)
4 -
丝状真菌如何确定敏感的MIC范围?
答:CLSI颁布的M-38P是丝状真菌肉汤稀释法抗真菌药敏试验,内容并无丝状真菌敏感性折点,只是描述了测试方案,包括试剂配制、操作方法、质量控制等程序。在临床应用中,按日剂量与MIC
5 -
抗真菌药敏试验对抗真菌药物的敏感折点是如何制定的?
答:主要根据以下5个因素制定折点:①该药物对各类真菌的MIC的分布;②该药物的血药浓度和组织浓度;③动物试验结果证明制定的折点的有效性;④临床试验结果证明制定的折点的有效性和
6 -
目前对折点制定加入哪些新的观点?
答:新的标准加入PK/PD参数作为抗菌药物临床评价新指标,传统制定折点的方法仅以体外药效学为准,按最低抑菌浓度(MIC)、最低有效浓度(MFC)、抗生素后效应(PAE)等,单一体外药效学数据不能
7 -
有哪些酵母样真菌或抗真菌药物不能用现有的标准评价它的敏感性?
答:①Candida krusei(克柔念珠菌)对氟康唑天然耐药,现已颁布的氟康唑对念珠菌的判断标准不适用,不管体外药敏结果均应报告耐药;②AMB对念珠菌目前无判断标准;③伊曲康唑的折点仅适
8 -
敏感性评价中“SDD”和“I”含义有什么不同?
敏感性评价中“SDD”(剂量依赖性敏感)和“I”(中介)含义有什么不同?答:“SDD”:其含义是敏感性依赖于用药剂量,如当FCZ的MIC在16~32mg/L时加大用药剂
9 -
为什么只在真菌药敏判断时才出现SDD的判断折点?
答:可能是因为只有浓度依赖性药物加大剂量后可以改善药物的疗效,而治疗真菌感染的药物大多是浓度依赖性的,所以在真菌药敏试验时参入SDD的折点更有其重要意义。
10 -
目前有哪些能用于真菌药敏试验的方法?
答:宏量肉汤稀释法;微量肉汤稀释法;琼脂稀释法;E-test方法;葡萄糖亚甲蓝琼脂扩散法;自动化系统ATB Fungus-3方法;氧化还原比色法;流式细胞仪测定法。但常用于临床的有:ATB Fungus-3方
11 -
ATB Fungus-3依据什么原理测试真菌药敏?
答:ATB Fungus-3试剂条包括16凹(cupules)形反应杯。第一对不含任何抗真菌剂,用作阳性生长对照。氟胞嘧啶包含一个高浓度一个低浓度2个稀释孔,另外的13对包含不同稀释度的4种抗真
13 -
葡萄糖亚甲蓝琼脂扩散法测定真菌药敏试验的原理是什么?
答:待测真菌均匀涂在葡萄糖亚甲蓝M-H琼脂上,贴浸泡了待测药物的纸片,经24~48小时培养,测定抑菌圈直径,按CLSI颁布的M-44-A的标准判断敏感性。
14