-
肉汤稀释法质控菌株MIC值(μg/ml)可接受范围有哪些?
答:肉汤稀释法质控菌株MIC值(μg/ml)可接受范围见表: 表4-3-4 结果解释和相应的MIC值注:MIC值适用于琼脂或肉汤稀释法药敏试验
1 -
如何阅读厌氧菌肉汤微量稀释法的药敏结果?
答:借助间接光源,在暗的无反射光的背景下检查每块平板。如果生长质控孔中的细菌生长不良或未生长,则不能读取结果。无细菌生长或几乎没有细菌生长的最低药物浓度为MIC终点。某
3 -
如何进行肉汤微量稀释板的接种?
答:操作步骤如下:①菌悬液的制备:配制与0.5麦氏浊度的菌悬液,最理想的是,在15分钟内用水或生理盐水稀释,调整接种菌液,使其接种后达到每孔细菌接种量为1 × 106CFU/ml,或每孔为
4 -
厌氧菌琼脂稀释法药敏试验时对培养基有什么要求?
答:CLSI推荐厌氧菌的药敏试验以布氏杆菌培养基为基础补充5%(v/v)脱纤维羊血、5μg/ml氯化血红素和1μg/ml维生素K1。采用液态稀释法时应补充冻融马血。配好的药敏试验平板
6 -
如何进行厌氧菌琼脂稀释法药敏试验?
答:琼脂稀释法药敏试验的操作程序:首先将不同稀释度的抗菌药加入已熔化并冷却至50℃左右的琼脂中,混匀后倾注平板,待其凝固后,使用接种器将接种标准化的被检菌株菌悬液分别接种在
7 -
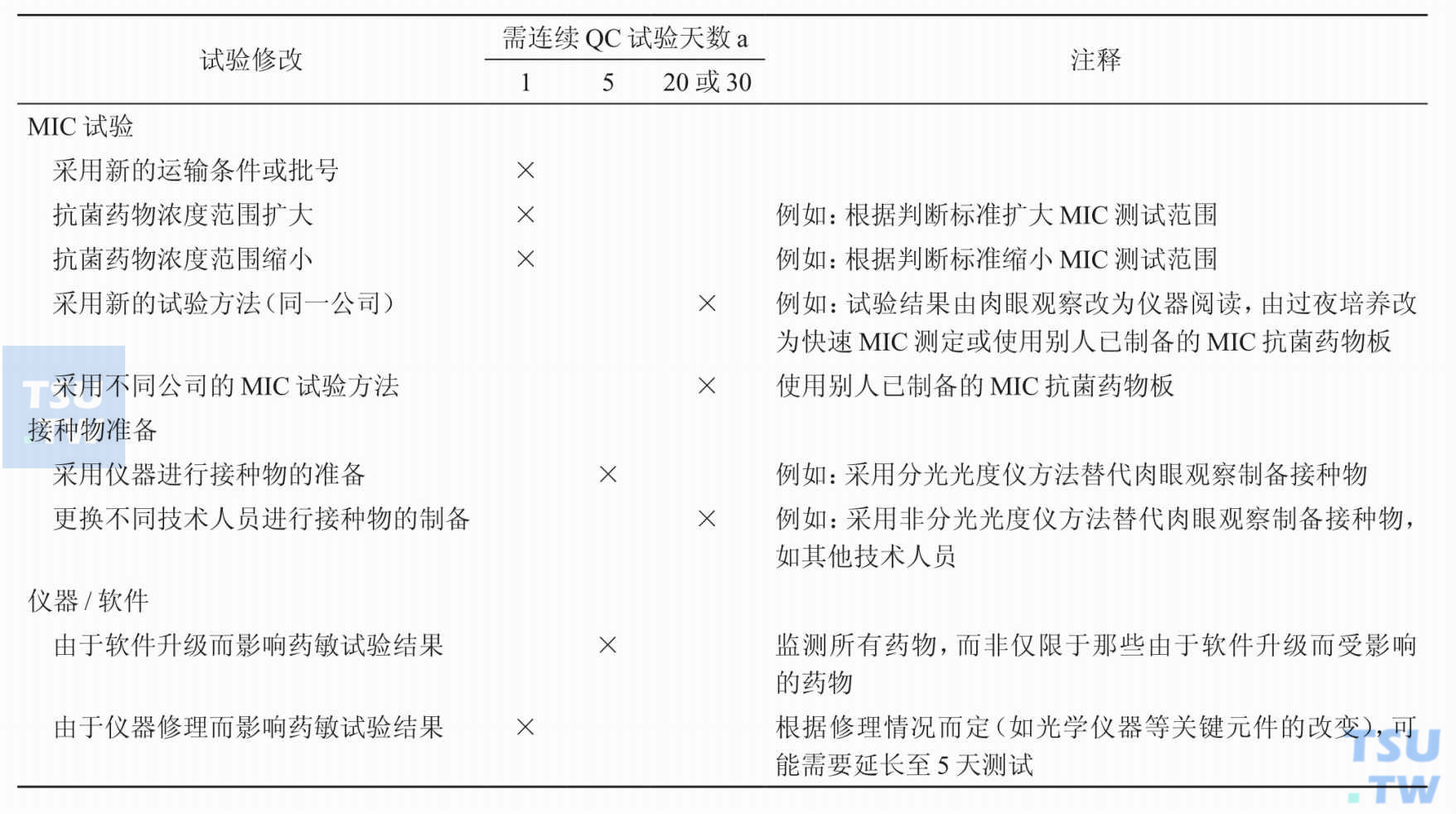
MIC法更改药敏试验中任一材料或方法时,如何做质量控制试验?
答:更改药敏试验中任一材料或方法时,应进行质控试验以确证这些更改不会对采用原有方法获得的结果产生影响。质控天数见表:MIC法药敏试验质量控制试验频率参考指南
8 -
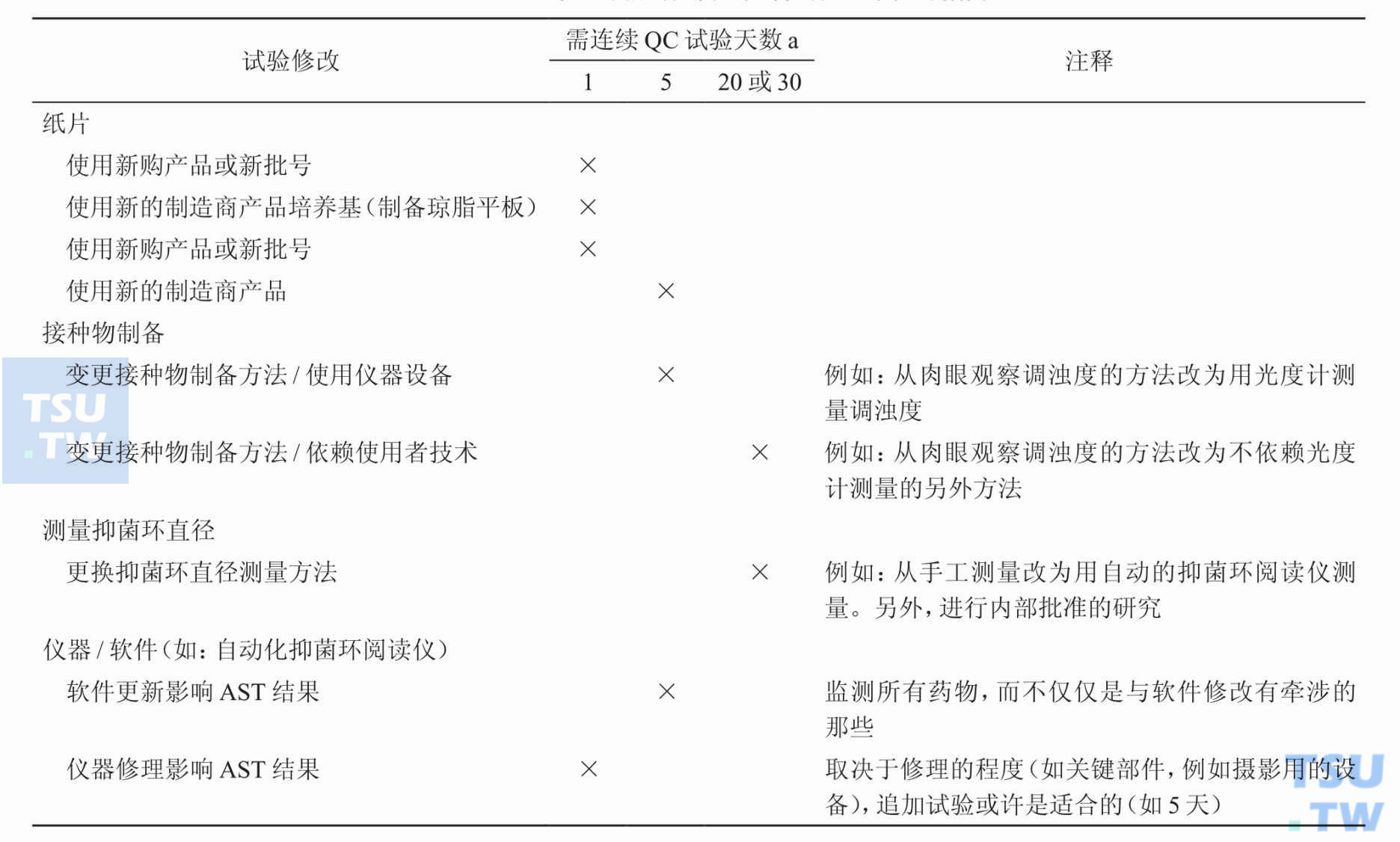
纸片法药敏试验中,更改药敏试验中任一材料或方法时,应如何做质量控制试验?
答:更改药敏试验中任一材料或方法时,应进行质控试验以确证这些更改不会对采用原有方法获得的结果产生影响。质控天数见表:纸片法药敏试验质量控制试验频率参考指南注1:使用本指
9 -
稀释法药敏的影响因素有哪些?
答:稀释法药敏的影响因素主要有:①M-H肉汤的pH及其中的阳离子浓度;②抗菌药浓度配制的正确与否;③细菌接种菌量的影响;④整个操作过程是否无菌操作;⑤其他人为因素,如操作失误等。
10 -
如何对新购买的M-H肉汤进行质控测试?
答:每批新制备的M-H肉汤都要用一套标准的质控菌株来评估,如果未达到预期的MIC值,就应对阳离子含量及其他变量和成分进行检查。为确定培养基是否适用于磺胺类药和甲氧苄啶的试验
11 -
新购买的M-H肉汤是否需要对其中的阳离子含量进行测定?
答:一般生产厂家提供的是阳离子含量已调整好的M-H肉汤,因此只有在生产厂家证实或是用原子吸收光谱法测量发现最初的M-H肉汤不含Ca2+、Mg2+或含量不够时,才可按下面方法调整阳离
12 -
M-H肉汤对其pH以及其中的离子浓度有何要求?
答:M-H肉汤在室温(25℃)下其pH应为7.2~7.4。肉汤中二价阳离子的合适范围应是:Ca2+为20~25mg/L,Mg2+为10~12.5mg/L。阳离子浓度不合适会影响氨基苷类对铜绿假单胞菌、四环素对所有细
13 -
CAMHB肉汤有哪些特点?
答:CAMHB肉汤为阳离子调节肉汤(cationadjusted Mueller-Hinton broth),是肉汤稀释法药敏试验的推荐培养基,具有以下几点:①对药敏试验显示较好的批间重复性;②对磺胺、甲氧苄啶和四
14 -
如何正确阅读稀释法药敏试验结果?
答:在读取和报告所测抗菌药对细菌的MIC前,应检查受试菌生长质控平板或对照管或对照孔(不含抗菌药)的细菌生长情况,以确定其是否被污染及接种量是否合适,以及抗菌药物对参与试验的
17 -
药敏平板孵育时有哪些注意事项?
答:点种受试菌的药敏试验平板应于室温下放置几分钟直至点种点的菌液被吸干,肉眼不见点种菌液,然后将平皿倒置,于35℃孵育16~20小时。在检测耐万古霉素肠球菌和耐苯唑西林葡萄球菌
18 -
在琼脂稀释法试验中应如何接种细菌?
答:可以采用多点接种仪进行受试菌的点种。点种前琼脂的表面必须干燥。点种的次序应按先点种不含抗菌药的质控平板(通常称受试菌生长质控平板),以检查接种菌的生长活性和纯度;随后
19 -
含有抗菌药的琼脂平板可保存多久?
答:新制备的供琼脂稀释法药敏试验的含药琼脂平板可在当天使用或密封于塑料袋中4~8℃保存。如果用于参与试验,平板最多保存5天,用于常规试验时可更长。对一些不稳定的抗菌药如亚
20