导管原位癌的鉴别诊断
导管原位癌(DCIS)的鉴别诊断包括普通型导管上皮增生(UDH)、非典型性导管上皮增生(ADH)、小叶原位癌、浸润性导管癌以及其他少见病变。
1.DCIS与UDH
DCIS与UDH的鉴别诊断往往并不困难。但有时实体型生长的中级别DCIS的肿瘤细胞可稍呈梭形,且分布不规则,类似于UDH中的细胞形态及流水样排列结构,因此易被误诊为旺炽型UDH。CK5/6和CK14免疫组化染色在两者的鉴别诊断中非常有意义。CK5/6和CK14在UDH中呈镶嵌样弥漫表达,而在DCIS中多数为阴性;部分基底样型DCIS可表达CK5/6和CK14,但其细胞核往往有显著非典型性。
2.DCIS与ADH
低级别DCIS的诊断标准一直存在争议,造成其与ADH鉴别诊断困难。两者在细胞形态上没有质的差别,主要是量的不同。诊断低级别DCIS最常见的量化标准是形态单一的异型导管上皮细胞至少达2个管腔或2mm。WHO工作小组对上述两个标准没有任何倾向,许多专家在临床工作中将两者结合使用。定量临界值的设定旨在为实际工作提供参考和标准,防止将非常小的低级别病变过度诊断为低级别DCIS,从而防止对类似病变患者的过度治疗。
3.DCIS与小叶原位癌
实体型DCIS的另一重要鉴别诊断为小叶原位癌,E-钙黏蛋白和P120免疫组化染色有助于两者的鉴别。DCIS中E-钙黏蛋白几乎均为阳性,而小叶原位癌中E-钙黏蛋白几乎均为阴性。P120在DCIS中显示细胞膜着色,而在小叶原位癌中显示细胞膜和细胞质同时着色。少数情况下可见DCIS和小叶原位癌作为两个相对独立的区域存在于同一病变中,更为少见的情况下可见DCIS和小叶原位癌共存于同一终末导管小叶单位中。此时应注意与小叶原位癌累及导管或DCIS累及小叶(小叶癌化)相鉴别。
4.DCIS与浸润性导管癌
高级别DCIS累及小叶单位或良性病变(如硬化性腺病、放射状瘢痕)时,易造成类似浸润的假象。反之,某些特殊类型的浸润性导管癌,如浸润性筛状癌或腺样囊性癌,其生长方式可类似于DCIS。另外,DCIS样的浸润性导管癌是一种较为罕见的病变,显示病变境界清楚,甚至圆形的细胞巢,其组织结构与DCIS极其相似而易误诊为DCIS。在上述情况下,仔细的形态学观察和肌上皮细胞标记免疫组化染色有助于正确诊断。
5.DCIS与胶原小球病
胶原小球病(collagenous spherulosis)是一种少见的良性增生性病变。其特征是球形小体内可见嗜酸性基膜样物或嗜碱性黏液样物,小体周围有肌上皮细胞围绕(图24-8)。胶原小球常见于乳腺良性增生性病变,少数情况也可见于小叶原位癌或DCIS及其他恶性肿瘤。由于其球状小体类似于筛孔状的圆形腺腔,因此易与筛状型DCIS混淆。形态上,筛状型DCIS腺腔周围为形态单一的上皮细胞,呈极性排列;而胶原小球病的假性腔隙周围为增生的肌上皮细胞。另外,肌上皮细胞标记免疫组化染色也有助于两者的鉴别。
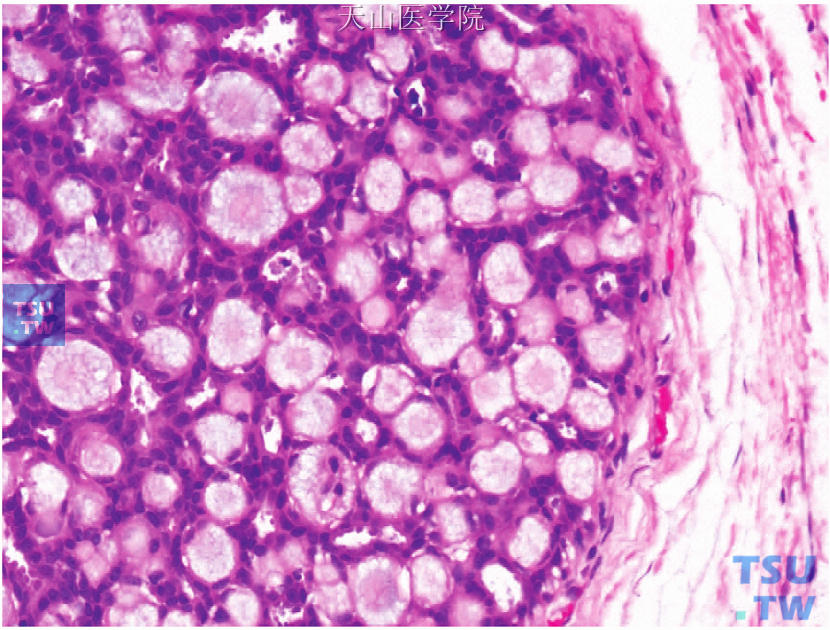
图24-8 胶原小球病,腔隙内可见嗜碱性黏液样物质和嗜酸性小球
导管原位癌伴微浸润
一直以来关于乳腺微浸润癌的定义存在较大差异,部分学者提出乳腺微浸润性癌需要浸润性肿瘤细胞超出特化的小叶间质。2012年版WHO乳腺肿瘤组织学分类将微浸润定义为:乳腺间质中存在一个或多个清晰且独立的肿瘤细胞浸润灶,每灶最大径≤1mm(图24-9)。微浸润可为单个肿瘤细胞、小簇实性细胞,甚至可见腺体形成。肌上皮细胞标记免疫组化染色有助于鉴别微浸润。若出现多灶微浸润,每个病灶需分别测量而不能相互叠加。微浸润常见于广泛高级别DCIS伴有显著导管周围炎性细胞浸润的背景中,当存在导管周围间质纤维化、结缔组织增生性间质反应、导管周围淋巴细胞浸润或高级别DCIS累及乳腺小叶时,应高度警惕微浸润性癌的存在。
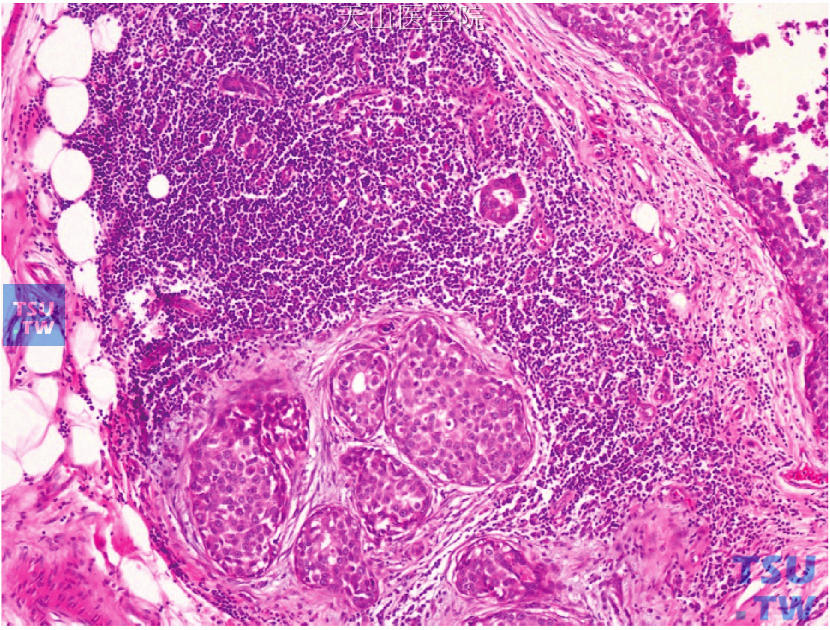
图24-9 导管原位癌伴微浸润,少量肿瘤细胞成簇状出现于导管原位癌周围富于淋巴细胞的间质内
DCIS伴微浸润需与DCIS、明显的浸润性导管癌(>1mm),以及穿刺导致的上皮细胞移位等鉴别。
DCIS累及终末导管小叶单位或良性病变(如硬化性腺病、放射状瘢痕或复杂性硬化性病变),或累及各级导管导致其分支或扭曲时,易误诊为微浸润。进一步深切片可能有助于鉴别。肌上皮细胞标记免疫组化染色在微浸润的鉴别诊断中具有十分重要的意义,染色显示微浸润灶周围没有肌上皮细胞包绕。常用的肌上皮细胞免疫组化标记包括calponin、SMA、MSA、SMMHC及p63。特别是p63较少与成肌纤维细胞产生交叉反应。与细胞角蛋白标记进行双染,更加有助于显示微浸润灶。借助于导管上皮细胞和Ⅳ型胶原基膜染色进行鉴别有时存在一定困难,DCIS病灶可显示不同程度的基膜消失,而微浸润灶至少部分区域可见基膜。
浸润灶的大小要精确测量,以除外明显的浸润性导管癌,两者的鉴别诊断同样可借助于肌上皮细胞标记的免疫组化染色。
DCIS伴微浸润还应与因术前曾行穿刺活检导致的上皮细胞移位进行鉴别。穿刺过程可能引起良性上皮(尤其是乳头状瘤)甚至DCIS细胞发生移位,导致与微浸润鉴别诊断困难。前者往往没有间质反应,同时伴有间质出血、含铁血黄素沉积、炎细胞浸润、肉芽组织增生等反应性改变,应注意寻找。当不确定是否存在微浸润,而可疑区域经深切片及免疫组化染色后不复存在时,建议诊断为“原位病变,没有确切证据证实有微浸润或浸润性癌”。
