机体对弥散性血管内凝血(DIC)具有多种防护和代偿功能,前者中和DIC的促凝部分,后者纠正DIC的病理生理过程。
微循环的内皮表面通过三种机制可有效地去除DIC过程中产生的凝血酶:①结合在内皮表面硫酸肝素上的抗凝血酶-Ⅲ(antithrombin-Ⅲ,ATⅢ)能中和凝血酶,继而生成凝血酶-抗凝血酶-Ⅲ(thrombinantithrombin complex,TAT)复合物。②在内皮细胞表面的凝血酶调节蛋白(TM),能与凝血酶相结合而废除后者对纤维蛋白原、因子XⅢ(FXⅢ)和血小板的促凝作用,同时凝血酶- TM(T- TM)复合物能活化血浆蛋白C。活化的蛋白C(APC)是一种生理性抗凝物,能使FⅤa、FⅧa降解,并通过中和PAI而刺激纤溶过程。③组织因子途径抑制物(tissue factor pathway inhibitor,TFPI)是一种内皮细胞生成的生理抗凝物。血浆水平<2nmol/L。在DIC中TFPI被消耗。在少量TF生成的情况下,TFPI能灭活TF-Ⅶa复合物,并抑制FⅩa活性。故对维持微循环灌注、微循环内皮细胞的功能、清除促凝活性至关重要。若大量促凝活性的生成或进入循环,压倒机体的防护功能即能引发DIC。
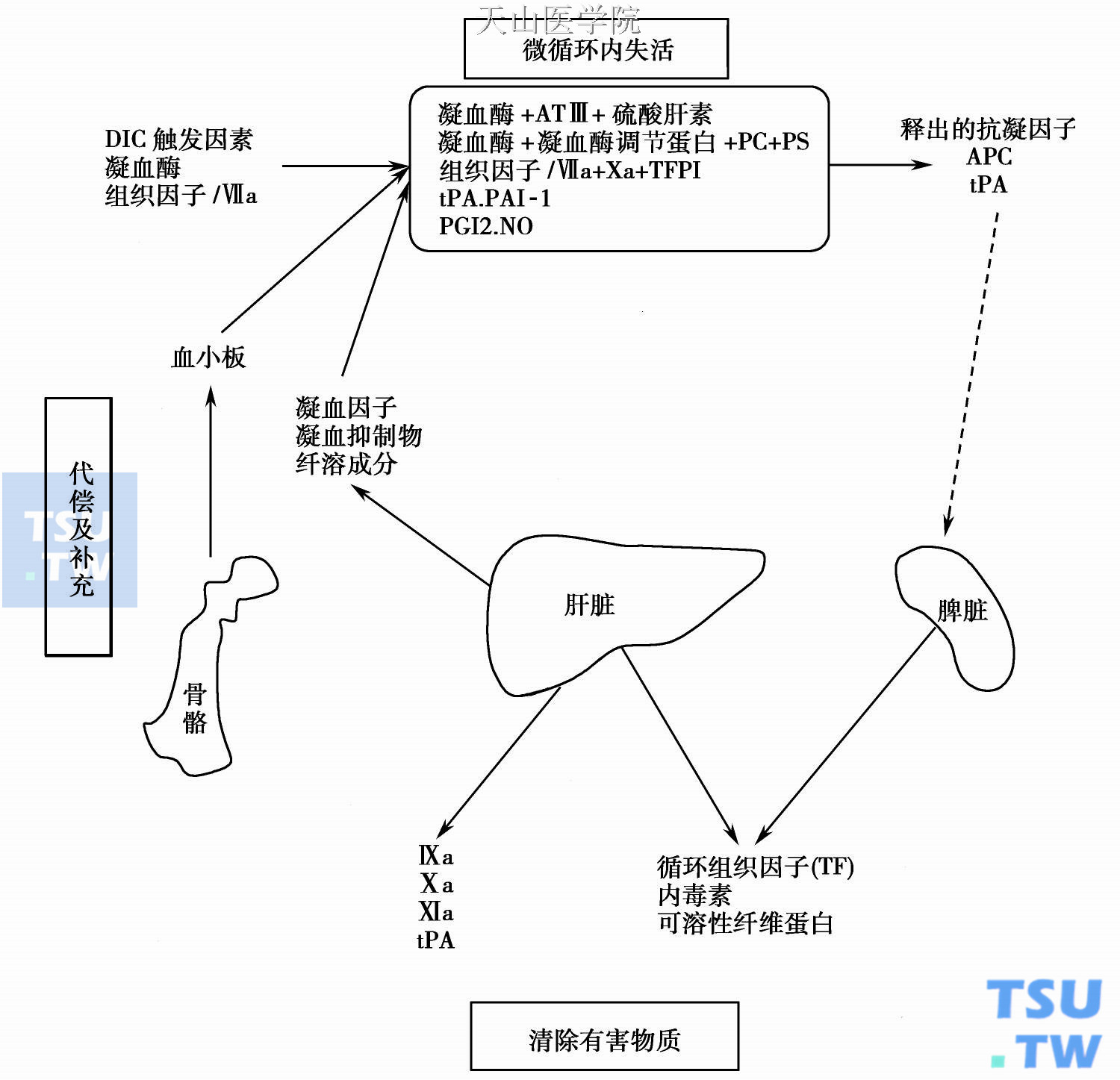
机体对DIC的防护和代偿功能
单核吞噬细胞系统能去除TF及可溶性纤维蛋白单体,故对DIC起着重要的代偿和防护功能。TF是一种膜蛋白成分,只有在病理情况下才暴露于血流并与单核细胞、内皮细胞或血液转移癌细胞表面结合。单核吞噬细胞系统则能有效地去除循环中结合在颗粒上的TF。肝实质细胞能清除循环中的FⅨa、Ⅹa、Ⅺa,并合成被消耗的凝血因子、纤溶因子,如纤溶酶原、α2抗纤溶酶原和蛋白C、蛋白S、ATⅢ等,故起着某种防护和代偿作用。骨髓通过增加血小板生成而对DIC起重要代偿作用,但是骨髓巨核细胞反应需一段时间,故在DIC发生之后,即使治疗有效,使循环血小板上升也需几天时间。
值得注意的是,所有诱发DIC的基础疾病都可使机体的防御和代偿功能受阻。例如白血病可抑制巨核细胞池,肝病可损害合成凝血因子和清除被活化凝血因子的功能。感染性休克的患者,因微循环灌注不足而削弱机体抑制凝血的功能。
