乳腺癌术后辅助治疗,完全依据临床分期制订治疗决策已经受到实践的挑战。随着对乳腺癌发生发展分子机制认识的逐渐深入,乳腺癌术后治疗决策在充分重视传统肿瘤负荷为基础的分期诊断的前提下,更多考虑肿瘤预后相关的组织学分期,以及治疗获益相关的分子指标。到了今天,治疗决策更加重视临床病理分型,这些历程的转变使得乳腺癌诊治理念日臻完善,充分体现更为精准的个体化治疗。当然,无论何时,准确判断肿瘤分期、利用分子指标评价预后是指导术后辅助治疗的关键所在。因此,对于常见组织类型的早期乳腺癌患者,依据传统危险度分析,结合其分子分型,制订辅助治疗方案是合理可行的。
乳腺癌术后复发风险评估及辅助治疗指南
2011年版中国抗癌协会《乳腺癌诊治指南与规范》
中国抗癌协会于2011年发布了《乳腺癌诊治指南与规范》。该指南与规范中对乳腺癌术后复发风险进行了分组(表37-1),可供全面评估患者手术以后的复发风险的高低,是制订全身辅助治疗方案的重要依据。
表37-1 乳腺癌术后复发风险的分组

注:a:组织学分级/核分级;b:瘤周脉管侵犯存在争议,它只影响腋窝淋巴结阴性患者的危险度分级,并不影响淋巴结阳性患者的分级;c:HER-2的测定必须是严格质量把关的免疫组化或FISH、CISH。
从表37-1中可以看到,中国抗癌协会的《乳腺癌诊治指南与规范》对复发风险因素评估分为低危、中危、高危3个分级,这种危险度分级更多地参照了2007年St. Gallen国际乳腺癌治疗专家共识中对乳腺癌复发风险的评估,并有所丰富。
2011年版St. Gallen国际乳腺癌治疗专家共识
2011年版St. Gallen国际乳腺癌治疗专家共识对乳腺癌复发风险的评估,更多的是依据临床病理分型(表37-2)来进行术后辅助治疗方案的决策。乳腺癌亚型可以通过基因列阵试验或免疫组化进行分类。由于获取基因表达微阵列信息并不总是可行的,Cheang等专家提议运用一种接近基因表达微阵列分析的简单分类方法,这种方法已经作为标准方法。运用临床病理标准确定亚型与本质上的亚型相似,但并不完全等同。
表37-2 乳腺癌临床病理分型定义
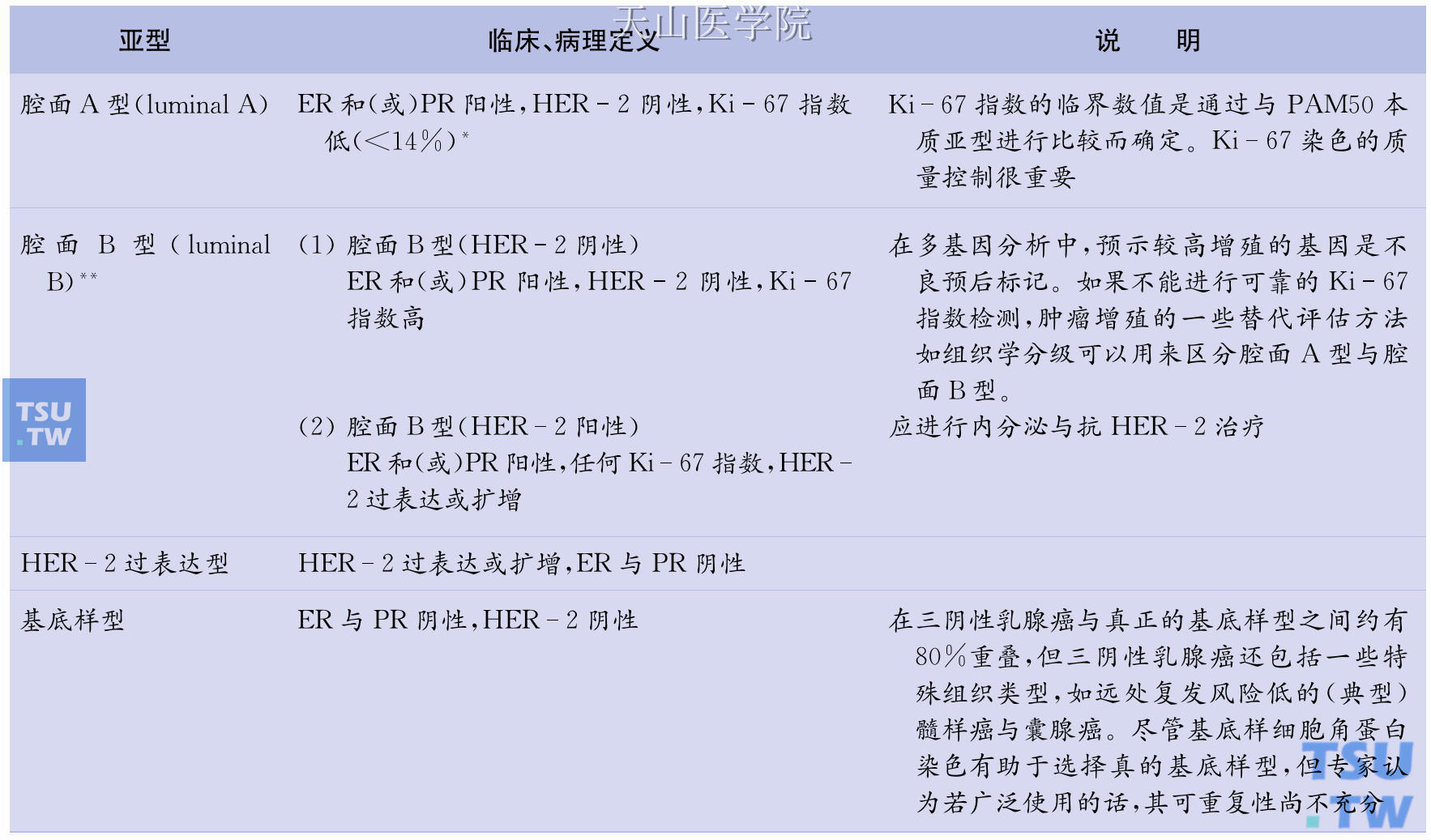
注:*该临界值是基于与作为预后因子的基因阵列数据相比较而得出的。预测内分泌治疗或细胞毒化疗有效性的Ki-67指数最佳临界值可能不同。
**某些患者同时过表达腔面基因和HER-2基因。
临床病理分型是运用免疫组化定义ER与PR,检测HER-2基因过表达或(和)基因扩增以及作为细胞增殖标记的Ki-67指数,依据这些指标来确定肿瘤亚型。这种临床病理学分类需要对上述指标可靠的检测。美国临床肿瘤学会(ASCO)和美国病理家协会(CAP)联合制定针对激素受体检测和HER-2检测的相关指南。Ki-67指数目前面临更重要的挑战,该指标的检测指南尚不成熟。但在该分类中,Ki-67指数的检测对区分腔面A型(luminal A)与腔面B型(HER-2阴性)非常重要。如果不能获取准确的Ki-67指数,可采用一些替代的测量细胞增殖的方法如组织学分级。
依据临床病理分型特点,St. Gallen专家共识也提出了相应的治疗策略(表37-3)。对于临床病理学分类为腔面A型乳腺癌(除外高风险患者),基本上推荐单用内分泌治疗;对腔面B型,推荐化疗和内分泌治疗;对HER-2阳性患者,加用抗HER-2治疗;对绝大多数三阴性乳腺癌,主要依赖化疗(浸润性导管癌)。
表37-3 乳腺癌不同亚型系统治疗的推荐策略

注:特殊组织类型的内分泌治疗反应型包括筛状癌、管状癌及黏液癌;内分泌无反应型包括顶分泌癌、髓样癌、囊腺癌及化生性癌。
2011年版NCCN乳腺癌治疗指南中文版
在临床工作中也会参考2011年版NCCN乳腺癌治疗指南中文版。针对术后辅助治疗的选择该指南指出,首先根据对内分泌治疗和曲妥珠单抗的反应(即激素受体状况和HER-2状态)进行分类,然后再根据解剖和病理特征(即肿瘤分级、肿瘤大小、腋窝淋巴结状态、血管淋巴浸润)提示的疾病复发风险作进一步分类。
前面所述的几个指南给出的推荐治疗总体来讲是一致的,在最终选择方案时要综合考虑肿瘤的临床病理学特征、患者方面的因素和意愿,以及治疗可能的获益和由此带来的毒性等。
激素受体状况和HER-2检测的说明
乳腺癌术后辅助治疗方案的制订需要依据临床病理学分类,而临床病理学分类需要对激素受体状况和HER-2状态进行可靠的检测。
2010年ASCO/CAP联合制定并公布了一份指南,该指南旨在提高免疫组化检测ER和PR的准确性,对于临床有针对性地进行内分泌治疗,避免不必要的不良反应具有重要意义,极大改变了目前全世界范围内ER/PR检测20%的不准确率。该指南推荐,对于每一例新诊断为乳腺癌的患者应进行ER和PR的检测,这是新诊断乳腺癌的标准程序。激素受体检测判定标准的变化是该指南最引人注目的内容,其推荐的ER和(或)PR阳性标准是:≥1%的细胞核染色阳性即是激素受体阳性,而以往是以10%作为标准。该指南明确提出在病理报告中应包括以下3个方面的内容:①记录和报告肿瘤细胞激素受体阳性染色的百分比;②记录和报告染色强度,分别为弱染色、中等强度染色和强染色;③受体阳性结果解释,即是否有至少1%的肿瘤细胞染色阳性。受体检测结果应该是阳性、阴性、不确定。当然,如果由于样本问题不能得出激素受体检测结果也应该明确标出。
该指南推荐区分激素受体阳性与阴性的临界值定为1%的肿瘤细胞核染色。当然,染色细胞的百分比能够提供更多的预测及预后信息。已有多项研究显示,乳腺癌患者预后指标如总生存率、无病生存率、内分泌治疗反应率等与ER受体水平的高低呈正相关,这就提示临床医师如果患者的激素受体水平较高,可能从内分泌治疗中的获益要好于激素受体水平较低者。因此,专家组成员同时指出,对于那些ER表达弱阳性(即1%~10%)的患者,是否应用内分泌治疗应该慎重,应根据数据讨论后由临床医师决定。
HER-2状态是乳腺癌患者重要的预测及预后因子,因此正确检测和评定乳腺癌的HER-2状态至关重要。目前,一般采用免疫组化(IHC)检测HER-2受体蛋白表达情况,应用荧光原位杂交(fluorescence in situ hybridization,FISH)和显色原位杂交(chromogenic in situ hybridization,CISH)法检测HER-2基因扩增水平。鉴于多种因素(如标本的固定及保存、抗体或探针的选择、结果的判读、操作者的经验等)均可导致检测结果的偏差,中国病理学专家及临床专家一起,根据国内外学术界最新的研究数据讨论后达成共识并制定《HER-2检测指南》。该指南强调检测中容易出现误差的环节、内部及外部质量控制和保证程序,旨在使HER-2检测的操作程序和结果的判读标准化,提高HER-2检测的可重复性和准确性,更准确地筛选出适宜曲妥珠单抗等药物治疗的乳腺癌患者。中国抗癌协会乳腺癌专业委员会专家组成员,根据现有国内外研究结果讨论后达成以下共识——HER-2检测和结果判定标准。
- HER-2是乳腺癌重要的预后指标,也是靶向HER-2药物的预测指标。
- 靶向HER-2药物治疗适应证为HER-2阳性乳腺癌。
- HER-2阳性的定义,可以是标准免疫组化检测HER-2为3+,或FISH法阳性。
- 如果患者免疫组化检测显示HER-2为3+,可以直接判断为HER-2阳性。如果免疫组化检测HER-2为2+,应该再进行FISH检测。如果合格实验室免疫组化检测结果HER-2为+或HER-2为-,则判定为HER-2阴性。
- HER-2阳性判断也可以通过FISH检测。在合格实验室进行的FISH检测,其比值>2.2,则可判断为HER-2阳性;<1.8则为HER-2阴性;如果所得结果为1.8~2.2的临界值,则应该结合免疫组化结果进行判断。
