随着研究的不断深入,逐渐认识到三阴性乳腺癌是一组异质性很大的疾病,2012年Journal of Clinical Oncology 一篇综述描述了目前认识到的关于三阴性乳腺癌的异质性。将三阴性乳腺癌细分成6种亚型(图51-3),分别为基底样型、BRCA相关性亚型、CK和EGFR高表达亚型、claudin-low亚型、其他病理亚型和免疫系统亚型,而最简单的容易得到的三阴性乳腺癌的表述处于此6种亚型的中心位置。换句话说,三阴性仅仅是复杂异质性的共同表现。今后随着技术的进步及认识的进一步深入,有可能再细分更多种亚型。对免疫系统亚型该文没有详细阐述,其他病理亚型在本章第一节已经详述,下面逐个分述另外4种亚型。
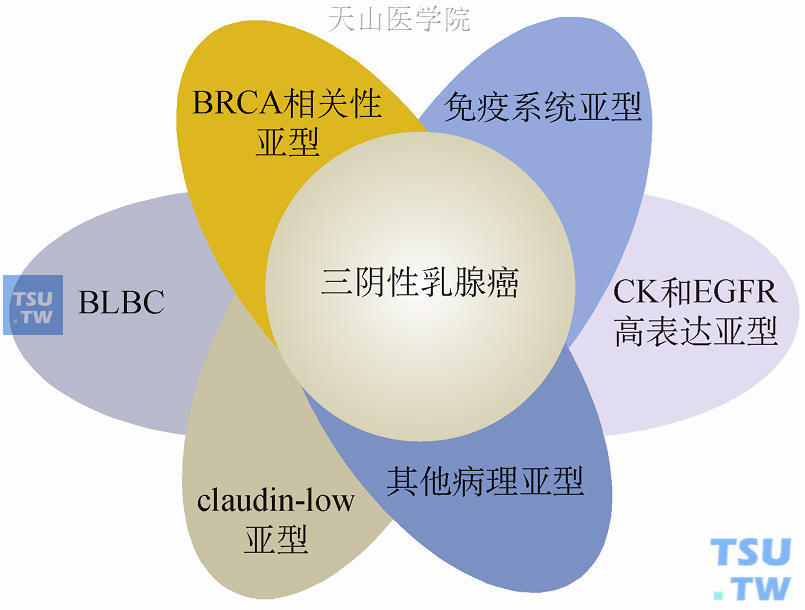
图51-3 三阴性乳腺癌的异质性(Metzger-Filho, et al. J Clini Oncol, 2012)
基底样型乳腺癌
BLBC为三阴性乳腺癌的主要组成,占70%~80%,是指具有基底细胞基因表型并不同程度表达基底细胞样CK和肌上皮标记(caveolin, CAV)的乳腺癌。多数学者认为CK5/6、CK14、CK17、EGFR阳性,同时ER、PR和HER-2阴性被界定为BLBC。但由于诊断BLBC的金标准是基因芯片,该方法操作复杂,目前还没有得到广泛推广。
正常乳腺组织的结构功能单位为终末导管小叶单位。乳腺导管及小叶上皮系统由特化的两层上皮细胞衬覆,内层为腺上皮细胞,外层为基底/肌上皮细胞。成熟腺上皮表达腺上皮角蛋白(如CK8、CK18),而基底/肌上皮细胞表达基底细胞样角蛋白(如CK5/6、CK14和CK17)和肌上皮相关蛋白(如SMA、p63、S100和CD10)。
BLBC的特点为基因表达谱与正常基底/肌上皮细胞的基因表达几乎完全一致,因而得名。基因表达谱中有CK5、7,层粘连蛋白和脂肪酸结合蛋白等表达,并不同程度地表达基底细胞样CK和肌上皮相关蛋白,免疫表型表现为CK5/6阳性、CK17阳性、EGFR阳性、p53阳性、ER阴性、HER-2阴性等特点。有学者将BLBC再细分以下几种:①ER阴性/HER-2阴性,CK5/6阳性和(或)EGFR阳性;②CK5/6阳性,CAV1阳性,CAIX阳性,p63阳性或CD117阳性;③CK5/6阳性和(或)CK14阳性;④CK5/14阳性。但此分类未得到广泛认可。
三阴性乳腺癌有许多生物学特征与BLBC相似,如绝经前患者占多数,组织学分级较差,且多伴p53突变,预后极差,但对化疗极为敏感。具有组织学级别高、发病年龄早(<50岁)、恶性度高、侵袭性强、术后复发转移风险高、内脏转移和脑转移概率较高、疾病进展快、临床预后差等特点。但两型的预后不同,两者之间存在某些基因表达谱和免疫表型上的差异,因此不能完全等同。下列一组数据可说明两者关系:10%~35%的三阴性乳腺癌患者根据基因表达的结果并不属于BLBC,仅40%~80%的三阴性乳腺癌在蛋白质水平表达基底样型的某些标记,超过45%的BLBC不是三阴性乳腺癌(即存在ER、PR或HER-2的表达)。
国外有学者认为将三阴性乳腺癌利用5个免疫标记进一步区分为两型具有可操作性和临床意义。该研究长期随访的结果显示各型5年和10年生存率分别为:ER阳性/PR阳性/HER-2阴性(2 625例)91%和79%;ER阳性/HER-2阳性(222例)75%和60%;ER阴性/PR阴性/HER-2阳性(258例)60%和55%;ER阴性/PR阴性/HER-2阴性/CK5/6和EGFR阳性(336例)68%和62%;ER阴性/PR阴性/HER-2阴性/CK5/6和EGFR阴性(303例)79%和72%。作者认为应该利用5个免疫组化标记(ER、PR、HER-2、CK5/6、EGFR)将三阴性乳腺癌进一步分为两型,有较好的临床及实践意义,一是易操作,二是两型之间预后存在显著差异,10年生存率绝对值相差10%,ER阴性/PR阴性/HER-2阴性/CK5/6和EGFR阳性者预后更差,组织学Ⅲ级比例高(87%),<40岁者常见(18.8%);而5个免疫组化标记阴性者组织学Ⅲ级及<40岁者分别为64.4%和10.2%。
英国诺丁汉大学一项报道1 277例浸润性导管癌,有232例(18%)为三阴性乳腺癌,在此基础上将CK5/6、CK14、CK17或EGFR至少一项阳性者定义为BLBC,而上述表型均为阴性者定义为TN3BKE阴性(TN, CK5/6、CK14、CK17、EGFR阴性)。结果165例(71%)为BLBC,其余67例(29%)三阴性乳腺癌为TN3BKE阴性。与TN3BKE阴性免疫表型和临床不同,BLBC高表达CK19、p53蛋白及低氧相关因子(CA9)和ER-β1,神经内分泌分化标记如嗜铬粒蛋白A或结合型嗜铬粒蛋白A、突触囊泡蛋白阳性,MHC-I型阳性,携带更高BRCA-1基因突变(OR = 13.0,P = 0.003),较高的肺及脑转移率,骨及肝转移率无差异,较短的DFS(P = 0.01);而年龄、原发灶大小以及病理分级、推挤性边缘、粉刺样坏死等病理特征无差异。另有报道,基底样型与非基底样型的免疫组化下列特征显著不同,ER、HER-2、CK5/6、c-kit、EGFR、p53突变、p53蛋白、细胞周期蛋白E、波形蛋白表达率。
BRCA相关性乳腺癌
BRCA突变与三阴性乳腺癌
BRCA基因(人类乳腺癌易感基因)致病性突变(pathogenic mutation)常见于BRCA-1和BRCA-2,其中BRCA-1突变与乳腺癌相关,与三阴性乳腺癌关系更密切。其相关特征为:①BRCA-1突变携带者发生乳腺癌绝大多数(60%~80%)为三阴性乳腺癌;②BRCA-1基因在乳腺癌突变的比例为4%~11%,而在三阴性乳腺癌为10%~34%;③BRCA-1基因突变在遗传性乳腺癌和犹太人乳腺癌患者中更明显;④生物学及临床表现三阴性乳腺癌与BRCA-1相关性乳腺癌有许多相同之处,如ER阴性、CK5/6阳性、Ki-67阳性、EGFR阳性、p53基因突变,多为浸润性导管癌,高组织学分级,对化疗敏感,但预后差,易出现转移及局部复发等;⑤由BRCA-1介导的通路在三阴性乳腺癌发病中发挥重要的作用。BRCA-1基因与DNA双链的断裂同源重组修复有关,当BRCA-1基因突变后BRCA-1通路失活,肿瘤缺乏BRCA-1介导的双链DNA修复功能,理论上对破坏DNA化学结构的细胞毒化疗药(如烷化剂、铂类、丝裂霉素)及放疗可能高度敏感,为探索针对三阴性乳腺癌分子分型为基础的化疗方案及靶向治疗靶点的选择提供了理论基础,也提示三阴性乳腺癌对某些细胞毒性化疗药敏感可能与BRCA-1突变有关。
美国洛杉矶南部加利福尼亚大学进行一项基于人口的研究(population-based study),对1 469例乳腺癌者标本资料完整的1 196例进行BRCA-1和BRCA-2测序,分析前剔除了29例BRCA-2突变者。最后分析符合下列条件:美国出生、会说英语、白种人(包括西班牙裔)或非洲裔美国人、当地诊断乳腺癌(既往无乳腺癌病史)、年龄20~49岁的所有1 167例乳腺癌患者(其中156例三阴性乳腺癌和1 011例非三阴性乳腺癌),结果显示4%(46/1 167例)的患者存在外显子2的185delAG及外显子20的5382insC等位点BRCA-1突变。但携带BRCA-1突变者约一半(48%,22/46例)为三阴性乳腺癌,而不携带BRCA-1突变者发生三阴性乳腺癌的概率只有12%(134/1 121例)。46例BRCA-1突变种族分布为犹太人13例、西班牙人7例、非洲裔美国人2例、其他24例。犹太人同时携带BRCA-1突变三阴性乳腺癌发生的概率(9/13; 69%)比非犹太人高5倍(OR = 6.38,P = 0.04),其他种族对比无显著差异。携带BRCA-1的三阴性乳腺癌患者发病中位年龄更轻(38岁对比44岁)、组织学Ⅲ级所占比例更高(95%对比65%)。美国纪念斯隆-凯特琳癌症中心(MSKCC)测序分析451例犹太人乳腺癌DNA样本BRCA突变(BRCA-1的185delAG、BRCA-1的5382insC及BRCA-2的6174delT),有48例(10.6%)BRCA-1(27例,6.0%)及BRCA-2突变(21例,4.7%)。64例三阴乳腺癌中有25例BRCA-1或BRCA-2突变(39.1%;19例BRCA-1,6例BRCA-2);携带BRCA-1突变发生三阴性乳腺癌(70.4%,19/27例)比BRCA-2突变三阴性乳腺癌(28.6%,6/21例)更加常见,而非BRCA突变者中仅有9.7%(39/403例)是三阴性乳腺癌(P < 0.)。犹太妇女BRCA-1和BRCA-2突变与三阴乳腺癌关系密切。三阴性乳腺癌且有家族性乳腺癌史,40%(6/15例)伴有BRCA突变。另一项检测了99例患者BRCA的突变情况,结果10例携带BRCA-1突变者中有8例为三阴性乳腺癌(P < 0.),7例携带BRCA-2突变者只有1例为三阴性乳腺癌(P > 0.05)。
最新一项希腊的研究进一步描述了三阴性乳腺癌与BRCA-1突变的相关性。403例三阴性乳腺癌BRCA-1突变测序(外显子5、11、12、16、20、21、22、23、24位点),结果16%(65/403例)三阴性乳腺癌患者携带BRCA-1基因突变,携带者诊断三阴性乳腺癌的中位年龄为39岁。106例患者诊断三阴性乳腺癌时年龄<40岁,其中38例(36 %)携带BRCA-1突变。诊断三阴性乳腺癌时年龄<50岁患者中有27%(56/208例)携带BRCA-1突变。家族中有乳腺癌或卵巢癌病史的三阴性乳腺癌48%(50/105例)携带BRCA-1突变。但值得注意的是,有23%(15/65例)携带突变者无家族史。携带者除1例外病理组织学分级均为Ⅲ级(98%)。作者认为对于年轻的三阴性乳腺癌患者,即使没有乳腺癌或卵巢癌家族史,也需要进行BRCA-1基因突变的检测。
BRCA相关性乳腺癌的预后
携带BRCA-1突变者发生乳腺癌绝大多数为三阴性乳腺癌,那么携带与不携带BRCA-1/2突变的三阴性乳腺癌的无复发生存期及OS有无差异。一项研究比较了1997~2010年227例三阴性乳腺癌的预后,50%(n = 114)携带BRCA-1/2突变,单因素及多因素分析年龄、种族、原发灶特征,在携带与不携带BRCA者无差异。中位随访3.4年,5年无复发生存率不携带与携带BRCA者分别为74%和 81%(P = 0.21),5年OS分别为85%和93%(P = 0.11)。经调整年龄及分期后,单因素及多因素分析显示,在诊断乳腺癌的前5年内携带与不携带BRCA者的无复发生存期(HR = 0.67,P = 0.17)和OS(HR = 0.51,P = 0.11)均无显著差异。
BRCA相关性乳腺癌、三阴性乳腺癌及BLBC三者的关系
BRCA-1相关性乳腺癌与三阴乳腺癌密切相关,而BLBC与三阴性乳腺癌高度重叠。BLBC、三阴性乳腺癌和BRCA-1相关乳腺癌三者之间关系密切。三阴性乳腺癌具有BLBC和BRCA-1相关性乳腺癌的大部分特征,三者有关联,但又不能相互替代。三者在形态学、免疫学、分子特点、治疗策略及预后方面的主要特征见表51-1。
表51-1 TNBC、BLBC、BRCA-1相关性乳腺癌及非TNBC的主要特征
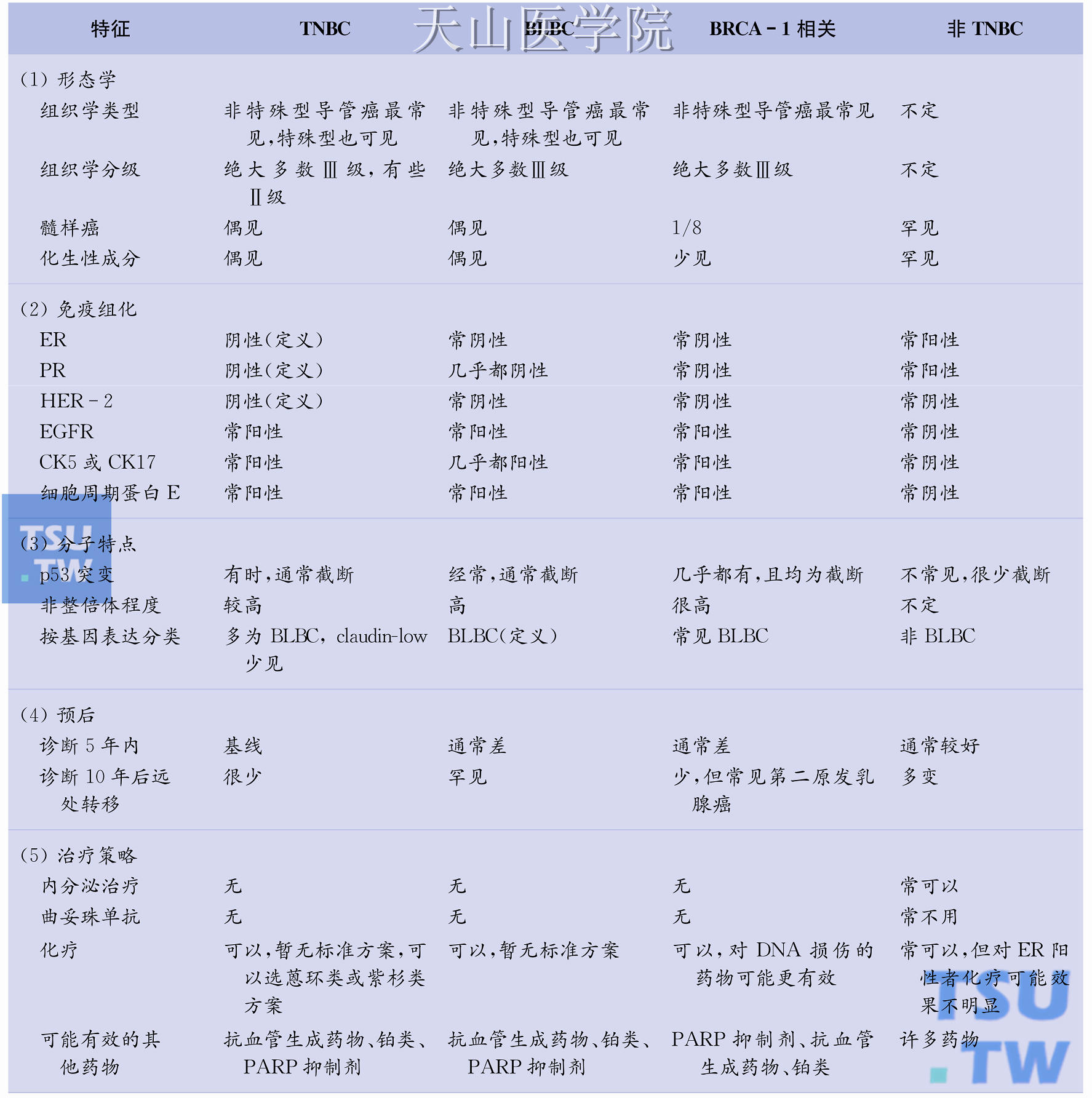
注:PRAP:多聚二磷酸腺苷核糖聚合酶;TNBC:三阴性乳腺癌。
CK和EGFR高表达型
许多研究表明,EGFR高表达在大多数三阴性乳腺癌的发生发展中起重要作用。Corkery等的研究认为与HER-2阳性细胞系比较,三阴性乳腺癌中存在EGFR的更高表达,并且EGF作用后可看到三阴性乳腺癌细胞系中EGFR的磷酸化。而EGFR的磷酸化可导致包括MEK/ERK和PI3K/Akt通路在内的下游信号转导通路的激活,引起相关基因的转录表达,从而抑制肿瘤细胞凋亡,促进肿瘤细胞生长、增殖、转移及血管生成,进而促进肿瘤发展。
EGFR信号通路是个非常复杂的网络,其中各种成分的基因表达水平在不同乳腺癌亚型中有所不同。三阴性/BLBC与EGFR/RAS/MEK通路中的许多基因如EGFR、转化生长因子-α(TGF-α)、MEK1、MEK2、Akt3等的高表达显著相关。而与三阴性乳腺癌的活化信号通路相关的几个基因,包括有丝分裂原活化蛋白激酶/细胞外信号调节激酶(MAPK/ERK)、PI3K/Akt、P38激酶和NF-κB在肿瘤中也比较常见。这些下游信号通路如PI3K/Akt通路、MAPK/ERK通路及NF-κB的活化在三阴性乳腺癌的发生发展中可能起关键作用,并可能作为三阴性乳腺癌治疗的靶点。
Umemura等发现三阴性乳腺癌中ERK1/2的磷酸化水平略高于其他组,而Akt激酶的磷酸化水平显著高于其他组。因此,他们认为Akt激酶的磷酸化水平增加是三阴性乳腺癌的特点,并且第一次在这种乳腺癌亚型中发现Akt通路的明显活化。其他研究者通过对三阴性乳腺癌肿瘤中表达的受体如EGFR、胰岛素样生长因子-1受体(IGF-1R)、HER-3和c-kit证实,肿瘤可通过Ras/Raf/MEK/ERK通路活化来增加细胞增殖潜力。Oliveras-Ferraros等在三阴性/BLBC MDA-MB-468细胞株的研究中也发现了这一现象,不仅检测到了EGFR过表达,还有EFGR细胞内下游信号通路的活化(如MEK/ERK通路和PI3K/Akt通路)。
因此,EGFR及其信号转导通路与三阴性乳腺癌的发生发展密切相关。该通路的异常活化能导致肿瘤细胞增殖、存活等,促进肿瘤发展。因此,阻断该信号通路的转导对于三阴性乳腺癌的治疗具有重大意义。
claudin-low亚型
claudin-low亚型以CD44+/CD24-/low作为标记特征,低表达封闭蛋白(claudin)及E-钙黏蛋白等细胞与细胞连接蛋白,高表达免疫应答基因,是上皮分化的较早阶段。大多数claudin-low亚型表现为三阴性乳腺癌,预后较差。
为了更好地将此型的特征进行标记,来自美国北卡罗莱纳大学的一项研究比较了一系列基因。与乳腺癌的其他类型相比,此型有1 308个基因处于明显高表达和359个基因低表达状态。主要表现为免疫应答(如CD79b、CD14和vav1)、细胞间趋化因子受体(C-X-C配体12)、细胞外基质(波形蛋白、成纤维细胞生长因子-7)、细胞分化(如KLF-2、白细胞介素-6)、细胞迁徙(整联蛋白-a5、膜突蛋白)和血管生成(血管内皮生成因子C、基质金属蛋白酶-9)等相关基因高表达;相反,上皮细胞与细胞间质黏附的相关基因如封闭蛋白3、4、7,闭合蛋白(occludin)和E-钙黏蛋白低表达或不表达,也缺乏管腔(luminal)分化标记如CK5、14、17,Ki-67增殖指数低。还有肿瘤干细胞或肿瘤起始细胞(tumor-initiating cell, TIC)标记CD44、CD24和ALDH1A1以及分化导管上皮细胞表面标记EpCAM、MUC1和CD49f。此型的CD24、EpCAM和MUC1低表达,而CD44、CD49f和ALDH1A1高表达。
此项研究还收集了分别来自UNC、NKI及MDACC 3个中心的337例、295例和133例患者的资料,将claudin-low亚型与其他5型的临床特征进行对比,结果此型占7%~14%,大多数ER/PR/HER-2均为阴性。相对于腔面A型,claudin-low亚型预后较差,其无复发生存期和OS更短。而与腔面B型、HER-2过表达及BLBC无显著差异。MDACC比较临床以蒽环类/紫杉类新辅助化疗后各型pCR率,显示claudin-low亚型的pCR率较BLBC低(38.9%对比73.3%,P = 0.08),但较腔面A型及腔面B型高。
