脑转移瘤较颅内原发肿瘤更为常见,常为多发性,亦可为单发性。好发部位为大脑中动脉供血区的灰白质交界区,亦可见于小脑及鞍区。其中13%~20%的原发癌为乳腺癌,成为继肺癌之后的第二大易发生中枢神经系统受累的疾病。乳腺癌脑转移常见于脑实质的转移,幕上转移多于幕下转移。50%~75%为多发性颅内转移灶,并且常伴有颅外转移,如淋巴结、肺、肝转移等。脑转移多出现在疾病的后期阶段。一旦出现脑转移,病情往往迅速恶化,预后大多不良。
流行病学及危险因素
近年来随着肿瘤患者生存期的延长和影像诊断技术的发展,乳腺癌脑转移的发生率逐年上升,有5%~21%的病例出现脑转移。尸检结果进一步证实,发生脑转移的比例达到26%~30%。乳腺癌患者初诊时的临床分期与乳腺癌脑转移的发生密切相关,早期局限性乳腺癌患者脑转移的发生率不到3%,局部晚期或高危乳腺癌患者脑转移的发生率为7%~8%,而晚期乳腺癌患者发生脑转移的比例达到10%~16%。乳腺癌发生脑转移病死率高,存活率低,严重影响患者的生存率和生活质量。
乳腺癌脑转移的危险因素包括年龄较轻(<50岁)、肿瘤负荷大(初诊时转移病灶>2个)、ER阴性、HER-2阳性以及组织学分级较高。底特律癌症检测系统统计结果显示,在20~39岁初诊为乳腺癌的患者中,有10%发生脑转移,而70岁以上患者脑转移发生率仅为3%。生物学危险因素中,研究最多的为HER-2状态与乳腺癌脑转移的关系。研究表明,HER-2阳性的乳腺癌患者发生脑转移的风险明显增高,为25%~40%。
转移途径及部位
脑实质转移瘤被认为是肿瘤细胞血行转移所致。转移灶的分布与人脑整体血运分布的一致性验证了这一观点。幕上是最常见受累的部位(80%),其次是小脑(15%)、脑干(5%)。此外,灰质白质交界处为常见的转移区域,与此处血管直径及血流变化有关。
早期试验表明,约有半数患者脑转移为单发病灶。然而随着MRI技术的引进,目前的一系列试验表明只有1/3~1/4的患者为单发转移灶。长期孤立的脑转移灶则常见于单纯脑转移而非全身转移的患者中。
临床表现
由于脑的影像学检查并不纳入无症状乳腺癌患者的常规检查中,脑转移多根据新发生的神经系统症状来诊断。患者可出现头痛、颅内压增高、局灶性神经功能障碍、认知功能障碍和癫癎发作等。
(一)头痛:大部分患者的首发症状为头痛,不久出现局灶性症状,这些症状可与颅内压增高的症状共同发展,日趋严重。
(二)颅内压增高的症状:颅内转移瘤即使结节很小,也能引起广泛的脑实质性反应和脑膜血管壁的渗透性损害,导致严重的脑水肿和脑脊液吸收障碍而造成明显的颅内压增高。由于颅内压增高出现早而急剧,且发展较快,其临床表现与颅内原发性肿瘤比较有一定差异。有些症状如头痛、智力改变、脑膜刺激征和嗅觉减退等表现较为明显,发生率也高。而另一些症状如视盘水肿、恶心呕吐的表现则较不明显,发生率也低。这一特点称为颅内压增高症状的两极分化现象。
(三)精神症状:颅内转移瘤患者的精神症状比原发肿瘤者多见且明显,这构成了诊断的重要依据。其表现可分为3型:①梦魇性谵妄症;②健忘症;③淡漠寡情与意志薄弱性症候群。开始时患者出现带戏谑性的躁狂情绪,逐渐对自己及周围情况的判断能力衰退,随之完全记忆缺失,然后患者显得软弱、淡漠寡情、意识错乱和定向不能,至晚期则进入昏睡状态。部分患者可有严重痴呆与谵妄发作。
(四)局灶症状的特点:单发转移的患者部分首先出现颅内压增高症状,少数患者则以局灶性症状发病,特别是位于额叶及顶叶的转移瘤患者。多发转移的患者其一般情况更为严重,恶病质早期出现,颅内压增高症状也更为显著,且常为暴发性的,发展迅速,患者很快进入垂危阶段。其局灶性症状可表现为偏瘫、失语及进行性意识改变等。转移灶分布在幕上和幕下都有者,出现局灶症状的同时,尚有极严重的阻塞性脑积水表现和小脑损害体征。
(五)癫癎:有10%~20%的乳腺癌脑转移患者主要症状为癫痫发作,且多出现在幕上转移的患者中,而在后颅窝受累的患者中较为罕见。
诊断
典型的脑转移瘤患者在乳腺癌发现后数周至数月出现脑部症状,对这种病例诊断不难。但有些病例,颅内转移症状可发生于乳腺癌根治以后多年,或转移症状不明显。这些病例诊断常有一定困难。各种辅助检查对确定颅内转移性肿瘤的诊断有一定意义。
(一)CT检查:CT平扫时脑内转移瘤可呈现低密度、高密度或等密度。这与肿瘤的细胞成分、血供情况、坏死或囊变程度,以及是否出血和钙化有关。典型的乳腺癌脑转移瘤多为低密度或等密度,也可为两者混杂密度,水肿明显。
CT强化能显示更多的病灶,绝大多数的转移瘤血供较丰富,经静脉注射的造影剂通过肿瘤血管渗入肿瘤内,故转移瘤经常显示不同程度的增强。在平扫时密度较高的转移瘤增强扫描时强化相对较弱,反之平扫密度较低者强化反而明显。实质性肿瘤往往显示均匀性增强,发生坏死、囊性变者则显示为不均匀增强,即肿瘤的实质部分增强,而坏死、囊性变区不增强。典型者不增强的坏死区、囊性变区为偏心性,轮廓不规则,即使坏死、囊变区较大增强的四壁也厚薄不均,可见有结节状突出。但也有部分病例表现为薄壁环状增强。
(二)MRI检查:脑转移瘤MRI表现为病灶多发,大脑半球或小脑内均可发生,病灶位于皮髓质交界区或皮质内,呈膨胀性生长,多呈圆形及类圆形,其外缘较光滑、清晰,大小一般为2.0~3.0cm,瘤内呈不均匀T1及T2信号,均有占位效应及水肿,常有坏死、囊变或出血。当早期转移病灶为单发时,肿瘤体积较小。增强后病灶呈不均匀性明显或中等度强化。
MRI增强扫描是目前公认的最佳检查方法,可以发现常规MRI平扫不能发现的较小转移灶。有学者认为,应用2倍或3倍剂量对比剂可以发现更多、更早的转移瘤,从而提高病灶的检出率,对无周围水肿的小病灶来说意义更大。由于血供丰富,脑转移瘤多有明显强化,在伴有囊变、坏死时,可呈环形强化;无囊变、坏死时,为均匀结节状强化(图59-1)。
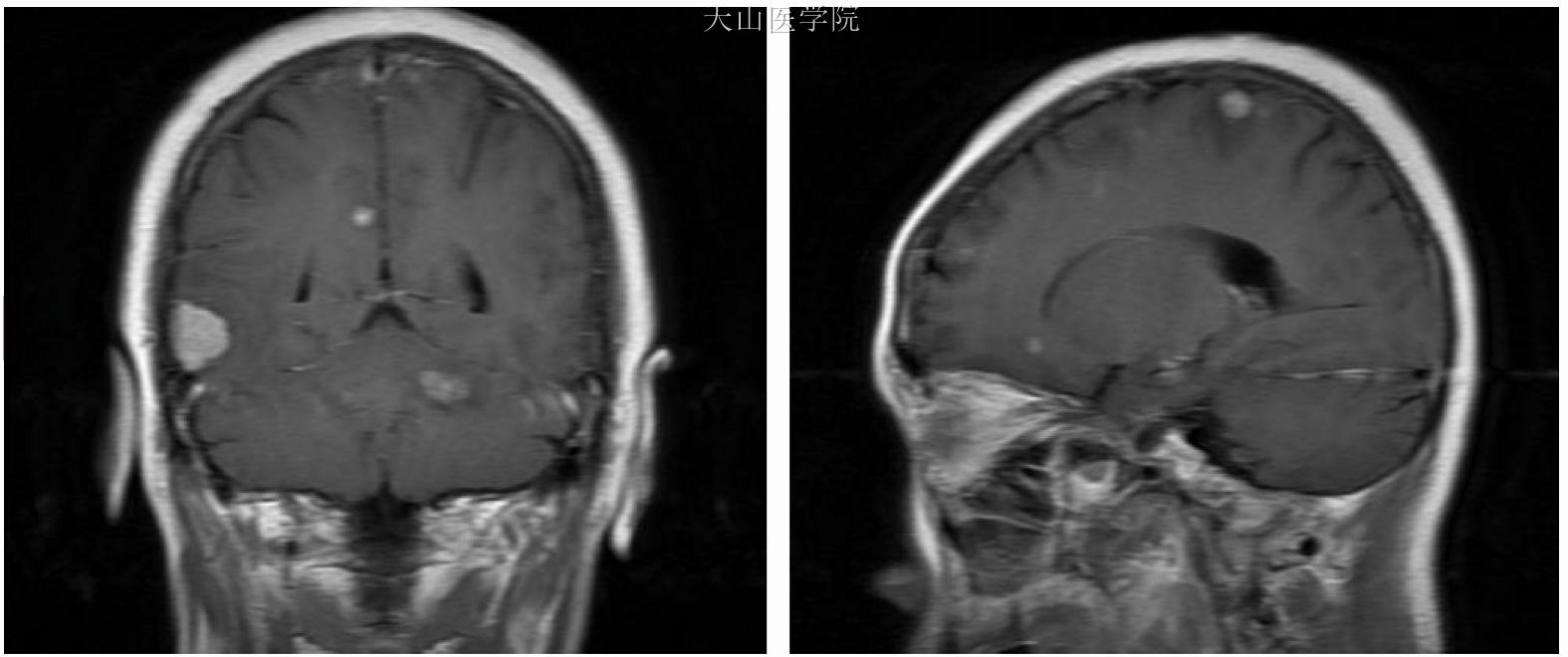
图59-1 乳腺癌脑转移的MRI表现
(三)X线检查:颅骨X线平片检查可发现部分脑转移瘤同时伴有颅骨转移,靠近颅骨的转移瘤,当侵及颅骨时X线平片可见颅骨骨质破坏甚至瘤结节,头颅X线上可有颅内高压迹象。
(四)同位素脑扫描:同位素脑扫描可在转移灶处见到同位素的积聚,特别是对于多发性转移灶常能据此作出鉴别。
(五)脑电图检查:如转移灶位于大脑半球,则脑电图上的病灶变化可很明显(δ波和Θ波),且范围大于病灶所居的位置。一般性变化也很明显和广泛。大脑多发性转移时,在脑电图上有时可看到一个以上的病灶性表现。
(六)周围血液检查:红细胞沉降率增高可见于约90%的患者。单发性颅内转移的红细胞沉降率平均为10~20mm/h,多发性脑内转移的红细胞沉降率平均为20~35mm/h;脑膜弥漫性转移的红细胞沉降率平均为30~60mm/h。
(七)脑脊液检查:颅内转移瘤患者的脑脊液变化有蛋白含量增高,糖含量常显著降低,而细胞数一般不增加。有些病例中可查到肿瘤细胞,以脑膜弥漫性转移时阳性率最高。
(八)其他检查:CT引导下穿刺活检是有创性检查,在CT引导下可准确地对肿瘤部位进行穿刺,获得病理学证据,排除原发颅内肿瘤,避免误诊误治。另外,如原发肿瘤已治愈多年,颅内孤立性病灶难以排除转移癌,或颅内占位性病灶诊断不明者,也可在经选择的条件下行手术探查确诊。脑血管造影曾是神经外科最常见的检查方法,由于造影引起痛苦较大,操作复杂,且有一定的危险性,患者常难以接受。
五、鉴别诊断
颅内单发转移瘤需与胶质瘤、脑膜瘤等鉴别,较为困难,容易造成误诊。多发性转移瘤需要与颅内多发性脑脓肿、多发性脑膜瘤、脑出血、脑梗死、血管网状细胞瘤、多发性硬化脑白质病等鉴别。
(一)胶质瘤:特别是胶质母细胞瘤在病史和影像上均与转移瘤有相似之处。但胶质瘤很少多发,无原发肿瘤病史,瘤周水肿多呈片状,而转移瘤多呈指套状。
(二)脑膜瘤:主要是幕下脑膜瘤与单发结节型脑转移瘤相鉴别。转移瘤可找到脑外原发瘤,与小脑幕无关系;而脑膜瘤无脑外原发瘤,与小脑幕关系密切,且重度强化,其程度远大于轻中度强化的结节型脑转移瘤。
(三)脑脓肿:脑脓肿和囊性转移瘤在影像上很难区分。一般靠病史鉴别,如多有感染病史、心脏病病史、中耳炎病史等,而转移瘤可有肿瘤病史。
(四)脑出血:当转移瘤卒中出血时,呈急性发病,需与脑出血相鉴别。一般强化CT和MRI检查在转移瘤的患者可见肿瘤结节。另外,还可根据出血的部位、形态、有无高血压病史来判断。
(五)血管网状细胞瘤:病灶多位于幕下小脑半球,呈囊实性改变,表现“大囊小结节”。增强扫描,小结节增强明显,瘤周可见流空血管影。
治疗
乳腺癌患者出现脑转移多提示预后不良,但是脑转移患者的死因不仅是由于神经系统症状导致,还包括了全身疾病的进展,所以局部治疗联合全身治疗,既可提高颅内肿瘤的控制率,还能改善全身症状。目前手术、立体定向放射外科学(stereotactic radiosurgergy, SRS)、全脑放疗(whole-brain radiotherapy, WBRT)为脑转移的一线治疗方法,但随着综合治疗的发展,化疗、内分泌治疗也取得了一些进展。
对症治疗
对病情危重不能耐受手术或急性恶化垂危的患者,首先给予药物对症治疗,如激素、脱水药等,一般都能迅速缓解高颅压的症状,待病情平稳后再采取其他治疗方法。激素是脑转移瘤的基础治疗,对70%的患者有效。但单用激素治疗的平均生存期只有2个月,故通常与其他治疗联合应用。控制颅内高压症状时还应使用脱水及利尿剂,控制癫痫采用苯妥英钠、地西泮等药物。
20世纪60年代,皮质激素被首次应用以降低转移瘤周围异常血管的通透性,减少肿瘤水肿或与放疗有关的水肿;在80%的患者,皮质激素常可在24小时内逆转神经系统症状。地塞米松由于其盐皮质激素活性低而最常应用。常在放疗期间给予激素,使用能控制神经系统症状的最低剂量。20%的患者长期服用激素以逆转或稳定神经系统症状。
全脑放疗
在过去的50年中,WBRT在脑转移的治疗中起核心作用。可改善49%~93%的患者的神经系统症状。神经系统恢复的程度与放疗前症状的严重程度成反比。对多发脑转移瘤或单发的手术难以接近的病灶可给予全脑外照射。WBRT的目的是根除显微镜下可见的肿瘤病灶。对于接受WBRT的乳腺癌脑转移患者,预期中位生存为4~6.5个月,而仅接受支持治疗的患者,其预期中位生存则为1~2个月。而且,WBRT可以有效缓解神经症状,70%~90%的患者神经症状可以得到持久改善或者保持稳定。同时也有研究显示,WBRT可以降低颅内病灶的复发,消除微转移病灶和降低因神经系统症状引起死亡的可能性。
1.WBRT的适应证:WBRT适用于颅内多发肿瘤、瘤体直径<3cm、肿瘤位于不适合手术或SRS以及一般状况尚可的患者。
2.WBRT的不良反应:尽管WBRT治疗乳腺癌脑转移能有效缓解患者症状,提高生活质量,延长患者生存期,但其并发症较多,包括急性和迟发性不良反应。急性不良反应发生于放疗后90天内,包括恶心、呕吐、脱发、失聪、急性或亚急性皮肤反应、嗜睡,大多数急性不良反应都可在治疗结束后消失。迟发性不良反应在放疗90天以后才出现,包括坏死、性格及记忆改变、认知缺陷等。
立体定向放射外科学
乳腺癌脑转移患者的局部治疗,除WBRT外还可选择SRS治疗。SRS是指利用γ线、X线或荷电粒子束和立体定向系统的精确定位,将高能量放射线聚焦照射在某一局部靶区内,摧毁该区域内的所有组织,或引起所需要的生物学效应。SRS因其高精确度、微创性等特点,目前已广泛应用于脑转移瘤的治疗。SRS适应于颅内1~3个转移灶、瘤体大小<3cm、全身疾病被控制及KPS评分较高者。有报道称SRS的局部控制率可达85%,最佳剂量为不少于18Gy。RTOG 90-05研究已确定,肿瘤最大直径为31~40mm、21~30mm和≤20mm的最大耐受剂量分别为15、18、24Gy。而最近的回顾性分析表明,对于直径≤20mm的肿瘤,剂量>20Gy不增加局部控制率而徒增毒性反应。还有研究结果显示,单独应用SRS治疗脑转移瘤患者的中位生存期为10.5个月。Firlik等报道30例经SRS治疗的乳腺癌脑转移患者的中位生存期为13个月。但是另有研究表明,单独进行SRS会增加脑转移患者的颅内复发风险,而SRS联合WBRT可提高局部控制率,降低局部复发风险,但在提高生存率方面无显著差异,同时增加了放疗的并发症。其联合应用仍在进一步研究中。
手术
手术治疗适用于浅表的转移病灶、病灶多为1~2个、KPS评分较高、无脑外转移灶及一般状况好的脑转移患者。手术治疗单发的乳腺癌脑转移患者的中位生存期可达12个月,这也与手术患者的一般状态较好有关。遗憾的是,临床上仅有20%~30%的脑转移患者适合手术治疗。术后辅助放疗可降低局部复发率,但并没有研究证实可以提高生存率。
两项回顾性随机试验对乳腺癌脑转移的患者手术治疗效果进行了评估。一项是由Patchell等报道,将48例存在单个脑转移的患者(6%原发部位为乳腺)随机分为手术联合WBRT组和单纯WBRT组。发现联合组总生存期较长(两组分别为40周和15周,P < 0.01)。Noordijk等的一项对63例脑转移患者(19%原发部位为乳腺)分析的临床试验也得到相似的结果,接受手术联合WBRT的患者较单纯WBRT组生存期延长,两组中位生存期分别为10个月和6个月(P = 0.04)。
对多发性脑转移瘤患者是否接受手术治疗,仍存在争议,且目前得到的数据仅为回顾性研究结果。多数研究认为,手术不能缓解高颅压的症状,但为延长患者生命和改善生活质量,也可手术切除占位大的“责任肿瘤”,位于“哑区”的转移瘤可行脑叶切除,待高颅压缓解后,再行放、化疗。手术定位要准确,力争全切肿瘤,如开颅后高颅压脑组织肿胀,可采取各种方法降低颅压,这样手术后效果佳、死亡率低。一项对56例多发脑转移患者手术治疗后的分析研究显示,相对于脑部仍留有未切除转移灶的患者而言,那些切除全部脑转移瘤的患者其生存期可得到改善。Wronski等报道了一项回顾性研究结果,70例乳腺癌脑转移患者中,单发脑转移与多发脑转移在接受手术治疗后,其生存并没有统计学差异。
化疗
对放射线不甚敏感,或无法接受手术和(或)放疗的患者,化疗是重要的姑息治疗手段。有效的化疗可以消除全身各处的微小转移灶及脱落的癌细胞,防止转移,放疗加化疗的中位生存期高于单纯放疗,是延长生存期的重要因素。有人认为化疗药物很难通过血-脑屏障,而另有学者认为脑转移瘤在形成转移灶的过程中,自始至终就没有形成完整的血-脑屏障,脑转移瘤对血-脑屏障有一定破坏,化疗对脑转移瘤有一定效果。到目前为止,尚没有化疗药物获得美国FDA批准用于治疗乳腺癌脑转移。一些病例报道及研究分析结果显示,环磷酰胺、甲氨蝶呤、卡培他滨、顺铂、依托泊苷、卡莫司汀等药物,在治疗乳腺癌脑转移方面可起到一定的积极作用。但由于耐药问题,后期疗效较差,一般不作为首选治疗手段,可以作为手术或放疗的辅助治疗。
靶向治疗
目前,越来越多的靶向治疗药物进入乳腺癌治疗的临床研发当中,包括那些抑制HER-2、Ras/Raf、PI3K和血管生成途径的药物。然而,除了少部分研究,起初的临床试验都将活跃的脑转移纳入排除标准。已有的研究结果显示,曲妥珠单抗、拉帕替尼、贝伐单抗等靶向治疗药物显示了良好的治疗潜力,进一步的研究正在进行当中。
预后
影响患者预后的因素包括全身器官及神经系统功能状况、年龄、原发瘤情况(病变部位及范围、病理类型、是否已控制)、脑转移瘤的数量及部位、手术切除情况、有无颅外转移灶、有无复发、原发灶至转移灶出现的时间间距等。Shu等认为,病灶体积小、无颅外转移灶、较高的KPS评分(≥70分)、年龄<70岁等对于延长生存期是积极因素。Rutiglian认为放射外科治疗脑转移瘤无论在一般状况、生存率、安全性及死亡率等方面均优于外科手术加全脑的普通外照射治疗。
