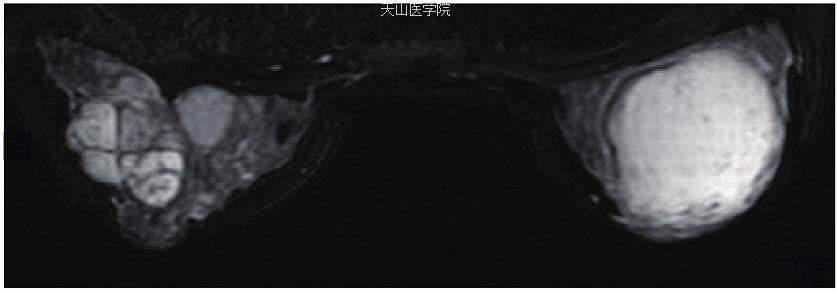
纤维腺瘤
病理及临床特点
纤维腺瘤是最常见的乳腺良性肿瘤,是来源于乳腺小叶内纤维组织和腺上皮的一种良性双向分化的肿瘤。有时间质成分可表现为富于细胞,并可见透明变性、黏液变性、化生及灶性囊变,完全性梗死较罕见。但纤维腺瘤中极少见导管原位癌和小叶原位癌发生。纤维腺瘤最常发生在育龄期妇女,尤其是30岁以下,但任何年龄均可发生。临床表现为无痛性、孤立、质硬、生长缓慢、可移动的界限清楚的结节。少数情况下肿瘤可同时或先后在同侧或双侧乳腺形成多发结节。有人认为大部分纤维腺瘤长至2~3cm即达稳定状态。也有研究认为经过一定时间的生长,40%的纤维腺瘤会自然消失,10%变小,20%基本不变,约30%的肿瘤则继续生长。有的肿瘤可生长达20cm,但主要发生在青春期,称为巨纤维腺瘤。随着MRI的广泛应用,越来越多的小的不可扪及的纤维腺瘤被发现。
影像学表现
MRI表现取决于其组织学成分,瘤内以腺管增生为主、纤维组织较少时称为腺纤维瘤(图11-55),多见于年轻妇女;以纤维组织增生为主、腺管数量少时称为纤维腺瘤,多见于绝经后妇女(图11-54);若含黏液较多时,则称为黏液样纤维腺瘤(图11-56)。
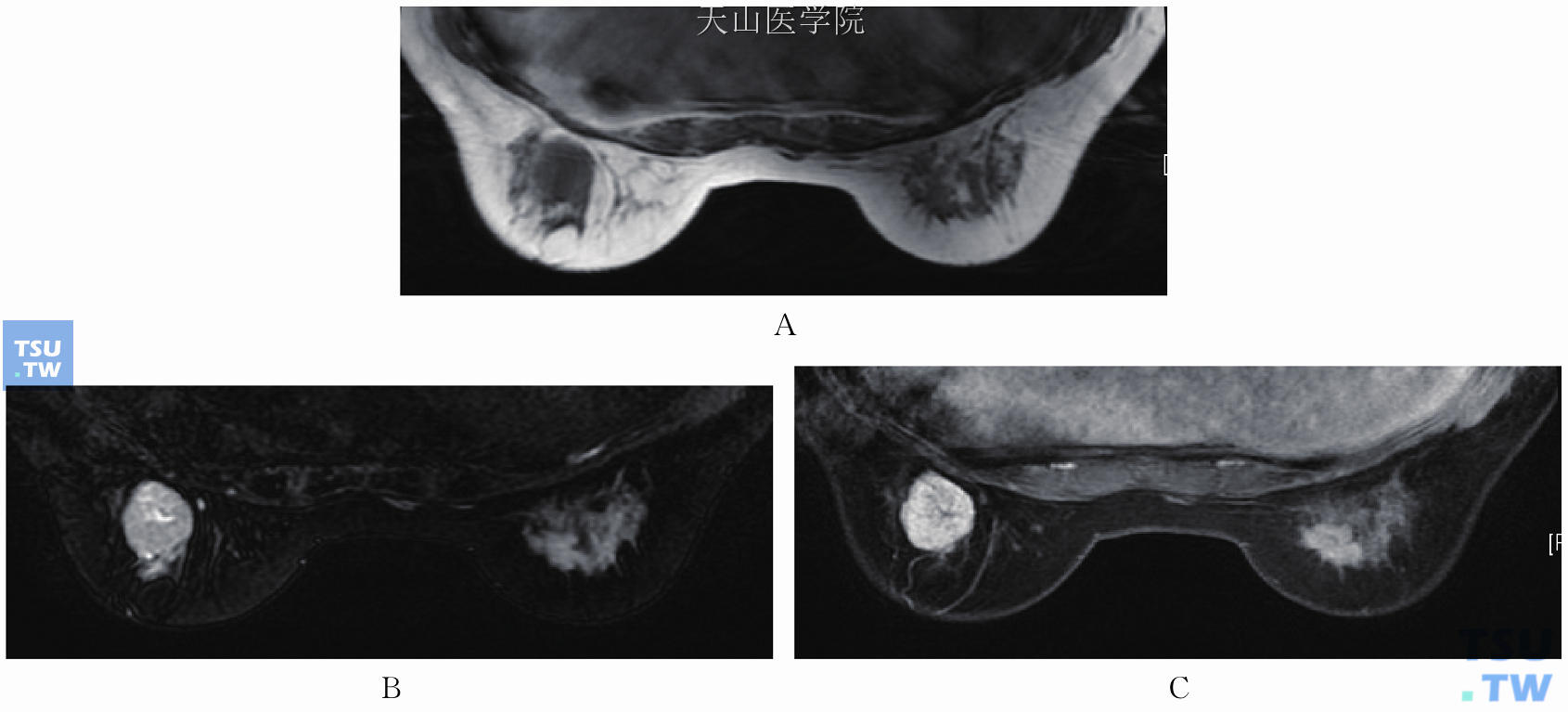
图11-55 左乳腺管纤维腺瘤。T1WI低信号(A),T2WI高信号内见裂隙状更高信号(B),提示肿瘤内囊性,增强后明显均匀强化(C),囊变区无强化。右乳星芒状肿块,为浸润性导管癌
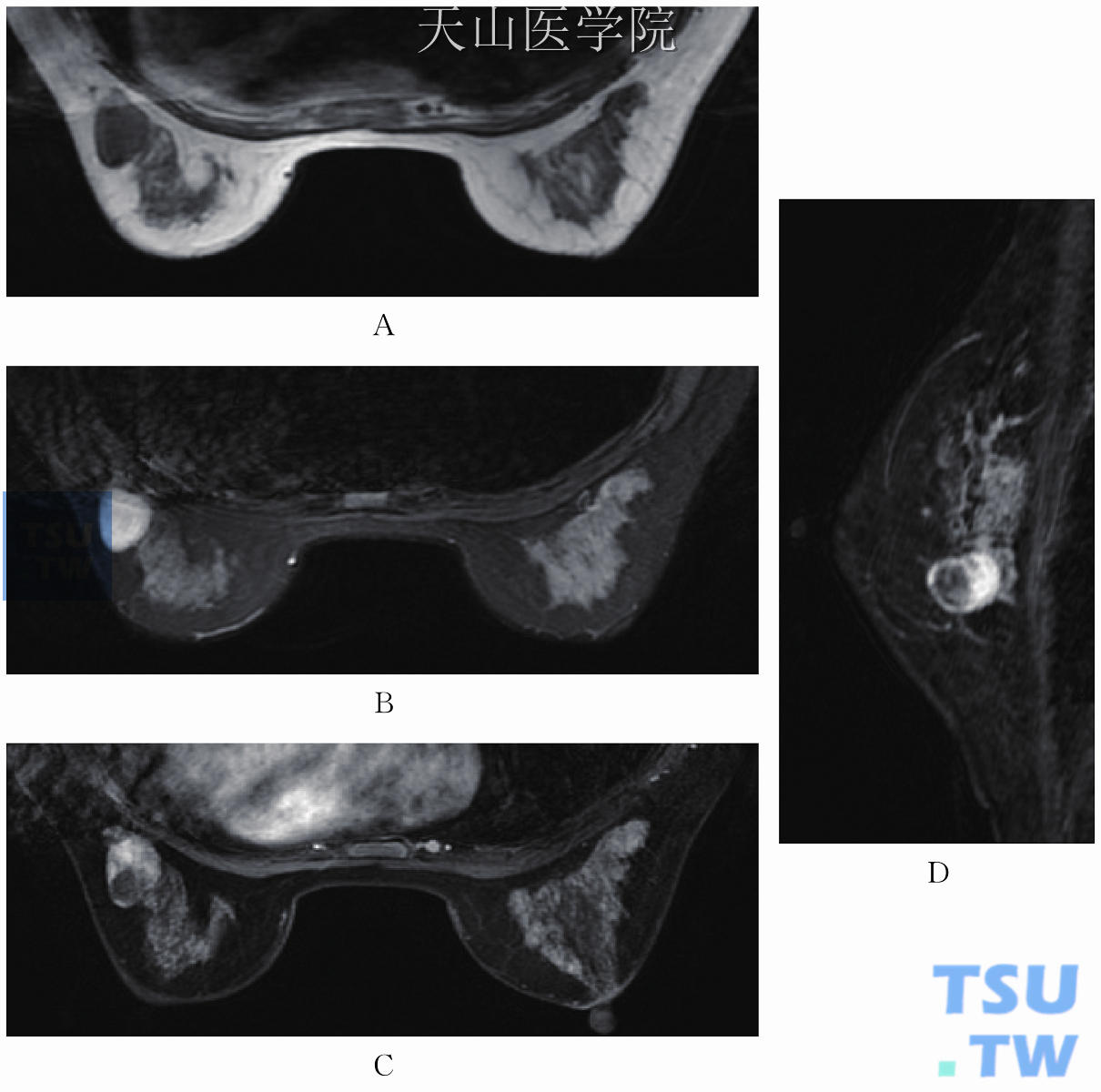
图11-56 左乳纤维腺瘤。T1WI低信号(A),T2WI高信号(B),增强扫描(C、D)提示实性部分明显均匀强化,囊性部分不强化
(1)形态学表现:纤维腺瘤在MRI上表现为圆形、类圆形或分叶状肿块,形状规则,边缘光滑,可有较完整包膜,内部信号均匀一致,多发者大小不一。病灶内信号因其组织成分,即肿瘤内细胞、纤维及水的含量不同而表现不同。T2WI平扫信号高低不一,细胞成分多者或有黏液变性者呈高信号,纤维成分多者呈低信号,钙化区无信号。T1WI多呈低信号,与周围腺体分界清晰或不清。肿瘤内细胞丰富者增强迅速,均匀一致;硬化、纤维成分较多的纤维腺瘤增强MRI不强化或轻度强化(图11-55)。肿物内部有T2WI低信号,增强后不强化的纤维分隔者为纤维腺瘤的典型表现(图11-57),特异度为86%~93%,见于40%~60%的纤维腺瘤。瘤内有广泛钙化或透明变性者可以不强化,完全性梗死罕见(图11-58)。
图11-57 左乳纤维腺瘤,右乳梗死性纤维腺瘤:T2WI显示左乳高信号的肿块内可见低信号的分隔;右乳肿块高信号,边缘见低信号的环
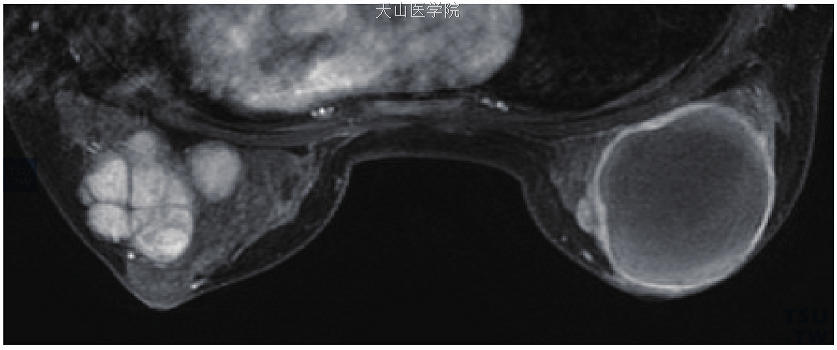
图11-58 为图11-57患者增强图像,左乳低信号的分隔未见强化,右乳仅见边缘强化
(2)时间-信号曲线:有60%~83%乳腺纤维腺瘤动态增强曲线为持续上升型,即表现为缓慢渐进性均匀强化或由中心向外围扩散的离心性强化。有11.5%~35%表现为平台型。廓清型较少见,约占2%,多发生在黏液性或乳腺纤维瘤中。
鉴别诊断
需与分叶状肿瘤、管内乳头状瘤、浸润性导管癌、淋巴瘤等鉴别。
囊肿
1.病理特点:乳腺囊肿是由于各种原因引起的导管、腺泡扩张或分泌物潴留,经包裹而形成。常见的有单纯性囊肿、积乳囊肿、表皮包裹囊肿等。囊肿可为单侧或双侧,单发或多发,多数囊肿合并其他病变存在。
2.影像学表现:囊肿根据囊液成分不同其MRI表现各异。单纯性囊肿呈典型T1WI均匀低信号,T2WI上显示为圆形,边缘光整锐利、均匀一致的高信号影,增强后无明显强化(图11-48)。
积乳囊肿因囊肿内成分不同其MRI表现也不同。早期因水样成分较多,MRI表现类似单纯囊肿。后期根据囊肿中脂质和蛋白含量的不同其表现的信号有所不同,脂肪和蛋白含量较高可表现为T1WI、T2WI高信号,抑脂后呈T1WI、T2WI低信号或等信号。
囊肿内出血可表现为T1WI、T2WI高信号,或T1WI高、T2WI低信号。
增强后一般囊壁和囊液均无强化,若囊肿感染则囊壁可呈环形强化。
3.鉴别诊断:单纯囊肿,MRI可明确诊断。积乳囊肿需与脂肪瘤(图11-53)鉴别。
乳腺病
病理及临床特点
乳腺病是一种常见的良性增生性病变,最常见于20~40岁的妇女,主要影响乳腺实质的小叶(腺泡)成分,可合并纤维化,导致腺体扭曲变形,形态可类似乳腺浸润癌,大体上缺乏特点,表现为非特殊的纤维性或囊性的乳腺组织。病灶通常较小,但可以广泛分布。乳腺小叶增生主要是腺泡数量增多,小导管扩张,小叶内及周围淋巴细胞浸润;乳腺囊性增生是小叶导管扩张并形成多个含液小囊;乳腺腺病是小叶内末梢导管或腺泡数目增多,同时伴有小叶内间质纤维组织不同程度的增生,部分腺病形成可触及的包块,称为结节性腺病或腺病瘤;硬化性乳腺病为乳腺小叶内管泡呈腺瘤样增生,伴有小叶纤维组织呈放射状增生,腺体扭曲变形,常常伴有钙盐沉积,无论在大体标本或显微镜下均酷似浸润癌;放射性瘢痕是由于硬化造成乳腺小叶结构破坏,导致影像学、大体和低倍镜检查类似浸润性乳腺癌的良性增生性改变。
影像学表现
(1)形态学表现:无特异性。T1WI、T2WI平扫多无阳性发现。增强后表现为非肿块样强化,呈区域性(图11-59)、点彩状或弥漫分布,部分病灶可不强化。由于伴有间质压缩或腺体扭曲,有时病变亦可呈星芒状结节或肿块样,与乳腺癌难以鉴别。以囊性增生为主的病变,在T2WI上某个区域可出现小的高信号小囊聚集,增强后无强化,但病变周围可出现斑片状浅淡强化;较大的囊肿,在T2WI上呈现接近水的高信号,增强后无强化;如果伴有感染,可出现囊壁的强化。
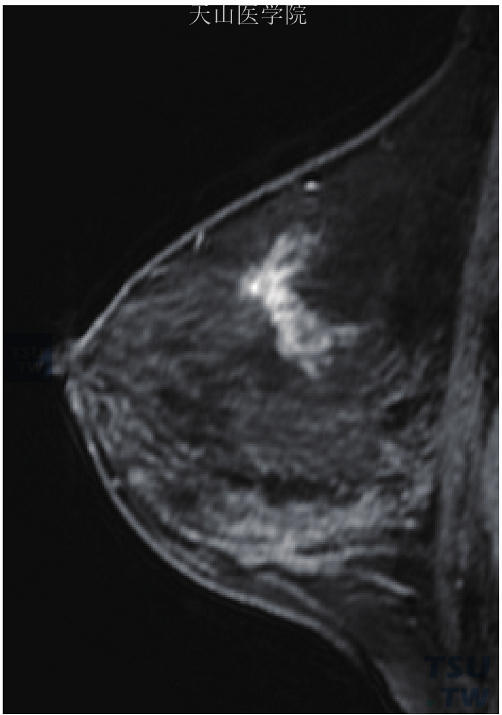
图11-59 左乳乳腺病,左乳外上区域性非肿块样强化,病灶与腺体垂直
(2)时间-信号曲线:乳腺病的强化方式随月经周期变化,腺体弥漫和局灶性强化在月经的第1周和第4周尤为明显,而第2周即月经中期时有改善,利于病灶边缘的显示。绝经后激素替代疗法的妇女也会出现弥漫和局灶性强化,一般建议停止治疗1个月后再进行MRI检查。乳腺病的强化多为持续上升型或平台型。
鉴别诊断
乳腺病的形态有时与恶性病变难以鉴别,需行活检。
(1)硬化性乳腺病:T1WI多为低信号,T2WI呈不均匀高信号,增强后持续明显强化,其内可见线样无强化影。以非肿块样强化及星芒状结节样强化多见,呈区域性(图11-60)或段样分布,肿块样强化相对少见。
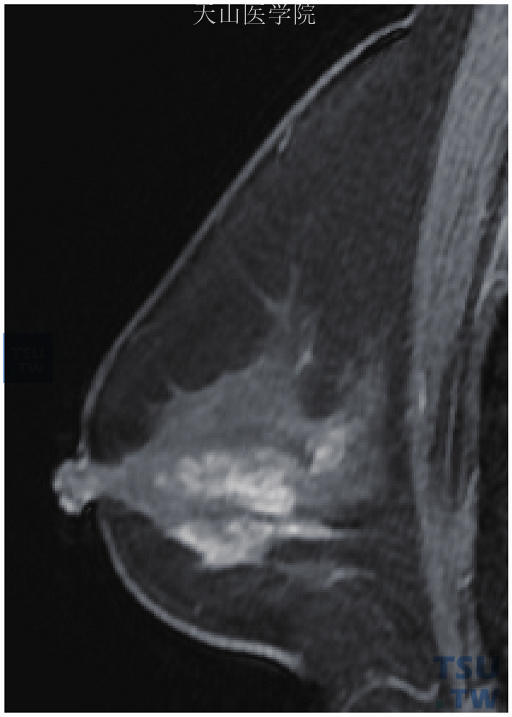
图11-60 右乳乳腺病,呈区域性分布的非肿块样强化
(2)手术后瘢痕:常表现为腺体结构紊乱,纠集呈放射状,钼靶上病灶的中心往往可见透光区,结合手术史,不难诊断。
(3)放射性瘢痕:在脂肪组织的衬托下可出现致密异常信号区,边缘见放射状长毛刺,不抑脂的T1WI图像上为低信号,动态增强后表现为轻度延迟强化。
(4)导管癌:乳腺病表现为肿块者,需与浸润性导管癌鉴别;表现为非肿块样强化,则需与导管原位癌、浸润性导管癌等鉴别。
导管内乳头状瘤
病理及临床特点
真正的导管内乳头状瘤发生在较大的乳晕下导管内,是引起浆液性或血清样溢液的最常见病变,起源于导管上皮,以纤维血管轴为支撑,肿瘤可位于导管系统内任何部位,从乳头到终末导管小叶单位。根据发生部位分为中央型(位于乳晕下区大导管内)和周围型(源自终末导管小叶单位)。中央型导管内乳头状瘤(central papilloma)常为单发,少数也可同时累及几支大导管。周围型乳头状瘤(peripheral papilloma)又称乳头状瘤病,常为多发,源自中、小导管,并可由此向更大导管延伸。通常一个导管内可见2~3个病灶,乳头溢液也少见,临床上往往有可触及的肿块。乳头状瘤病往往伴有非典型增生、导管原位癌,甚至恶性病变。有研究发现,乳头状瘤病与乳腺癌风险增高相关,但任何增高的风险几乎都与上皮非典型性增生的区域密切相关,而不是乳头状瘤本身(图11-61)。
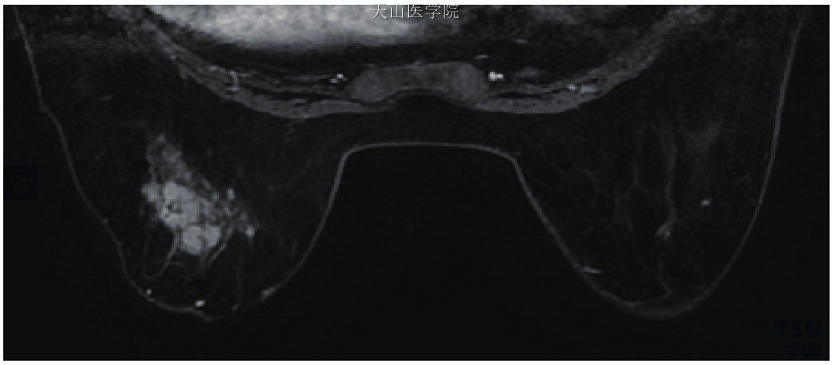
图11-61 左乳乳腺病伴导管内乳头状瘤(周围型),导管上皮高度增生伴局部癌变,左乳晕后方多发小结节
导管内乳头状瘤占乳腺肿瘤的1%~1.5%,多见于经产妇,以40~45岁较多见。发病与雌激素过度刺激有关。临床症状主要为单侧乳腺血性或浆液性乳头溢液,较少形成可触及的肿块,肿块直径很少超过3cm。
影像学表现
(1)形态学:导管内乳头状瘤典型的MRI表现为小于3cm的单发肿块,边缘光整伴导管扩张(图11-62)。囊性乳头状瘤可表现为乳腺内肿块,位于乳头后方大导管区或外周,T1WI低信号、T2W1中等或高信号影;纤维含量较高的乳头状瘤如硬化性乳头状瘤,可表现为T1WI、T2WI低信号。大导管内乳头状瘤常伴有导管扩张,但扩张导管多位于近乳晕的部分,而不一定在肿瘤梗阻的远端,可能与上皮的分泌、吸收功能失调有关,而不是单纯梗阻引起的机械性改变。扩张导管的信号表现不一,蛋白含量高者多呈T1WI高信号,蛋白含量低者则呈T1WI低信号、T2WI高信号。
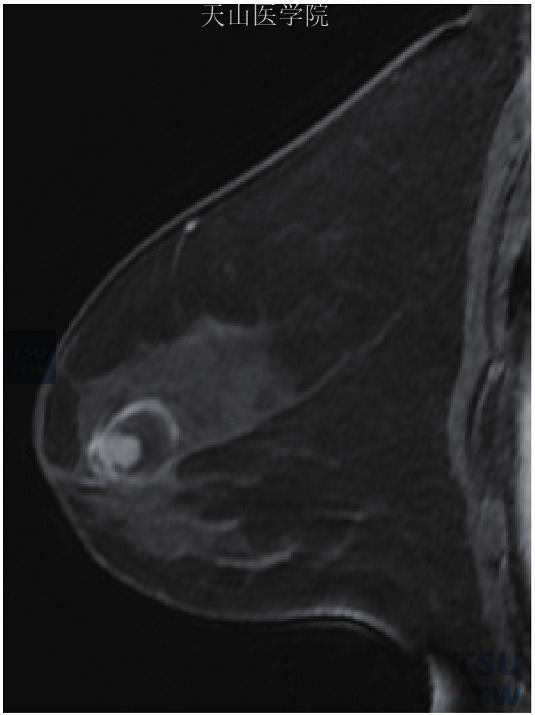
图11-62 左乳导管内乳头状瘤,左乳晕后方圆形囊性结节伴囊内持续强化的小结节
(2)时间-信号曲线:增强扫描后多数乳头状瘤呈不同程度的强化,以延迟强化多见,时间-信号曲线多为持续上升型,也可为平台型,少数为廓清型。硬化性乳头状瘤可无强化或强化较轻。
鉴别诊断
导管内乳头状瘤以乳头溢液为首发症状,首先需与引起乳头溢液的疾病相鉴别,如乳腺导管扩张或导管周围炎症、囊内乳头状癌、导管原位癌或浸润性导管癌等,可通过乳腺导管镜来明确。其次需与纤维腺瘤鉴别。
乳腺炎
病理及临床特点
乳腺炎症(mastitis)在临床上并不少见,根据临床病程可分为急性炎症和慢性炎症。也可分为哺乳期乳腺炎(puerperal mastitis)和非哺乳期乳腺炎(non puerperal mastitis)。
乳腺急性感染常见于妊娠或哺乳期妇女,尤以初产妇多见。由于产后乳汁淤积、细菌侵入、排乳不畅引起,有明显的患侧乳房红、肿、热、痛、皮肤增厚等临床表现,可有腋窝淋巴结肿大。急性乳腺炎少见的原因也包括外伤或手术后。临床上具有起病急、症状重、变化快等特点。急性乳腺炎若治疗不当或不及时,可转为慢性炎症。
非哺乳期乳腺炎包括许多亚型,如新生儿乳腺炎、乳头炎、输乳管细菌感染伴脓肿及窦道形成、浆细胞性乳腺炎、肉芽肿性乳腺炎等,以导管周围炎和浆细胞性乳腺炎最常见。临床特点为全身症状不明显,而乳腺局部症状较为明显,几乎所有患者都有可触及的肿块,有反复发作倾向,发病率不到10%。
影像学表现
急性乳腺炎MRI常表现为形状不规则、边界不清的斑片状或大片T1WI低信号、T2WI高信号影。周围的导管、腺体组织等结构紊乱,纤维组织及血管局限性扭曲。如累及皮肤,则局部皮肤增厚。增强后病变区呈不规则的斑片状或弥漫性轻到中度强化,延迟强化多见(图11-63)。
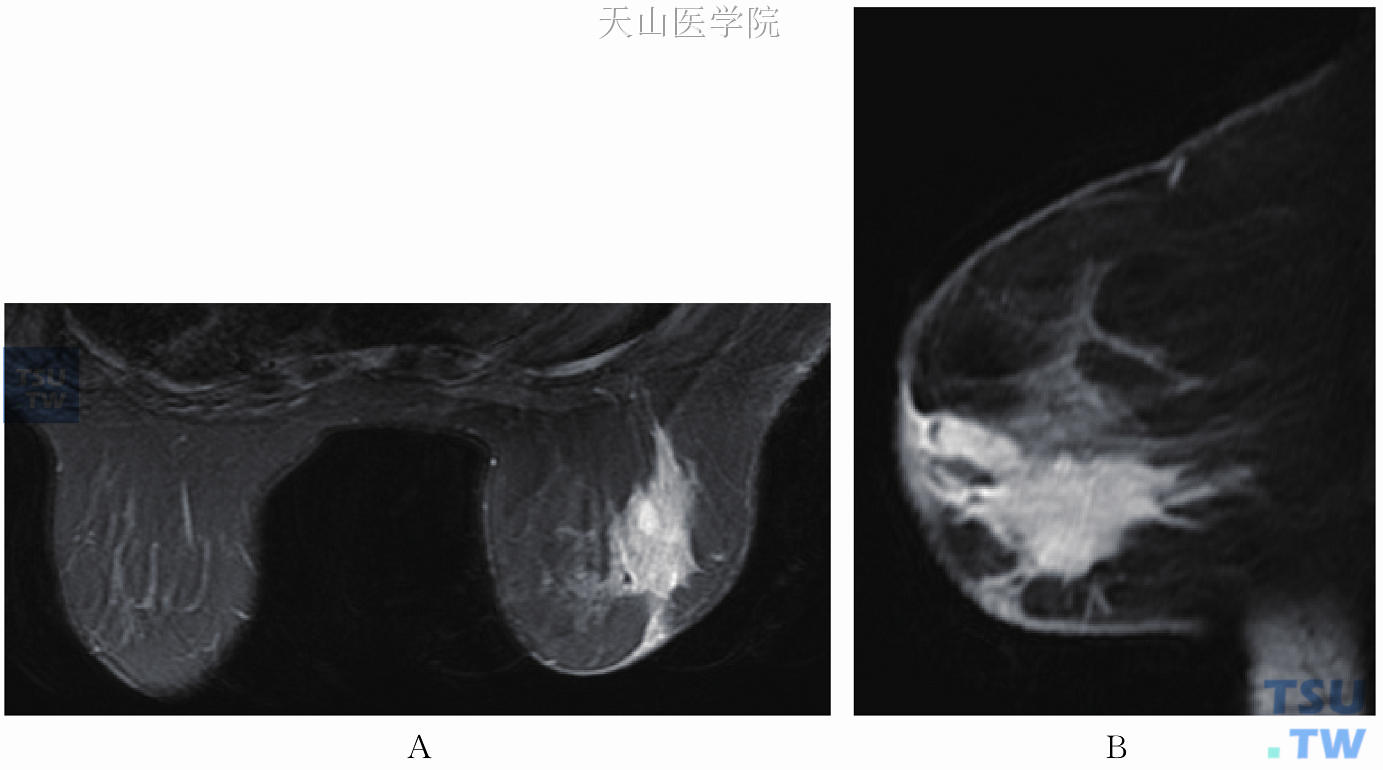
图11-63 患者43岁,发现右乳肿块。T2WI大片高信号内见更高信号(A)。增强后弥漫性持续强化,呈段样分布,局部累及皮肤伴Cooper韧带增厚(B)。病理诊断为右乳慢性炎症伴化脓性炎症及肉芽肿形成
急性乳腺炎若进一步发展则形成脓肿(图11-64)。脓肿可扩大向浅部穿破皮肤,若引流不畅可形成乳瘘;向深部可穿至乳腺与胸肌间的疏松结缔组织,形成乳腺后脓肿。脓肿在MRI上表现为边界清晰或部分清晰的T1WI低信号、T2WI高信号,呈圆形或类圆形。脓肿壁可表现为T1WI略高信号或等信号,T2WI高信号或等信号的环。脓肿不成熟时,环状壁可厚薄不均;脓肿成熟后,脓腔壁厚薄均匀完整。中心坏死区呈T1WI低信号、T2WI高信号,周围可见水肿,或炎症刺激形成的长短不一的条索状影。增强后脓肿壁呈均匀环状强化,强化程度随脓肿不同时期而异。中心坏死及周围水肿无强化。
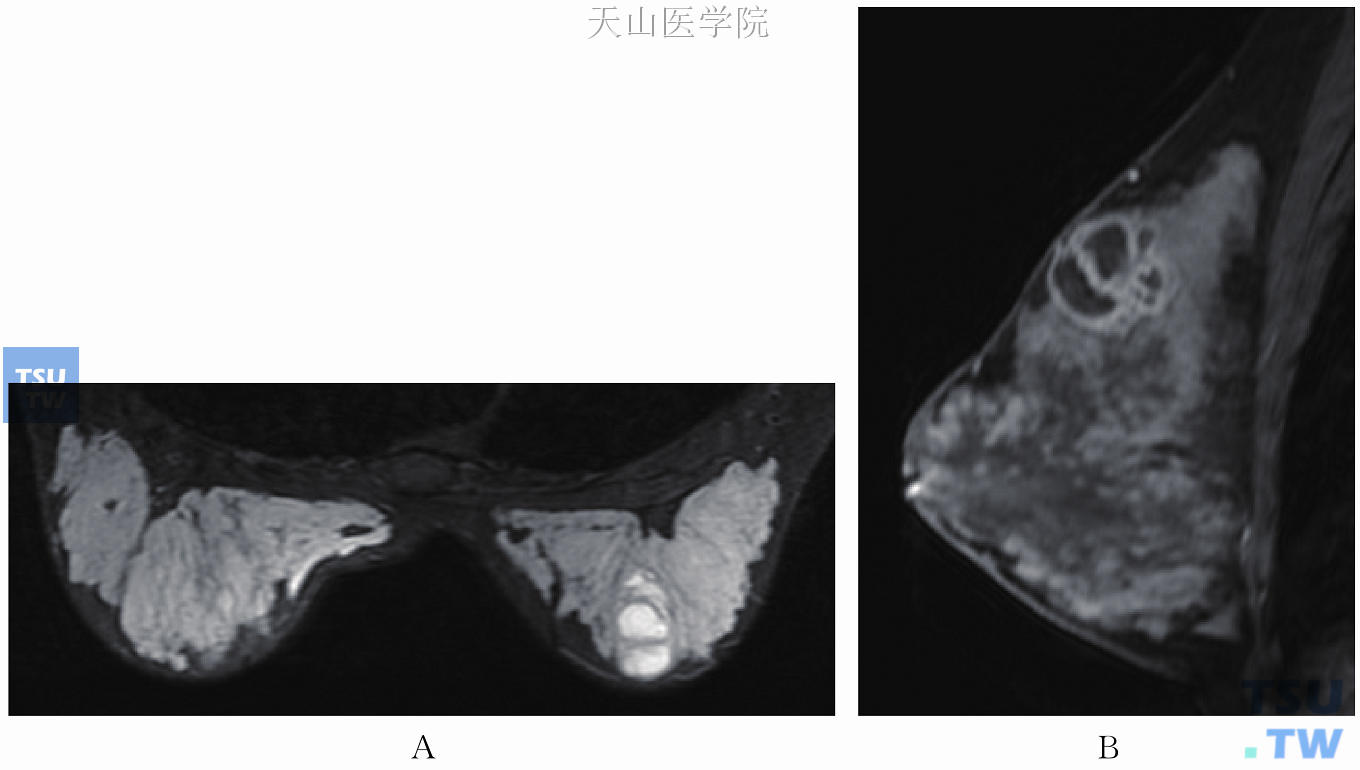
图11-64 患者22岁,哺乳3个月,哺乳期乳腺炎伴脓肿形成。右乳内上肿块,T1WI低信号伴等信号的脓肿壁(未显示),T2WI高信号伴等信号的环(A);增强后脓肿壁呈均匀的环形强化,中心坏死无强化(B)
非哺乳期乳晕炎以非肿块样强化常见,段样(图11-65)、区域性或弥漫性分布,不均匀强化为主,环形或环形样强化多见,中心低信号的环形强化。在T2WI上环形的中心往往表现为高信号,提示脓肿形成或囊肿伴感染。这些囊肿并不是单纯囊肿,超声往往提示囊肿的壁增厚,囊内有实性成分。
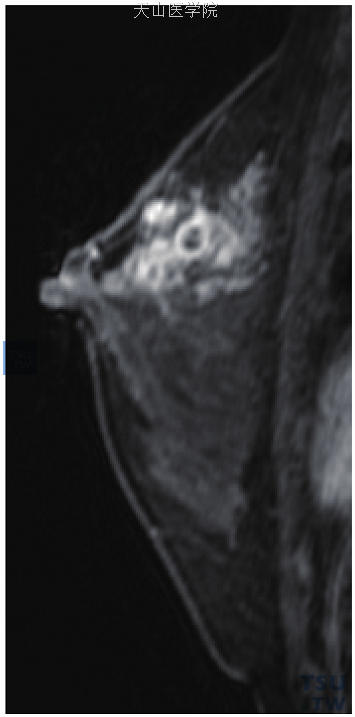
图11-65 患者31岁,左乳急性化脓性乳腺炎。左乳外上段样分布的强化伴环形强化
鉴别诊断
(1)炎性乳腺癌:急性乳腺炎很少发生于哺乳期外,红、肿、热、痛的体征与炎性乳腺癌类似,但急性乳腺炎有类似流感症状,可与炎性乳腺癌鉴别。急性乳腺炎常表现为非肿块样强化,与炎性乳腺癌类似,但乳腺炎的时间-信号曲线很少表现为廓清型,很少在T2WI上看到低信号的肿块,很少浸润胸大肌,病灶周围、乳后间隙及肌肉内水肿也很少见。原因是急性乳腺炎是感染,而非癌细胞浸润淋巴系统。
(2)导管扩张症:尤其伴有周围炎症时,很难鉴别。
(3)伴大片坏死并以导管原位癌为主的浸润性导管癌者,往往也表现为肿块伴非肿块样强化,环形或环形样强化,与非哺乳期乳腺炎很难鉴别。当环形强化的中央低信号在T2WI表现为高信号时,可提示非哺乳期乳腺炎;浸润性乳腺癌T2WI信号不会比乳腺炎信号高,但鉴别仍需活检。
(4)特异性乳腺炎:如浆细胞性乳腺炎、脂肪坏死性乳腺炎、肉芽肿性乳腺炎、结核性乳腺炎,以上各种炎症在影像上均无特征性表现,相互鉴别需要依靠病理检查。
导管扩张症
病理及临床特点
导管扩张(mammary duct ectasia)既非炎症,也非肿瘤,而是由于乳晕区输乳管上皮细胞萎缩,分泌功能丧失,上皮细胞碎屑及含脂性分泌物聚集并充满乳晕下输乳管及大导管使其扩张所致。病因尚不明,可能与先天性乳头畸形或发育不良有关。病变起始于乳晕区的大导管,然后向中等导管扩展,最后形成肿块。早期常表现为乳头溢液,呈淡黄色、棕色或血性;晚期由于导管内积存的脂类分解产物渗出管壁,引起导管周围炎性反应。在炎性反应阶段,可有浆细胞、淋巴细胞浸润,故有浆细胞性乳腺炎之称,部分病例临床表现类似癌。有人认为这种现象是一种与年龄相关的现象。
浆细胞性乳腺炎(plasma-cell mastitis,PCM)是非细菌性感染的病变,临床上可表现为长期的肿块形成、乳晕下肿块、乳头回缩、乳腺胀痛、乳腺脓肿或瘘管形成。病因不明,可能与乳房外伤、哺乳障碍、内分泌失调和乳腺退行性病变及自身免疫性因素有关,好发于年轻女性。有学者认为PCM和导管扩张症为同一疾病的不同发展时期。
影像学表现
乳腺导管扩张症可因病变不同的发展阶段而有不同的MRI表现。早期在T2WI上可显示乳晕区扩张的导管影,呈高信号;当扩张的导管内存在淡黄色或白色脂样分泌物、蛋白样物质、出血等,T1WI呈高信号。如果扩张的导管内存在钙化,T1WI、T2WI均可呈低信号。扩张的导管有积液时,T1WI低信号,T2WI明显高信号。后期病变区可出现肿块,T1WI可表现为等信号或低信号,T2WI多为不均匀高信号,边界欠清。增强后轻至中度强化。
谭文莉等根据手术结果将PCM分为炎症期、脓肿期和瘘管期。炎症期主要表现为非肿块样强化,以段样、区域性分布为主,平扫病灶往往不明显,增强后由于炎症区域反应性充血而明显强化。脓肿期表现为脓肿形成(图11-66),由于脓肿期为炎症期未得到有效控制,使得病灶范围较炎症期进一步增大。瘘管期主要是脓肿期病灶向皮肤表面破溃而形成窦道,MRI显示窦道能力欠佳。可能是因为窦道偏细小,且穿行于腺体组织中,降低了窦道与周围组织的对比。
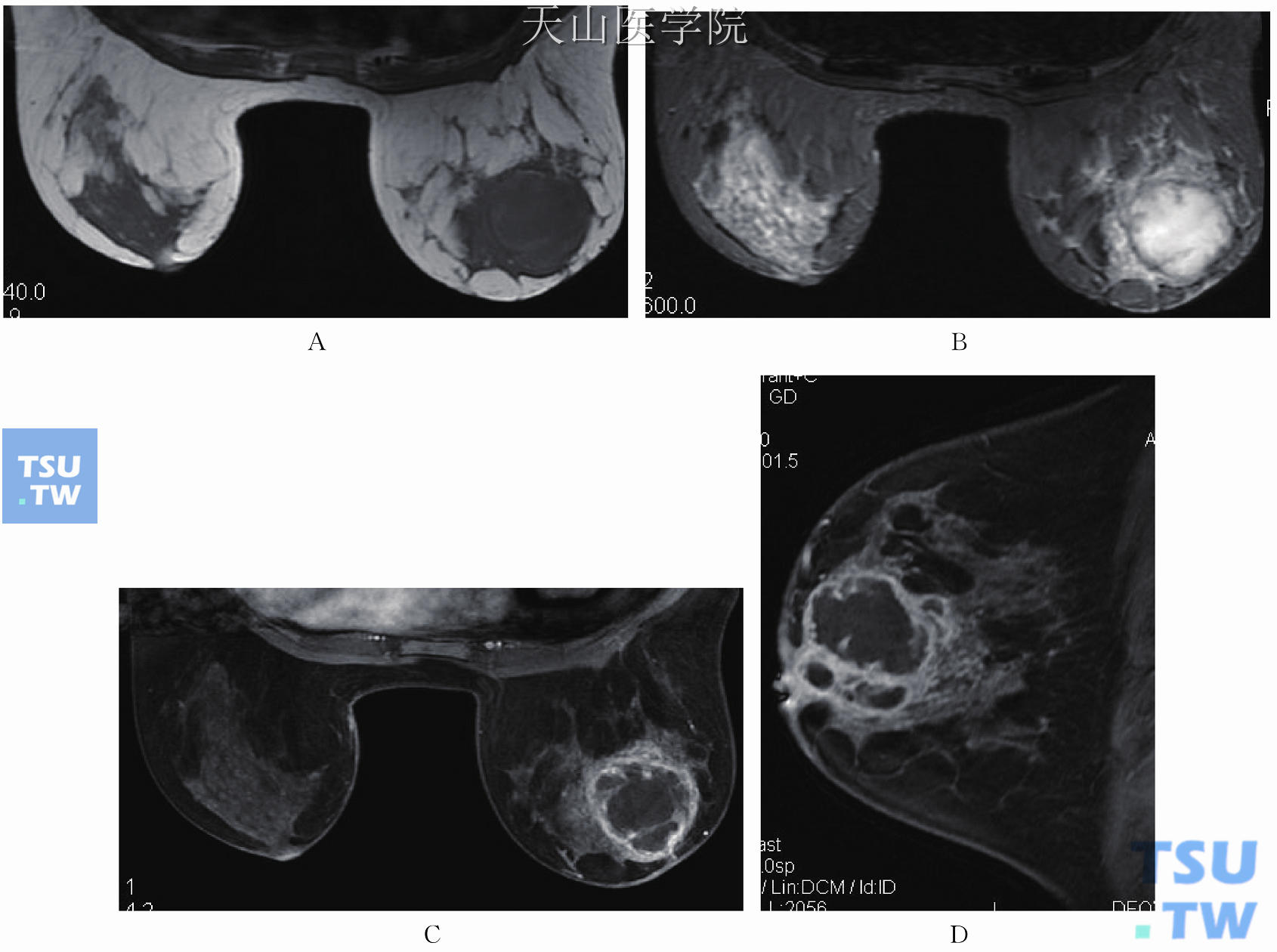
图11-66 右乳浆细胞性乳腺炎。(A)右乳晕后方囊性为主占位,T1WI不均匀稍高信号,囊壁为等信号;(B)T2WI高信号,囊壁为等信号,肿块周围见片状高信号;(C、D)增强后肿块呈环形强化,囊壁厚薄不均匀,其内分隔亦见强化,中心坏死区无强化
鉴别诊断
(1)导管扩张症和管内乳头状瘤都可表现为乳晕下导管扩张,前者主要累及大导管;后者可累及各级导管,可行乳腺导管镜下活检来鉴别。
(2)乳腺导管囊性扩张需与囊肿鉴别:前者多表现为导管呈囊状、串珠状扩张,囊肿往往与扩张的导管相连,而单纯囊肿一般不伴有导管扩张。
(3)PCM需与乳腺癌鉴别:炎症期PCM病灶多局限,呈局灶性或区域性强化,主要分布于乳晕周围,时间-信号曲线多表现为持续上升型或平台型。肿块期,与乳腺癌的鉴别存在一定的难度。脓肿期PCM累及范围广泛,形态多不规则,有脓腔形成,脓腔内壁光整,壁较均匀,周围可伴腺体不同程度的强化。
错构瘤
病理及临床特点
乳腺错构瘤约占乳腺良性肿瘤的0.7%~5%,主要由脂肪构成,同时混杂不同比例的腺体和纤维组织。肿瘤有包膜,边界清楚,可呈纤维囊性或萎缩状。病变的形态结构给人一种“乳腺中的乳腺”的感觉。可发生于任何年龄,主要发生在绝经前后的妇女。临床常无症状,仅在影像学检查时发现。非常大的病变可造成乳房变形。由于肿块分界清楚,因此易于剜除,病变切除后无复发倾向。
影像学表现
乳腺错构瘤多呈圆形、卵圆形或扁圆形,大小1~20cm。
根据肿瘤内成分的不同而MRI表现有所不同。以脂肪为主的,在不抑脂的T1WI和T2WI上均表现为高信号为主的肿块,其内可见低信号或中等信号的分隔;以腺体和纤维成分为主的,T1WI呈低信号,T2WI为等信号或高信号,肿瘤内可见条带状的高信号脂肪组织。脂肪抑制序列上高信号的脂肪组织呈低信号。增强后肿块内腺体成分可见显著的强化(图11-67)。
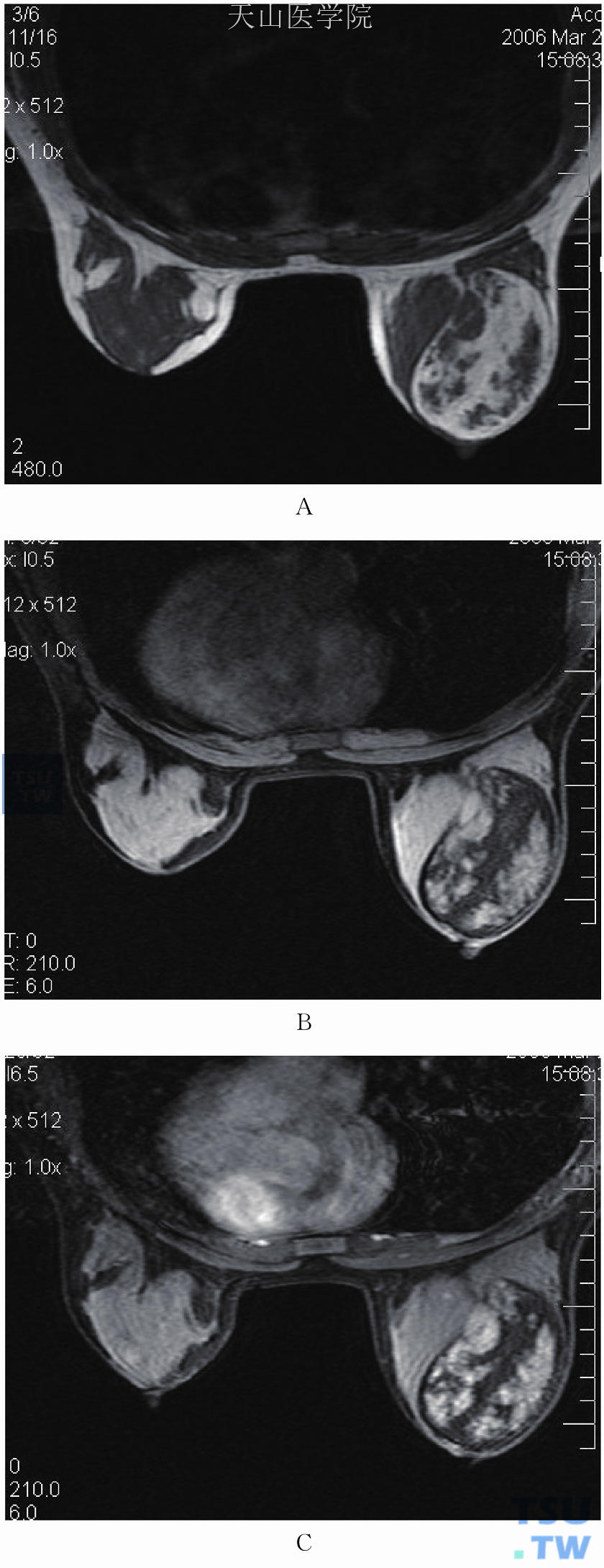
图11-67 右乳外侧错构瘤。(A)T1WI示右乳外侧椭圆形肿块,内见片状高信号;(B)抑脂T2WI显示T1WI为高信号的脂肪信号被抑制,呈低信号;(C)增强后肿块内呈片状强化,脂肪成分不强化
3.鉴别诊断
含多量脂肪的错构瘤需与脂肪瘤及积乳囊肿鉴别。含多量腺体和纤维组织者,需与纤维腺瘤鉴别。
脂肪瘤
1.病理特点:乳腺脂肪瘤(lipoma)是一种由成熟的无异性型的脂肪细胞组成的肿瘤。虽然脂肪组织是乳腺的重要组成成分,但发生在乳腺内的脂肪瘤很少见,患者年龄大多在40~60岁。
2.影像学表现:脂肪瘤一般边缘清晰,包膜光整,直径常<5cm,圆形或卵圆形的肿块影,可因肿瘤内纤维组织存在而发生一些囊性变。在不抑脂的T1WI、T2WI上均为高信号,脂肪抑制序列呈低信号,增强后无明显强化(图11-53)。
3.鉴别诊断:主要与含脂肪的肿瘤如错构瘤、积乳囊肿等鉴别。
脂肪坏死
病理特点
脂肪坏死(fat necrosis)是一种少见的乳腺非化脓性炎症。与轻微钝伤、挫伤有关,是外伤后脂肪坏死引起的无菌性炎症。乳腺的各种穿刺、手术活检、乳腺的保乳术及成形术,也可以造成医源性乳腺脂肪坏死。病变多位于浅表的皮下脂肪组织,除医源性患者外,较少见于乳腺实质组织。脂肪细胞破裂,脂肪溢出为巨噬细胞吞噬,纤维包裹形成脂性囊肿。如果损伤的脂肪细胞析出脂肪酸,引起化学性炎症,形成小的结节,有或无痛感,质坚硬,切面呈灰黄色放射状瘢痕性实变,常与乳腺表面皮肤粘连,临床上易误诊为乳腺癌。好发于40岁以上妇女,特别是体形肥胖、皮下脂肪丰富、乳腺下垂者。
影像学表现
脂肪坏死的影像与其病理基础以及病变发展的不同阶段而有所不同,早期呈脂性囊肿的表现,晚期表现复杂,多表现为肿块。T1WI平扫示形状各异的肿块,病灶中心可见高信号的脂肪成分(图11-68A),周围可见条索状低信号影。抑脂T2WI上T1WI高信号的脂肪呈明显低信号(图11-68B)。增强后边缘呈厚壁环形或不规则中度强化(图11-68C),有时可见强化分隔。
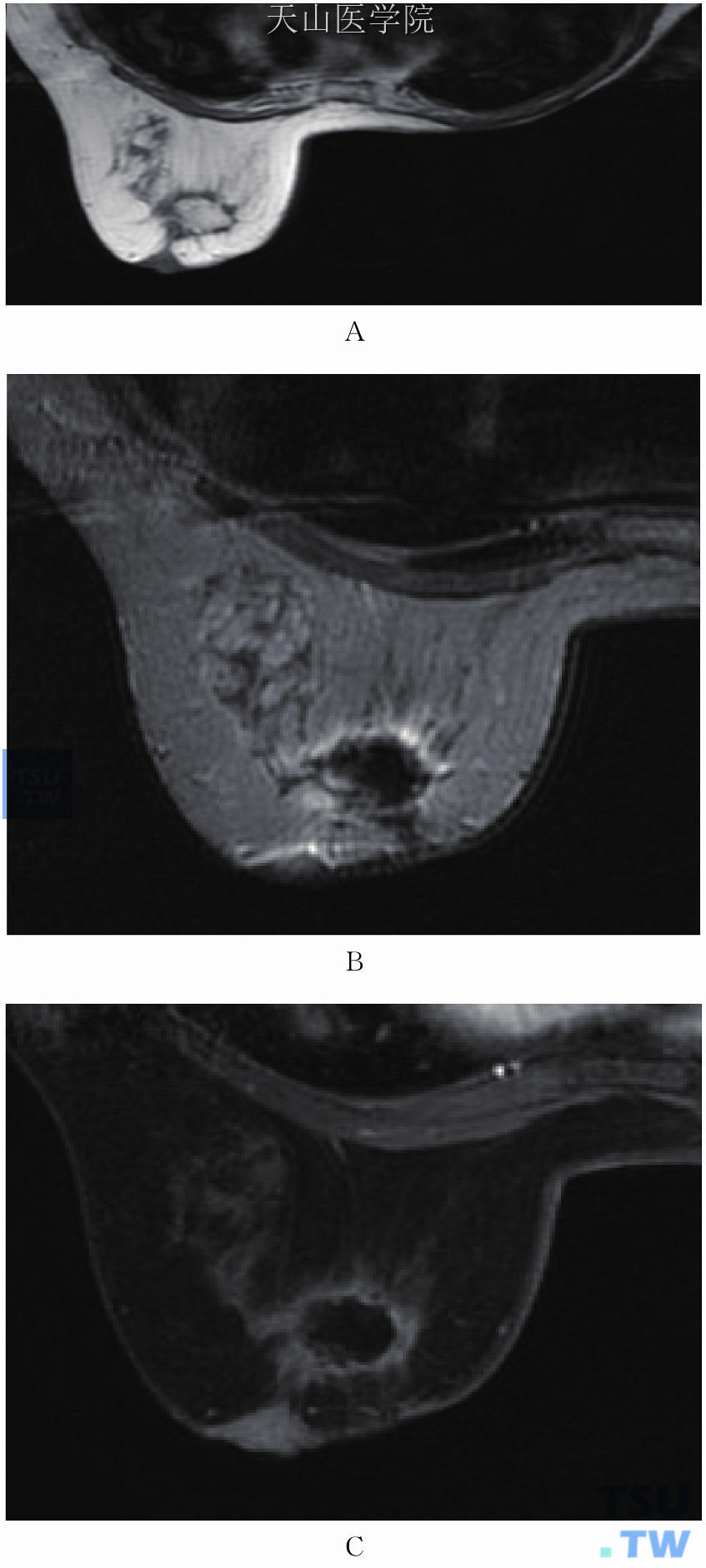
图11-68 右乳腺癌、左乳乳腺病术后,左乳内上占位性病灶。(A)T1WI病灶为高信号;(B)T2WI呈低信号;(C)增强后环形强化
鉴别诊断
表现不典型时需与硬化性乳腺病、乳腺癌等鉴别,外伤、手术史及肿块内脂肪信号有助于两者的鉴别。