乳腺磁共振检查的适应证
乳腺病变性质的确诊
当乳腺X线摄影或超声检查不能确定病变性质时,可以考虑采用MRI做进一步检查,MRI检出浸润性乳腺癌的敏感度接近100%,即MRI检查阴性者可排除浸润性乳腺癌的存在。然而,也有许多关于MRI假阴性的报道,包括漏诊浸润性导管癌(IDC)、浸润性小叶癌(ILC)和导管原位癌(DCIS)等。同日常工作中MRI提示乳腺明显异常、高度可疑乳腺癌而钼靶及超声检查均为阴性的患者一样,如果钼靶和超声检查提示可疑乳腺癌,而MRI检查为阴性的病变,也必须活检。不推荐仅做乳腺平扫的MRI检查。
乳腺癌的术前分期
对已明确为乳腺癌的患者,可进行更准确的术前分期。MRI有助于发现其他影像学检查所不能发现的多灶和多中心病变;有助于显示和评价肿瘤对乳后脂肪间隙和胸肌的浸润等(图11-1)。当然,乳腺癌的MRI分期也存在缺陷,有时会将乳腺癌伴发的良性病灶误诊为多灶性乳腺癌而进行活检,使保乳患者的美观效果大打折扣。
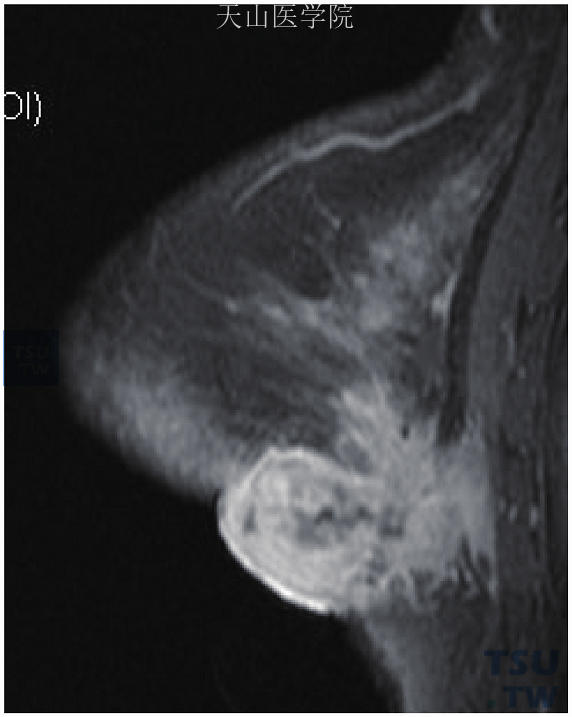
图11-1 右乳浸润性导管癌,肿瘤累及皮肤、乳后脂肪间隙及胸肌
拟保乳手术的患者,建议常规MRI检查
对乳腺癌以外的任何可疑病灶(可疑病灶是指星芒状或不规则肿块伴不均匀或环形强化;导管样、段样和区域性分布的非肿块样强化;时间-信号曲线为廓清型等),不能仅凭MRI结果进行手术。推荐对乳腺MRI发现的可疑病灶做第2次超声检查(首次超声检查未能检测到MRI提示的可疑病灶),可在超声引导下对可疑病灶定位并活检。如第2次超声检查仍未能检出病灶者,可进一步在MRI定位下取样活检。
鉴于MRI引导下定位活检术目前在国内尚不能完全开展,可选择体表定位(即可疑病灶的中心距同侧乳房横断面及矢状面的垂直距离与钟面定位,见图11-2)。体表定位可因MRI检查和手术体位的不同、乳房的大小及致密程度的不同而有不同的偏差。如可疑病灶为多中心病灶,选择其中最怀疑的可疑病灶做活检,如为恶性病变,不推荐选择保乳手术;如为良性病变,可以推测其他病灶亦为良性病变,建议保乳术后定期随访。
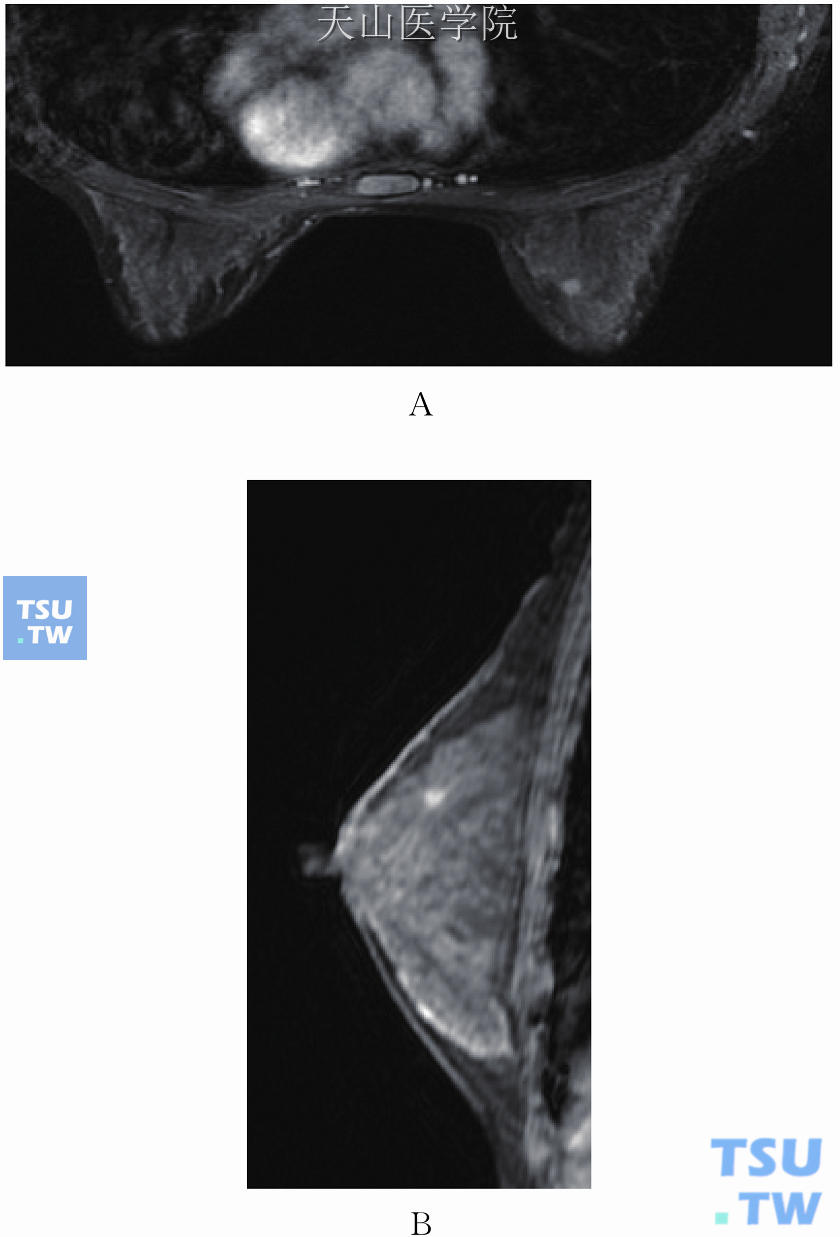
图11-2 右乳内上象限近中线斑点状强化,周围见长毛刺,良性的可能性大,BI-RADS 3。MRI体表定位病灶距横断面及矢状面的垂直距离分别为4.7mm(A)及17.5mm(B)。术后病理检查为右乳硬化性乳腺病
一侧乳腺癌患者
患者一侧有乳腺癌,检查对侧乳腺是否存在可疑病灶。
保乳术后的随访
保乳术后的随访,包括切缘阳性的残留病灶的评估,切缘阴性的保乳手术后是否乳内有肿瘤残留,术后是否存在复发或仅为术后纤维化改变,以及评估对侧乳房是否存在转移灶或第二原发肿瘤等。
腋窝淋巴结转移,原发病灶不明者
对于腋窝转移性淋巴结,MRI有助于发现乳腺内的原发癌灶(图11-3),其敏感度、特异度及准确率分别为95.2%、71.4%和85.7%。这些结果支持将MRI用于腋窝淋巴结出现转移、而钼靶和临床检查未发现原发肿瘤的患者。对这部分患者,MRI既可发现原发肿瘤,进行分期,又可指导治疗计划,尤其是给一些原本需要乳腺切除的患者提供了保乳的机会。
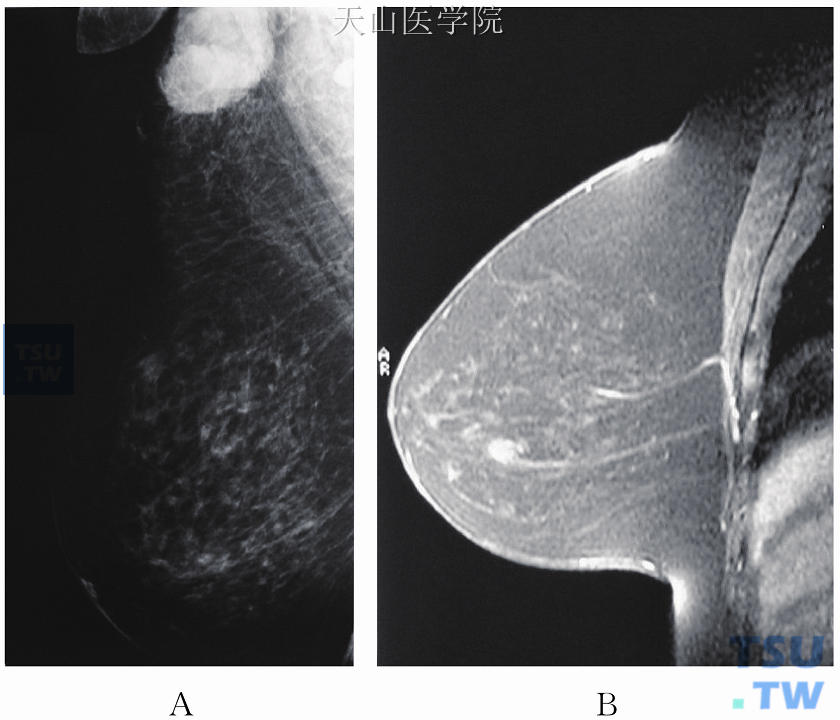
图11-3 右腋窝淋巴结肿大,病理检查为腺癌,钼靶检查示右腋窝淋巴结肿大,右乳内未见明显异常,BI-RADS 1(A)。增强MRI矢状位示右乳下方强化小结节,术后病理检查为导管原位癌(B)
新辅助化疗疗效的评估
MRI可通过对比增强的病灶信号是否降低来判断化疗反应,这种方法甚至可以在发现肿瘤大小变化之前就监测到化疗反应。
通过MRI的功能成像(functional MRI,fMRI),既可测量肿瘤的体积变化,有效评估瘤体内的生理、生化代谢状况,又可动态重复监测。fMRI可在病灶大小尚未发生改变之前,通过病灶的表观扩散系数(ADC)值的变化来预测化疗疗效。治疗前、后的ADC值与肿瘤退缩率呈负相关,即治疗前ADC值越低,治疗后肿瘤退缩越明显,反之亦然。原因是ADC值与细胞密度呈负相关、与肿瘤分化程度呈正相关,即治疗前ADC值较低,代表肿瘤细胞密度高,血供丰富,肿瘤周围药物浓度相对较高;而ADC值较高的肿瘤细胞分化较好,细胞密度相对较低,肿瘤血供较少,药物浓度相对较低。因此,治疗前ADC值较低即分化差的肿瘤更容易得到化疗药物的作用,从而获得较好的疗效。
采用质子磁共振波谱成像(1H-MRS)上测得磷酸胆碱(Cho)升高,强烈提示病灶为恶性肿瘤。因为Cho是细胞膜的组成部分,肿瘤患者Cho水平升高是因为细胞增殖加快。在乳腺癌新辅助化疗过程中,化疗有效病例的肿瘤细胞增殖活性降低,生长代谢明显减弱,细胞逐渐凋亡、坏死,细胞密度下降,Cho的含量随之降低,1H-MRS谱线上的Cho峰亦随之降低。反之,病情进展者瘤体内Cho的含量明显增高,1H-MRS谱线上的Cho峰随之升高。
新辅助化疗后,有效病例的容量转移常数(Ktrans)、速率常数(Kep)较治疗前明显降低,无效病例的Ktrans、Kep值较前升高。这是因为新辅助化疗后,抗肿瘤药物抑制肿瘤新生血管生成,病变血供减少,癌细胞供血不足发生崩解坏死,部分病理血管闭塞消退,血管通透性减低,局部癌组织微血管的血流灌注降低。
由于fMRI在乳腺方面的应用研究尚不成熟,在检查技术及评估方法上存在不足,因此如何提高对化疗疗效评价的准确率,是fMRI在新辅助化疗疗效评价中亟须解决的问题。而且MRI尚不能检出小灶性癌的残留病灶,故影像完全缓解与病理完全缓解不完全匹配。
乳腺靶病灶的疗效评估,不推荐钼靶和超声作为一线影像评估手段。因为钼靶会低估病灶的大小(无论是恶性钙化还是肿块),超声检查与操作者的技术水平相关性太大。最佳的乳腺靶病灶的影像评估,首推乳腺MRI检查。增强的胸部CT检查原则上不推荐作为乳腺靶病灶评估的最佳手段,但可作为评估乳腺非靶病灶的影像手段。
高风险人群筛查
高风险人群是指BRCA-1、BRCA-2基因携带者,明显家族史及患有小叶原位癌等。乳腺MRI检查主要的局限之一是相对较低的特异性,增强后一些良性病变以及正常的腺体和癌组织一样会强化,相互之间有重叠,导致活检数量明显增加。因此,除临床试验以外,目前并不提倡将MRI检查作为常规乳腺癌普查的方法。
乳房隆胸术后的评估
对于隆胸术后的乳腺,不论是乳腺的钼靶检查还是超声检查都需压迫乳房,有造成假体继发破裂或水凝胶扩散的危险。MRI不存在该问题,而且能有效显示假体及乳内病灶并对病变进行解释。
MRI引导下定位及穿刺活检
目前国内MRI引导下的定位及活检技术尚未开展,复旦大学附属肿瘤医院乳腺癌多学科团队从2010年底起开展此项技术。近期在随机配送的MRI定位支架基础上研发了适合相对小乳腺的定位支架及与之配套的软件定位系统,截止2012年1月已完成50余例MRI引导下定位,1例MRI引导下活检的临床试验。影像学检查引导下的定位,原则上首选超声引导下定位,方便、经济、患者较舒适;其次是钼靶引导下定位;当超声和钼靶都不能定位时,才考虑MRI引导下定位(图11-4)。活检亦如此。
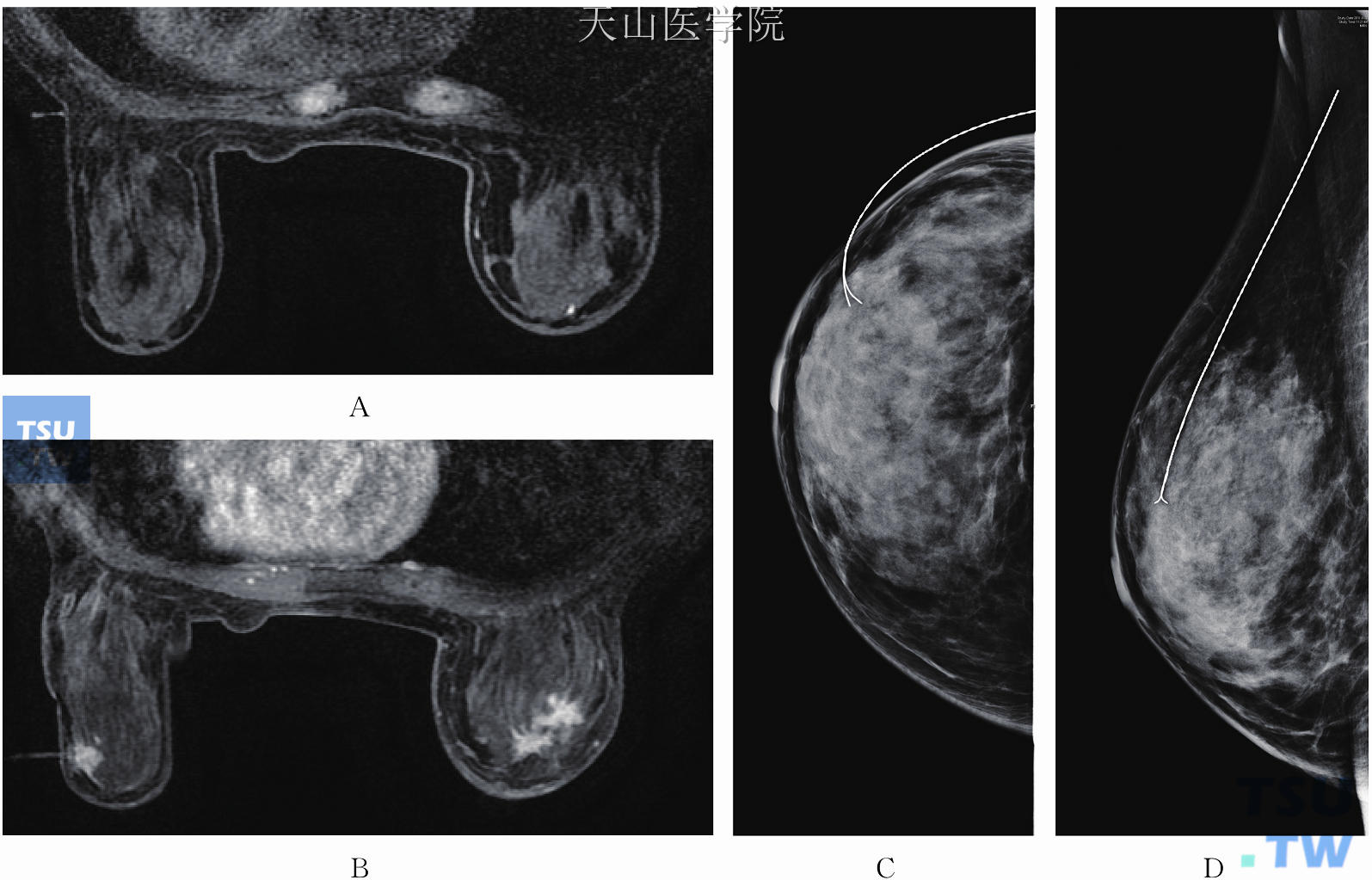
图11-4 左乳仅MRI提示外上可疑病灶,BI-RADS 4。左乳外上病灶拟MRI引导下定位:(A)显示Marker;(B)显示穿刺套管的中心位于病灶的中央;(C,D)MRI引导下定位术后常规钼靶摄片,显示定位针位于左乳外上(进针深度为针的总长度减去进针后体外针的长度)。左乳外上病灶术后病理检查为左乳乳腺病伴间质胶原化。钼靶、B超及MRI均提示右乳外上恶性病变,BI-RADS 5。右乳单纯切除术后病理检查为以导管原位癌为主的浸润性导管癌,呈多灶性
乳腺磁共振检查的禁忌证
常规MRI检查的禁忌证亦是乳腺MRI检查的禁忌证,如体内安装起搏器、外科金属夹等铁磁性物质,患有幽闭恐惧症及造影剂过敏者。另外,不能俯卧位检查者如妊娠妇女等都不适合做乳腺MRI检查。原则上,不提倡乳腺平扫MRI检查。鉴于CT检查有辐射和造影剂过敏的危险性,应尽量避免用CT检查来评估乳腺内的病变。
