趋化因子
细菌或组织坏死会产生大量的代谢物,有些物质具有引诱中性粒细胞的性质,有些则经与血浆中蛋白质作用形成复合物(也称调理作用)后也具有引诱中性粒细胞的性质,这些物质扩散形成浓度梯度可以诱导中性粒细胞运动直至感染源。这些能刺激中性粒细胞引诱其游走的物质称为趋化因子(chemotactic factor)或称化学吸引剂(chemoattractant),也有泛称为激动剂(agonist)。近年已把广义细胞因子中对各种白细胞亚类如中性粒细胞、单核细胞和淋巴细胞中具有趋化和预活化作用的低分子量(8~10kD)蛋白专称作趋化因子(chemokine),并根据其4个保守的半胱氨酸残基中前两个的位置不同而分成α趋化因子(CXC)和β趋化因子(CC)两个亚族。英文缩写中“C”代表半胱氨酸,“X”代表任一其他氨基酸。相对上述提到的趋化因子,显然这里是一种狭义的趋化因子,而且在英文名称上二者也不相同。但近年对后者的功能作用已开展广泛深入的研究。
广义的趋化因子或称趋化物已有许多,至今仍有新的发现,属蛋白类的主要有补体系统产物,如C5a和C3bi等,由凝血酶和纤维蛋白溶酶原激活剂激活产生的激肽释放酶(kallikrein)、血凝与纤溶系统的纤维蛋白B肽(fibrinopeptide B)、纤维蛋白降解产物和纤溶酶原激活物等。属多肽类的有细菌释放或人工合成的趋化三肽(FMLP)及其类似物,属脂代谢产物的有血小板脂氧合酶途径的产物12-羟二十碳四烯酸(12-HETE)、LTB4和血小板活化因子(PAF)等。近年更发现有多种细胞因子对中性粒细胞有强刺激作用,而且发现在中性粒细胞表面有相应受体,如G-CSF、GM-CSF、IL-1、IL-8和TNF等受体。中性粒细胞表面上具有上述各趋化因子的受体,这进一步证明了中性粒细胞功能的多样性和重要性。
趋化物之间有一定的内在联系,一种因子可以激活或引发另一种因子,如补体C5a和细菌产物(特别是内毒素)能激活Hageman因子。活化的Hageman因子又可激活激肽释放酶原为激肽释放酶。激肽释放酶是一种较强的趋化因子并能增加中性粒细胞的黏附性。循环血流中的中性粒细胞是静息细胞,在生理功能上是“钝化”的,而且表面具有极少的低亲和性受体。中性粒细胞自血管逸出、游走到感染源要经过活化和复杂的黏附作用。近年已对中性粒细胞与内皮细胞黏附作用的分子基础有了较深入的了解;中性粒细胞从流速很快的循环血中穿过血管内皮细胞层必须有一个相对静止的条件与内皮细胞接触,始有可能穿过内皮细胞层进入组织,而中性粒细胞和内皮细胞上黏附分子的激活和相互识别,以及进而发生的黏附作用正好满足了这种需要。前已介绍中性粒细胞-内皮细胞的黏附作用分别由中性粒细胞表面黏附分子和内皮细胞表面黏附分子共同作出贡献。
中性粒细胞黏附性增加的分子基础是整合蛋白β2亚族的CD11/CD18在趋化因子作用下表达增加并被激活。内皮细胞上的黏附分子主要是免疫球蛋白超家族的ICAM-1和VCAM-1及E-选择素,它们被细胞因子或细菌产物内毒素等激活,通过配体-受体反应相互识别发生相互黏附作用的结果。先使较快速度运动的中性粒细胞减速逐渐沿血管内皮细胞表面滚动,然后更牢固地黏附在内皮细胞层。中性粒细胞黏附在内皮细胞表层是中性粒细胞通过变形从内皮间隙中“挤”出去的先决条件,因为随循环血流快速运动的中性粒细胞能穿透内皮细胞层是不可能的。对中性粒细胞-内皮细胞黏附作用本质及意义的认识,是近年白细胞功能分子基础研究的重要发展,事实上白细胞黏附分子的缺陷是白细胞功能异常疾病的重要方面。可能还存在一种不依赖于CD11/CD18的中性粒细胞透过内皮细胞的机制。下述将对中性粒细胞与血管内皮细胞相互黏附并逸出的详细机制做一介绍。
中性粒细胞与血管内皮细胞的黏附作用
黏附作用是中性粒细胞的重要功能之一,其与血管内皮细胞的黏附作用是炎症前期的重要内容,黏附作用能使中性粒细胞接受信息并作出相应的反应以调节细胞行为。中性粒细胞的黏附作用包括细胞-细胞、细胞-胞外基质(extracellar matrix,ECM)的黏附作用,此处着重介绍中性粒细胞与内皮细胞相互黏附的分子机制。
虽然对中性粒细胞-内皮细胞黏附作用的许多细节仍不清楚,但近年的研究结果已可以肯定至少有三种黏附分子家族的成员参与了中性粒细胞-内皮细胞的黏附作用,它们是免疫球蛋白族、选择素族和整合蛋白族。免疫球蛋白族的主要成员有:细胞间黏附分子-1和2(intercellular adhesion molecule-1&2,ICAM-1,ICAM-2)和血管细胞黏附分子(vascular cell adhesion molecule,VCAM)。ICAM-1 和ICAM-2分布在中性粒细胞、单核细胞、内皮细胞和淋巴细胞。ICAM-2在内皮细胞上也有表达,相应受体为LFA-1、Mac-1和P150,95。VCAM-1在单核和淋巴细胞上有表达,相应受体是VLA-4。
选择素族的成员主要有选择素-E(E-selecting)也称内皮细胞黏附分子-1(endothelial leukocyte adhesion molecule,ELAM-1),选择素-P也称颗粒膜蛋白-140(granular membran protein-140,GMP-140),以及选择素-L,由于选择素-L分布在所有白细胞上,也称白细胞黏附分子-L(leukocyte adhesion molecule-1,LAM-1)。选择素-E只在内毒素细胞因子激活的血管内皮细胞上表达,相应受体是CD15,后又进一步确定选择素-E的受体是粒细胞及单核细胞上的唾液岩藻乳糖胺寡糖(sialyl fucosyl lactosamine oligosaccharide)。选择素-P分布在血小板的α颗粒和内皮细胞的Weibel-Palade体内。经凝血酶、组胺或白三烯C4等刺激后,选择素-P可被动员与质膜融合而在细胞表面表达,参与内皮细胞、血小板与中性粒细胞和单核细胞间的黏附作用,促使炎症与血栓形成。
参与中性粒细胞黏附反应的整合蛋白家族成员主要是β亚族中的β2亚族,由于该亚族中的三个主要成员(LFA-1、Mac-1和GP150,95)前已介绍,此处不再重复。
有关中性粒细胞如何通过黏附分子与内皮细胞发生黏附作用,详细机制有待研究,但Karloss Rosales和Kuby Juliano(1995)在总结前人基础上提出了“白细胞黏附性复合体的信息传递模式”来解释中性粒细胞等白细胞与内皮细胞相互黏附的分子机制。
未活化的中性粒细胞和单核细胞有一低水平的黏附到培养的内皮细胞层的能力。这种黏附作用仅部分受到整合蛋白主要是LFA-1的调节,在单核细胞中是GP150,95,Mac-1则极少参与。炎症期间,中性粒细胞与内皮细胞的黏附作用分三个步骤进行。
第一阶段:中性粒细胞并未受到炎性因子刺激而激活,中性粒细胞与血管内皮细胞的相互作用主要通过选择素-P调控(下图)。选择素-P迅速增加识别中性粒细胞上的相应配体CD15上的糖类配基(唾液酸化的路易士抗原,SLex),而中性粒细胞上的选择素-L也可识别血管内皮细胞上的Lex。由于这类受体-配体结合不需中性粒细胞激活,只需Ca2+存在,因而易于发生。结果是循环血中的中性粒细胞减速,逐渐向血管壁靠近并沿着内皮细胞表面滚动。
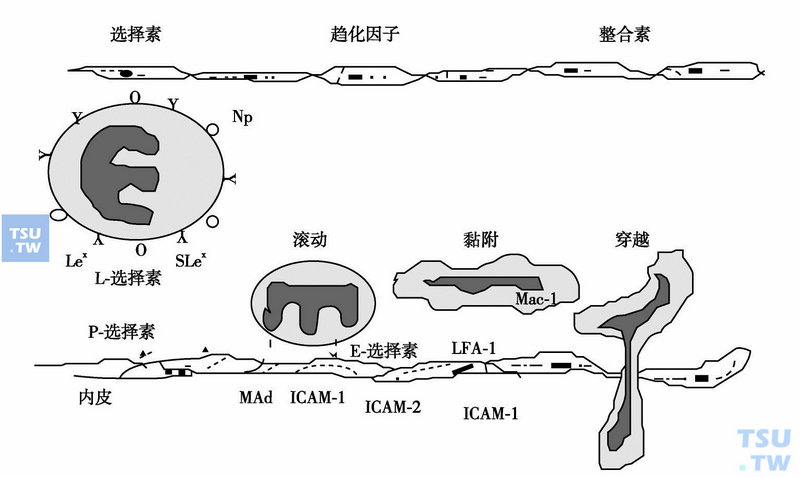
中性粒细胞黏附到炎症部位血管内皮细胞时的分子整合作用
第二阶段:由于炎性因子LPS、TNF或FMLP等对中性粒细胞和内皮细胞均产生激活作用,促进两种细胞表面黏附分子受体(或配体)的表达和活化,如中性粒细胞表面的LFA-1、Mac-1,内皮细胞上的ICAM-1和选择素-E。另一方面内皮细胞激活后又可产生细胞因子,直接作用于中性粒细胞,增强黏附性,如在凝血酶刺激下,内皮细胞产生PAF,结果使中性粒细胞终止滚动,黏附在内皮细胞上。这时选择素-L自中性粒细胞脱落。
第三阶段:当内皮细胞暴露在免疫调节剂如γ-干扰素、TNF或LPS后(4~24小时),中性粒细胞黏附性的驱动主要是通过内皮细胞活化产生的ICAME和选择素-E进行。ICAM-1与中性粒细胞表面整合蛋白LFA-1和Mac-1结合。黏附在血管内皮细胞上的中性粒细胞通过整合蛋白分子调整自身细胞骨架,通过变形从内皮细胞间隙中“挤”出去。ICAM-1和选择素-E在中性粒细胞穿越内皮细胞层过程中起重要作用。然后,脱离血管的中性粒细胞在趋化因子作用下,顺浓度梯度通过趋化运动到达感染源。单核细胞与淋巴细胞的迁移情况与中性粒细胞的迁移过程基本相同。
中性粒细胞-内皮细胞的黏附作用有几个特点:
- 中性粒细胞在上述三个阶段中功能状态的变化表明整合蛋白起到沟通ECM和细胞内骨架的作用,整合蛋白通过调整细胞骨架传递信息并且把细胞调节的生化应答返转出去,在细胞内传递信息中表现为第二信使功能。
- 中性粒细胞激活时产生的黏附作用主要是Mac-1(CD11b/CD18)参与,其次是LFA-1(CD11a/ CD18)。在内皮细胞激活条件下,中性粒细胞的黏附作用LFA-1是主要参与者。Mac-1仅作部分贡献。但三种β2亚族的成员协同参与黏附作用。
- 中性粒细胞-内皮细胞黏附作用受到Ca2+、血流剪切力和内皮细胞激活方式的调节。
(1)Ca2+的影响:Ca2+浓度的变化与许多受体的信息传递相关联,这是众所周知的。已有一些实验结果表明黏附作用有Ca2+参与。在炎症初期,选择素-P在Ca2+存在下可直接与未激活的中性粒细胞结合。中性粒细胞的Mac-1和血小板整合蛋白α11b/β3均可促进胞内Ca2+上升。此外,淋巴细胞上的LFA-1与抗α链抗体反应可引起磷酸肌醇的水解和Ca2+的升高。在纤连蛋白或玻璃粘连蛋白层培养的内皮细胞中Ca2+也升高。这些结果表明整合蛋白具有诱发这重要第二信使的能力,也表明Ca2+与整合蛋白分子参与的黏附作用相关联。在一些细胞型中整合蛋白配体还可导致酪氨酸磷酸化。
(2)血流剪切力的影响:近年对黏附性受体驱动吞噬细胞-内皮细胞黏附作用的研究中发现,这种黏附作用还依赖于细胞的剪切力。在低剪切力(0. 5dyn/cm2)下依赖白细胞整合蛋白CD18的黏附作用占主导地位,例如在炎症部位。在生理允许的高剪切力(2~3dyn/cm2),主要由不依赖于CD18的黏附性分子参与,例如中性粒细胞与活化的内皮细胞作用。表明激活中性粒细胞是在低流速下进行,而与内皮细胞结合并获得强黏附作用是在高剪切力下实现的,最好的证据是黏附性受体LFA-1缺乏的病人,其中性粒细胞在低剪切力下不能与内皮细胞发生黏附,但当置于高剪切力下则能和正常中性粒细胞一样与内皮细胞发生黏附。
(3)内皮细胞被激活方式的影响:凝血酶和LTC4在30分钟内可直接快速引起内皮细胞合成黏附中性粒细胞的蛋白质,而对白细胞整合蛋白的依赖程度仅只20%。同样,组氨酸和佛波酯可激活内皮细胞产生GMP140,介导中性粒细胞的黏附性而不须通过白细胞整合蛋白。但IL-1、TNF和LPS诱发的内皮细胞表面黏附蛋白合成,所引起的中性粒细胞黏附性的增长则在4小时以后出现,而且对白细胞整合蛋白的依赖程度很大,达70%。
胞内信息传递与刺激的耦联反应
胞内信息传递及刺激的耦联反应是研究中性粒细胞功能的核心部分,也是众多学者近年注重的热点。中性粒细胞的防御功能自表面受体感受趋化物质开始,趋化物质与受体结合起一种“扳机”(trigger)作用。触发细胞内一系列相互连贯的变化。首先是引起膜电位的改变,在4~10秒内先出现一快速的去极化,随即出现一持续的超极化。质膜的去极化可刺激钙通道开放使Ca2+内流,这可能是去极化引起电压依赖性钙通道开放之故。与此同时,与受体耦联的异三聚体G蛋白被激活也促使钙通道开放使Ca2+内流。此外,钙通道复合体中存在Ca2+和cAMP依赖性磷酸化位点,通过复合体磷酸化作用的加强或去磷酸化作用的抑制,均可增加其对电压变化的敏感性,使通道更易对电压变化作出反应,有利于Ca2+更多、更快地流入胞内,使胞内钙离子浓度增高,胞内Ca2+增高对中性粒细胞防御功能的几个关键进程是必需的。
中性粒细胞胞内信息传递与百日咳毒素敏感性异三聚体G蛋白和多种膜酶等效应器分子的耦联密切相关,G蛋白的耦联作用使外部信息经过G蛋白得以分流,使细胞各个效应机构有节奏、有条理地协同作用。因此,异三聚体G蛋白与其他蛋白分子的耦联作用在胞外信息导入胞内传递中起枢纽作用。
迄今,G蛋白的耦联作用,除了与Ca2+通道外,已确定的分别还有磷脂酶C(PLC)、磷脂酶A2 (PLA2)、腺苷酸环化酶(AC)和微管蛋白(G蛋白的α亚基上有β微管蛋白N端的结合位点)。耦联作用导入的信息与中性粒细胞的主要功能:移动、趋化、吞噬及呼吸暴发密切相关。现分别介绍:
G蛋白-PLC耦联传递途
径 趋化物质与受体结合形成受体-配体复合体引起与之耦联的G蛋白活化,促使与异三聚体(αβγ)G蛋白中的βγ亚基自G蛋白上脱落下来,与PLC2结合。激活了PLC2,随即特异性地分解4,5-二磷酸磷脂酰肌醇(PIP2)为1,4,5-肌醇三磷酸(IP3)和二乙酰甘油(DAG)。IP3和DAG是非常重要的胞内第二信使,IP3与内质网上受体结合促使内质网Ca2+库释放Ca2+,使Ca2+浓度迅速增高,Ca2+浓度增高对Ca2+依存性蛋白激酶(PKC)的激活是必需的。PKC与质膜紧密结合可调节与分化、增殖功能有关的胞质蛋白磷酸化(如肌动蛋白轻链与另一些在溶酶体脱颗粒作用中起作用的收缩蛋白)功能。而蛋白磷酸化作用又是NADPH氧化酶激活产生呼吸暴发,生成超氧化合物的必要条件之一。
DAG的产生除了PLC2分解PIP2直接产生外,尚有一条直接的途径产生:磷脂酰胆碱(PC)在磷脂酶D(PLD)作用下分解产生磷脂酸(PA)。PA在磷酸水解酶作用下转变为DAG。DAG的主要功能是激活细胞内的Ca2+和磷脂酰丝氨酸依存性的蛋白激酶(PKC),近年又知还可激活蛋白激酶A、肌球蛋白轻链激酶和Ca2+/钙调蛋白激酶11等,从而调节细胞功能。可见由G蛋白介导的经与PLC耦联的信息传递途径主要是促使PKC激活,使功能蛋白分子磷酸化进而产生各种细胞应答反应。佛波酯(PMA)可直接激活PKC使中性粒细胞产生呼吸暴发,已证实PKC是PMA的受体。
IP3和DAG都是细胞功能的重要调节分子,具有第二信使功能,平行地激活各自的途径、互相协调调节细胞反应,并都具有生成快、效应高以及一旦刺激撤除消退很快等第二信使的典型特点,IP3主要负责应答的触发,DAG则主要在维持应答方面起作用。
由于IP3和DAG均通过磷脂酰胆碱(PC)-特异性磷脂酶(PLC)(简称PC-PLC系统)产生,基于它的重要性,近年PC-PLC系统被一些学者看作胞内信息传递中的“黄金通道”,已发现IL-1、TNF、CSF-1、IL-3、IFN(α,γ)、EGF和EPO等10多种细胞因子,在近30种不同类型的细胞中均需通过PC-PLC系统传递信息。
现已确认,蛋白质磷酸化是真核细胞中信息传递最普遍的机制之一。在整个细胞功能活动中起调节作用。蛋白质的磷酸化/脱磷酸化作用可能是调节的中心环节。在上述趋化因子(例如FMLP)受体-G蛋白介导的信息传递途径中有关蛋白激酶的研究近年又有新的进展,即除了上述Ca2+依存性PKC外,还存在非Ca2+依存性PKC途径。从蛋白激酶催化磷酸化作用的位点角度看,除了丝/苏氨酸蛋白激酶(PKC属此例)外还存在酪氨酸蛋白激酶。业已证实,在中性粒细胞中至少有4种丝/苏氨酸激酶存在,其中一种已经鉴定是分子量为41kD,属于丝裂原活化蛋白激酶(MAPK)家族。所以,现在比较统一的看法是中性粒细胞胞内信息传递途径比原来想象的要复杂得多。激活途径可能是多层次的,可能有多种平行的途径同时激活:Ca2+-PKC依存性途径、Ca2+-PKC非依存性途径,以及随即出现的既包括酪氨酸激酶又包括丝/苏氨酸激酶的复杂反应,可能是信息瀑布系统中的重要环节和替补系统。但MAPK与中性粒细胞激活特别是与呼吸暴发的相关性尚在探索中。
G蛋白-PLA2耦联
G蛋白激活通过其α亚基的脱落激活与之耦联的PLC,而对PLA2的激活可能是通过其β和γ亚基起作用,从而导致PLA2分解PC产生花生四烯酸(AA)和溶血卵磷脂,也可从DG转化而来。花生四烯酸也是很重要的信息分子,其通过5’-脂氧合酶途径生成5-氢过氧化二十碳四烯酸(5-HPETE),再经脱水作用生成5-羟二十碳四烯酸(HETE)和一组称作共轭白三烯(leukotriene,LT)的代谢物,包括LTB4、LTC4、LTD4和LTE4,其中LTB4是花生四烯酸产生的强趋化因子。LTB4的产生一方面作为强趋化因子增强中性粒细胞的趋化应答,有正反馈的作用。另一方面LTB4在Ca2+存在时促进PKC激活,花生四烯酸又可通过环氧合酶途径产生前列腺素E(PGE2)。PGE有降低中性粒细胞-内皮细胞黏附作用的性质,可避免过多中性粒细胞逸出血管。
溶血卵磷脂可进一步形成血小板活化因子(PAF)。PAF也是强趋化因子,和LTB4一样可加强中性粒细胞的趋化反应。
G蛋白-腺苷酸环化酶(AC)耦联
与AC耦联的G蛋白可能是另一类G蛋白,分别是Gs(stimulatory G proteins)和Gi(tnhibitory G proteins)。两种G蛋白协同控制腺苷酸环化酶的活性,双重调节cAMP的量,发挥其第二信使的作用。近年有报道指出,AC也是钙调蛋白的目标酶,钙调蛋白与Ca2+结合引起构象变化,并与AC结合促使AC活化,从而提高cAMP水平,进而影响cAMP为第二信使的蛋白激酶A(PKA)。CAMP的增高可促使肌动蛋白的聚集。
G蛋白-钙通道耦联
G蛋白与钙通道的耦联可引起钙通道开放使Ca2+内流,目前缺乏较详细的材料。
在趋化因子受体介导的信息传递途径中至少有4种G蛋白参与中性粒细胞的激活。
据此可知,由于受体-G蛋白耦联介导的信息传递具有多层次、综合性的特点,在研究中性粒细胞功能时需明白要鉴别某一单一功能的信息机制是非常困难的。
