通过调节靶基因的转录而表达其生物作用的激素有类固醇激素、1,25-(OH)2D、甲状腺激素(thyroid hormone,TH)和视黄酸(retinoic acid)等。这些激素的作用机制十分相似。靶细胞以扩散、主动摄取或“转位”(translocation)等方式使类固醇激素进入细胞内,与受体结合形成激素-受体复合物(分布于胞质和核内),受体发生变构效应(allosteric effect),形成的“活性复合物(activated complex)”与DNA结合部位结合,导致邻近基因活化(或抑制)、mRNA和蛋白质合成。后者可改变细胞的功能或引起细胞生长、分化等反应。以转录调节因子方式实现激素生物作用的激素并非仅有类固醇激素,绝大多数肽类激素(如GH)也可以通过调节基因转录来发挥生物作用。
类固醇激素主要通过核受体发挥作用
类固醇激素受体有下列特点:
- 受体浓度:靶细胞含有一定数量的受体,可用性受体具有可饱和性特征,但受体的浓度差别很大,以受体蛋白占细胞蛋白的总量计,自0.001%(醛固酮受体)至0.1%(孕酮受体)不等,可相差数十至数百倍;但是,一般靶细胞内的受体数目显著高于非靶细胞;
- 结合亲和力:一般激素受体与激素结合的亲和力很高;
- 专一性:激素受体的专一性(特异性)只是相对的,有时受体可与同类激素、激素类似物、激素激动剂或拮抗剂结合,故在较大程度上,这种专一性是由激素(配体)的量和分子特性决定的,并遵循可逆性竞争结合的一般规律。
1. 与类固醇激素受体超家族成员结合的因子
可与类固醇受体超家族成员结合的因素很多,除已认识的肾上腺皮质激素、性腺激素、甲状腺激素、维生素D和视黄酸外,现已鉴定出50多种可与受体结合的物质,如COUP-TFⅠ、COUPTFⅡ、ERR1、ERR2、TR2和NUR77等,这些DNA区段所贮存的遗传信息未明,称为孤儿基因(orphan gene,orphon)。但是,类固醇激素受体的结构保守性高,种族差异较肽类激素小得多。类固醇激素受体N端的A/B区含有活化功能区1(AF1)、C端含有由4个半胱氨酸残基形成的两个Ⅱ型锌指(Zinc fingers)结构(与DNA结合有关)。C区和D区的保守序列较短(交链区,hinge domain),C末端为E区(与配体结合有关,含第二活化功能AF2区),该区可通过招募辅因子,抑制启动子(promotor)的活性,有些受体还含有F区,其作用未明。此类受体的3个共同肽段分别称为Ⅰ、Ⅱ、Ⅲ区,Ⅰ区为富含半胱氨酸残基的DNA结合片段,而Ⅱ、Ⅲ区的变异较大。
在类固醇受体超级家族中,糖皮质激素、盐皮质激素、孕激素、雄激素(雌激素除外)的受体-激素结合区的氨基酸序列相似,同源序列达50%,各种受体与相应激素之间有交叉结合亲和力,这种交叉结合亲和力是发生受体作用“对话”(cross-talk)的物质基础。
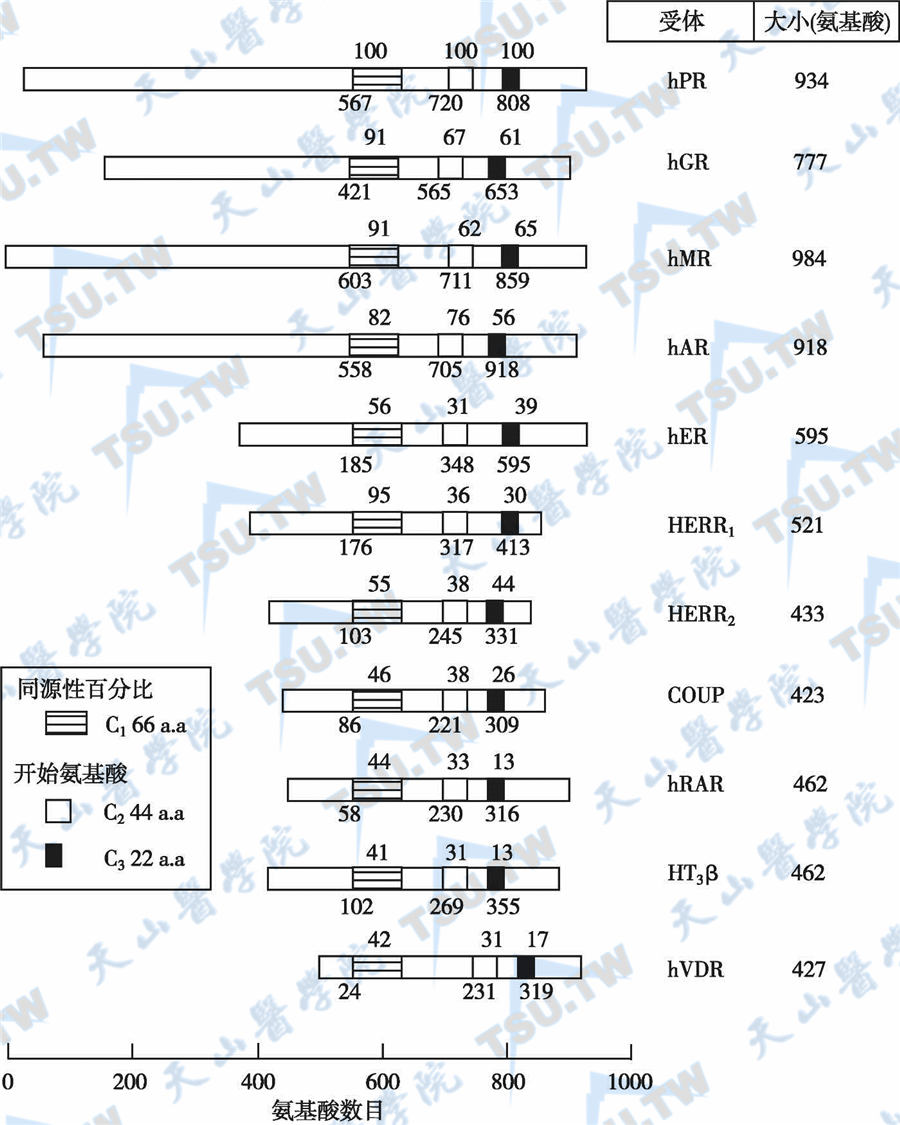
类固醇类激素家族的同源序列
注:序列同源性分布于Ⅰ、Ⅱ和Ⅲ三个区段;Ⅰ区段为DNA结合区,含66个氨基酸残基;Ⅱ区段含42个氨基酸残基;Ⅲ区段含22个氨基酸残基。hAR(human androgen receptor):人雄激素受体;hGR(human GH receptor):人生长激素受体;hMR(human melatonin receptor):人褪黑素受体;hER(human estrogen receptor):人雌激素受体;HERR1(human estrogen receptor-related receptor 1):人雌激素受体相关受体1;HERR2:人雌激素受体相关受体2;COUP:Chicken Ovalbumine Upstream Promotor;hRAR(human retinoic acid receptor):人维甲酸受体;HT3β(human T3 receptor):人T3β受体;hVDR(human vitamin D receptor):人维生素D受体
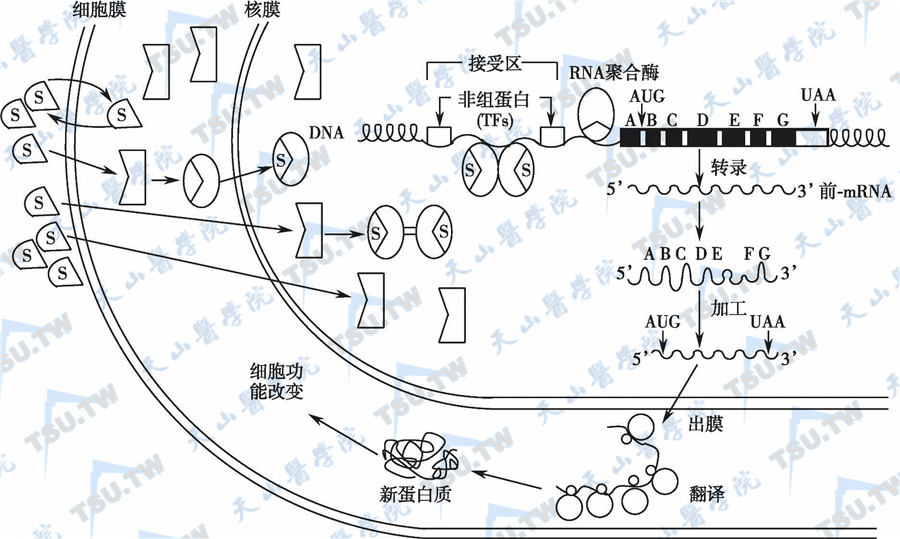
类固醇激素作用机制
注:※:类固醇激素与受体结合后,激素-受体复合物发生变构效应;激素-受体复合物与DNA应答元件结合,激活或灭活相关基因表达而发挥生物学作用。TFs为非组蛋白;S为类固醇类激素
2. 激素-受体复合物与DNA特异核苷酸序列结合
类固醇激素受体的特异性由受体分子特异性、受体结合区特异性和DNA接纳区(激素反应元件,HRE)特异性决定,所以尽管受体结构、受体结合区和HRE均有同源性,但激素效应最后表达的特异性是很高的。激素-受体复合物与DNA作用后,激素与受体因亲和力下降而离解,激素离开靶细胞被灭活,而受体可被再循环利用。
各种类固醇激素的具体作用机制有一定差异,但下列几点是共同的:
- 受体的结构类似,位于胞质内;
- DNA特异序列(应答元件,response element)只与激素-受体复合物的特异结合区结合;
- 均通过激活或阻抑相关基因的表达而发挥生物学作用;
- 均存在受体结合的激动剂(agonist)和拮抗剂(antagonist);
- 存在胞膜结合受体或结合位点,激素与膜受体结合诱导非基因转录性信号传导,使磷脂酶活化,生成三磷酸肌醇、二酰基甘油、激活蛋白激酶C和调节钙通道等,其作用迅速,与肽类激素的作用机制很相似。
3. 类固醇激素膜受体功能
目前发现,几乎所有的类固醇激素(如糖皮质激素、盐皮质激素、孕激素、雄激素、雌激素、维生素D)都存在非经典的快作用途径,这些类固醇激素与相应的膜受体结合后,激活特殊的信号通路,调节细胞功能。例如,雌激素靶细胞表达3种雌激素核受体(estrogen nuclear receptors,ER),分别称为ERα66、ERα46和ERβ。2005年,人们发现G蛋白耦联受体30(GPR30)可作为雌激素的非经典受体而发挥作用。因而人们普遍认为,G蛋白耦联受体30 (G protein coupled receptor 30,GPR30)介导了雌激素的非经典膜效应,也可被ERα和ERβ拮抗剂他莫昔芬(tamoxifen)和氟维司群(fulvestrant)激活,故认为GPR30为G蛋白耦联的雌激素受体(G-protein-coupled estrogen receptor,GPER)。后来的研究证明,GPR30通过结合ER-α36基因启动子区的激活蛋白-1(AP-1)位点而促进ER-α36表达;GPR30表达被抑制后,ER-α36表达也减弱。因此,GPR30介导的雌激素膜效应是通过ER-α36实现的,雌激素膜受体并非GPR30,而是通过ERα36实现的。
类固醇激素受体与蛋白质相互作用改变激素功能
受体单体可聚合成同二聚体,有利于激素-受体复合物与DNA结合,但受体蛋白也可与非受体蛋白结合。例如,与热休克蛋白(heat shock protein,HSP)结合,使受体与激素形成的复合物失去与DNA结合的功能。正常情况下,HSP存在于胞质中;应激时HSP集聚于核内,可活化与应激有关的基因表达。另外,类固醇激素受体均为磷蛋白,通过磷酸化途径可调节激素-受体的结合力。一般来说,受体分子中的酪氨酸被磷酸化后,激素结合力提高,磷酸化受体蛋白的电泳速度下降,表观分子量增加。
类固醇激素受体激动剂增强激素作用而拮抗剂相反
受体激动剂强化激素作用,延长激素的半衰期,增加激素-受体的亲和力等;激素受体拮抗剂则相反,可阻滞激素的作用,使靶细胞的激素作用减弱或消失。一般拮抗剂有多种类型,例如,雌激素受体拮抗剂可分为3类:①短效拮抗剂(如雌三醇);②长效拮抗剂如他莫昔芬(tamoxifen)和氯米芬(clomiphene);③生理性拮抗剂(如孕酮、雄激素、糖皮质激素等)。这些拮抗剂有与雌二醇相似的分子结构,易与雌二醇受体结合;如受体底物结构与正常激素差异较大(如睾酮),可通过受体“对话作用”表达拮抗效应。另一方面,有些拮抗剂也可表达雌二醇的某些生物学作用,如出现子宫内膜增生反应,但由于与受体结合的时间短,亲和力低,所以不会引起子宫肥大及子宫内膜增生。
孕激素拮抗剂主要来源于孕酮及其衍化物。这些拮抗剂可对抗孕酮的作用,中断子宫内膜黄体期发育,具有避孕作用。例如,孕酮受体激动剂诱导的变构效应可抵抗蛋白酶对受体的消化降解,米非司酮(mifepristone,RU486)与孕酮受体结合后,发生的受体变构效应与孕酮所诱导的反应不同。点突变分析表明,受体的C端存在阻抑区(repressor domain),当受体与激动剂结合时,阻抑区不转至分子表面而不能活化,故受体可激活基因转录过程;但当受体与拮抗剂结合时,阻抑区游离至分子表面,抑制基因转录。
