细胞因子和生物反应调节剂(BRMs)代表了一大类治疗药物,可调节宿主对肿瘤或肿瘤治疗的反应。表157- 1汇总了目前临床应用的或正在进行临床评估的生物学治疗药物。然而,生物反应调节剂这一名称不等同于肿瘤的免疫治疗,许多此类药物显示出直接抗肿瘤细胞的生物学效应,并具有调节细胞分化、抗增殖、和(或)具有细胞毒性等,这些作用并不依赖于它们的免疫调节活性。二十余年,应用细胞因子和BRMs治疗肿瘤患者始终被引起关注。
表157-1 细胞因子/生物效应调节剂
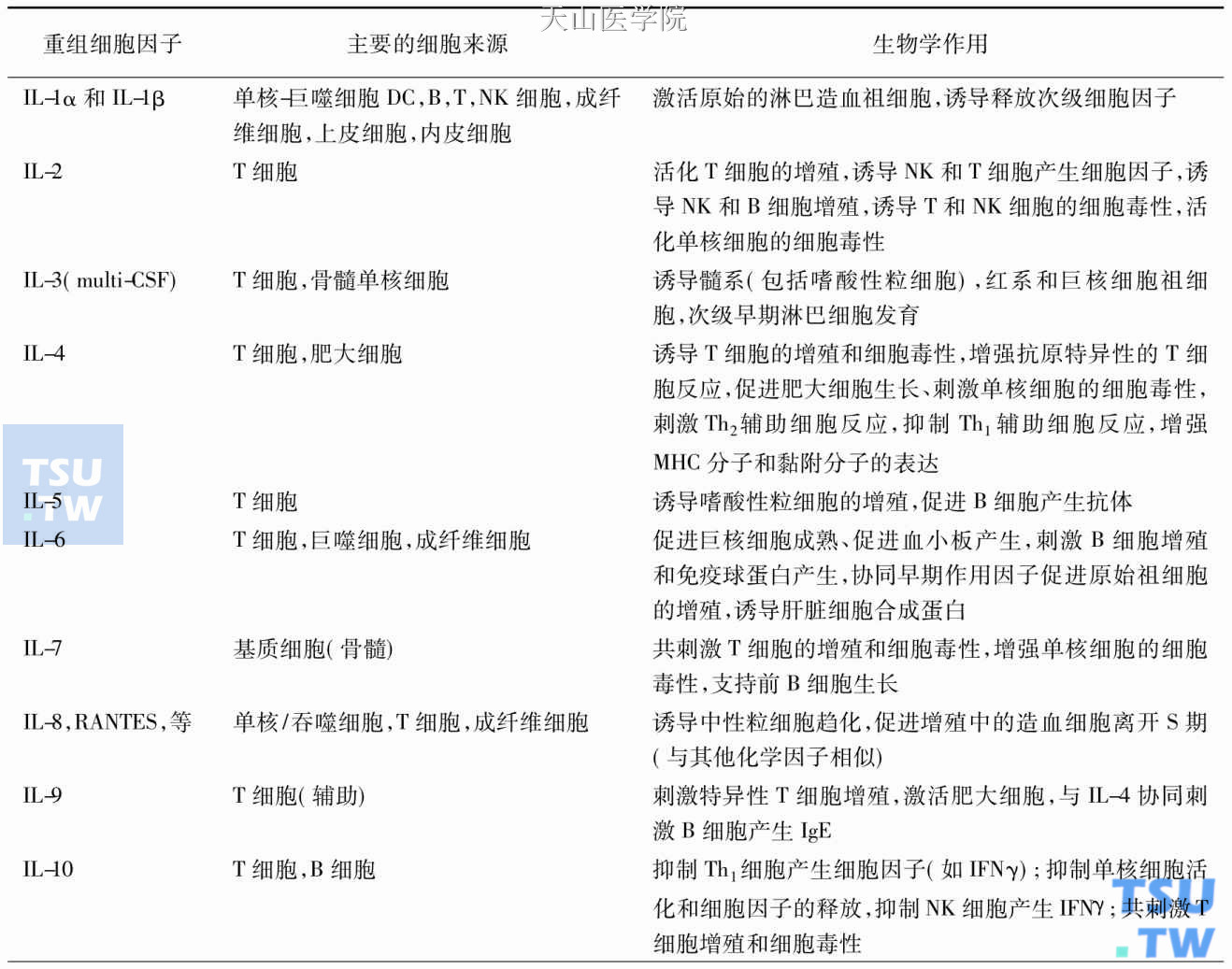
续表
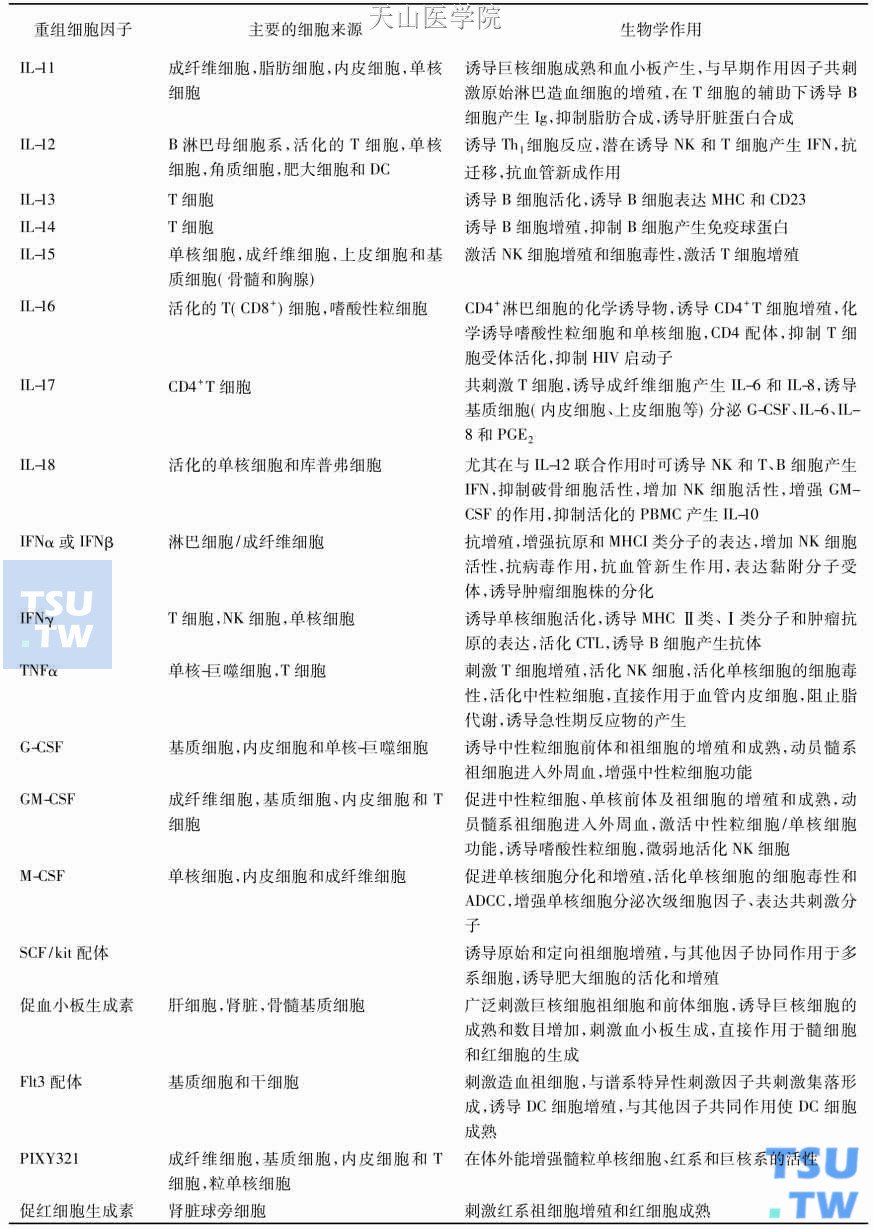
免疫细胞分泌两类可溶性蛋白,一类是免疫球蛋白(Ig)分子(抗体),与可溶性抗原结合,通过细胞表面的Ig受体活化B细胞。另一种可溶性分子由淋巴细胞和单核细胞分泌,作用于免疫系统内外的多种细胞。白介素这一名称的含义就是指白细胞间的活性。
在过去的10年中,细胞因子的治疗使血液病患者和肿瘤患者的治疗获得突破性进展。CSFs和造血生长因子(HGFs)的应用使患者可以接受大剂量的化疗,也明显减低了化疗相关毒性。此外,细胞因子治疗使许多肿瘤患者,尤其是血液系统恶性肿瘤的治疗选择进一步扩大。
当应用细胞因子治疗恶性肿瘤时,不可忽略的是,造血系统恶性细胞可不正常地表达一些细胞因子,通过自分泌和旁分泌环可能在肿瘤细胞增殖中参与其发病机制。IL- 1和TNF已经发现在所有髓系和淋巴系白血病细胞持续表达。毛细胞白血病(HCL)和B细胞慢性淋巴细胞白血病(CLL)细胞表面可检测出TNF受体,体外试验显示TNF对这些恶性细胞有促进增值和诱导分化作用。编码TNF、IL- 1和IL-6的mRNA在一些恶性淋巴细胞可被检测到。有关CLL细胞表达细胞因子和这些细胞因子对白血病细胞增殖作用,有不同的研究结论。目前,除急性髓细胞白血病(AMLs)外,没有发现细胞因子能在体内对恶性肿瘤有增殖作用。
治疗的一般原则:
细胞因子是小分子量(1 540 000Da)的糖蛋白,主要是以旁分泌或自分泌的方式发挥作用,因此是短程调节因子。细胞因子一般与细胞表面受体结合,该类受体是造血因子受体超家族的一部分,它们全部是跨膜糖蛋白,有四个位置固定的保守半胱氨酸、一个保守的WSXWS序列和Ig、纤连蛋白Ⅲ区域。这些分子的细胞内部分包括2个区域,其中一个有脯氨酸和疏水区,另一个有二个带电荷的氨基酸和疏水区。
这些区域是与细胞内分子结合的关键部分,细胞内分子如JAK激酶结合后,多数通过被称为胞质内STAT分子家族传导信号,并传至细胞核内激活基因转录。最终可通过蛋白合成的变化导致细胞增殖改变、生长抑制、细胞毒性增加,产生次级细胞因子,和(或)改变其他细胞因子的生物学效应。许多细胞因子有多重和叠加功能。一种细胞因子的作用可能取决于其局部浓度、靶细胞类型、可用的效应细胞和其他信号分子的存在。
细胞因子的治疗原则与传统的化学治疗不同。首先,对多数细胞因子而言,不存在简单的剂量依赖效应。在许多病例中,尚不清楚是否最佳的生物学剂量就是最大可耐受剂量,同时是否也是最佳抗肿瘤效应剂量。其次,化疗一旦起效,其效果迅速,相反,细胞因子的治疗反应缓慢出现,需要数月的时间才能观察到。此外,细胞因子治疗的毒性反应独特,包括发热、寒战、流感样症状,多数制剂在剂量增加时,还可出现毛细血管渗漏综合征。副作用的发生一般较急、时间短暂,随治疗终止而减轻。长期慢性的毒性反应很少,但也可发生,包括自身免疫现象和心脏毒性。
经过FDA批准应用于临床的细胞因子数量为数不多,包括粒细胞-集落刺激因子(G- CSF)和粒/单核细胞集落刺激因子(GM- CSF),主要应用于化疗或骨髓移植后骨髓抑制造成的粒细胞缺乏的恢复。促红细胞生成素(EPO),用于治疗化疗相关的贫血,人免疫缺陷病毒(HIV)相关的贫血,和肾功能衰竭导致的贫血。白介素- 11(IL- 11)用于预防化疗导致的严重血小板减少,干扰素(IFN)治疗慢性髓细胞白血病(CML),低度恶性非霍奇金淋巴瘤,毛细胞白血病(HCL),艾滋病(AIDS)中卡波西肉瘤,以及高危黑色素瘤和某些病毒感染综合征的辅助治疗。IFN还可以治疗多发性硬化,慢性肉芽肿性疾病。白介素- 2(IL- 2)用于治疗转移性肾细胞癌和转移性黑色素瘤。
本章节主要介绍造血生长因子和生物反应调节剂的临床应用,因篇幅所限,没有过多介绍这些细胞因子的生物学作用。
