阿片类镇痛药
常用阿片类药物
1)吗啡:
吗啡因为药效确切、价格低廉,经过一百多年的使用目前仍然是使用最为广泛的阿片类药物之一。单次静脉注射吗啡后几分钟即可起效,30分钟达高峰,持续2~3小时。皮下和肌内注射吗啡的峰效应时间为45~90分钟,作用持续3~4小时。口服即释吗啡30分钟左右起效,1~2小时达峰效应,作用时间4~5小时。吗啡控释片(美施康定)起效较慢,达峰值时间3~4小时,但能维持8~12小时相对稳定的血药浓度。
吗啡在临床上主要用于中、重度急性疼痛和癌痛治疗,某些重度慢性非癌性疼痛如神经病理性疼痛也可适当应用。国内可供选择的剂型有口服的吗啡即释片、吗啡缓释片和吗啡控释片,以及吗啡注射液。
吗啡能通过胎盘,可能抑制新生儿呼吸,所以一般不用于孕妇。同时吗啡还有组织胺释放作用,哮喘和COPD患者慎用。其他不良反应见下文。
2)芬太尼:
芬太尼和吗啡一样是μ阿片受体强激动剂,作用强度是吗啡的50~100倍。目前剂型有静脉注射液和经皮贴剂。单次给药后5分钟左右达到峰效应,作用持续约60分钟。用于急性疼痛治疗时通常单次给药0. 5~2. 0μg/kg,或使用静脉PCA给药。芬太尼由于脂溶性好,静脉持续给药容易产生蓄积,应警惕副作用的产生。慢性疼痛也可使用芬太尼静脉PCA治疗。
经皮芬太尼贴剂(多瑞吉)是通过皮肤吸收的新型芬太尼制剂。其优点是使用方便、血药浓度较稳定、适用于无法口服用药的患者等,缺点是可调性欠佳、首次使用起效较慢等。未使用过阿片类药物的患者应先进行剂量估算,可通过口服吗啡或静脉PCA预先估算出每天对镇痛药物的大致需要量,然后换算成多瑞吉剂量。
3)羟考酮:
羟考酮是μ和К阿片受体的激动剂,除了类似吗啡的药理作用,对于内脏痛效果更佳,镇痛作用强度是吗啡的1. 5~2倍。控释型羟考酮(奥施康定)服用后约3小时达到峰值,由于采用了特殊的AcroContin控释技术,药物作用持续约12小时。该药必须整片吞服,严禁嚼碎或研磨后服用,因为破坏了该控释系统后,羟考酮快速释放、迅速吸收将导致严重的不良后果。
4)舒芬太尼:
舒芬太尼对μ受体的亲和力比芬太尼强7~10倍,静脉给药3~4分钟后起效,单次给药作用时间与芬太尼相似。非麻醉状态下单次用药一般给予0. 1~0. 3μg/kg。但由于舒芬太尼脂溶性是芬太尼的两倍,更易在体内蓄积,所以连续给药时清除半衰期明显延长。舒芬太尼的安全指数(半数致死剂量/半数有效剂量)为2521,明显高于芬太尼(277)和吗啡(69. 5)。
5)哌替啶:
即度冷丁,是μ受体激动剂,对К 和δ受体也有中度亲和力。镇痛强度是吗啡的1/ 10。临床上常用50mg哌替啶肌注治疗成人急性疼痛,也可静脉注射25~50mg哌替啶。哌替啶相对其他阿片类药物对呼吸的抑制作用较轻,但静脉给药仍需注意给药速度,以免过度镇静引起呼吸道梗阻。
哌替啶对δ受体的兴奋导致幻觉和欣快感的产生,使该药比吗啡和芬太尼更容易成瘾。临床上长时间使用哌替啶镇痛,容易导致患者在疼痛消失后仍有觅药行为,其根源是追求用药后的欣快感。此外,哌替啶的代谢产物去甲哌替啶有药理活性,可导致中枢兴奋、肌阵挛、震颤甚至惊厥。因此,不建议长时间大剂量使用哌替啶治疗急性疼痛,也不建议使用哌替啶治疗慢性疼痛包括癌痛。
药物的选择
对于不同程度的疼痛应采取不同的药物和治疗方案(表155- 1、155- 2)。根据世界卫生组织(WHO)制定的镇痛阶梯方案,轻度疼痛患者可以使用非阿片类药物,包括阿司匹林、对乙酰氨基酚等。中度疼痛患者可使用中效阿片类药物辅以上述非阿片类镇痛药物,前者包括:可待因、羟考酮、曲马朵等。严重疼痛时,需要选择使用强效阿片类药物如吗啡、羟考酮、氢吗啡酮、美沙酮和芬太尼。同时合并使用非阿片类药物。(表155- 1和表155-2)
表155-1 常用镇痛药物的使用方法
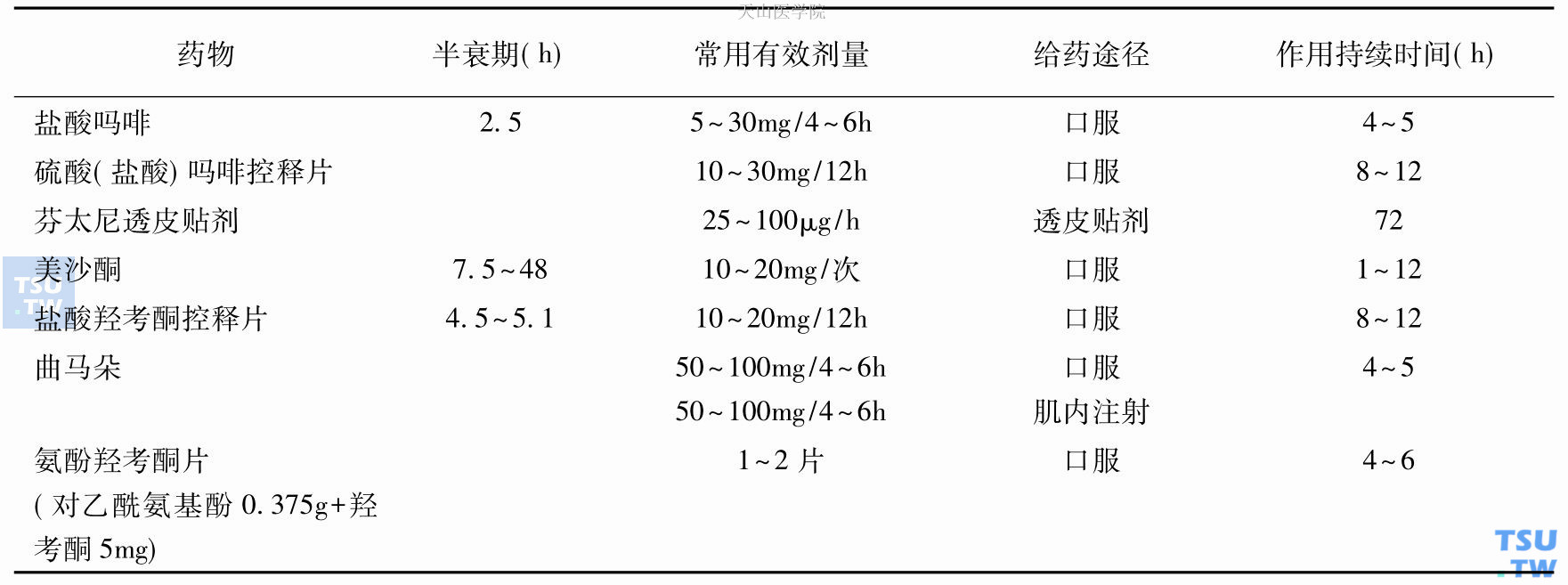
表155-2 阿片类药物剂量换算表
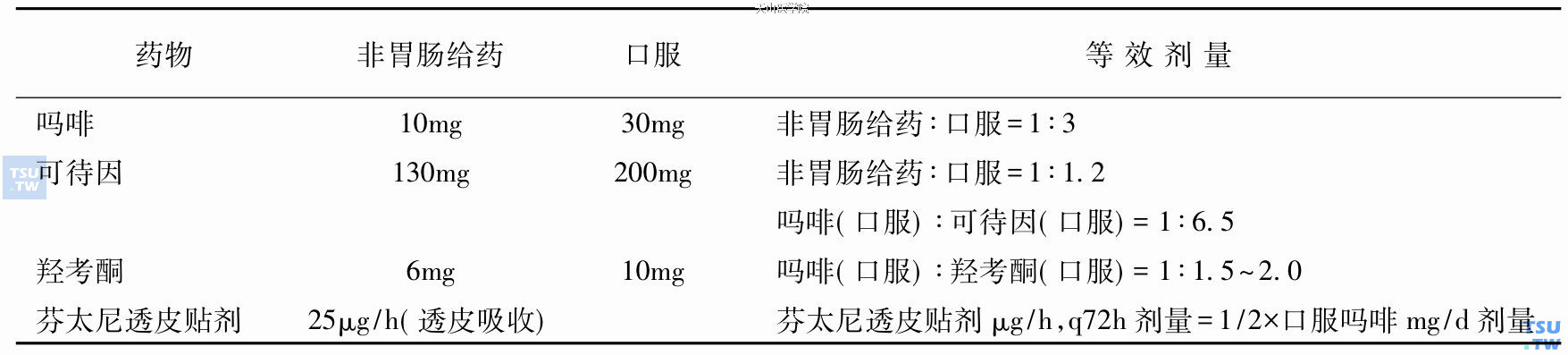
WHO对慢性疼痛的治疗原则还包括:
1)从口服用药开始;
2)定时给药;
3)镇痛方案个体化;
4)按阶梯给药。
给药途径的选择
镇痛药物有多种给药途径:无创给药途径包括口服、经直肠(塞肛)、经皮、经黏膜,有创途径包括静脉、肌注、皮下、椎管内等。给药途径的选择决定于:①疾病和疼痛本身因素;②患者因素:患者全身情况、患者的主观要求;③用药途径和药物的因素:药效、起效速度、持续时间、使用方便性等。
从起效速度而言,单次静脉给药的起效速度较快,适用于急性疼痛或慢性疼痛患者的爆发痛(breakthrough pain)。经静脉单次给予阿片类药物应该警惕血药浓度迅速达到峰值时可能产生的阿片类药物相关副作用,尤其是可能威胁生命的呼吸抑制。经静脉连续小剂量给药可以避免峰药浓度和峰效应的产生,但对于突发性疼痛或疼痛程度变化较大的情况镇痛效果较差。通过病人自控镇痛装置(patient- controlled analgesia device,PCA)可以在一定程度上解决这种矛盾。PCA是一种由病人自己控制给药的镇痛装置,可通过静脉、皮下或椎管内给药。其机制是通过少量单次给药,使血药浓度相对稳定,以便在减小给药总量的同时尽量达到最佳镇痛效果和最少的不良反应。在突发疼痛或疼痛程度变化时患者可通过自行给药减轻疼痛。
肌内注射对于没有静脉通路的患者或者暂时无法建立静脉通路的患者如小儿是较方便迅速的选择。肌注给药起效比静脉给药慢,而且起效速度不确定,与是否注射在肌肉内和局部血液循环有关。由于镇痛效果和时间的可控性较差,加之有注射痛,肌肉镇痛的应用日趋减少。
经皮芬太尼贴剂(多瑞吉)的吸收途径是先聚集在皮内,然后被皮下血管吸收,所以起效时间较慢。首次使用后12~20个小时才能达到稳定的血药浓度;揭除该贴剂24小时后,仍有50%的药物存留体内。经鼻黏膜给予常规剂量芬太尼5~10分钟后可以达到血浆药物峰浓度,适用于儿童镇痛和爆发痛的治疗。由于药物可能从咽部流失,每次给药量一般小于0. 15ml。经口腔黏膜给予枸橼酸芬太尼4~5分钟起效,约22分钟达到血浆药物峰浓度。
对于慢性疼痛患者,能够口服的患者建议口服用药。中、重度慢性疼痛患者因为各种原因无法口服用药时,可以考虑非胃肠道用药,主要包括经皮芬太尼贴剂、静脉连续用药、病人自控镇痛装置等。
阿片类药物的副作用
阿片类药物的副作用与其镇痛作用一样,也是阿片受体激动效应的表现。其中后果最严重的是呼吸抑制,发生率最高的则是恶心和呕吐。恶心、呕吐、镇静、呼吸抑制和尿潴留是短暂的副作用,在持续用药数天或1~2周后均会减轻或消失。
1)呼吸抑制:
呼吸抑制是阿片类药物最危险的副作用,多见于药物过量。阿片类药物导致的呼吸抑制特点是呼吸变深变慢。如果不存在过度镇静引起的呼吸道梗阻,呼吸频率大于每分钟8次的患者一般尚能保证通气,无需特殊处理。但存在其他低氧高危因素如小儿、肺部疾病尤其是COPD和睡眠呼吸暂停综合征、合并使用其他镇静药物、合并颅内疾患可能导致中枢性抑制者,有发生低氧血症的危险。
对于呼吸抑制的患者首先应该保证呼吸道通畅,然后给予纯氧,同时予以辅助通气。通过托下颌和使患者头后仰可以改善舌后坠,患者意识不清且舌后坠严重者可放入口咽通气道或鼻咽通气道,有凝血功能障碍的患者应注意保护黏膜避免出血。必要时应行紧急气管插管和机械通气,以保证氧合,缓解呼吸抑制引起的高二氧化碳血症。确认或高度可疑患者发生了阿片类药物导致的呼吸抑制和低氧时,应使用阿片受体拮抗药如纳洛酮进行拮抗。单次给予0. 1~0. 2mg纳洛酮,可重复给药,但应注意在拮抗了阿片类药物的作用后,患者会很快出现疼痛,甚至发生疼痛加重、心率加快,严重时还可能发生肺水肿。而另一方面,也要注意阿片类药物的作用时间可能比纳洛酮时间(4~6小时)更长,必要时应重复给药。
2)恶心和呕吐:
恶心呕吐的产生机制是药物刺激了中枢化学感应带、前庭核以及胃肠道阿片受体。止吐药物主要包括:促进胃肠蠕动的药物、5-HT3受体拮抗剂、丁酰苯类、甾体类。多潘立酮(吗叮啉)和甲氧氯普胺(胃复安)均可促进胃肠蠕动,对轻度恶心呕吐有效。5- HT3受体拮抗剂主要有昂丹司琼(4~8mg,2次/d,iv)、格雷司琼(3mg,1~2次/d,iv)、托烷司琼(5mg,1次/d,iv),是作用较强的抗呕吐药物。丁酰苯类药物氟哌利多治疗恶心效果很好,但可能引起QT间期延长和室性期前收缩。注意对于有窦缓和心脏传导阻滞的患者应谨慎或禁用,用药时从小剂量开始,0. 5~1. 0mg即有效,没有明显心血管副作用的情况下可酌情少量重复用药。目前对于严重、顽固性恶性呕吐患者,可以使用三联治疗方案,即联合使用5- HT3受体拮抗剂-氟哌利多-地塞米松,从不同机制进行镇痛,副作用小且效果很好。
3)便秘:
便秘是阿片类药物唯一不能产生耐受的副作用,主要由于阿片类药物延缓胃排空、减低肠道前向蠕动、括约肌收缩、消化液分泌减少等所致。治疗方法主要包括粪便软化剂、膨化剂、促进胃肠蠕动的药物,轻度便秘时可采取高纤维饮食、使用山梨醇、乳果糖或福松,效果不佳时可使用番泻叶、硫酸镁等较强的导泻药物。但严重便秘时首先应排除肠梗阻,必要时使用开塞露也可促进排便。
4)其他副作用:
阿片类药物的其他副作用还包括肌强直、尿潴留、皮肤瘙痒等。
非阿片类镇痛药
曲马朵
曲马朵是中枢性镇痛药,作用机制复杂,主要是抑制神经元重新摄取去甲肾上腺素和5-羟色胺,以及兴奋μ受体(作用较弱)。口服曲马朵50~100mg对中度疼痛有较好的效果,静脉用药可单次给予曲马朵注射液2~3mg/kg。由于对μ受体的兴奋作用较弱,阿片类相关的副作用(如呼吸抑制)也较轻。正因如此,曲马朵被认为是安全性较高的药物。副作用主要包括嗜睡、恶心、呕吐、头晕等。
非甾体类抗炎药(NSAIDs)
非甾体类抗炎药适用于轻度和中度疼痛的治疗,也可合并阿片类药物用于重度疼痛的治疗。NSAIDs药物的作用机制是通过抑制环氧化酶(COX)减少参与疼痛产生的炎性介质的产生。COX分为正常组织中的COX-1以及酶诱导产生的COX- 2。NSAIDs通过对COX- 1 和COX- 2作用的选择性不同,可以分为三大类。NSAIDs对COX- 2的选择性抑制可以抗炎镇痛,而对COX- 1的抑制,则可导致对消化道、肾脏、血小板等的不良影响。在使用NSAIDs药物时,如果药物对COX- 1具有较高的选择性抑制,则应充分了解患者是否有消化道溃疡、消化道出血史、是否有出血倾向、肝肾功能不全等病史。在用药上注意严格掌握适应证和禁忌证;小剂量、短时间用药;联合用药以减轻副作用。
1)非特异性COX抑制剂:同时抑制COX- 1和COX- 2,如布洛芬、萘普生、大剂量阿司匹林等。在消炎镇痛的同时,可产生对消化道等的不良反应。不宜长期大剂量使用。
2)特异性COX- 1抑制剂:只抑制COX- 1,不抑制COX- 2。只有小剂量阿司匹林属于此类。
3)选择性COX- 2抑制剂:在抑制COX- 2时并不明显抑制COX- 1,大剂量用药时也抑制COX- 1。如美洛昔康、尼莫舒利等。
4)特异性COX- 2抑制剂:由于对COX- 2的选择性极高,可近似地认为这类药物只抑制COX- 2,不抑制COX- 1。代表药物有罗非昔布、塞来昔布和帕瑞昔布。
辅助性镇痛药
1)抗惊厥药物:
抗惊厥药物是治疗神经病理性疼痛的重要药物,主要通过阻断钠通道、改变钙通道、稳定神经元细胞膜、影响GABA受体、P物质的产生等机制起作用。用于镇痛的这类药物主要有:加巴喷丁、普瑞巴林、卡马西平、拉莫三嗪等。
加巴喷丁的患者耐受性较好,国内一般推荐600mg/d开始,分3次服用。为降低主要副作用如头晕、嗜睡和思维混乱等,一般采用逐渐加量和逐渐增加用药次数的方法达到合适剂量,比如第一天200mg/次,夜间服用;第二天200mg/次,服用2次;第三天200mg/次,服用3次。国外报道最大剂量达到3600mg/d,但每周增加剂量最好不超过300mg。该药从肾脏代谢,肾功能不全患者清除时间延长。
卡马西平常用于治疗三叉神经痛(NNT:NUMBER- NEED- TO- TREAT为2),也可用于其他神经病理性疼痛的治疗。临床主要用法为:初始剂量100mg/次,3次/d。可逐步加量,建议每日剂量不超过1200mg。主要副作用为嗜睡、头晕、共济失调、恶心呕吐等,部分患者因为这些副作用而放弃用药。此外,还要注意血液系统的副作用如粒细胞减少和再生障碍性贫血。长期服用卡马西平的患者建议至少半年复查一次血常规。
2)抗抑郁药物:
慢性疼痛患者、神经病理性疼痛患者常有抑郁,抑郁也可加重患者对疼痛的感觉。但使用抗抑郁药物治疗神经病理性疼痛并非因为这些药物有抗抑郁作用,其镇痛机制比较复杂,主要包括:①5-羟色胺、去甲肾上腺素神经递质的调节作用;②阿片受体激动作用;③钠离子通道阻断作用;④NMDA受体阻断作用;⑤GABA受体激动作用。
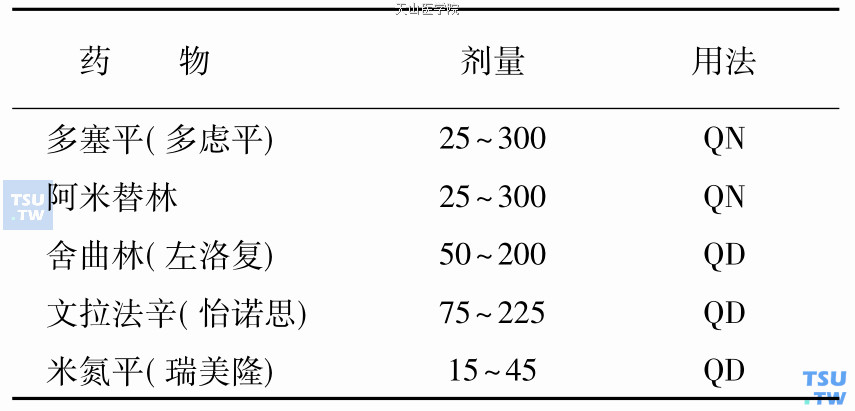
用于疼痛治疗的抗抑郁药物主要有三环类抗抑郁药物(TCAs)、选择性5- HT和DA再摄取抑制剂(SNRIs)、非典型抗抑郁药等。选择性5- HT再摄取抑制剂(SSRIs)对神经病理性疼痛效果微弱。其中TCAs代表药物为阿米替林和多塞平。由于具有M1受体阻断作用,患者可出现中枢性抗胆碱能症状如谵妄、舞动症等,还可能出现外周性抗胆碱能症状如口干、视力模糊、便秘、尿潴留等。文拉法辛是SNRIs类药物,在治疗多发性神经痛时NNT约5. 5。米氮平作用机制与上述药物不同,通过阻断中枢突触前α1受体和异源的肾上腺素受体,加强对去甲肾上腺素能和5- HT能的神经传导。该药有良好的耐受性,相关的副作用发生率低。应该避免不同抗抑郁药物之间联用产生多重抑制,也应避免曲马朵与抗抑郁药联用,因为曲马朵也作用于单胺能系统(表155- 3)。
表155-3 常用抗抑郁药物的使用方法