-
激素治疗前列腺癌副作用的处理
因为睾酮是男性激素的基础,它的缺少与一系列的副作用有关。直到最近,雄激素剥夺治疗(ADT)的研究聚焦在睾酮缺少出现的副作用上,如潮热、性欲下降、情绪不稳、心情忧郁等,虽然很少
1 -
治疗前列腺癌中放射治疗的新辅助激素治疗
目前针对各种不同的癌症类型,采用系统化治疗(化疗和激素疗法)与局部疗法相结合的方法,使治疗效果取得了进步。当确定治疗目标为控制局部病情,那么初始化的系统性辅助和(或)伴随治疗
2 -
前列腺癌治疗间歇性雄激素剥夺疗法
20世纪80年代中期开始,雄激素剥夺疗法(ADT)采用了黄体生成素释放激素(LHRH)激动剂,并逐渐成为治疗晚期和复发性前列腺癌的主要方式。和其他可选择的治疗方式相比,LHRH激动剂具有可
3 -
雄激素剥夺治疗前列腺癌的时机
目前,关于即刻还是延迟使用雄激素剥夺治疗(ADT)前列腺癌,成为新的争论焦点。对于伴有症状的前列腺癌患者和那些处于进展期的患者而言,很显然需要采取迅速有效的治疗措施。一般而
4 -
前列腺癌的内分泌治疗治疗适应症
内分泌治疗用于治疗晚期前列腺癌已有超过60年的历史了,但是,目前仍有一些争议性的问题,比如治疗时机的选择、治疗持续时间及药物种类的选择、给药的方式等。特别是前列腺癌内分
5 -
抗雄激素药物治疗及联合放疗前列腺癌的疗效分析
现有治疗方式包括采取抗雄激素单药治疗、黄体生成素释放激素(LHRH)激动剂单药治疗,以及放疗联合使用抗雄激素治疗。通过睾丸去势和类似物降低雄激素往往与性欲减退、性功能障碍
7 -
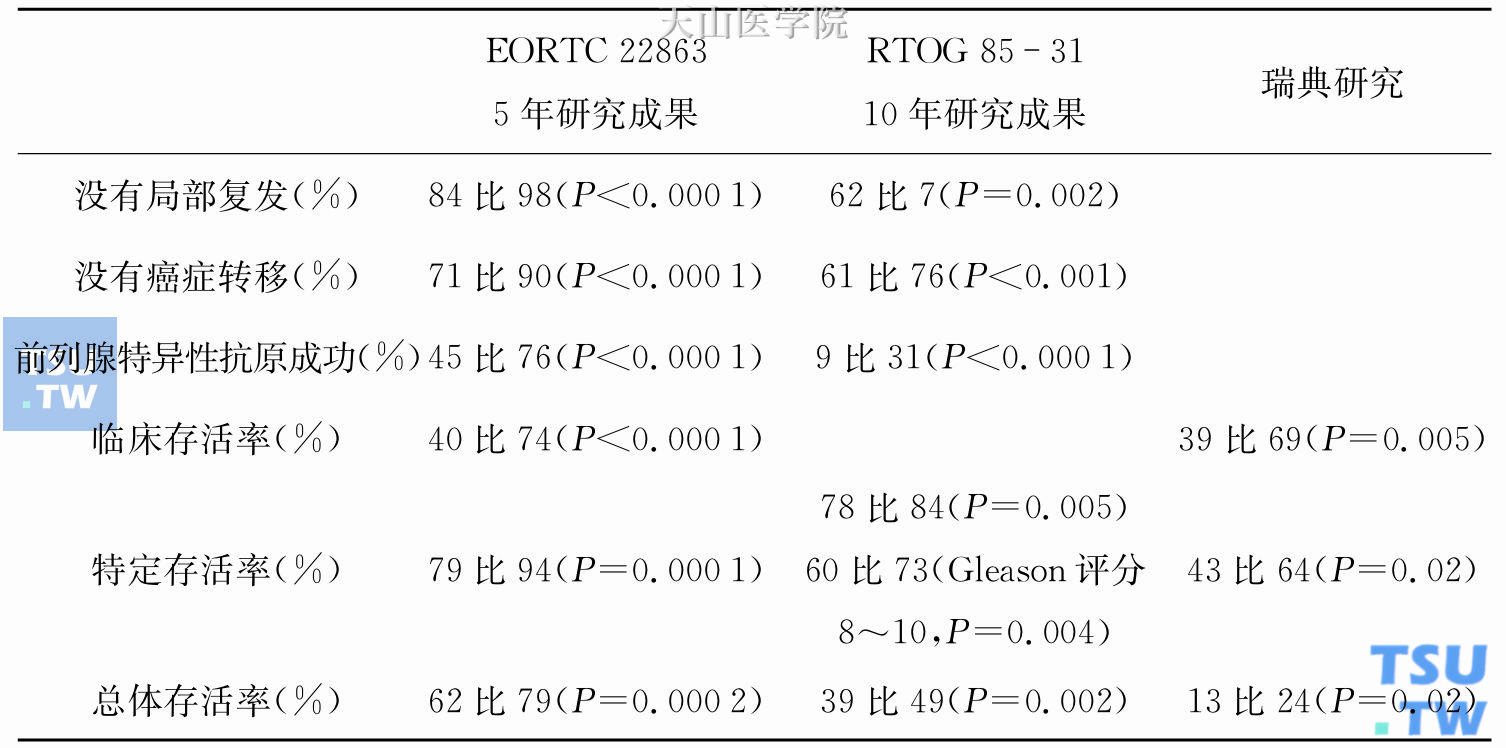
辅助雄激素剥夺疗法对前列腺癌放射疗法的作用
如前所述,长期辅助雄激素剥夺疗法的原理就是采用了“空间协作”的治疗手段,即有效治疗微转移灶而不仅仅限于局部治疗。现在普遍认同,辅助雄激素剥夺疗法已对乳腺癌的
8 -
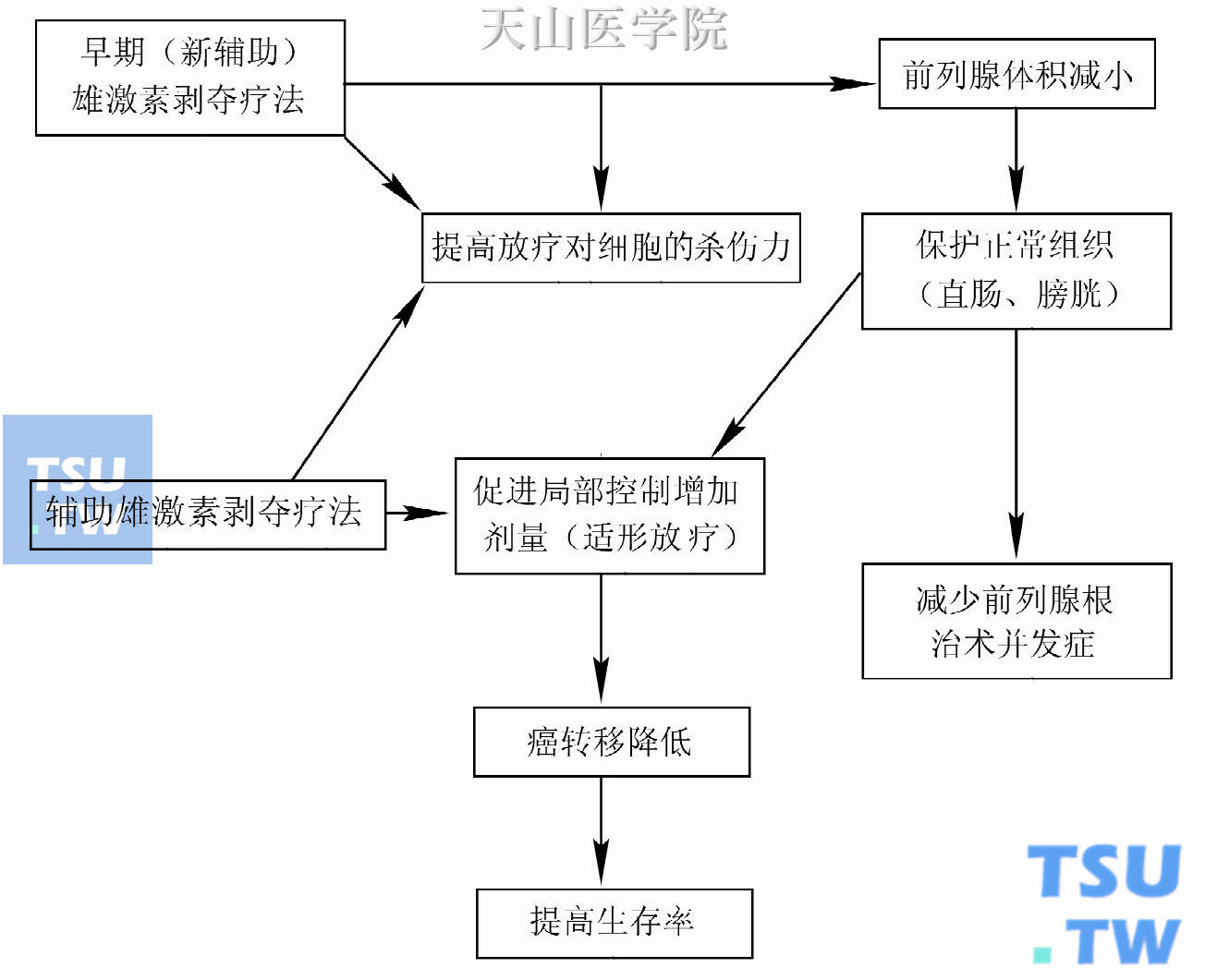
新辅助雄激素剥夺疗法对前列腺癌放射疗法的作用
新辅助雄激素剥夺疗法能够在两个方面提高前列腺癌放疗的治疗率。首先,联合治疗方式在一个额定的放疗剂量下,比单一前列腺癌放疗能够杀死更多的肿瘤细胞。这一机制可能依赖于两
9 -
有关前列腺癌放射治疗的新辅助激素治疗
目前针对各种不同的癌症类型,采用系统化治疗(化疗和激素疗法)与局部疗法相结合的方法,使治疗效果取得了进步。当确定治疗目标为控制局部病情,那么初始化的系统性辅助和(或)伴随治疗
10 -
前列腺癌药物雄激素剥夺治疗后睾丸激素的恢复
在过去,雄激素剥夺治疗仅仅在晚期疾病中使用,并仅使用相对短的一段时间,现在由于分期的变化及关于放疗并辅助雄激素剥夺治疗的Ⅲ期临床试验结果,这一做法发生了改变,间歇治疗也引
11 -
间歇内分泌治疗前列腺癌
间歇内分泌治疗(intermittent hormonal therapy,IHT)是指前列腺癌患者内分泌治疗一段时间后血清睾酮水平下降至去势水平,PSA降至正常水平以下即停止治疗,然后根据肿瘤进一步发展
12 -
前列腺癌全雄激素阻断治疗
雄激素剥夺治疗可显著抑制睾丸产生睾酮,去势后可去除血清中90%的睾酮,但另外10%的肾上腺来源的雄激素仍有可发挥作用。而65岁以上的男性,其睾酮的产生与年青人不同,其60%的睾酮
13 -
前列腺癌抗雄激素治疗
20世纪60年代末至70年代初研制出了可以阻断睾酮受体的抗雄激素药物。根据其分子结构的不同,分为甾体类和非甾体类两种。甾体及非甾体抗雄激素或雄激素受体拮抗剂(AA,如比卡鲁胺
14 -
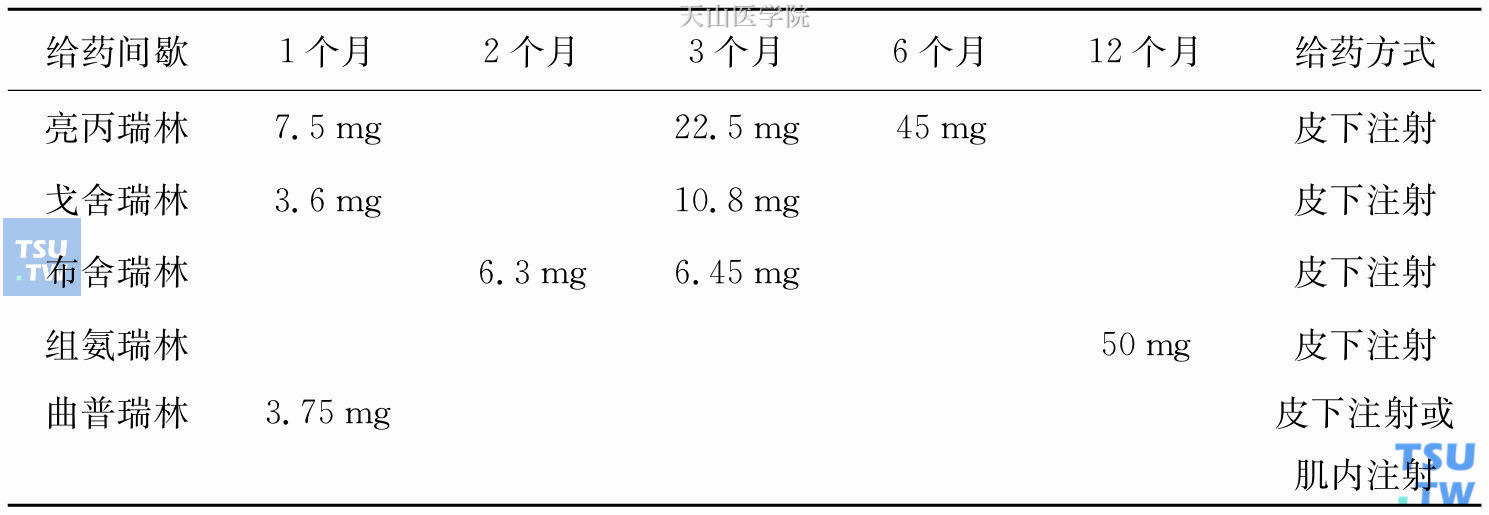
前列腺癌雄激素剥夺治疗:LHRH激动剂及拮抗剂
雄激素剥夺治疗(androgen deprivation therapy,ADT)指采用LHRH激动剂(LHRH-a)或拮抗剂来降低体内的雄激素,是目前临床上较为常用的去除雄激素的药物治疗方式。LHRH激动剂20世纪70
15 -
雄激素治疗前列腺癌
研究表明,血液中大量雌激素能抑制下丘脑LHRH的分泌,从而减少垂体黄体生成素(LH)的释放,进而减少睾丸间质细胞产生睾酮。此外,雌激素还能够竞争性地与雄激素受体结合以降低睾酮对前
16 -
睾丸切除术治疗前列腺癌
外科去势通常被认为是去除睾丸激素的金标准。双侧睾丸切除可迅速、有效地降低体内的雄激素,是目前国内外转移性前列腺癌雄激素阻断治疗的标准手段。1941年8月,Huggins等报告了
17 -
前列腺癌的内分泌治疗
1941年,Huggins和Hodges首次证实了手术去势和雌激素对前列腺癌的治疗效果后,前列腺癌的内分泌治疗即在临床上得到了广泛的应用,研究者们对前列腺癌的内分泌治疗进行了大量的研
18 -
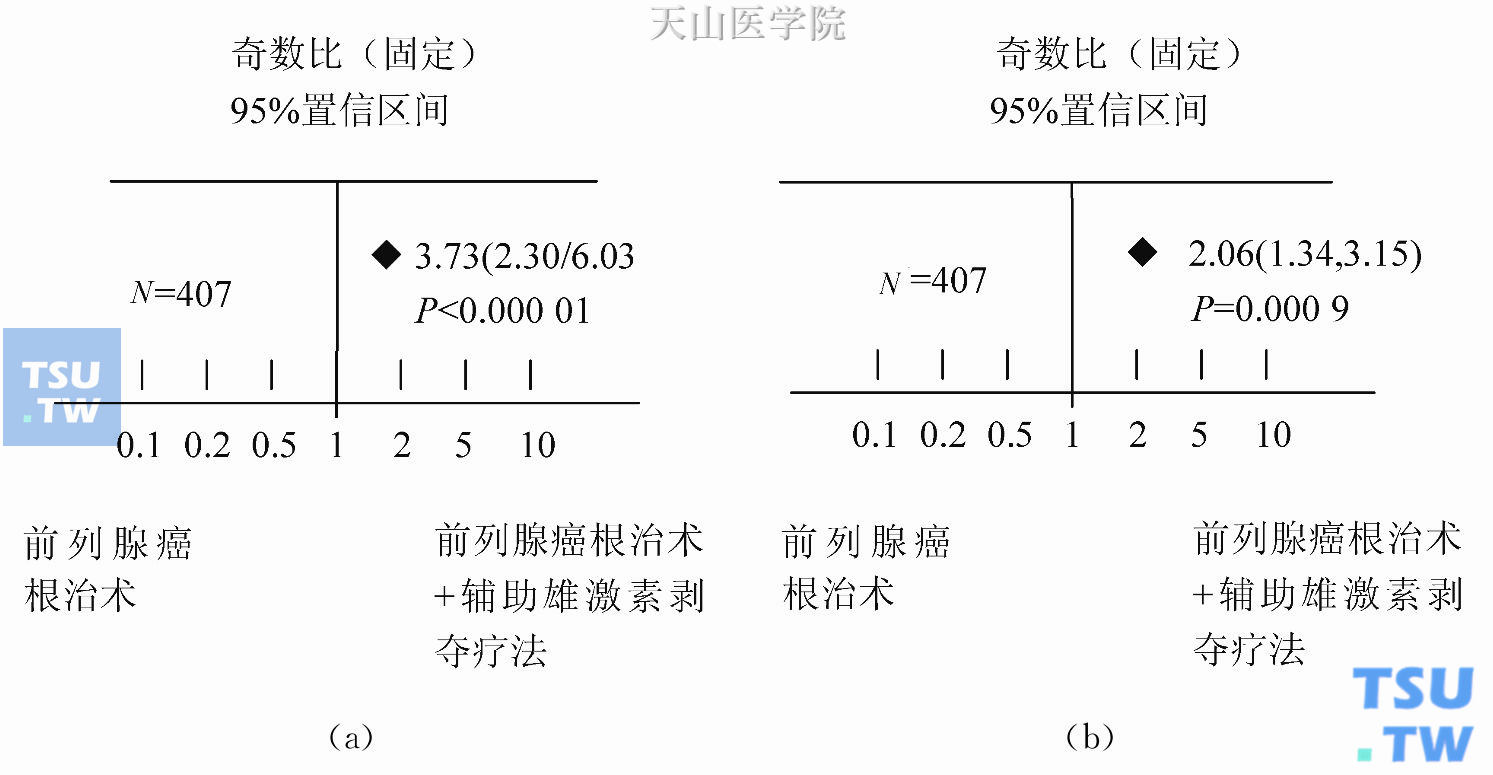
前列腺癌根治术后辅助雄激素剥夺疗法
前文所述的Meta分析结果表明,在前列腺癌根治术后进行雄激素剥夺疗法与仅采取前列腺癌根治术相比,并不能获得总体存活率方面的优势,但是对5年期(P<0.000 01)(图12-1a)和10年期(P=0.000
19 -
前列腺癌根治术的新辅助雄激素剥夺疗法
根据Cochrane的Meta分析,前列腺癌根治术(RP)结合3个月新辅助雄激素剥夺疗法,对促进总体存活率或者无进展存活率并无多大作用。然而,手术切缘阳性率明显下降(P<0.000 01),而且对其他病
20