新辅助雄激素剥夺疗法能够在两个方面提高前列腺癌放疗的治疗率。首先,联合治疗方式在一个额定的放疗剂量下,比单一前列腺癌放疗能够杀死更多的肿瘤细胞。这一机制可能依赖于两种治疗方法诱导细胞凋亡对细胞死亡的协同增强作用,从而改善局部病情控制。其次,初步收缩的前列腺和前列腺癌组织,能够影响放射治疗量的有益修正。辐射靶体积的减小,降低放射治疗量可能对治疗率产生积极影响,与标准辐射治疗剂量相比,能够降低对邻近器官的后遗症影响;或者通过提高辐射剂量(使用适形放射技术),在维持辐射并发症水平的基础上提高肿瘤控制率。
前列腺体积缩小和辐射量的关系
雄激素剥夺疗法能使患者在3~6个月时间里,前列腺的体积减小20%~50%。在这些类似的研究中前列腺体积缩小的程度不一,可能是因为这些患者本身的前列腺体积不同。研究证明,雄激素剥夺疗法中前列腺肿瘤组织的体积减小程度比良性前列腺组织更大。如果将激素治疗后的前列腺体积,用来建立临床治疗靶体积,那么这个高密度治疗区域中的直肠体积可以减小。
Dearnaley等人报道了一个前列腺癌适形放疗的剂量递增研究,在三阶的试验研究中,127名男性患者被随机分成接受64Gy和74Gy的两个组。同时这些患者又被随机分成临床靶目标体积各向同性边缘余量1 cm和1.5 cm两个组。2年跟踪随访表明,两组患者取得等效的前列腺特异性抗原控制率。然而,美国放疗协助组报告,2年后1 cm组和1.5 cm组的直肠的毒性评分分别为13%和21%,证明放疗体积对直肠毒性有影响,这项研究结果同时被Fiorino等人报告证明。因此,人们使用新辅助雄激素剥夺疗法,希望降低直肠并发症的风险和潜在的增加剂量可能。但必须注意,确保在雄激素剥夺疗法治疗的前2个月内不能安排前列腺放射疗法,在前列腺放疗完成之前前列腺体积仍旧在收缩,可能会增加直肠照射量,导致直肠毒性增加。
新辅助雄激素剥夺疗法和放射治疗的试验模型
由于缺乏现成的试验模型,采用新辅助雄激素剥夺疗法和放射治疗的联合治疗试验研究一直受到阻碍。然而两个研究小组,对这项研究做出了贡献。马萨诸塞州综合医院的Zietman及其同事依靠裸鼠的移植Shionogi雄激素依赖性乳腺癌细胞,对联合采用雄激素剥夺疗法和放射疗法进行了探讨。在采用放射疗法的12 d之前对睾丸完成预期处理(新辅助疗法),TCD50的指标有了明显下降(也就是说,肿瘤细胞的50%得到了控制)。与仅采用放射疗法和联合疗法相比,TCD50从86Gy下降为43Gy。有趣的是,在放射疗法后的1~12日内处理睾丸则会取得很小的治疗效果(TCD50分别为69Gy和75Gy)。安德森癌症中心的研究人员,利用Dunning R3327-G老鼠的前列腺肿瘤进行实验,也同样证明雄激素剥夺疗法和放射疗法之间存在着超依附性的联系。但是雄激素剥夺疗法要比放射疗法提前3 d实施,这个时候细胞凋亡指数和对照组相比增加了5~10倍。研究提示如果雄激素剥夺疗法和放射疗法一起实施,就没有效果。这些研究表明,对联合采用雄激素剥夺疗法和放射疗法的时间安排和前后顺序对能否取得良好的结果至关重要。
新辅助雄激素剥夺疗法和放射疗法的相关临床试验
主要有5个随机对照试验(RCT)报道了放射疗法同时采用雄激素剥夺疗法和不采用雄激素剥夺疗法之间的差别。所有的这些试验证明,同时采用这两种疗法无论对患者整体存活率还是防止PSA指数失败都有促进作用。
首次三阶试验是由美国肿瘤放疗协助组(RTOG)实施(86-10协议),随机抽取了471名患有较大的原发性肿瘤的患者(T2~T4期),这些患者没有发生转移现象。在采用体外放射疗法联合雄激素剥夺疗法组或者仅采用体外放射疗法组的患者中,在治疗前2个月和治疗期间,分别给他们每4周3.6 mg戈舍瑞林和每日3次250 mg氟他胺。对1987~1991年之间所有接受治疗的患者,采用雄激素剥夺疗法联合外照射放疗组与仅采用外照射放疗组的平均随访时间分别为11.9年和13.2年。最近所有报告的试验结果继续显示,联合疗法对10年间的特定疾病死亡率具有极显著效益(雄激素剥夺疗法结合外照射放疗死亡率为23.3%,单独外照射放疗为35.6%,P=0.011)。联合疗法和外照射放疗的10年的发生远处转移的失败率,分别为34.9%[95%置信区间(CI),28.5%~41.3%]和46.9%(95%CI,40.3%~53.3%)。10年间联合疗法和外照射放疗的生化失败率分别为65.1%(95%CI,58.6%~71.6%)和80%(95%CI,74.7%~85.4%)。据统计10年间无病生存率也得到了明显进步,联合疗法和外照射放疗的无病生存率分别为11.2%(95%CI,7.0%~15.6%)和3.4%(95%CI,1.0%~5.8%)。虽未经统计,但联合疗法相对外照射放疗10年间对总体存活率优势分别为42.6%(95%CI,35.9%~49.3%),33.8%(95%CI,27.5%~40.1%)。也许这项试验最具临床意义的结论是雄激素剥夺疗法对疾病远处转移率的影响。接受外照射放疗的患者中40%在治疗5年后发生骨转移。而接受联合疗法的患者中,40%在13年后被诊断发生骨转移。
目前为止,测试新辅助雄激素剥夺疗法益处的最大规模的三阶RCT是由泛塔斯曼海峡放射肿瘤学组(TROG)实施的。在这个三组对照研究中,818名患者被随机分配到不同治疗组中。单独采用外照射放疗(66Gy,2Gy/d,计33次,对前列腺和精囊腺连续使用6.5~7周(对照组))。外照射放疗联合3个月雄激素剥夺疗法,每月3.6 mg戈舍瑞林采用皮下注射,250 mg氟他胺,每日3次口服,在放射疗法前2个月实施(对照组相同的方案)。或者采用外照射放疗联合6个月雄激素剥夺疗法相结合,在放射疗法前5个月实施(对照组相同的方案)。平均随访5.9年后,试验证明单独放射疗法、外照射放疗联合3个月雄激素剥夺疗法、外照射放疗联合6个月雄激素剥夺疗法的5年生化无瘤存活率分别是38%、52%和56%(P<0.01)。无病生存率在统计学上也有显著增加,外照射放疗对比外照射放疗联合3个月雄激素剥夺疗法、外照射放疗联合6个月雄激素剥夺疗法的治愈率分别是32%、49%和52%(P≤0.000 1)。外照射放疗联合6个月雄激素剥夺疗法组78%患者免于补救治疗,具有明显优势;相比而言,仅使用外照射放疗组63%患者需要补救治疗,两者有显著统计学意义(P<0.03)。外照射放疗联合3个月雄激素剥夺疗法对补救治疗的要求也明显降低。然而,这些结果未能达到5年的统计学意义。大约94%的外照射放疗联合6个月雄激素剥夺疗法治疗的患者,5年前列腺癌特异性存活率为94%,相比而言单独外照射放疗的存活率为91%(P=0.04)。而外照射放疗联合3个月雄激素剥夺疗法,没有降低疾病的死亡率。总体而言,3个月的雄激素剥夺疗法能够降低疾病生化复发率,提高了无病生存率和减少补救治疗。6个月的雄激素剥夺疗法对以上方面都有促进,同时能够增加前列腺癌特异性存活率。整体存活率则没有相关的报告。
波士顿医疗组发布了一项小规模的前瞻性随机对照试验,测试患者采取6个月新辅助全雄激素阻断疗法(CAB,黄体生成素释放激素和非甾体类抗雄激素的组合)。206名随机分类的患者接受对前列腺和精囊的总剂量为70Gy,日治疗量1.8~2Gy的三维适形放射治疗(3D-CRT),同时各接受2个月的新辅助、伴随及辅助的全雄激素阻断疗法。结果显示接受三维适形放射治疗和雄激素剥夺疗法(3D-CRT+ADT)的患者和仅接受3D-CRT的患者相比,5年内存活具有明显优势,两者的5年总体存活率分别约为88%(95%CI,80%~95%)和78%(95%CI,68%~88%)。风险比(HR)为2.07(95%CI,1.02~4.20)。雄激素剥夺疗法组的前列腺特异性抗原生化复发的HR为2.86(95%CI,1.69~4.86)。
加拿大泌尿肿瘤学组对208名B2~C期前列腺癌患者进行了一个小型研究并公布了研究数据。这些患者被随机分类成接受12周醋酸环丙孕酮(CPA)先期治疗然后再进行放射疗法(组一),仅接受放射疗法(组二)。总体上,采用联合疗法的患者的PSA比较低,而且组一的更多患者能免于临床复发(71%相对46%,P=0.02)和生化复发(47%相对99%,P=0.001)。此外,18个月后,前列腺活检阴性患者的症状明显改善。魁北克省的一个更大规模的三组对照研究,则将患者随机分类为接受放射疗法、初期3个月辅助全雄激素阻断疗法联合放射疗法和初期11个月的辅助全雄激素阻断疗法联合放射疗法。2年后的前列腺活检结果显示,以上三类治疗方案的疾病残留率分别为65%、28%和5%。5年后的中期随访表明,7年期生化无病证据(BNED)分别为42%、66%和69%。相对于仅采用放射疗法的患者而言,采用组合疗法的患者的生化无病证据明显不同(P=0.003),然而采用不同激素疗法的两个小组并无差别。Denham等人的数据,也得到相同的结论。
这些临床研究结果(如表13-1所示)强有力地证明,早期采用雄激素剥夺疗法比仅采用体外放射疗法更能控制病情发展。波士顿研究组的研究,有效说明了早期采用雄激素剥夺疗法对生存率的优势,然而仍有待令人信服的长期随访结论。非随机性的放射疗法试验研究也得出了类似结论。例如,在一个剂量不断调整提高的放射治疗中,先期采用了激素疗法的患者中的前列腺活检阳性率为10%(31人中3人),而仅采取放射疗法的患者中的活检阳性率为46%(105人中48人)。在一个采用超分割放射疗法的报告中,如果没有进行激素治疗,前列腺活检的阳性发生率为50%(18人中9人),而采用激素治疗的发生率为零(23人中无人)。对450名患者采用组合疗法的研究,得出了与随机研究相同的结论。特别是对45名患者连续研究中,根据先期呈现的特点,80%~90%的患者的2年期前列腺活检报告为阴性。
表13-1 单独采用放射疗法和联合采用3~6个月雄激素剥夺疗法
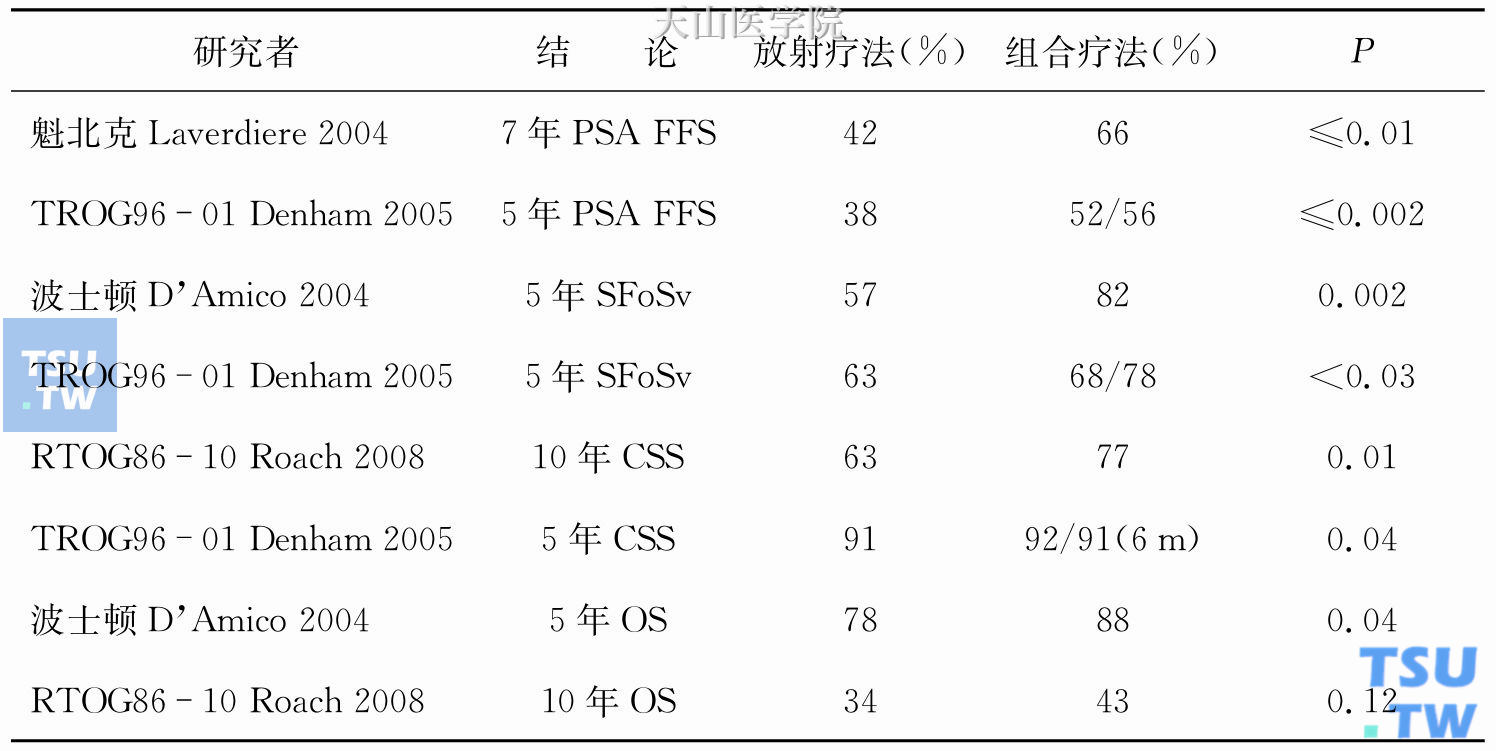
注:FFS,失败生存率;SFoSv,无激素残余存活率;CSS,死因存活率;OS,总生存率。
Lamb等人发布了TROG96.01的试验数据,评估了患有局限性晚期前列腺癌患者接受短期辅助雄激素剥夺疗法的可能性。患者在接受特定放射治疗前被随机分成接受6个月、3个月和不接受新辅助的最大限度雄激素剥夺疗法(MAD)。随访1年,对所有患者进行评估。这些患者中,36%在接受任何治疗前性行为活跃,36%中的绝大部分(97%)接受MAD后性行为不活跃。然而,接受放射疗法12个月后,不同治疗手段的性生活都类似(12.1%~18.6%),这表明短期的MAD对性功能的影响是可逆转的。TROG在准备期使用了黄体生成素释放激素(LHRH)类似物,即每月皮下注射3.6 mg戈舍瑞林。报告表明,即使激素水平能够恢复,联合治疗后的阳痿率可能比较高,达到43%,而放射疗法的阳痿率为23%(P<0.001)。然而,3个月的LHRH类似物准备期的影响时间明显较长,睾丸激素水平的平均恢复期为9~13.6个月,这也许能说明当采用3个月准备期时睾丸激素的差异原因。
新辅助雄激素剥夺疗法的疗程
新辅助雄激素剥夺疗法的疗程在3个三阶研究中都有说明,美国肿瘤放疗协助组(RTOG)(协议99-10)患者的情况见表13-2。
表13-2 短、中期辅助雄激素剥夺疗法和放射疗法

总而言之,加拿大的研究者证明辅助雄激素剥夺疗法时间长短,对控制PSA水平没有影响,4年期为65%,5年期65%。这样,高危患者采取8个月的辅助治疗,并没有显著益处。Denham等人发布的大型三阶研究报告证明,3个月辅助治疗和6个月辅助治疗的PSA控制水平类似,分别为5201和56%,P=0.2。然而,进行较长时间的激素治疗能显著降低将来失败率,22%对比13%,P=0.02。魁北克研究所发布的治疗满2年后前列腺活检结果表明,两个激素阻断组的残留癌率分别为28%和5%。活检时的睾酮水平没有报道,而使用10和11个月激素治疗组的结果,可能由于持续使用雄激素剥夺疗法而被混淆。
D'Amico等人重新评估了波士顿的随机对照试验(RCT),评估6个月雄激素剥夺疗法的好处。在这次试验中,患者随机接受6个月LHRH激动剂和抗雄激素治疗。共计102名男性患者,被随机分类到接受辅助全雄激素阻断疗法。其中,30%的患者在6个月治疗完成前中止了抗雄激素治疗。在平均追踪随访8.2年后,结果表明,在对已知预后因素调整后,每增加1个月抗雄激素治疗,复发的危险性就明显降低(调整HR,0.81,95%CI,0.72~0.92,P=0.001)。此后随机分析提出了这样的假说,短期的全雄激素剥夺疗法,可能对非转移性前列腺癌患者具有临床优势。目前全雄激素剥夺疗法不是标准治疗,需要有前瞻性的研究评估这一问题。
