因珠蛋白基因突变引起珠蛋白肽链氨基酸组成改变导致的高铁血红蛋白,称血红蛋白M(HbM)。本病的珠蛋白肽链氨基酸变异多发生在与血红素有关的位置上。自1955年开始将HbM后面再追加地名以资区别,目前已发现5种HbM。
HbM种类
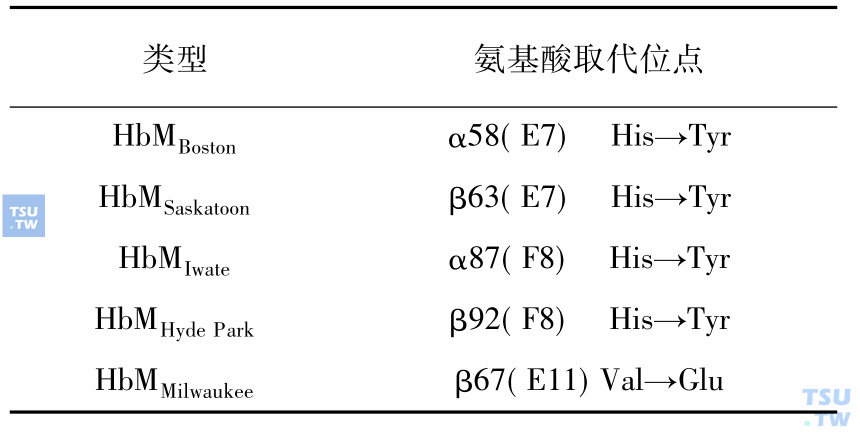
病理机制
HbM病在世界各地均有散在病例报道。我国已发现两种:HbMIwate及HbMHyde Park。高铁血红蛋白分子的4个亚单位中如有2个亚单位异常而不能携带氧即形成HbM。血红蛋白4个亚单位的血红素袋中各有一个血红素。血红素袋位于E及F段α螺旋之间。铁原子与血红素平面中的4个吡咯环的氮原子联结,并与F8上的近端组氨酸(α87,β92)联结。在血红素的另一侧,铁原子对着E7的远端组氨酸(α58或β63)。当Hb脱氧时,血红素铁处于亚铁(Fe2+)状态;与氧结合时,氧分子进入血红素袋的Fe2+与远端组氨酸之间,并与Fe2+分受铁原子的电子:Fe2++O2→Fe3 ++O2-。此时铁原子滑进卟啉环的平面内,引起血红蛋白三级和四级结构的改变,使血红蛋白由脱氧的T型(紧张型,脱氧构象)变为氧合的R型(松弛型,氧合构象),有利于其他氧分子与血红素的结合(即血红素-血红素相互作用)。
上述5种HbM中,有4种的氨基酸替代是珠蛋白螺旋段E7(α58或β63)的远端或F8(α87或β92)的近端组氨酸均被酪氨酸替代。结果酪氨酸酚侧链上的氧原子与血红素的铁原子形成铁-酚盐复合物,改变了血红素袋结构,将铁固定于Fe3+状态,并阻碍了红细胞内还原系统将高铁转变为Fe2+的作用,使血红蛋白失去携氧功能。至于HbMMilwaukee,其β链67位替代的谷氨酸亦面向血红素基,谷氨酸的羧基阴离子与铁原子结合,使之固定于Fe3+状态。由于α链与铁原子的结合很牢固,α链有变异的HbM不发生溶血性贫血。β链有变异的HbMSaskatoon及HbMHyde Park,其β链与铁原子的结合不牢固,血红素与珠蛋白可脱离而变成轻度不稳定血红蛋白,故临床表现有轻微溶血性贫血。
临床表现
α链异常的HbM患者出生时即有发绀,无杵状指和劳累后气促、发绀加重表现,无贫血或其他症状,预期寿命一般正常。β链异常的HbMSaskatoon及HbMHyde Park患者出生时无发绀,出生后约6个月当γ链的合成被β链大部分替代时开始出现发绀。可有轻度溶血性贫血,并伴有轻度黄疸和脾大。服用氧化剂类药物(如磺胺类)可明显加重溶血。HbMMilwaukee患者只有发绀,无贫血症状。
诊断与鉴别诊断
HbM在分光光度计上的吸收光谱既不同于氧合HbA,亦不同于其他高铁血红蛋白,通过分光镜检查可确定HbM并以资鉴别;用pH 7. 1缓冲液作电泳,可将HbM与HbA分开,HbM病患者均为杂合子,其HbM水平为20%~35%。
本病应注意与青紫型先天性心脏病相鉴别。青紫型先天性心脏病患常伴有活动后心慌﹑气急及青紫加重等问题;体格检查可发现有杵状指﹑响亮且粗糙的心前区杂音及其他心脏病体征。动脉血氧饱和度降低,其静脉血于空气中振荡后即转为鲜红色。心脏彩色超声、影像学检查可确诊先天性心脏病类型。
治疗
本病患者预后良好,患者寿命不受影响,一般不需要特殊治疗。
