遗传性乳腺癌的发生与明确的基因突变有关,其中最多见的为BRCA-1和BRCA-2相关性乳腺癌,还有Li-Fraumeni综合征等。
BRCA-1和BRCA-2突变的流行病学分布
1990年,有研究发现人类染色体17q21带上存在与早发性乳腺癌发病有关的基因,后来被命名为BRCA-1基因。最初估计BRCA-1的突变与45%的家族性乳腺癌患者有关;而在发病年龄早的家族性乳腺癌患者中,这一比例大大升高。在发病年龄小于45岁的家族性乳腺癌患者中,BRCA-1的突变高达70%。
1994年,在22个早发性女性乳腺癌合并至少1例男性乳腺癌的家系中进行的连锁分析显示,在人类染色体13q12-13带上存在与乳腺癌发病相关的基因,就是BRCA-2基因。
通过直接检测基因突变的方法,研究者发现在整个乳腺癌人群中BRCA-1和BRCA-2基因突变的发生率为2%~3%。在合并乳腺癌和卵巢癌的家系中,BRCA-1/2基因的突变率最高可达55%,而在同时患有乳腺癌和卵巢癌的个体中则高达75%。
BRCA-1和BRCA-2基因结构和突变种类
1、BRCA-1基因:具有24个外显子,编码具有1863个氨基酸的蛋白质。BRCA-1基因序列全长100kb,包含了很多Alu重复序列,这使BRCA-1基因很容易发生碱基大片段(包括整个外显子)缺失。这种缺失用传统的DNA测序方法无法检出,所以往往漏检。在美国的一项研究中,在合并卵巢癌和乳腺癌,并且BRCA- 1/2全基因序列测定突变阴性的家系中,碱基大片段缺失的比例高达12%。目前已发现的BRCA-1编码区序列改变超过500种,这些突变都罗列在BIC(breast cancer information core)网站上。
2、BRCA-2基因:具有26个外显子,编码区长度为11.2kb,大约为BRCA-1的两倍。BRCA-2基因不像BRCA-1那样具有很多的重复序列,所以碱基大片段缺失并不多见。迄今为止,已有超过250种BRCA-2基因突变被发现,同样罗列在BIC网站上。
3、BRCA-1和BRCA-2的共同特点:两者都具有很多种类的突变,且突变位点遍布整条基因,找不到固定的突变“热点”,这给基因筛查带来很大困难。两者的突变都罕见于散发性乳腺癌病例,提示对散发性乳腺癌的形成作用不大。
BRCA-1和BRCA-2基因突变的种族差异性
BRCA-1和BRCA-2突变的种类具有明显的种族差异性,在不同的种族中存在着不同的“始祖突变”。有一篇综述描述了不同人群的突变发生率、外显率和突变的特点,在白种人群中,根据不同的种族,“始祖突变”至少被分为9类,包括冰岛、芬兰、匈牙利、俄罗斯、法国、荷兰、比利时、以色列、瑞典、丹麦和挪威。同时,BRCA-1和BRCA-2在家族性乳腺癌中的突变频率,也因不同种族而改变。例如BRCA-1在家族性乳腺癌的突变频率:俄罗斯为79%,以色列为47%,意大利为29%。同时,俄罗斯人和以色列人的BRCA-1突变种类较少,而意大利人携带有更多种类的BRCA-1突变。在冰岛人群中,BRCA-2基因突变检出率要远高于BRCA-1基因突变。
但是,也存在着相同的BRCA-1和BRCA-2突变相对集中于同一人群的现象。在Ashkenazi犹太人群中,BRCA-1基因中的185delAG及5382insC突变和BRCA-2基因中的6174delT突变很常见,185delAG及5382insC各占所有突变的10%。在整个Ashkenazi犹太人群中,BRCA-1基因上述两个突变的发生率为1%,而在整个白种人群中的突变频率小于0.1%。该研究扩展到整个犹太人群,发现在乳腺癌发病年龄小于40岁的犹太妇女中,185delAG突变的出现频率达20%。更值得注意的是,有30%~60% Ashkenazi犹太妇女卵巢癌患者携带有BRCA-1或BRCA-2的常见突变。另外,在冰岛妇女中,有8.5%发病年龄小于65岁的乳腺癌患者具有BRCA-2基因的999del5突变。
在亚洲,日本及高加索人种的BRCA-1/2的流行情况已有报道,居住在新加坡及香港的中国人中的流行情况也有报道。
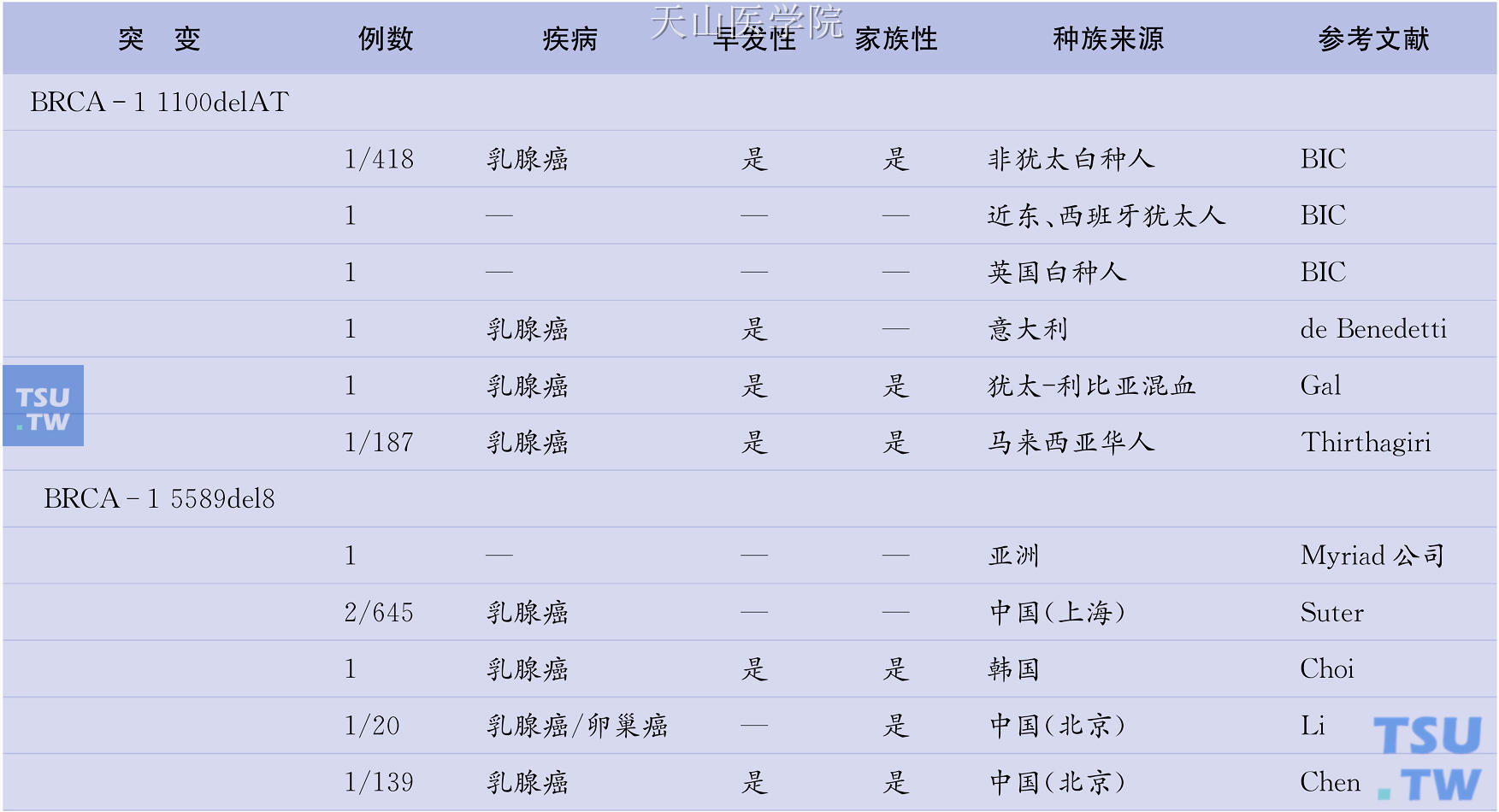
2000~2007年,我国开展的一项多中心研究,对来自复旦大学附属肿瘤医院、辽宁省肿瘤医院、山东省肿瘤医院、中山大学附属第二医院和青岛大学医学院附属医院的早发性/家族性乳腺癌患者进行研究(后期加入的有湖南湘雅医院资料,但未进行统一分析)。研究完成了489例早发性/家族性乳腺癌的BRCA- 1/2检测,共发现23例BRCA-1突变和21例BRCA- 2突变,发现在早发性乳腺癌患者(发病年龄≤35岁)中,BRCA-1/2基因突变的检出率为8.2%,而家族性乳腺癌中则为12.2%。研究同时发现在中国人群中,BRCA- 1基因上具有两个频发突变位点——1100delAT和5589del8,各占4例。为验证这两个突变是否是中国人群的“始祖突变”,在426例散发性乳腺癌和564名健康对照中进行这两个位点的检测,结果在426例散发性乳腺癌中发现2例5589del8突变,在564名健康对照中发现1例1100delAT突变。在6例携带5589del8突变的患者中,1例来自辽宁,3例来自上海,2例来自浙江;在5例1100delAT患者中,辽宁1例,山东2例,上海1例,广东1例。所以,这些重复突变并没有明显的地域聚集性。单倍型分析同样显示,重复位点具有相同或相似的单倍型。通过对已经发表的文献和BIC数据库的综述发现,1100delAT主要分布于白种人中,唯一的亚洲报道为马来西亚的华人;而5589del8则集中分布于亚洲黄种人中,其中包括北京的2项报道、上海散发性乳腺癌中的1项报道和Myriad公司在一个旅美亚裔家系中的发现。更有趣的是,在韩国乳腺癌患者中也发现了这个位点的突变(表3-1)。所以,1100delAT和5589del8特别是5589del8很有可能是中国人群特有的“始祖突变”。
表3-1 “始祖突变”的文献报道
BRCA-1和BRCA-2相关性乳腺癌的病理学特征
BRCA-1和BRCA-2突变相关性乳腺癌的病理学特征有很大的不同,与散发性乳腺癌也有差别。BRCA-1相关性乳腺癌中ER阴性者最高可达90%,同时还有组织分化差的特点。另外,BRCA-1相关性乳腺癌中p53基因的突变率或p53的免疫检测阳性率高于散发性乳腺癌,HER-2/neu高表达的比例则低于散发性乳腺癌。还有研究显示,BRCA-1相关性乳腺癌中髓样癌的比例高于BRCA-2相关性乳腺癌及散发性乳腺癌。BRCA-2突变相关性乳腺癌的病理学特点与散发性乳腺癌相比差别没有这样大。有研究发现,BRCA-2突变相关性乳腺癌的高肿瘤分级的比例高于散发性乳腺癌,而ER阳性的比例则高于BRCA-1相关性乳腺癌。
笔者对中国遗传性乳腺癌研究中筛查出的18例BRCA-1基因突变携带者与210例非携带者的肿瘤组织病理学和免疫组化特征进行了比较,发现两者的病理学类型没有显著的差别。在文献报道中,BRCA-1突变携带者的髓样癌比例显著高于非携带者。而在笔者的研究中采用2003版世界卫生组织(WHO)乳腺肿瘤病理诊断标准后发现,典型性乳腺癌的比例在突变阳性和阴性人群中髓样癌的比例分别为5.6%和2.4%,没有显著的差别。免疫组化特征的比较发现,与突变阴性者相比,突变阳性者具有肿瘤组织学分级为III级的比例高、三阴性肿瘤(ER、PR和c-erbB-2三者都为阴性)的比例高等特点,这与文献报道一致。
BRCA-1和BRCA-2的生物学功能
BRCA-1和BRCA-2都是抑癌基因,它们编码的蛋白有可能在多条细胞通路中发挥作用,包括转录和细胞周期调控等。BRCA-1和BRCA-2蛋白在DNA双链损伤的修复中发挥重要作用,从而维持基因组的稳定。其中BRCA-1的作用更为广泛,主要是识别和标记损伤的DNA并帮助其修复。在正常细胞中,BRCA-1蛋白在细胞周期中可增强其他重要基因的转录,调控S期、G1期、G2期、M期的“检查点”,确保已经损伤的DNA不参与复制;在DNA损伤部位改变染色体和核小体的结构,并使“修复复合体”可以进入,从而启动DNA的修复。
BRCA-2蛋白在维持基因组稳定性方面的功能比较有限,主要是调控RAD-51蛋白的活性,这是修复DNA双链损伤的重要途径——同源性重组(homologous recombination, HR)的关键成分。BRCA-2与RAD-51的结合对无差错的DNA双链损伤修复是非常重要的。RAD-51与DNA损伤区域的结合必须依靠BRCA- 2蛋白,从而形成核蛋白而进行DNA重组并完成修复。
细胞DNA损伤的修复通路有两条:一条是无差错的修复途径——同源性重组;另一条是非同源性末端连接(nonhomologous end joining,NHEJ)。后者是更容易出错的修复过程。而同源性重组又有两条不同的通路:一条是不容易出错的基因转换(gene conversion, GC);另一条是容易出错的单链退火(single-strand annealing, SSA)。在正常细胞中,DNA损伤的修复依靠同源性重组通路。在BRCA-1和BRCA-2突变细胞中,正常的修复通路被抑制,因此,DNA的修复更多地应用单链退火通路和非同源性末端连接通路,故更容易出错。
在BRCA-1或BRCA-2突变细胞中,由于DNA损伤的修复无法正常进行,导致基因组不稳定,包括染色体异常和断裂。这些DNA的差错在细胞内不断地积累,如果应用对DNA具有损伤作用的药物,特别是导致DNA交联的药物时,这些差错会加重,从而更容易导致细胞的死亡。
BRCA-1和BRCA-2基因突变状态对治疗敏感性的影响
一些研究发现,BRCA-1和BRCA-2基因突变的乳腺癌细胞对导致DNA交联的药物更敏感,这些药物包括卡铂、顺铂和丝裂霉素。由于这些药物对DNA损伤需要DNA的同源性重组来修复,而BRCA-1和BRCA-2基因的缺陷使这种修复功能也受到损伤,从而使细胞对药物更敏感。另外,有研究显示紫杉醇诱导的细胞死亡需要正常功能的BRCA-1蛋白参与,而BRCA-1基因突变导致对这类药物耐药,这一理论同样在临床研究中得到证实。
由于BRCA-1和BRCA-2基因是DNA损伤修复基因,因此,理论上基因突变的乳腺癌应该对放疗更敏感。一个在BRCA-1和BRCA-2基因突变乳腺癌患者中进行的保乳手术的研究显示,在接受了双侧卵巢切除术的突变阳性患者中,保乳手术加放疗后中位随访时间为6~8年,同侧乳腺肿瘤复发率与突变阴性患者相同,而对侧乳腺癌的发生率则远高于阴性者,同时,突变携带者的正常乳腺组织放射性损伤要高于突变阴性者。
BRCA-1和BRCA-2基因突变乳腺癌的新药
在人体内,聚二磷酸腺苷核糖聚合酶(PARP)家族有17个成员,其中PARP-1在DNA单链损伤的修复中发挥重要的作用。当PARP-1受到抑制时,细胞DNA单链损伤的修复无法完成,最终容易形成DNA双链损伤。前面已详细说明,同源性重组是DNA双链损伤修复中的重要环节,而此环节主要由BRCA-1和BRCA-2蛋白参与完成。所以,在BRCA- 1和BRCA-2蛋白功能缺陷(基因突变)的细胞中由于PARP-1被抑制,细胞的DNA损伤修复将无法正常完成,从而导致细胞死亡。因此,PARP-1抑制剂作为一种新药而进行临床试验。由于基因突变阳性乳腺癌与三阴性乳腺癌的相关性,这类药被认为在这类难治性乳腺癌中具有广阔的前景。虽然PARP-1抑制剂在BRCA-1和BRCA-2基因突变乳腺癌以及三阴性乳腺癌的II期临床试验中获得了令人振奋的效果,但是,在三阴性乳腺癌的III期临床试验中效果不佳,所以这类药物的前景尚不明朗。
