高效液相色谱法(HPLC)因具有分离效能高、分析速度快等特点,在发展过程中曾被称为高速液相色谱法、高压液相色谱法和高分辨液相色谱法等。在生物医药学领域和临床疾病诊断中,HPLC被广泛用于分离分析各种蛋白质、氨基酸、生物碱、核酸、甾体类化合物、脂类、维生素、药物及无机盐类等。HPLC装置见下图。
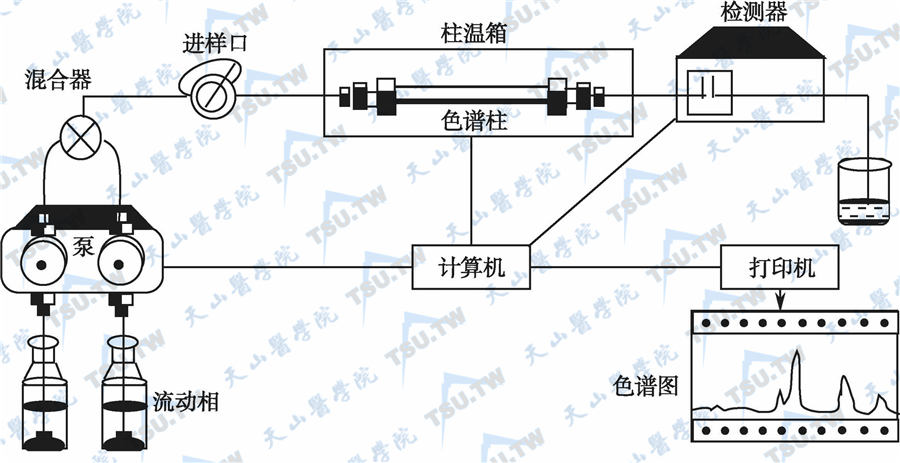
高效液相色谱仪结构示意图
HPLC常用两种方法进行分类,按固定相的聚集状态可将HPLC分为液-液分配色谱法和液-固吸附色谱法两大类型,液-液分配色谱法又分为正相色谱法和反相色谱法,后者还可分为离子对色谱法和离子抑制色谱法等;按分离机制可将HPLC分为分配色谱法、吸附色谱法、离子交换色谱法、分子排阻色谱法、亲和色谱法、化学键合相色谱法和胶束色谱法等类型。
液-液色谱法分离目标物
液-液分配色谱法(liquid-liquid distribution chromatography)系指流动相和固定相都是液体的色谱法。其分离机制是利用样品在流动相与固定相中的溶解度不同,造成不同组分的分配系数(K)存在差别而得以分离。组分的分配系数是指其在流动相与固定相中处于平衡状态时在两相中的浓度,即K=Cs/Cm(Cs表示组分在固定相中的浓度;Cm表示组分在流动相中的浓度)。组分的K大,在色谱柱中停留的时间就长,反之则短。在液-液分配色谱法中,流动相的性质是影响分配系数的重要因素,在实际应用中,常通过调整流动相的极性(或浓度)来改变各组分间的分配系数和合适的保留时间,以达到分离的目的。按照固定相与流动相的极性差别,液-液分配色谱法被分为正相与反相色谱法两类。正相液-液分配色谱法是指流动相极性小于固定相极性的色谱法,其分离作用主要依赖于组分间的极性差别,常用于分离溶于有机溶剂的极性和中等极性的分子型物质。流动相极性大于固定相极性的色谱法称为反相液-液分配色谱法,在分离过程中,样品中极性大的组分先流出色谱柱,极性小的组分后流出,与正相色谱法完全相反。反相色谱法是应用最广的色谱法。
液-固吸附色谱法分离目标物
液-固吸附色谱法(liquid-solid adsorption chromatography)是指流动相为液体和固定相为固体吸附剂的色谱法。其分离机制是吸附剂对样品中各组分的吸附系数(K)不同而得以分离。K也称吸附平衡常数,K=[Xa]/[Xm](Xa为组分被吸附剂吸附的浓度;Xm为流动相中的组分浓度)。与吸附剂亲和力大的组分(Xa大) K大,在柱内的停留时间长,出峰就晚。组分在分离过程中,其分子只吸附于吸附剂的表面,而不进入其内部,是各组分的分子与流动相分子争夺吸附剂表面活性中心的结果。
分子排斥色谱法分离目标物
分子排斥色谱法(molecular exclusion chromatography)又称空间排斥色谱法(steric exclusion chromatography)或凝胶色谱法(gel chromatography),该法所用固定相是具有一定孔径范围的多孔性凝胶,当流动相为有机溶剂时称为凝胶渗透色谱法(gel permeation chromatography),为水溶液时称为凝胶过滤色谱法(gel filtration chromatography)。此法的分离机制是利用被分离组分的分子大小与凝胶的孔径大小之间的相对关系而分离,流动相不影响组分的分配系数。在分离过程中,大尺寸的分子只能渗入到少量的大孔,因此在色谱柱中所经过的路径较短,则停留时间较短。当某些组分的分子尺寸大到不能进入凝胶的任何孔穴时,则随流动相从固定相间隙通过,经过的途径最短,保留时间最短。反之分子的尺寸越小,可进入凝胶的孔穴越多,经过的路程越长,保留时间越长。具有相同化学组成的高分子化合物,其分子尺寸大小与分子量成正比,因此凝胶色谱法还被用于研究高分子化合物的分子量。
亲和色谱法分离目标物
亲和色谱法(affinity chromatography)利用或模拟生物分子之间具有特异性结合的原理,从复杂的生物样品中分离和分析特定物质的一种色谱法。在生物分子中,如抗原与抗体、酶与抑制剂、激素和药物与其细胞受体、维生素与结合蛋白及基因与核酸等,相互之间都具有特异性的亲和力,能形成可逆性复合物。其分离机制是将具有生物活性的配基(如酶或抗体等)键合到非溶性载体或基质表面上形成固定相,利用蛋白质或生物大分子(如酶抑制剂或抗原等)与固定相表面上的配基进行特异性结合而分离。在分离过程中,待分离物质与其配基具有亲和力则形成复合物(图2-5-28),而其他杂质与配基无亲和作用,随流动相直接流出色谱柱。然后再选择适当的洗脱剂(另一种流动相,具有解离复合物的作用)将结合在配基上的物质洗脱分析或收集起来。
离子色谱法分离目标物
离子交换色谱法(ion exchange chromatography)以离子交换剂为固定相,利用样品中可电离组分对离子交换剂的亲和力不同,达到分离离子型或可离子化物质的方法称为离子交换色谱法。该法的基本分离机制是基于样品中的待测离子与固定相含有的可交换基团在交换能力(交换系数)上的差异而分离。常用的离子交换剂有以交联聚苯乙烯为基体的离子交换树脂和以硅胶为基体的键合离子交换剂,可通过化学反应方法在基体上引入不同的离子交换基团,根据引入的基团不同,离子交换树脂可分为阳离子交换树脂[引入某些酸性基团,如磺酸基(—SO3H)、羧基(—COOH)和酚羟基等]和阴离子交换树脂[引入某些能电离出OH-的碱性基团,如季胺基[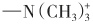 ]、氨基(—NH2)、仲胺基[—NH(CH3)]等。根据分离目的不同,离子交换色谱法又分为离子色谱法(ion chromatography,IC)和离子排斥色谱法(ion exclusion chromatography,IEC),IC常用于分离无机阴离子和酸性或碱性较强的有机物(如各种糖、氨基酸以及DNA和RNA的水解产物等),IEC则主要用于分离和分析各种有机酸。
]、氨基(—NH2)、仲胺基[—NH(CH3)]等。根据分离目的不同,离子交换色谱法又分为离子色谱法(ion chromatography,IC)和离子排斥色谱法(ion exclusion chromatography,IEC),IC常用于分离无机阴离子和酸性或碱性较强的有机物(如各种糖、氨基酸以及DNA和RNA的水解产物等),IEC则主要用于分离和分析各种有机酸。
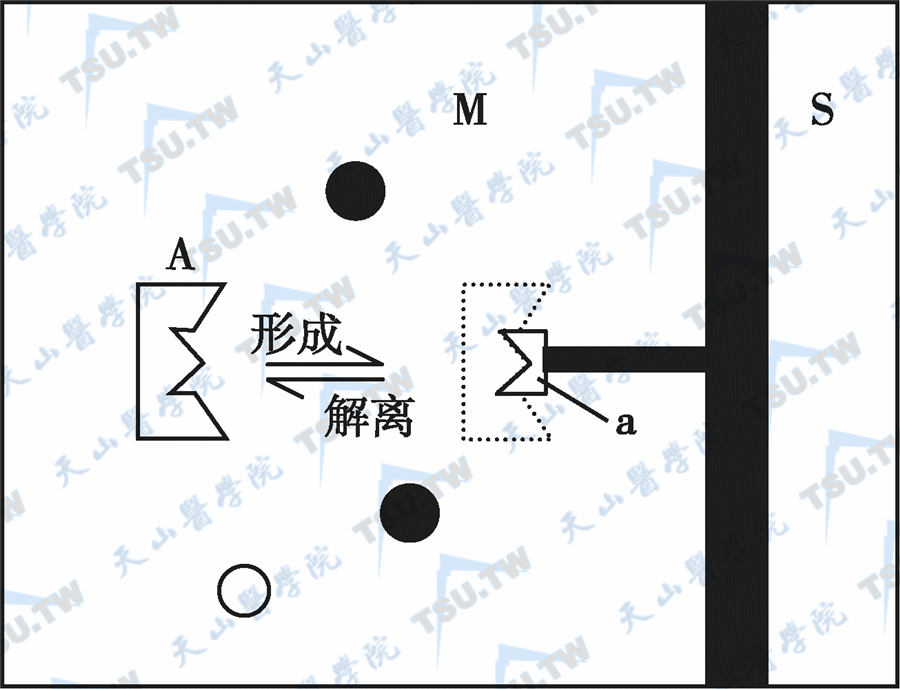
亲合色谱示意图
注:M:流动相;S:载体;A:待分离组分;a: 配基
键合相色谱法分离目标物
键合相色谱法(bonded phase chromatography,BPC)将起分离作用的官能团用化学方法键合到载体(如硅胶等)表面形成的键合相称为化学键合相,以化学键合相为固定相的色谱法称为键合相色谱法。化学键合相可用作液-液分配色谱法、离子交换色谱法、亲和色谱法及手性化合物拆分色谱法等的固定相。根据固定相和流动相的极性不同、固定相所涂渍(键合)或流动相所含(离子对)试剂的性质及被分离物的种类不同等,BPC可分为反相BPC、正相BPC、离子对色谱法(ion pair chromatography)和离子抑制色谱法(ion suppression chromatography)。键合相色谱法是应用最广的色谱法,其中反相BPC被认为可以解决80%的液相色谱课题。该法的分离原理有疏溶剂理论学说、范德华作用力和离子对模型等。
