雄激素是男性最常见的恶性肿瘤前列腺癌发病的重要病因,所以,采用雄激素拮抗剂来降低前列腺癌发病危险,已成为相关的研究重点。5α-还原酶拮抗剂是前列腺癌预防研究的首选药物,前列腺癌预防试验(PCPT)是全球第一个大样本的前列腺癌预防试验研究。从目前的一些研究资料提供的信息来看,应用雄激素拮抗剂降低前列腺癌发病率是有可能的。
一些科学家在临床观察到一种现象,患有遗传性2型5α-还原酶缺乏症的患者,不易患良性前列腺肥大症以及前列腺癌,这促进了研制5α-还原酶抑制剂工作的开展。而且还有一些研究发现,非洲裔的美国人其双氢睾酮和5α-还原酶水平明显偏高,与此对应的是前列腺癌发生率及由此所引起的死亡率亦较高,这一现象提示5α-还原酶抑制剂很可能对前列腺癌具有一定的预防作用。5α-还原酶抑制剂可以阻断睾酮转化为双氢睾酮。双氢睾酮可以促使前列腺增大,从而导致良性前列腺肥大症,并且是促进前列腺癌发生的关键性因素。由此看来,采用5α-还原酶抑制剂来治疗和预防前列腺疾病,不失为一种非常合适的方法。
双氢睾酮是促进前列腺发育和生长的基本物质。双氢睾酮是睾酮经过5α-还原酶作用,导致5α-还原而最终合成的。最近的研究发现,人体中5α-还原酶有两种同工酶,即1型5α-还原酶(或称5α-还原酶1)和2型5α-还原酶(或称5α-还原酶2)。1型5α-还原酶分布于身体的诸多部位,任何有5α-还原酶表达的部位,例如皮肤、肝脏、脂肪的腺体、大多数毛囊和前列腺等,都有它的存在。而2型5α-还原酶主要分布于前列腺,以及其他生殖组织和生殖器的皮肤、胡须以及头皮的毛囊,而且还与男性胎儿的男性化有关。1型5α-还原酶和2型5α-还原酶,这两种类型的酶的不同之处在于它们在前列腺里的分布状态,以及在整个前列腺疾病的良性或恶化进展时的表达。1型5α-还原酶所起的具体作用,迄今在很大的程度上尚未明确。
从小鼠中提取的1型5α-还原酶可使分娩延缓,提示这个同工酶具有阻滞小鼠正常分娩的作用。然而,这种观察结果对人类究竟有何意义,目前尚未知晓。2型5α-还原酶是腺体组织的同工酶,其中也包括前列腺在内。与2型5α-还原酶缺乏有关的一种腺体疾病,即假两性畸形,其男性腺体发育的条件受到抑制,尽管前列腺能呈现出其雏形,却并没有进一步地发育。这就表明了2型5α-还原酶对前列腺的生长及其功能具有重要作用。近来,3型5α-还原酶的同工酶已被发现,看来是对前列腺癌组织性激素耐受的表达,而并不存在于正常的前列腺组织之中。在生物体外的研究中,阻滞3型5α-还原酶在细胞内大量减少了雄激素去势疗法的产物,这种产物来源于性激素耐受的前列腺癌。在鼠的研究中发现,虽然两种同工酶对合成代谢和分解代谢都有作用,但1型酶主要对雄激素和其他类固醇激素的分解代谢起作用,而2型酶则主要对雄激素的合成代谢起作用。在正常前列腺组织、良性前列腺增生(BPH)患者和前列腺癌患者的前列腺的所有区域(包括外周区、移行区和中央区)都有两种5α-还原酶的mRNA,但是在前列腺癌组织中只有1型5α-还原酶的表达增加。
类固醇的结构特征,这个对阻滞人类包皮5α-还原酶活性的重要结构,是由Hsai和voight在20多年之前首先发现的。他们当初所得出的结论,仍是形成在下列这种情况之下理解结构与活性之间关系的基础:一个3-单氧-△4,5结构参照17β而不是被17α所取代。从那时起在它们之中有两个5α-还原酶抑制剂(5α-Rls)开始在临床上得到应用:一个为非那雄胺,(finasteride),2型5α-还原酶抑制剂;另一个为度他雄胺,(dutasteride)1型和2型5α-还原酶其中之一的抑制剂。非那雄胺和度他雄胺两者均是4氮杂类固醇。
非那雄胺的化学名称为“氮叔丁基-3-氧代-4-氮杂-5α-雄甾烷-1-烯-17β甲酰胺”(N-tert-butyl-3-oxo-4-aza-5-androst-1-ene-17-carboxamide)。药物别名为非那司提、非那甾胺、芬甾酮等,其制剂商品名为保列治、普洛平等。其化学分子式为C23H36N2O2。化学结构式见图16-1。
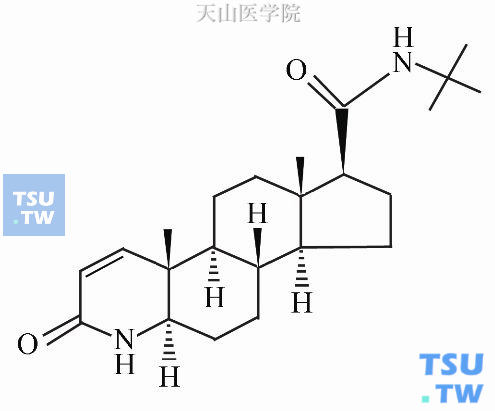
图16-1 非那雄胺
而度他雄胺有一种相似的物质2,5-双(三氟甲基)苯基-结构在其中代替非那雄胺的叔丁基结构。使度他雄胺失去2型5α-还原酶的酶学特征而更加亲脂。化学名为:(5,17)-N-[2,5-bis(trifluoromethyl)phenyl]-3-oxo-4-azaandrost-1-ene-17-carboxamide。药物别名为度他硝胺。其化学分子式为C27H30F6N2O2。化学结构式见图16-2。
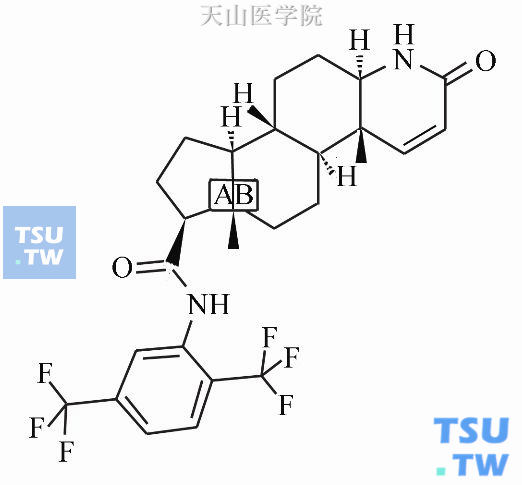
图16-2 度他雄胺
早在20世纪90年代,美国的一家著名医药公司研制开发了新一类选择性2型5α-还原酶抑制剂,即非那雄胺。非那雄胺可显著降低双氢睾酮的水平,在治疗良性前列腺肥大症方面已取得显著疗效。一项“非那雄胺长期疗效和安全性研究(PLESS)”的研究结果显示,在为期4年的设有安慰剂对照组的试验中,良性前列腺增生患者每日服用非那雄胺5 mg,其前列腺的体积缩小,尿流率增加,前列腺症状评分降低,急性尿潴留和外科手术的风险显著降低。在另一项安慰剂对照研究中,120名接受前列腺癌根治术的患者,采用非那雄胺每日10 mg进行治疗,其结果显示,非那雄胺可延缓血清PSA水平的升高,推迟复发。经非那雄胺治疗12个月之后,患者水平的增高延缓了9个月,治疗24个月后,其水平的升高可延缓14个月。对应用非那雄胺预防前列腺癌的相关文献进行综合分析后发现,患者经非那雄胺治疗时其血清和组织中双氢睾酮的水平大多比较低,而且,血清水平也相应降低。这样可能会对控制前列腺增生和前列腺癌发展具有重要影响。
非那雄胺和度他雄胺两种药物都是建议用于治疗良性前列腺增生时下尿路症状(LUTS)的处方药。可使增大的前列腺体积减小,而且能减缓良性前列腺增生时下尿路症状进程。
对用于临床的可能而言,5α-还原酶抑制剂非那雄胺和度他雄胺常常被认为是相似的,然而没有长期(>1年)直接的对比试验来证明这个假说。事实上,这两种药物在药理学、以及它们可能对血清和前列腺组织中的较低双氢睾酮水平的亲和潜能都显示出显著的不同。更进一步讲,长期的临床试验从两种药物中所得出结果的资料显示,其时间过程和斜率也不相同。
5α-还原酶抑制剂作用的正确机制目前尚未完全了解。有证据显示,作用机制之一是导致前列腺里的细胞凋亡程序。然而,与其他类型的雄激素去势对比,细胞凋亡的现象看上去相当温和。如,与安慰剂治疗的患者对比,病理学的研究并不能显示出所收回的雄激素典型标记物,包括在长期5α-还原酶抑制剂治疗的患者的前列腺组织样本中的改变。另外,在良性前列腺增生时有下尿路症状的患者中,前列腺的体积的减少平均不超过最初体积的25%,而且在第一年治疗之后,PSA水平减少仅大约50%。
许多体外和体内研究以及小范围的临床试验已经显示,非那雄胺能减少前列腺的血流和微血管的形成,以及阻滞血管内皮细胞生长因子(VEGF)。这与良好建立前列腺内强有力的血管生长因子双氢睾酮的功能有关。
5α-还原酶阻滞靶位的能力,根据酶的亲合力和酶的数量的不同而进行调节,并发生相应变化。这就可以解释所观察到对治疗的临床反应的各种不同的变化。
正如上面所提到的,非那雄胺仅仅作用于2型5α-还原酶,而度他雄胺可以阻滞1型和2型5α-还原酶两种酶。有趣的是,与2型5α-还原酶相比,在具有下尿路症状的良性前列腺增生患者的前列腺组织中,1型5α-还原酶似乎仅以低量方式出现。在良性前列腺增生时下尿路症状的治疗中,这种酶的条件性阻滞作用的重要性因此而受到怀疑。
随着研究的进一步深入,除了它们对具有下尿路症状的良性前列腺增生患者所带来的益处受到质疑之外,两种药物在预防前列腺癌发生中所发挥的作用也都受到了质疑。1型5α-还原酶在高级别的前列腺内皮瘤中是增加的,在原发癌和转移癌中有进一步的增加。
与具有下尿路症状的良性前列腺增生的患者对照,存在一个很大的潜在可能,那就是1型和2型5α-还原酶在前列腺癌中都能被非那雄胺所阻滞。当分析各阶段的前列腺癌切片时,与具有下尿路症状的良性前列腺增生的组织相比,大量的1型5α-还原酶在高级别前列腺上皮内瘤(HGPIN)中有很大程度的增加,而且从原发性前列腺癌到转移性的前列腺癌有进一步的增加。
再看几组数据:2型5α-还原酶在复发的癌和转移性前列腺癌的平均着色区域与良性前列腺增生的(58.8±7.2)%相当,但是与高级别前列腺上皮内瘤的(21.1±5.5)%比较是增加的(与复发癌比较P=0.000 2,与转移癌比较P<0.001)。
2型5α-还原酶在复发的癌和转移性前列腺癌的平均着色区域与原发前列腺癌的34.8%±6.7%相比均是增加的(与复发癌比较P=0.012,与转移癌比较P=0.000 2)。因此,对于阻断前列腺癌的进展,度他雄胺是否具有另外的潜在能力超过非那雄胺作用,这是相当令人感兴趣的。度他雄胺目前的试验,是具有一定风险的,因为它还可能导致男性前列腺癌的发展,但目前尚未获得验证。这种用度他雄胺以减少前列腺癌的发生而进行的研究,称之为“度他雄胺减少前列腺癌事件试验(REDUCE)”。
直到今日为止,只有非那雄胺是唯一具有A级证据可以用于减少患前列腺癌风险的有效预防药物。其他的药物仍有待于未来更多研究来证明。
