垂体促性腺激素包括间质细胞刺激素(ICSH)或称黄体生成素(LH)和滤(卵)泡刺激素(FSH),是由垂体前叶分泌的两种糖蛋白。其中ICSH作用于睾丸间质细胞(Leydig cell),引起睾酮的产生和分泌,而FSH主要作用于睾丸曲细精管生精上皮中的支持细胞(Sertoli cell),使后者分泌雄激素结合蛋白(androgen-binding protein,ABP)和各种生长因子。在性腺功能减退的患者,促性腺激素水平增高(高促性腺激素性性腺功能减退症),而促性腺激素水平降低,则会发生继发性性腺功能不足(低促性腺激素性性腺功能低下症)。目前,有许多方法可用于检测血液和尿液中的ICSH、FSH水平,本节主要介绍RIA法、CLIA法、ECLIA法。
FSH检测
放射免疫测定法
一、原理
同睾酮的测定。
①Ag+Ag*+Ab1 [Ag*Ab1]+[AgAb1]+Ag*+Ag
[Ag*Ab1]+[AgAb1]+Ag*+Ag
患者标本及125I标记的FSH与定量抗体(一抗)反应,形成抗原抗体复合物。
②[AgAb1]+[Ag*Ab1]+Ab2→[AgAb1]Ab2↓+[Ag*Ab1]Ab2↓
在①反应达到平衡后,加入第二抗体及PEG,使结合部分与游离部分分离。离心后弃上清液用γ-计数器测量沉淀部分的放射性强度。
二、材料
- 125I-FSH溶液:含<10μCi 125I标记的FSH和PBS。
- FSH抗体(Ab1):含兔抗人FSH抗血清和PBS。
- FSH标准物:7瓶,浓度分别为0、5、10、20、40、100、200mIU/ml的FSH血清。
- 质控血清:2瓶,含正常水平和高浓度FSH的人血清。
- 沉淀抗体(Ab2):含驴抗兔血清及PEG。
三、方法
(1)2h温育法:试管编号后按下表程序进行操作。
FSH放射免疫检测程序(两小时法)
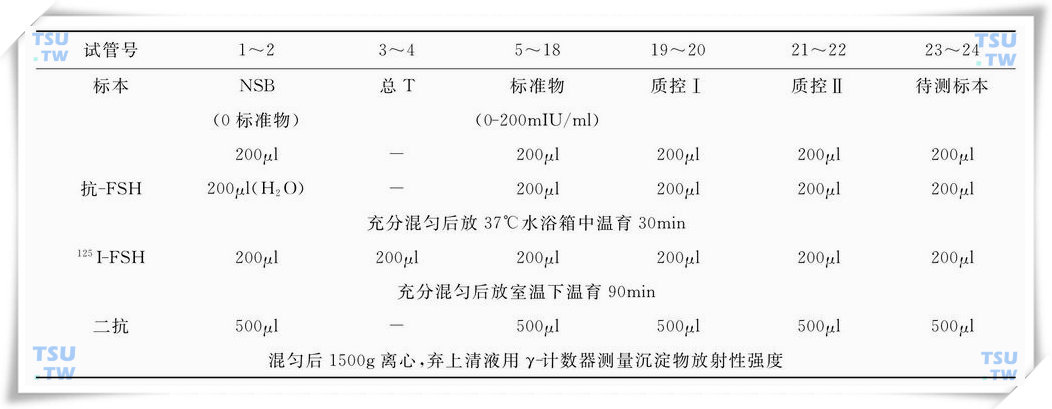
(2)过夜温育法(下表)
FSH放射免疫测定程序(过夜法)
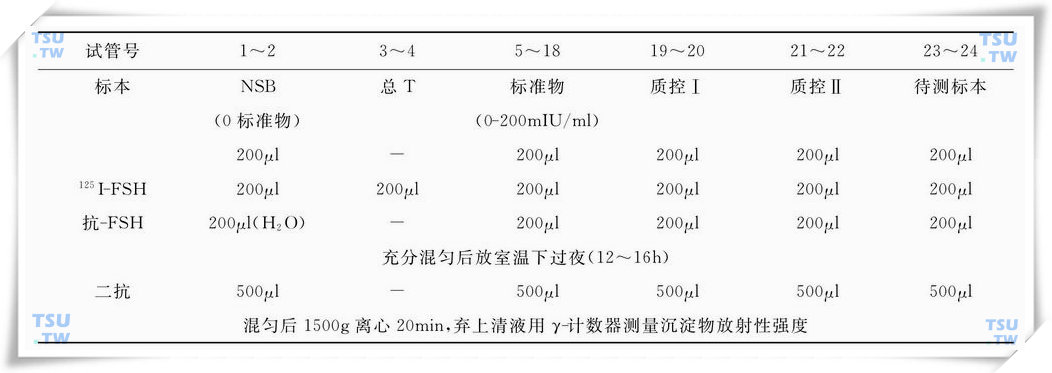
四、结果计算
一、测出每份标本双管的cpm,并计算出平均数。
二、按下式分别计算各标准管、质控和患者标本的B/B0%:
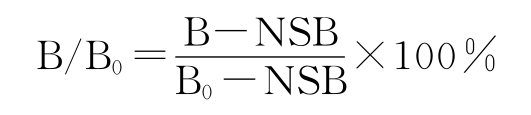
B=每对试管算出计数率的平均值,B0=0标准双管计数率均值,
NSB=非特异性结合计数率的均值。
三、以各标准管B/B0为纵轴,标准物浓度Log为横轴在半对数坐标纸上绘制标准曲线。
四、在标准曲线上查出质控血清及各标本的FSH浓度。
CLIA法
一、原理
将一定量的荧光素标单克隆抗体和酶标单克隆抗体加入标本、标准品和质控品中,置37℃孵育。荧光素标单克隆抗体和酶标单克隆抗体分别与促卵泡激素分子的不同表位结合,形成“三明治”结构。加入过量的结合着磁性微粒的抗荧光素抗体,它快速地与促卵泡激素-抗体复合物发生特异性结合。在外加磁场中直接沉淀,不需离心即可分离。倒去上清液,清洗沉淀的复合物,然后加入酶促化学发光底物。底物在酶作用下被催化裂解,形成不稳定的激发态中间体,当激发态中间体回到基态时便发出光子,形成发光反应,即可使用发光仪检测反应的发光强度。在检测范围内,发光强度与样本中的FSH浓度成正比,通过内插法就可以从标准曲线上读取待测样本的FSH含量。
二、试剂
- FSH试剂:含荧光素标FSH单克隆抗体和碱性磷酸酶标FSH单克隆抗体。
- FSH标准品:包括浓度分别为0、1、3、10、50和150mIU/ml,以小牛血清配制而成。
- 分离试剂:含包被着抗荧光素抗体的磁性微粒。
- 清洗液浓缩液:内含表面活性剂、防腐剂。
- 底物溶液:含酶促化学发光底物。
- FSH质控品:为冻干品,含一定量的FSH。
三、操作
不同型号的仪器操作程序不同,若使用自动化的仪器,则由仪器自动操作所取代,请严格按照仪器使用说明书执行。
四、质量控制
FSH质控品测定值应在规定范围内。
五、参考范围
- 男性:成人 1.67~11.98mIU/ml
- 女性:卵泡期 3.43~10.44mIU/ml
- 排卵期 7.87~20.66mIU/ml
- 黄体期 1.46~11.47mIU/ml
- 绝经期 36.77~132.91mIU/ml不同地区、不同个体、不同设备以及不同方法进行检测,所测得的FSH水平也有所不同,建议各实验室建立自己的正常值范围。
六、注意事项
- 标本应放-20℃贮存,避免反复冻融,严重溶血、黄疸、高脂血症的标本会影响结果。
- 试剂应贮存在2~8℃冰箱内,在有效期内使用,不同批号试剂盒不能混用。
- 待测标本及试剂上机前均应恢复至室温。
- 由于FSH呈脉冲式分泌,故血中浓度变化较大,慎将一次测定的结果用于临床。
- 测定结果高于标准曲线时应用“O”标准液稀释重测。同时应注意某些激素、药物、体内一些活性物质对测定结果的影响。
ECLIA法
一、原理
采用双抗体夹心法原理。待测样品、生物素化的抗卵泡刺激素(FSH)单克隆抗体与钌(Ru)标记的抗卵泡刺激素(FSH)另一位点单克隆抗体混匀,形成双抗夹心的抗原抗体复合物,加入链霉亲和素包被的微粒与之结合,在磁场作用下,微粒通过磁铁吸附到电极上,未结合的物质被清洗液洗去,电极加电压后产生化学发光,通过光电倍增管进行测定。
二、试剂
购买与仪器配套的试剂盒,主要包括以下几种试剂。
- 链霉亲和素包被的微粒,粒子浓度0.72mg/ml,生物素结合能力:470ng生物素/mg粒子,含防腐剂。
- 生物素化的抗FSH单克隆抗体,10ml/1瓶,pH6.0,含防腐剂。
- [Ru(bpy)3]2+标记的抗FSH单克隆抗体
- 质控(Q.C)血清。
三、操作:同睾酮。
四、参考范围
- 男性:成人 1.5~12.5IU/L
- 女性:卵泡期 3.5~12.5IU/L
- 排卵期 4.7~21.5IU/L
- 黄体期 1.7~7.7IU/L
- 绝经期 25.8~134.8IU/L
不同地区、不同个体、不同设备以及不同方法进行检测,所测得的FSH水平也有所不同,建议各实验室建立自己的正常值范围。
五、注意事项
- 此方法不受溶血、高脂血症、黄疸及类风湿因子的影响,接受高剂量生物素(>5mg/d)治疗的患者,至少要等最后一次摄入生物素8小时后才能采血。
- 标本放-20℃贮存可稳定6个月。只能冻融一次,避免反复冻融。
- 试剂应贮存在2~8℃冰箱内,在有效期内使用,不同批号试剂盒不能混用。
- 待测标本及试剂上机前均应恢复至室温。
LH检测
放射免疫测定法
一、原理
采用双抗体放射免疫法:
①Ag+Ag*+Ab1 [AgAb1]+[Ag*Ab1]+Ag*
[AgAb1]+[Ag*Ab1]+Ag*
含LH的患者标本及125I标记的LH与定量的抗体(Ab1)反应,形成抗原抗体复合物。
②[AgAb1]+[Ag*Ab1]+Ab2→[AgAb1]Ab2↓+[Ag*Ab1]Ab2↓
在①反应达到平衡后,加入第二抗体(Ab2)及PEG,使结合物与游离部分分离,离心后弃上清液,用γ-计数器测量沉淀物的放射性强度。
二、材料
- 125Ⅰ-LH溶液:含<10μCi的125Ⅰ标记的LH和PBS缓冲液。
- LH抗体(Ab1):兔抗人LH抗血清和PBS。
- LH标准物:7瓶,浓度分别为0、5、10、20、40、100、200mIU/ml的LH血清。
- 质控血清:2瓶,含正常水平及高浓度LH的人血清。
- 沉淀抗体(Ab2):含驴抗兔血清及PEG。
三、方法
试管编号后按下表。
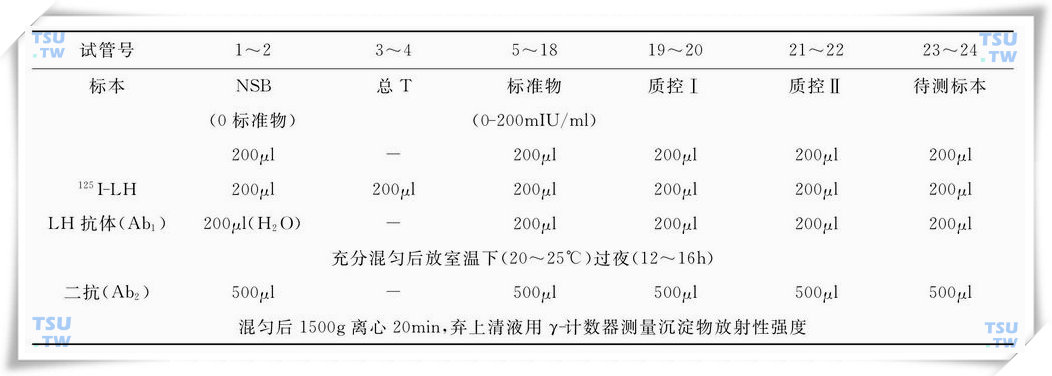
LH放射免疫检测操作程序(2h温育法)
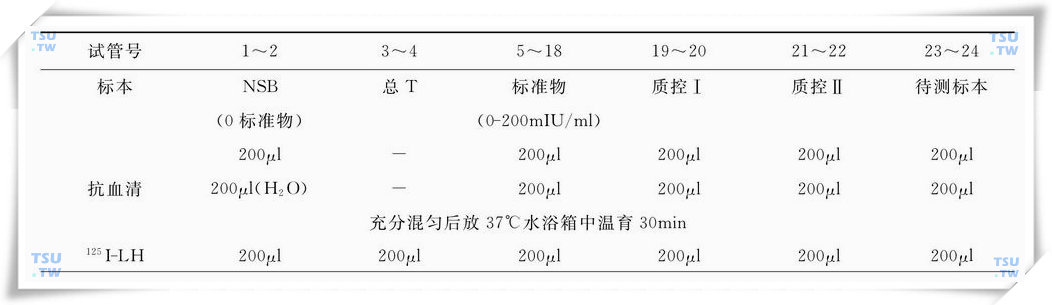

LH放射免疫检测操作程序(过夜温育法)
四、结果计算
一、测出每份标本双管的cpm,并计算出平均数。
二、按下式分别计算各标准管、质控和患者标本的B/B0%:
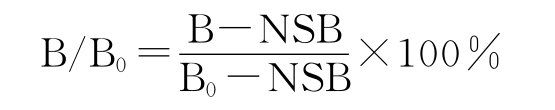
B=每对试管计数率的均值,B0=0标准双管计数率的均值,NSB为非特异性结合双管计数率的均值。
三、以各标准管B/B0为纵轴,标准物浓度Log为横轴,在半对数坐标纸上绘制标准曲线。
四、在标准曲线上查出质控血清及各标本的LH浓度。
五、正常值范围
垂体FSH、LH是脉冲式分泌的,其分泌每间隔6h都有1~3次脉冲波动。FSH波动范围小,LH波动范围很大。脉冲的频率和数值在所有正常男性和性腺功能紊乱的患者中几乎是相似的。在许多性腺功能低下症患者中,促性腺激素的基础水平可能与正常范围重叠。所以,单次取血测得值的可靠性受到怀疑。各实验室应根据自己的条件和接触的人群,做出自己的正常值范围。一般LH每隔20min取血一次,共2~3次,将血清混合后测定其基础值。FSH则于上午取血1~2次,取其均值。表32-6所列正常值范围仅供参考。
血清促性腺激素浓度正常值 ±SD)
±SD)
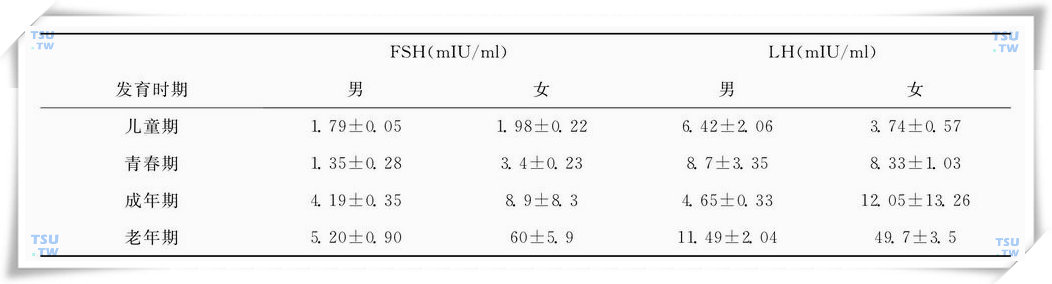
(胡自正等,1982)
六、注意事项
- 采血,FSH可于上午取血一次,LH取血1~2次。对于放射免疫检测的FSH、LH数值,应结合性腺轴中其他激素水平及患者临床表现综合分析。必要时可重复检测。
- 严重溶血标本不能用,2~8℃保存不得超过48h,否则应放-20℃保存,但应避免反复冻融。
- 若待测标本FSH或LH浓度>200mIU/ml,则应用0标准稀释后重做。
- 弃上清液应注意不得损失沉淀物,否则会严重影响测定结果。不同批号的试剂不能混用。
- 必须做NSB,且NSB/T应小于5%,每份标本应做双管重复。
- 一切操作和处理应按放射免疫实验规定进行。
CLIA法
一、原理
将一定量的荧光素标单克隆抗体和酶标单克隆抗体加入标本、标准品和质控品中,置37℃孵育。荧光素标单克隆抗体和酶标单克隆抗体分别与促黄体生成素分子的不同表位结合,形成“三明治”结构。加入过量的结合着磁性微粒的抗荧光素抗体,它快速地与促黄体生成素——抗体复合物发生特异性结合。在外加磁场中直接沉淀,不需离心即可分离。倒去上清液,清洗沉淀的复合物,然后加入酶促化学发光底物。底物在酶作用下被催化裂解,形成不稳定的激发态中间体,当激发态中间体回到基态时便发出光子,形成发光反应,即可使用发光仪检测反应的发光强度。在检测范围内,发光强度与样本中的LH浓度成正比,通过内插法就可以从标准曲线上读取待测样本的LH含量。
二、试剂
(1)LH试剂:含荧光素标LH单克隆抗体和碱性磷酸酶标LH单克隆抗体;
(2)LH标准品:包括浓度分别为0、1、3、10、50和200mIU/ml,以小牛血清配制而成;
(3)分离试剂:含包被着抗荧光素抗体的磁性微粒;
(4)清洗液浓缩液:内含表面活性剂、防腐剂;
(5)底物溶液:含酶促化学发光底物;
(6)LH质控品:为冻干品,含一定量的LH。
三、操作:不同型号的仪器操作程序不同,若使用自动化的仪器,则由仪器自动操作所取代,请严格按照仪器使用说明书执行。
四、质量控制:LH质控品测定值应在规定范围内。
五、参考范围:
- 男性:成人 1.26~8.76mIU/ml
- 女性:卵泡期 1.36~13.31mIU/ml
- 排卵期 12.79~87.67mIU/ml
- 黄体期 0.51~20.21mIU/ml
- 绝经期 14.9~51.11mIU/ml
不同地区、不同个体、不同设备以及不同方法进行检测,所测得的LH水平也有所不同,建议各实验室建立自己的正常值范围。
六、注意事项
- 标本应放-20℃贮存,避免反复冻融,严重溶血、黄疸、高脂血症的标本会影响结果。
- 试剂应贮存在2~8℃冰箱内,在有效期内使用,不同批号试剂盒不能混用。
- 待测标本及试剂上机前均应恢复至室温。
- 由于LH呈脉冲式分泌,故血中浓度变化较大,慎将一次测定的结果用于临床。
- 测定结果高于标准曲线时应用“O”标准液稀释重测。同时应注意某些激素、药物、体内一些活性物质对测定结果的影响。
ECLIA法
一、原理
采用双抗体夹心法原理。待测样品、生物素化的抗促黄体生成素(LH)单克隆抗体与钌(Ru)标记的抗促黄体生成素(LH)另一位点单克隆抗体混匀,形成双抗夹心的抗原抗体复合物,加入链霉亲和素包被的微粒与之结合,在磁场作用下,微粒通过磁铁吸附到电极上,未结合的物质被清洗液洗去,电极加电压后产生化学发光,通过光电倍增管进行测定。
二、试剂
购买与仪器配套的试剂盒,主要包括以下几种试剂。
- 链霉亲和素包被的微粒,6.5ml/1瓶。粒子浓度0.72mg/ml,生物素结合能力:470ng生物素/mg粒子,含防腐剂。
- 生物素化的抗LH单克隆抗体,10ml/1瓶,pH8.0,含防腐剂。
- [Ru(bpy)3]2+标记的促黄体生成素(LH)-多肽。
- 质控(Q.C)血清。
三、操作:同睾酮。
四、参考范围
- 男性:成人 1.7~8.6IU/L
- 女性:卵泡期 2.4~12.6IU/L
- 排卵期 14~95.6IU/L
- 黄体期 1.0~11.4IU/L
- 绝经期 7.7~58.5IU/L
不同地区、不同个体、不同设备以及不同方法进行检测,所测得的LH水平也有所不同,建议各实验室建立自己的正常值范围。
五、注意事项
- 此方法不受溶血、高脂血症、黄疸及类风湿因子的影响,接受高剂量生物素治疗的患者,至少要等最后一次摄入生物素8小时后才能采血。
- 标本放-20℃贮存可稳定6个月。只能冻融一次,避免反复冻融。
- 试剂应贮存在2~8℃冰箱内,在有效期内使用,不同批号试剂盒不能混用。
- 待测标本及试剂上机前均应恢复至室温。
