-
表观遗传学异常与白血病的发生
不改变DNA核苷酸序列,而对基因表达水平进行调控的机制被称为表观遗传学,主要包括四种:①DNA甲基化;②组蛋白共价修饰;③核小体重塑;④microRNA。在肿瘤的发病过程中,除了核苷酸序列
101 -
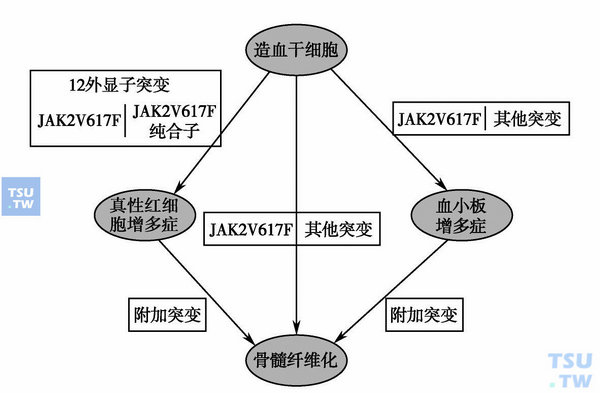
JAK2基因突变
JAK2蛋白包含7个同源结构域(JH1-7),其中JH1是激酶活性结构域,而JH2是假激酶结构域,可以抑制JAK2的激酶活性。JAK2基因敲除的小鼠由于没有红系造血而死于胚胎期,而且JAK2缺失的造血
102 -
BCL-2蛋白
bcl-2家族蛋白是哺乳动物细胞重要的凋亡调节因子,其中除bcl-2外,还有Bax和Bcl-X等。bcl-2家族成员既有抗凋亡的,又有促进凋亡的。bcl-2通过与Bax结合成二聚体复合物发挥作用,二
103 -
间变性淋巴瘤激酶与白血病
t(2;5)(p23;q35)见于间变性大细胞型淋巴瘤,间变性大细胞型淋巴瘤起源于活化的T细胞,表达IL-2受体,通常表达CD30(Ki-1)。t(2;5)易位导致非核糖体核仁磷酸蛋白(NPM)基因与间变性淋巴瘤激酶(ALK,
104 -
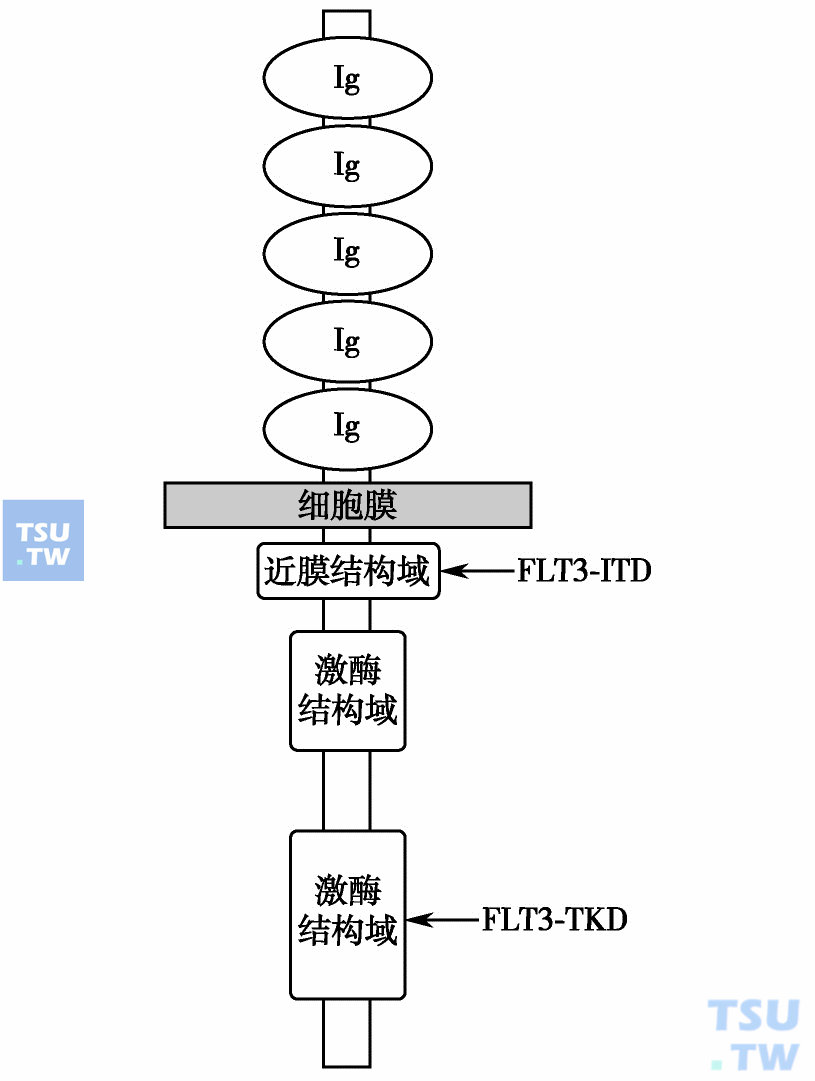
FLT3异常与白血病
FLT3基因位于染色体13q12,属于Ⅲ型受体酪氨酸激酶亚家族成员,与其配体(FL)在造血干/祖细胞的增殖和分化中起重要的调节作用。近年研究发现,FLT3基因的突变与急性白血病的发生密切
105 -
ABL基因异常与白血病
t(9;22)(q34;q11)染色体易位称为Ph染色体。现已明确CML、1%~2%AML、5%的儿童ALL以及15%~30%成人ALL伴有t(9;22)。Ph染色体为9号染色体长臂上的ABL基因与22号染色体上的BCR(breakpoint cl
106 -
T细胞急性淋巴细胞白血病的转录因子突变
T细胞肿瘤的染色体断裂点常会累及染色体14q11的TCRα位点或7q35的TCRβ位点,通过染色体易位使TCR基因的增强子与其他转录因子并置,导致这些转录因子过表达而使细胞转
107 -
C-Myc在白血病和淋巴瘤中的过度表达
C-Myc基因定位于8q24,是调控细胞增殖、分化和凋亡的转录因子。C-Myc在细胞由静止期进入增殖的细胞周期时发挥作用,除促进增殖外,C-Myc还有阻碍分化的作用。C-Myc可与MAX形成异
108 -
E2A基因重排与白血病
t(1;19)(q23;p13)发生在5%~6%的儿童ALL和更小比例的成人前B-ALL中。t(1;19)易位使位于19p13的E2A和1q23上的PBX1相融合。完整的E2A作为转录因子包括转录激活结构域和bHLH结构域,E2A有促
109 -
NPM1突变与白血病
NPM1(nucleophosmin 1)基因位于人类染色体5q35,包含12个外显子。NPM1是一个高度保守的磷酸化蛋白,在各种组织中广泛表达。虽然NPM1可以在胞核和胞质之间穿梭,但绝大部分NPM1分布
110 -
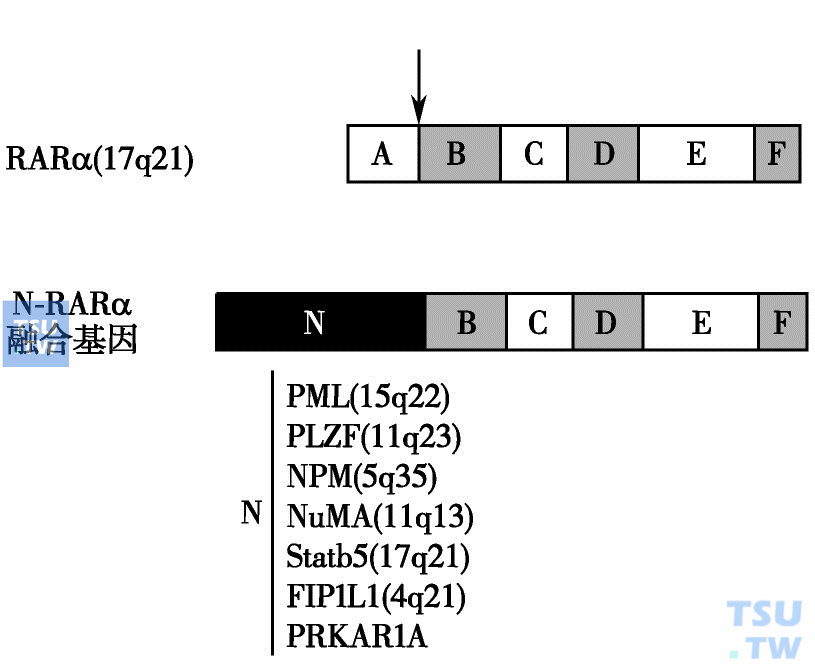
维A酸受体的异常与白血病
急性早幼粒细胞白血病(acute promyelocytic leukemia,APL)最为常见的染色体易位为t(15;17)(q22;q12),其他几种少见的染色体易位有t(11;17)(q23;q12)、t(5;17)(q35;q12)、t(11;17)(q13;q12)、der(17)、t(4;17)(q
111 -
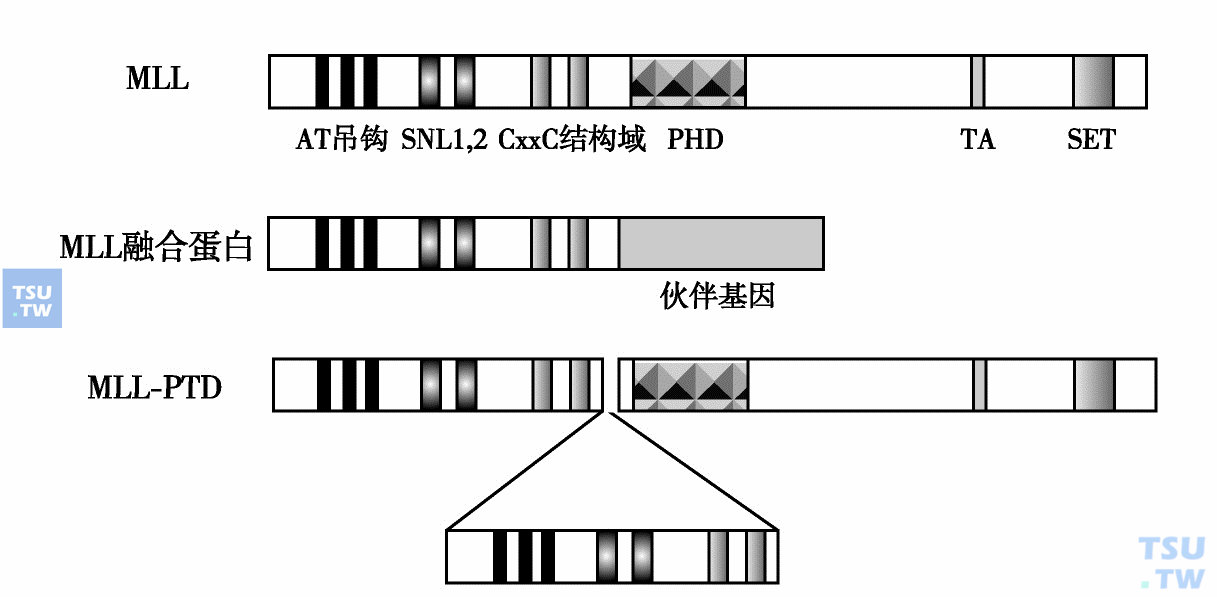
MLL基因(ALL1、HRX)异常与白血病
MLL基因(myeloid/lymphoid leukemia或mixed lineage leukemia)也称为ALL1(acute lymphocytic leukemia 1)或HRX(homolog of trithorax),具有三个区域与果蝇三胸蛋白同源。累及MLL基
112 -
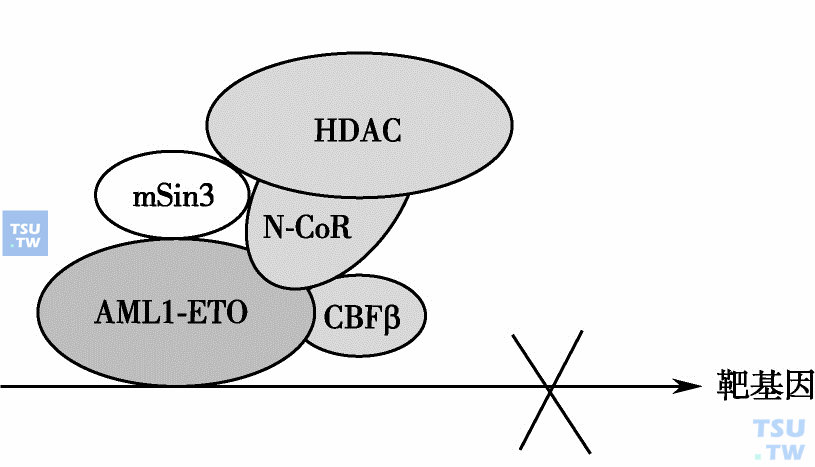
核心结合因子(core binding factor,CBF)的异常与白血病
CBF也称为多瘤增强子结合蛋白2(polyoma enhancer binding protein 2,PEBP2)。CBF是一个异二聚体转录因子家族。构成异二聚体的一方是CBFβ(PEBP2β),另一方是三种CBF&alph
113 -
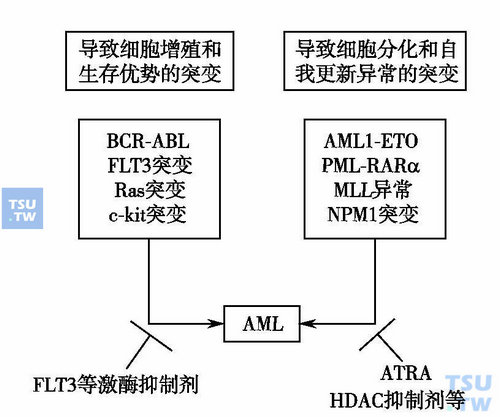
细胞分子遗传学异常与白血病的发生
血液系统恶性肿瘤的发生至少需要两个遗传学打击才能发生病变。就急性白血病而言,其生物学行为除了细胞增殖能力增强和凋亡障碍之外,与其他实体肿瘤不同的特征是细胞分化发育障
114 -
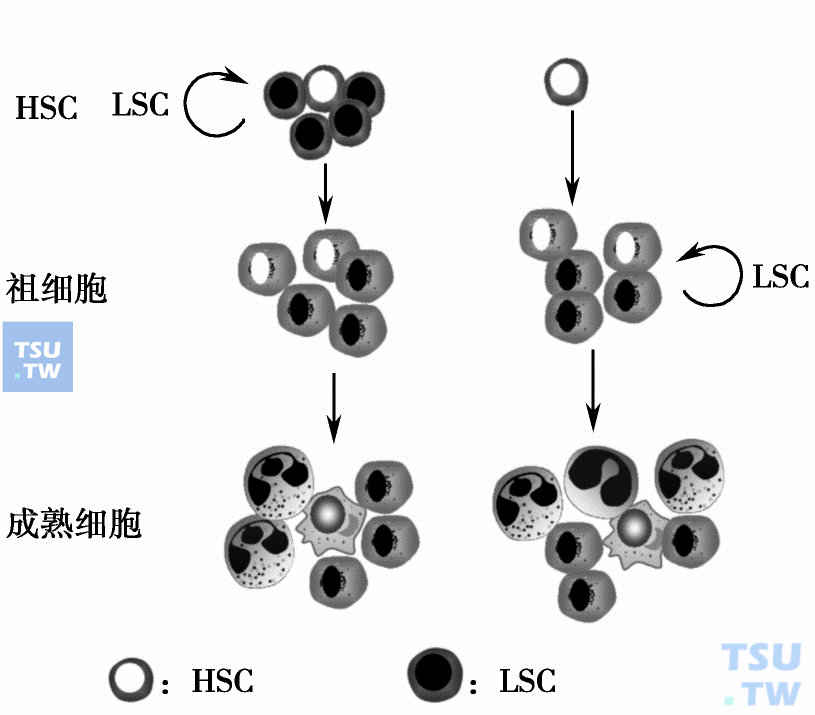
白血病干细胞
白血病细胞到底是来源什么细胞?正常造血是有级层的,包括一小部分具有自我更新能力的造血干细胞(hematopoietic stem cells,HSCs)和数量众多但没有自我更新能力的祖细胞。近年的研
115 -
白血病的病因:遗传因素
遗传因素对白血病致病有重要的影响。文献中有时会报道一个家庭或同一家族相继发生多例白血病病例。例如Gunz等报道一家3代293人先后有13人患白血病,而染色体核型未见异常。Pe
116 -
白血病的病因:病毒因素
1908年Ellerman和Bang用无细胞滤液成功地诱发了鸡白血病,这是最早发现病毒可致白血病的实验证据。后来的研究证实病毒可诱导鼠、猫和牛等哺乳动物发生白血病和淋巴瘤。动物白
117 -
白血病的病因:化学物质与药物
化学致癌物历来受到人们重视。人们在日常生产和生活中经常接触的某些化学物质具有一定的致白血病作用,即白血病致病与某些职业和日常生活习惯有一定关系。某些医疗药品,特别是
118 -
白血病的病因学(放射、化学、遗传、病毒致病)研究
白血病有明确的诱发因素。大量流行病学调查和生物学试验已经证明,离子射线、某些化学物质、病毒感染和遗传因素等都与白血病的致病有关。不同病因通过不同机制引起正常造血干
120