病例与思考
患者,男性,58岁,因上腹痛半年,加重伴腹胀半个月入院。查体:贫血貌,左锁骨上淋巴结肿大,肝脏肋下3cm,剑突下5cm,质地韧,双下肢轻度水肿,余查体未见异常。KPS评分80分。入院后CEA 237ng/ml。血常规正常。肝肾功能正常。腹部增强CT提示:胃窦占位性病变,胃周淋巴结及腹膜后淋巴结转移,肝脏多发转移。肺部CT未见肿瘤证据。胃镜及病理提示低分化腺癌。结合病史、症状、体征、辅助检查,临床诊断为胃低分化腺癌、腹腔转移、肝脏转移。入院后无化疗禁忌,给予奥沙利铂+卡培他滨方案化疗3个疗程,化疗第3疗程间歇期出现白细胞减少,血常规示白细胞2.1×109/L,中性粒细胞1.15×109/L,淋巴细胞0.7×109/L,单核细胞0.12×109/L,同时伴有轻度贫血,血小板正常。经对症支持治疗后升至正常。3个疗程化疗后进行病情评估:疾病稳定。患者出院回家休养,拒绝后续治疗。每月间断于门诊化验血常规提示轻度贫血,其余正常。肝肾功能正常。4个月后患者腹痛加重,伴近期消瘦明显,再次入院。结合影像学检查,病情评估疾病进展。营养评估:恶液质。血常规示白细胞2.6×109/L,中性粒细胞1.4×109/L,淋巴细胞0.8×109/L,单核细胞0.3×109/L,同时伴有中度贫血,血小板正常。肝功示转氨酶轻度增高,胆碱酯酶1768U/L,肾功能正常。
- 患者出现两次白细胞减少,综合分析白细胞减少发生的原因?
- 为明确白细胞减少原因,还需补充哪些检查内容?
- 对于上述两次白细胞减少,应给予什么样的处置?
概述
白细胞是血液中的一类细胞。白细胞也通常被称为免疫细胞。正常人体内的白细胞包括中性粒细胞、嗜酸性粒细胞、嗜碱性粒细胞、淋巴细胞、单核细胞等。白细胞除存在于血液和淋巴中外,也广泛存在于血管、淋巴管以外的组织中。它们的功能包括细胞的吞噬作用以及产生免疫作用。白细胞减少是指外周血液循环中白细胞数量的减少。白细胞减少按病因分类可分为原发性和继发性,其中继发性较为常见。
营养不良是能量、蛋白质和其他营养素缺乏、过剩或失衡的营养状况,可对组织机体的形态、生理功能和临床结局产生可观察到的不良反应。恶液质是营养不良的后期表现。营养不良的病因学分类主要包括饥饿相关性营养不良、慢性疾病相关性营养不良、急性疾病或创伤相关性营养不良。其中肿瘤患者营养不良的发生率较高,同时恶液质也是肿瘤患者死亡最常见原因之一。
白细胞减少可继发于伴有恶液质的肿瘤患者,主要由恶液质因素、肿瘤本身因素和肿瘤治疗相关因素引起。白细胞减少可出现各个系统的感染,包括呼吸系统、消化系统、泌尿系统等的感染,甚至发生败血症危及生命。同时白细胞减少也可以限制肿瘤放化疗的治疗,加重炎症反应,甚至进一步促进肿瘤的发生。这里主要就伴有恶液质的肿瘤患者的白细胞减少的病因、发病机制、临床表现及不良结局等方面进行阐述。
病因及发病机制
伴有恶液质的肿瘤患者可出现白细胞的减少,从而患者免疫力有所下降,可进一步加重基础疾病,同时一定程度上限制抗肿瘤治疗。总结伴有恶液质肿瘤患者白细胞减少原因,包括以下几个方面:首先恶液质患者由于营养不良还可引起造血干细胞及骨髓造血微环境的改变进而引起白细胞生成减少;其次,肿瘤患者的营养物质异常代谢例如能量、糖类、脂类、蛋白质代谢的异常可以引起蛋白质及营养素如氨基酸、锌、铁、维生素等的缺乏,白细胞的合成数量及功能均受到影响;另外手术、放疗、化疗也可从不同方面引起白细胞的减少,以下进行相应的阐述。
1. 恶液质可引起造血干细胞及骨髓造血微环境的改变引起白细胞生成减少
正常造血依赖于造血干细胞和功能完整的骨髓微环境,骨髓微环境也被称为造血干细胞的“土壤”,最早于20世纪70年代提出niche的概念。骨髓微环境包括间充质干细胞、细胞外基质和多种细胞因子,可直接或间接的促进造血细胞的再生、增殖和分化,细胞因子的产生与多个信号转导通路有关。骨髓微环境为造血干细胞提供赖以生存的基础,与造血生成调控、干细胞的动员等生命活动密切相关。
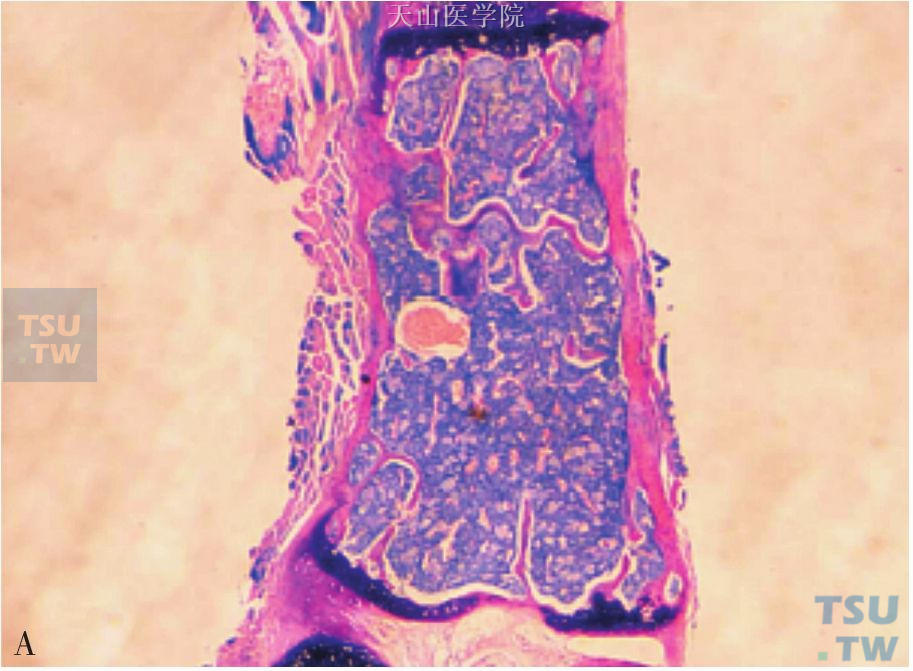
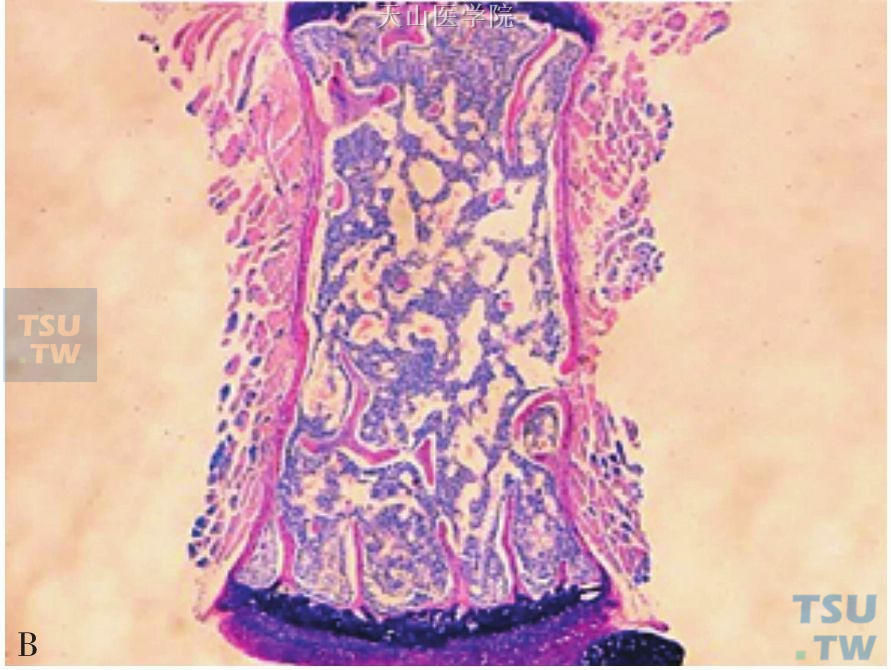
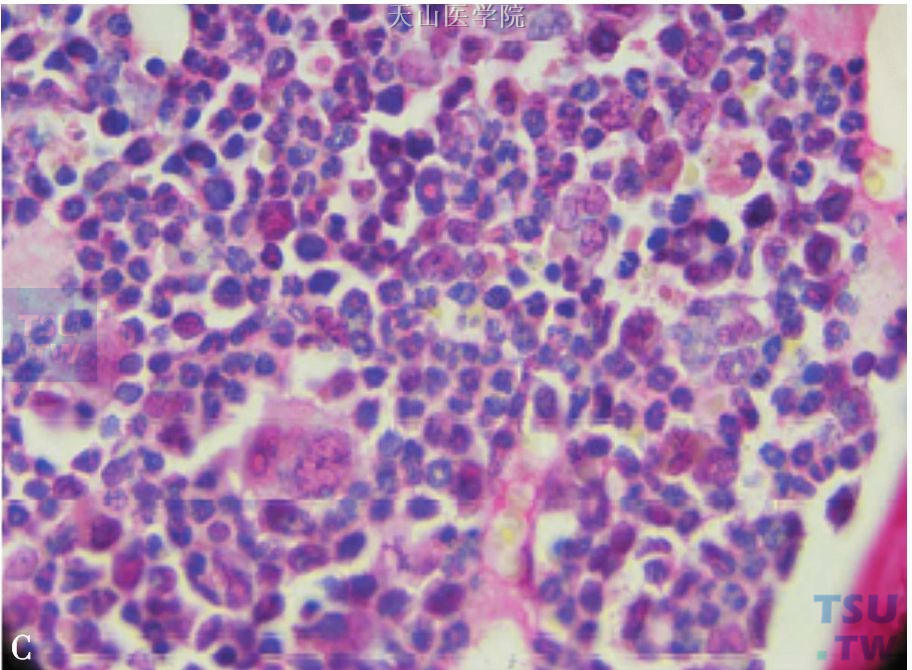
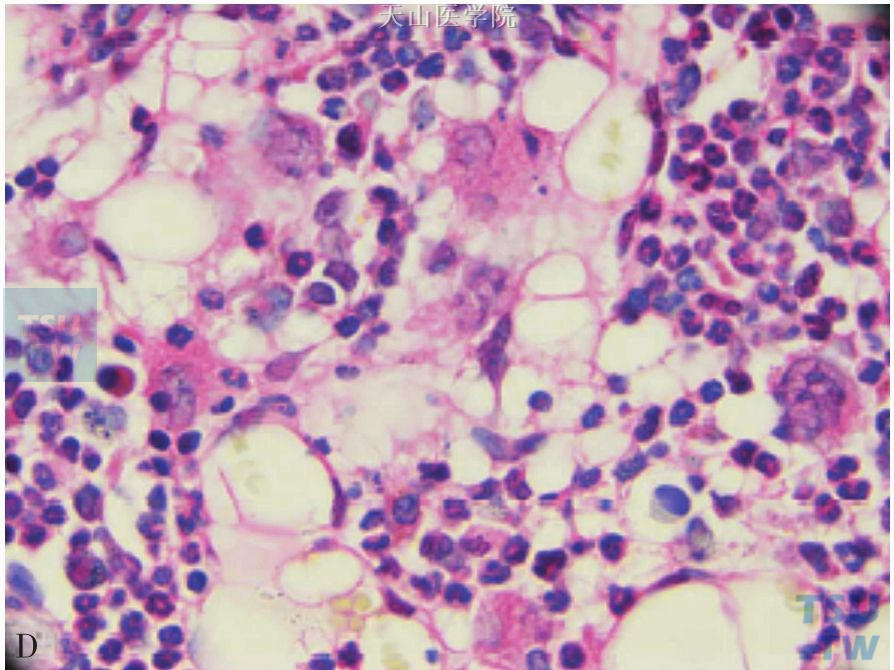
图6-5-1 A、C为正常小鼠骨髓涂片染色;B、D为营养不良小鼠骨髓涂片染色。营养不良小鼠骨髓腔内增生不良、脂肪细胞增多、正常造血细胞受抑
造血组织像其他再生和增殖能力强的组织一样,需要足够的营养供应才能正常行驶功能。营养不良尤其是恶液质可以使细胞生成减少,导致骨髓增生不良。早在18世纪40年代,Kornberg等人发现在营养不良的小鼠可出现白细胞减少及贫血等表现。此后有关营养不良与白细胞减少的相关研究陆续有报道。营养不良可通过改变骨髓组织和结构特征来影响成年鼠的造血功能。也有研究认为营养不良可使造血前体细胞阻滞在GO/G1期,降低造血细胞产生的速率。还有研究证明营养不良可引起淋巴器官或胸腺的结构改变从而影响免疫反应,还可影响骨髓造血功能导致骨髓增生不良,淋巴细胞生成减少。此外,营养不良引起白细胞减少,部分原因是由于造血细胞和骨髓中间充质干细胞的异常改变引起。最近发表在Plos One 上一项研究针对营养不良小鼠的白细胞减少机制进行了比较深入的研究,结果表明:①营养不良小鼠白细胞计数,其中包括中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞、嗜碱性粒细胞,较正常小鼠明显下降(图6-5-1);②骨髓脂肪化、骨髓增生不良在营养不良小鼠中也尤为明显;③在营养不良小鼠模型中,调节脂肪合成的转录因子PPAR-γ生成显著增加,这与骨髓脂肪化,增生不良密切相关;④营养不良小鼠的间充质干细胞体外培养产生G-CSF和GM-CSF的能力明显低于正常小鼠(图6-5-2),这也可能是白细胞减少的原因。
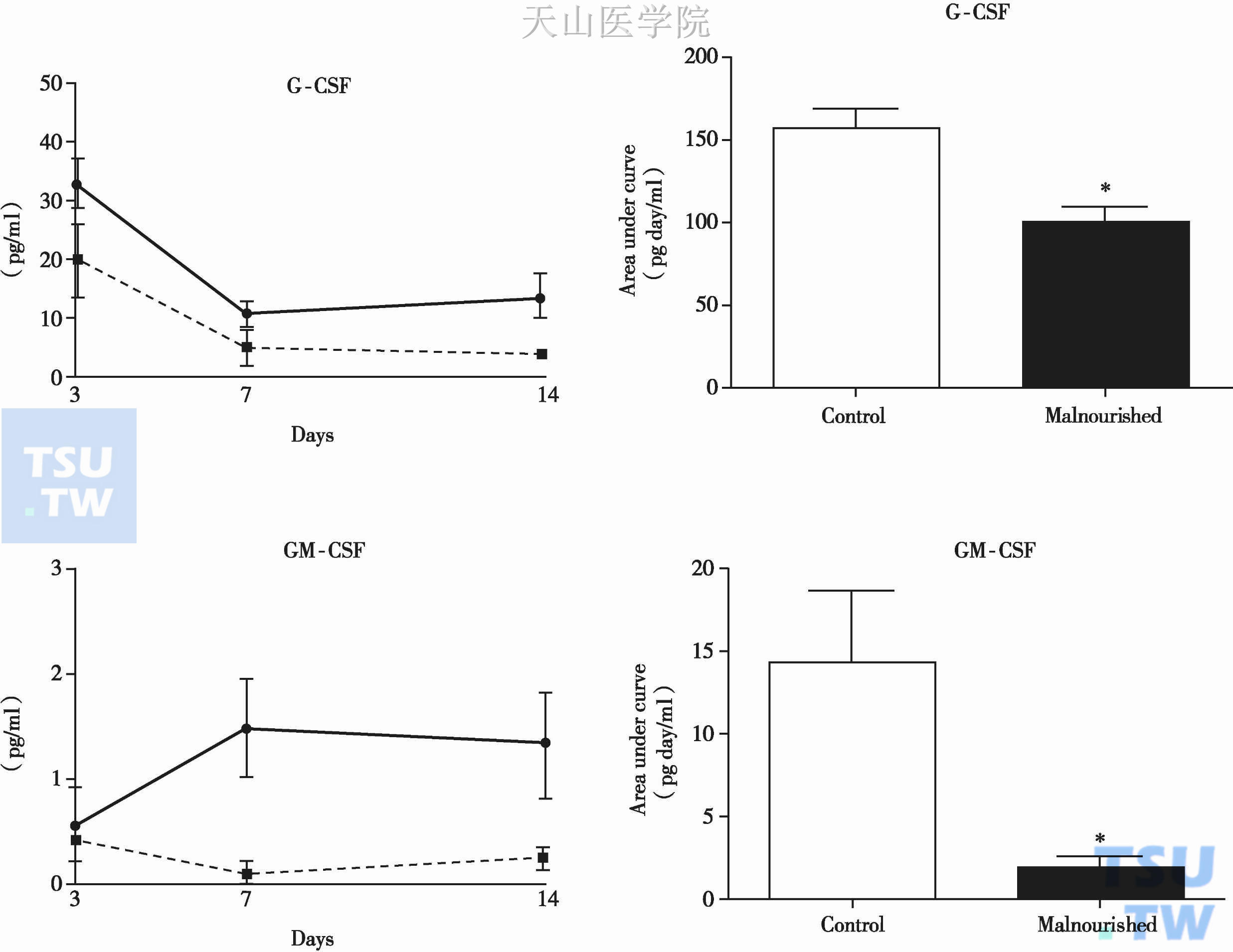
图6-5-2 营养不良小鼠的间充质干细胞体外培养产生G-CSF和GM-CSF的能力明显低于正常小鼠
基于目前针对营养不良与白细胞减少相关研究都是通过动物实验模型进行的,因此对于恶液质患者与白细胞减少的具体机制需要大规模的针对患者的临床研究进一步证实。
2. 肿瘤患者异常代谢所致白细胞合成减少
(1) 肿瘤患者的能量代谢:静息能量消耗量(REE)是指机体禁食2小时以上,在合适温度下,平卧休息30分钟后的能量消耗,占总能量的65%~70%。肿瘤患者往往处于高代谢状态,约比正常人的计算值大10%。
(2) 肿瘤患者的糖代谢:早期可能由于胰岛素的减少,或是周围组织对胰岛素的抵抗引起糖耐量的增加。这除了肿瘤本身的原因外,还与长期卧床、体重下降、感染等相关。在肿瘤患者中葡萄糖乳酸循环也增高,周围组织释放葡萄糖后被代谢成乳酸,而乳酸又在肝脏再次合成葡萄糖。这一过程耗费的能量较大,合成葡萄糖需要6个ATP,这个循环产生2个ATP,因此此循环无效。
(3) 肿瘤患者的脂类代谢:Klein认为,肿瘤患者的脂肪分解速率增快,主要通过以下4种机制实现:①由于摄入食物的减少与营养不良,故增加脂肪分解的速度;②由于体重的减少并相对增加去脂组织的比例,脂肪分解增加;③由于疾病的应激反应,刺激了肾上腺髓质分泌儿茶酚胺,同时增加了对胰岛素的抵抗,从而提高了脂肪分解;④癌肿本身分泌的细胞因子,加速了脂肪分解。
(4) 肿瘤患者的蛋白质代谢:随着肿瘤患者病情的发展、体重下降,蛋白质代谢异常表现在蛋白质转换率增加、血浆支链氨基酸下降;体内蛋白分解加快,从而导致蛋白缺失。
上述几方面的代谢异常可导致耗能增加,同时蛋白质、氨基酸、叶酸、锌、铁、维生素等缺乏,白细胞的合成数量及功能均受到影响。蛋白质及氨基酸的缺乏,可影响淋巴细胞的生成及产生抗体,从而使肿瘤患者的免疫力进一步下降。锌是90多种含金属酶的辅因子,可参与DNA的转录等作用,锌的缺乏,可以引起淋巴组织的萎缩,T细胞的成熟和更新需要锌。蛋白质的缺乏可引起血中运铁蛋白的含量低,造成铁缺乏,铁的缺乏可引起淋巴组织萎缩,减少血中淋巴细胞数量。含铁的酶也参与中性粒细胞的合成,因此,铁缺乏也可引起中性粒细胞的缺乏。维生素D合成的1α,25-(OH)2D3能够调节造血细胞包括白细胞的生长和分化,它的缺乏,也可引起白细胞数量的减少。此外多种维生素的缺乏,可以使动物淋巴组织萎缩,淋巴细胞减少。其他微量元素也会对免疫细胞的合成产生或多或少的影响,这里不一一叙述。总之,就目前所知,蛋白质的缺乏,对免疫细胞的影响最大。
3. 肿瘤患者骨髓转移引起白细胞减少
患者骨髓转移,转移癌细胞占据了骨髓腔,影响骨髓正常造血,可以出现白细胞减少、贫血、血小板减少。
4. 术后肿瘤患者白细胞减少
肿瘤患者于术后复查血常规时常常发现白细胞总数减少,尤其对于消化道肿瘤患者更为常见,可能原因主要由于消化道肿瘤术后患者由于术中切除了部分及大部胃肠,从而导致营养物质的吸收减少,由此引起了白细胞合成减少。
5. 化疗引起肿瘤患者白细胞减少
由于恶性肿瘤细胞与正常细胞之间缺乏根本性的代谢差异,因而大多数抗癌药物在杀灭癌细胞的同时也对人的正常组织细胞造成损害,特别是对增殖较快的骨髓造血干细胞损害更为明显,从而引起白细胞减少。
6. 放疗引起肿瘤患者白细胞减少
白细胞减少是放疗患者常见的一个副作用,射线直接损伤白细胞DNA,从而杀伤白细胞。由于正常细胞耐受放射量比肿瘤细胞低,因此如何在让瘤细胞受到高剂量照射,又能同时保护周围正常组织不受损伤是放疗界研究的主要课题。
临床表现及不良结局
中性粒减少相关性发热是肿瘤患者本身及治疗过程中最为常见的并发症。可出现呼吸系统、消化系统、泌尿系统等各个系统的感染,常表现为发热,乏力,咳嗽、咳痰,腹痛、腹泻,尿频、尿急、尿痛等。中性粒细胞减少时严重时可伴有败血症甚至危及生命。尽管经验性抗生素的应用是有效的,然而这种中性粒减少相关性发热带来的后果还是较为严重的。且有时抗感染治疗本身就有很多毒性及副作用,同时增加了较大的医疗费用。由于中性粒细胞减少使肿瘤治疗相关手段如放化疗的剂量及治疗频率受到限制,从而使肿瘤的治疗手段不能有效地发挥出来。
另外,早在1863年,Rudolf Virchow等人在一定程度上揭示了营养、炎症与肿瘤之间的关系。急性应激、慢性疾病、营养不良都可引起炎症因子活化。一方面,活化的炎症因子可引起ROS、RNS损伤DNA,进一步导致肿瘤的发生。另一方面,炎症因子的活化可引起NF-κB的、NO及COX-2增高,从而使细胞增殖、血管生成及具有浸润性,导致肿瘤的发生(图6-5-3)。白细胞减少可以进一步加重感染的发生,使上述进程加重,恶性循环。
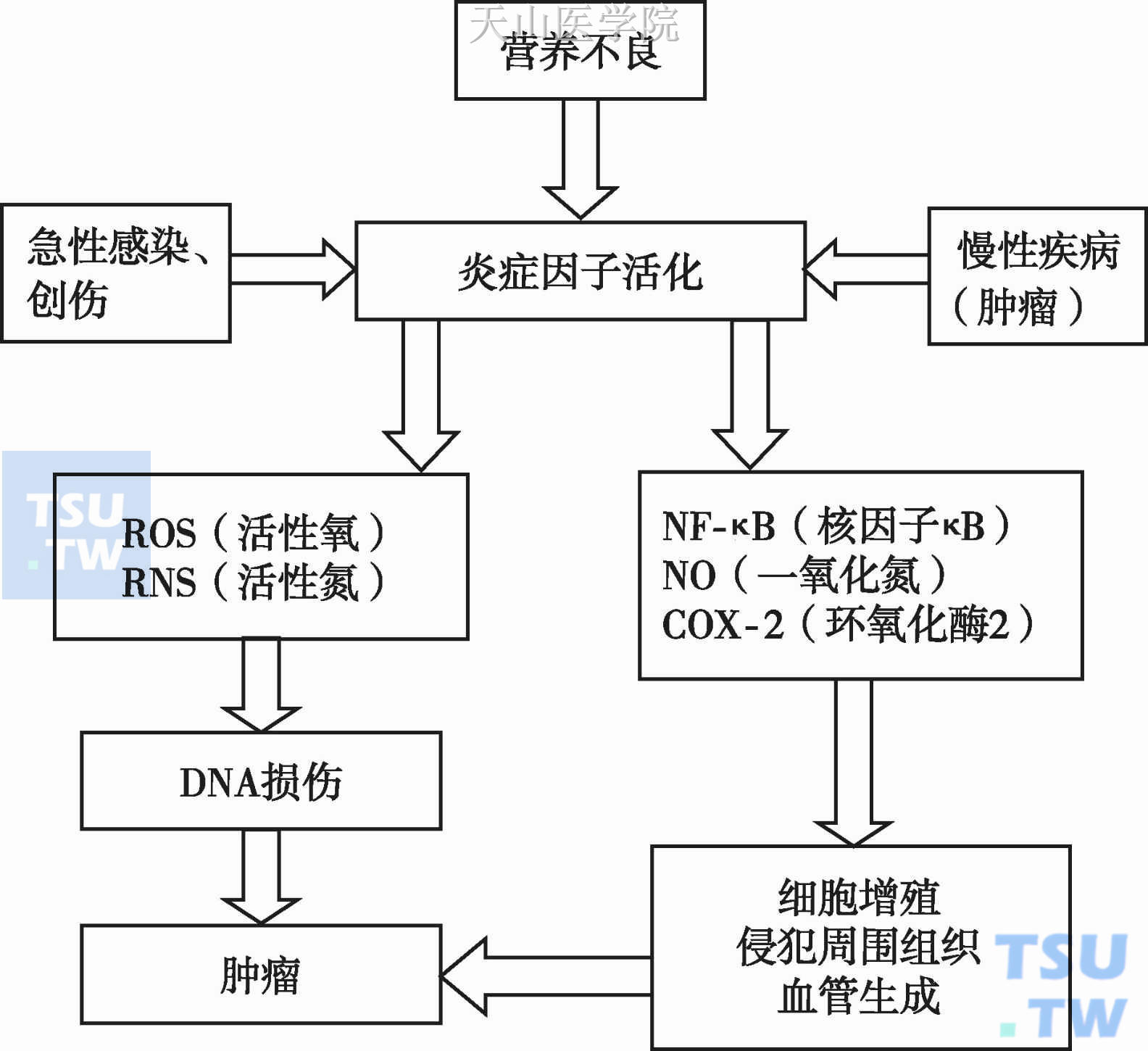
图6-5-3 炎症因子活化导致肿瘤的机制
治疗
针对白细胞减少可以由肿瘤本身因素、肿瘤治疗相关因素、恶液质等方面引起,治疗上主要包括病因治疗、营养支持治疗、对症支持治疗等。
1. 病因治疗——抗肿瘤综合治疗:对于部分肿瘤患者能够在一段时期、一定程度上控制疾病进展,提高生活质量、延长生存期。
2. 营养支持治疗:定期评估患者营养情况,早期判断恶液质的发生,多学科会诊,选择恰当的营养途径、制订正确的营养配方,争取逆转早期恶液质。
3. 对症支持治疗
(1) 适时应用抗生素:中性粒细胞减少与感染有非常密切的关系,当粒细胞计数<1.0×109/L 时感染的持续时间及程度明显增加,尤其是中性粒细胞计数低于0.5×109/L后,感染的发生率急剧上升。适时应用抗生素可控制感染。
(2) GCSF和GMCSF的应用:及时使用GCSF和(或)GMCSF对治疗炎症白细胞减少患者较为重要,缩短了患者处于白细胞计数严重低下状况的时间,减少了继发感染的可能性。
小结
白细胞是血液中的一类细胞。正常人体内的白细胞包括中性粒细胞、嗜酸性粒细胞、嗜碱性粒细胞、淋巴细胞、单核细胞等。白细胞除存在于血液和淋巴中外,也广泛存在于血管、淋巴管以外的组织中。它们的功能包括细胞的吞噬作用以及产生免疫作用。营养不良是能量、蛋白质和其他营养素缺乏、过剩或失衡的营养状况,可对组织机体的形态、生理功能和临床结局产生可观察到的不良反应。恶液质是营养不良的后期表现。肿瘤患者营养不良的发生率较高,同时恶液质也是肿瘤患者死亡最常见原因之一。白细胞减少可继发于伴有恶液质的肿瘤患者,主要由恶液质因素、肿瘤本身因素和肿瘤治疗相关因素引起。白细胞减少可出现各个系统的感染,包括呼吸系统、消化系统、泌尿系统的感染,甚至发生败血症危及生命。同时白细胞减少也可以限制肿瘤放化疗的治疗,加重炎症反应,甚至进一步促进肿瘤的发生。治疗上包括抗肿瘤综合治疗、肿瘤患者的营养支持治疗、抗生素、GCSF和GMCSF的应用等。正确分析白细胞减少的原因,给予恰当的治疗,是治疗伴有恶液质的肿瘤患者白细胞减少的关键所在。
思考题答案
1. 第一次白细胞减少出现于肿瘤化疗间歇期,对症治疗后可升高至正常。此后间断复查血常规提示白细胞正常。考虑与化疗造成的一过性骨髓抑制有关。
第二次白细胞减少出现于伴有恶液质的肿瘤晚期阶段,此时未行相关抗肿瘤治疗。综合分析白细胞减少原因如下:①肿瘤因素:肿瘤异常代谢可导致营养物质的缺乏,造血原料缺乏引起白细胞合成减少;同时也不除外骨髓转移癌的可能。②恶液质因素:恶液质是营养不良后后期阶段。此时为重度营养不良。营养不良可引起造血干细胞及骨髓造血微环境的改变进而引起白细胞生成减少。
2. 补充叶酸、维生素B12的检测,铁代谢、转铁蛋白的检测、锌的检测及微量元素的检测。骨髓穿刺涂片及活检除外骨髓转移癌。
3. 第一次白细胞减少出现于肿瘤化疗间歇期,考虑与化疗造成的一过性骨髓抑制有关。治疗上可应用粒细胞集落刺激因子升白细胞治疗。
第二次白细胞减少出现于伴有恶液质的肿瘤晚期阶段,综合分析白细胞减少原因考虑与肿瘤因素及恶液质因素有关,治疗上,建议若一般状态允许,评估各脏器功能,若无化疗禁忌,多学科会诊,可考虑抗肿瘤治疗,即病因治疗;针对恶液质,若评估为早期恶液质,建议给予营养支持治疗,多学科会诊,给予个体化的营养治疗,制定合理的营养配方,争取逆转或减缓恶液质的进一步恶化,为抗肿瘤治疗提供相应保障。
(王轶卓 李薇)
