病例与思考
患者,男性,39岁。因“鼻咽癌放、化疗后2年余”入院。患者2年前确诊为鼻咽低分化鳞癌并骨转移,曾行根治性放疗及6个周期的化疗。入院诉头痛,口渴喜饮,咽干口燥,食欲下降,牙龈肿痛,面颊胀痛,听力下降,体重近3月减轻10kg。查体:身高1.72m,体重49kg,消瘦,中度贫血貌。浅表淋巴结不肿大,心肺肝脾无异常,颈部皮肤放射性损伤变坚硬,左耳听力下降,卡氏评分50。辅助检查:血常规:Hb 102g/L,RBC:3.2×1012/L,WBC:3.1×109/L,PLT:194×109/L,CRP 25mg/L,ALT 125U/L,AST 87U/L,TBIL 32U/L,DBIL 15.5U/L,ALB26.8g/L,PA 80mg/L;ALP 312U/L,GGT 127U/L,Cr 8µmol/L,Ua 313µmol/L,BUN 3.6mmol/L,GLU 6.62mmol/L,TG 0.17mmol/L,GHO 1.65mmol/L,K+ 3.64mmol/L,Na+ 139mmol/L,Cl- 99mmol/L,Ca2+ 2.21mmol/L,ECT检查提示鼻咽癌伴颅骨转移。诊断:鼻咽癌放化疗后复发并骨转移。
- 根据目前的证据,患者是否存在恶液质?营养支持治疗方案应注意哪些问题?
- 根据目前的证据,是否推荐患者使用生长激素?
- 根据目前的证据,生长激素适合应用于哪类疾病导致的恶液质状态?
恶液质是一种进行性的体重减轻,肌肉、脂肪组织减少,功能下降的综合征。通常由代谢异常、宿主免疫系统产生致炎细胞因子与分解代谢因子、厌食及早饱导致的摄食减少等因素引起。常见于恶性肿瘤、艾滋病(AIDS)、慢性阻塞性肺疾病、心功能衰竭与慢性肾衰竭的患者。机体通过不同的激素调节身体组成。其中,对恶液质患者最具影响的促进合成代谢的激素包括生长激素(growth hormone,GH)与胰岛素样生长因子(insulinlike growth factor,IGF)。两者参与调节蛋白质的合成与降解,脂肪的动员与氧化,葡萄糖的吸收与代谢。恶液质的患者通常会存在GH缺乏或抵抗,使体内合成代谢信号通路受阻。近20年,随着基因工程技术的突飞猛进,基因重组人生长激素(recombinant human growth hormone,rhGH)的问世,为慢性消耗性疾病的患者带来新的希望。
GH的生理作用
GH是由腺垂体分泌的一种含有191个氨基酸的蛋白质激素。它受下丘脑生长激素释放激素(growth hormone releasing hormone,GHRH)与生长激素抑制激素的双重调节,呈脉冲式分泌。生长激素通过直接作用和间接作用促进骨、软骨、肌肉以及其他组织细胞分裂和增殖。它的间接作用主要通过与肝细胞膜上的GH受体结合,产生具有促生长作用的肽类物质。因为这种肽类物质的化学结构与胰岛素相似,所以称为胰岛素样生长因子(IGF)。目前已分离出两种胰岛素样生长因子,包括IGF-1和IGF-2。IGF-2对胚胎时期的生长和发育起重要的调节作用。而IGF-1则对机体此后的生长调节起重要作用。目前已发现人体消化道、淋巴组织、神经组织、脂肪组织、骨和软骨组织上有生长激素受体分布。此外,肌肉、肾脏、心和肺都能产生IGF并以旁分泌的方式在局部起作用。除了上述促进机体生长的作用以外,GH还对能量代谢及免疫功能有调节作用。GH通过IGF促进氨基酸进入细胞内,加速蛋白质的合成;并且促进脂肪的分解,增加游离脂肪酸及酮体的生成;它的释放能引起胰岛素水平的下降,抑制外周组织摄取与利用葡萄糖,减少葡萄糖的消耗,提高血糖水平(图14-1-1)。
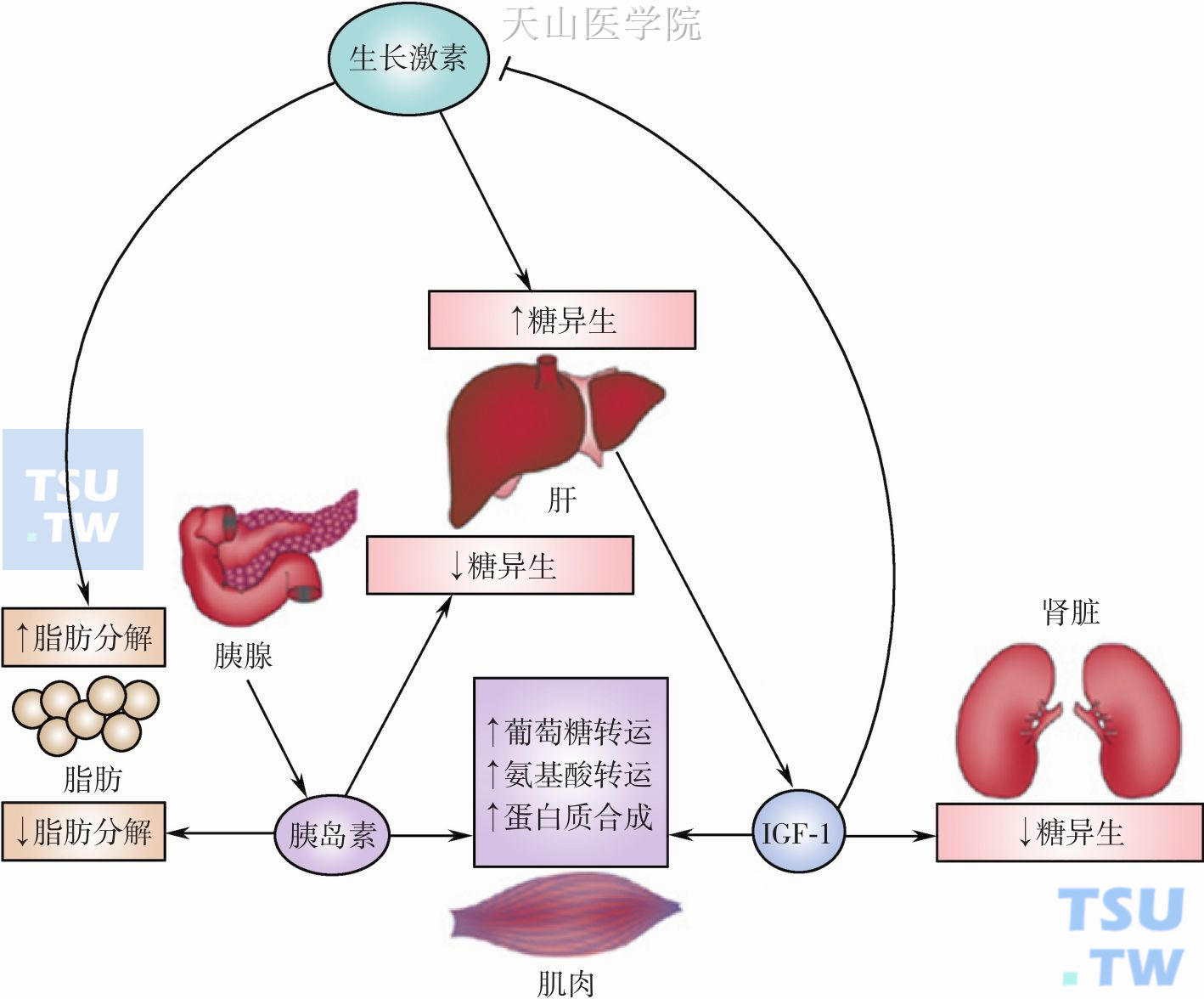
图14-1-1 生长激素的生理作用
GH/IGF、IGF-1受体、IGF结合蛋白
GH的间接作用是通过IGF-1、IGF-2介导,IGF的分泌量受GH的调节,由于两者之间的密切关系,构成了生长激素-胰岛素样生长因子轴(GH-IGF axis)。IGF家族由两种低分子多肽(IGF-1、IGF-2)、两类特异性受体(receptor,IGF-1R和IGF-2R)、及六种结合蛋白组成。IGF的生物学功能是通过与特异性的靶细胞表面的受体结合而实现的。生理状态下的IGF能促使肿瘤细胞系发生有丝分裂,它不仅是生长激素的主要传导介质,还在细胞癌变的发生、分化与转化的过程发挥不可忽视的作用。大量的研究表明在乳腺癌、前列腺癌、结肠癌、脑膜瘤等细胞中有IGF-1R的分布,抑制IGF-1R的表达不仅能终止细胞的转化还能逆转细胞的恶变。IGF与其他的生长因子不同,不论在血清,细胞外液及细胞培养液中都与特异性的结合蛋白结合形成胰岛素样生长因子结合蛋白(insulin-like growth factor binding protein,IGFBP),并被运送到全身各处。到目前为止,已发现6种结合蛋白:IGFBP1~6。它们与两种IGF都具有高亲和力,而不与胰岛素结合。在血液及组织液中以IGFBP3含量最高,它对IGF的效应有抑制作用。生理情况下,IGF与其结合蛋白的亲和力大于或近似等于与其受体的结合(图14-1-2)。
GH对免疫系统的调节
GH能增加胸腺素的合成和分泌及刺激人胸腺上皮细胞的增殖。给缺乏GH的动物及老年动物补充GH,能增加胸腺细胞的数量,增加胸腺素的合成,恢复退化的胸腺形态结构。淋巴组织中有GH受体的分布,GH与其受体结合之后,促进IGF-1的产生,继而促使原始骨髓细胞、T细胞在内的免疫原始细胞从骨髓向胸腺转移、分化。体外实验表明在培养的混合淋巴细胞培养液中加入基因重组人生长激素(recombinant human growth hormone,rhGh),CD4细胞的数目随着剂量增大而增多,而CD8细胞的数目随着剂量的增大而减少。刘权焰等进行的一项随机双盲对照试验表明,将100例接受手术的消化道肿瘤患者分为两组,对照组单纯接受胃肠外营养,受试组在接受胃肠外营养的同时皮下注射rhGh(8IU/d)。一周以后抽血检查两组患者的免疫指标,发现受试组CD3与CD4下降不明显,而对照组CD3和CD4显著低于受试组。Bresson等的研究表明人体外周血单个核细胞中30%表达GH受体,几乎所有的B淋巴细胞与单核细胞是GHR阳性细胞。此外,外周血中自然杀伤细胞(natural killer,NK)细胞表面也存在GH受体。动物实验表明,垂体切除的大鼠NK细胞活性降低,补充外源性GH之后,能恢复NK细胞的活性。GH缺乏的儿童虽然NK细胞数量正常,但是活性下降,补充GH以后,NK细胞的活性比治疗前显著改善。
GH在恶液质中的应用
GH在心、肺疾病致恶液质中的应用
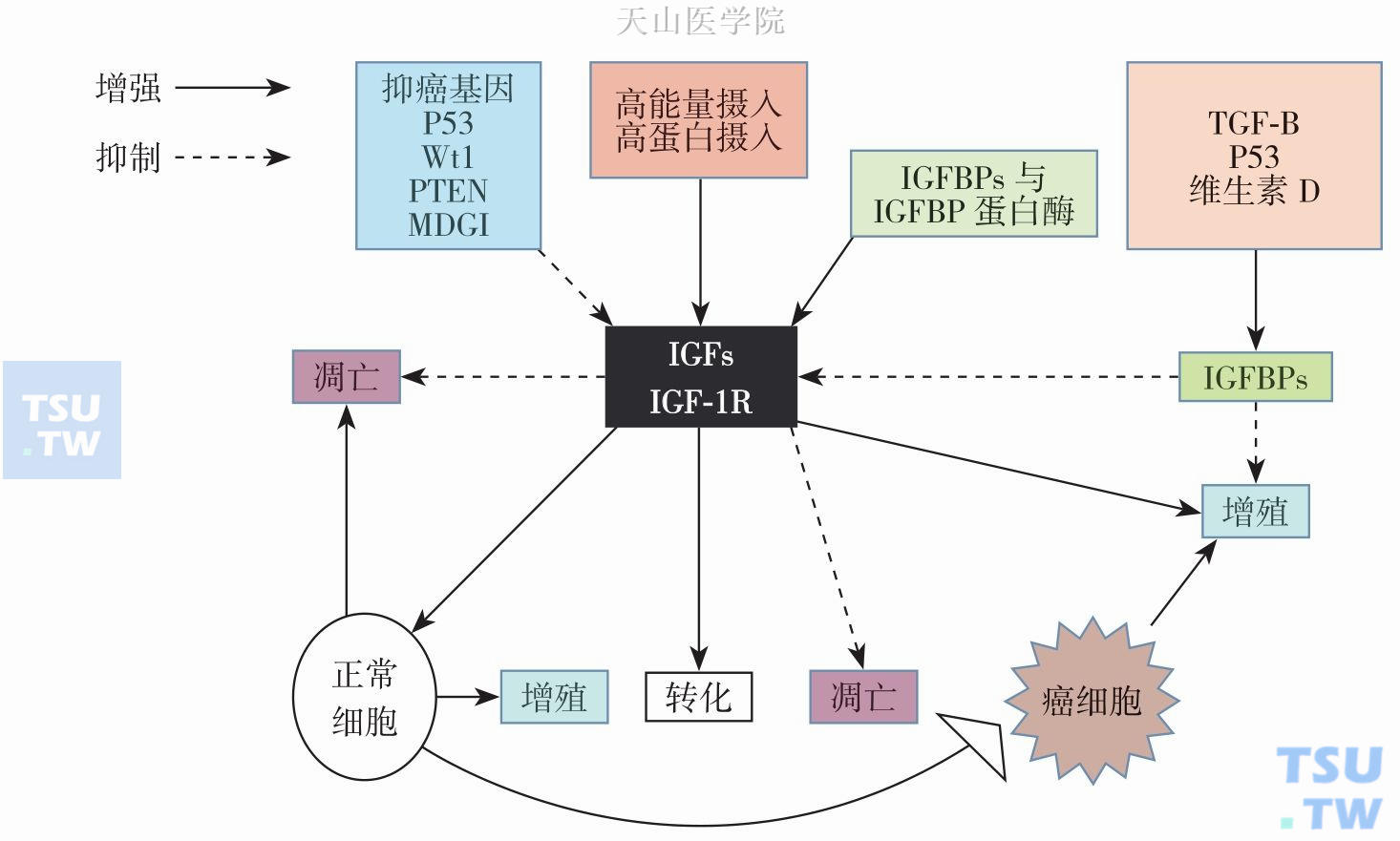
图14-1-2 IGF-1与IGF-1R分别对癌细胞与正常细胞的作用
一项小样本的随机对照研究,将GH 0.06mg/kg•d给予慢性阻塞性肺疾病(Chronic obstructive pulmonary disease,COPD)的营养缺乏患者,3周后,与对照组相比,瘦体组织显著增加(2.3±1.6 vs. 1.1±0.9kg,P<0.05)。然而,两组间的最大呼气压力、握力、运动能力及主观感觉未见显著差异。大约20%的心功能衰竭患者会出现恶液质的现象,合并恶液质的心功能衰竭患者的死亡率高达50%以上。有报道指出,罹患如慢性心功能衰竭、恶性肿瘤等慢性疾病的患者,体内GH水平增高,伴随IGF-1的降低,提示存在GH抵抗。此外,上述患者还存在胰岛素抵抗的现象。因此,参与促进肌肉中蛋白质合成、抑制蛋白质分解的GH与胰岛素均表现为信号通路受损。尽管目前对上述现象的具体作用机制仍未明确,可以肯定的是,GH抵抗与胰岛素抵抗参与了肌肉蛋白和瘦组织群消耗的过程。国外几项随机对照研究显示,针对存在GH抵抗的患者,rhGH对其伴随的肌肉消耗、体重减轻、食欲下降等临床表现没有改善。另一项较新的随机单盲对照研究提示,针对存在GH缺乏的心功能衰竭的患者,给予补充GH能显著增加峰值摄氧量、血管反应、左心室功能以及生活质量。
GH在艾滋病相关消耗综合征中的应用
在AIDS相关消耗综合征患者中,同样出现GH水平降低,IGF-1水平增高,提示机体存在GH抵抗。从20世纪90年代开始,学者们开始观察给这类患者使用rhGH,能否改善其分解代谢的情况。大部分的研究结果均表明,无论患者是否存在GH抵抗,外源性给予的GH治疗都能显著增加瘦体组织、体重以及运动能力(表14-1-1)。一项大型的临床干预研究,纳入对象为555名HIV感染,伴随体重在近期1月内下降10%,BMI<20或体重<理想体重90%的患者。他们被随机分为三组:其中166名患者每天皮下注射rhGH(剂量为0.1mg/(kg•d),最大剂量为6mg/d);190名患者接受同等剂量,但是隔天注射;另外199名患者为对照组。治疗时间持续12周。结果显示:两组接受GH治疗的患者,瘦体组织与体重的增加、运动能力及生活质量的提高显著高于对照组。其中,瘦体组织(每天使用GH:+5.2kg vs.隔天使用GH:+3.3kg)与体重(每天使用GH:+2.2kg vs.隔天使用GH:+1.5kg)的增长呈剂量相关性,每天使用组优于隔天使用组。然而,应用GH伴随而来的体液潴留、血糖增高、关节疼痛等不良反应在每天使用组表现的更为突出。
表14-1-1 GH在艾滋病相关消耗综合征中应用的随机双盲对照研究
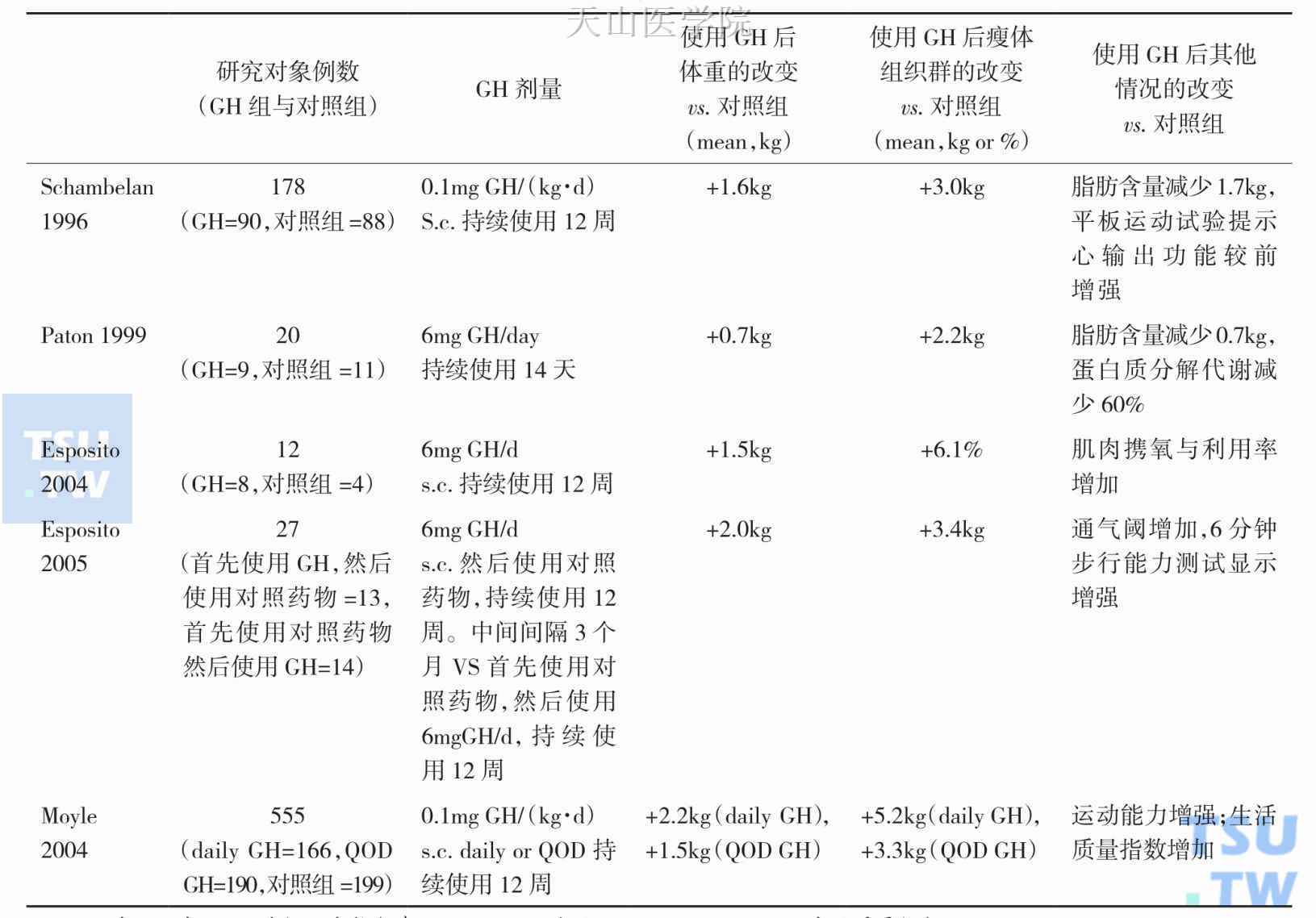
s.c.:皮下注射;GH:重组人生长激素;QOD=隔天使用administration;QOL=生活质量指数
GH在肿瘤恶液质中的应用
肿瘤终末期伴随恶液质时,机体主要以肌肉和脂肪的分解来供能,是一种耗能的高分解代谢状态。此时,胰岛素水平增高,但血糖未能相应降低,提示可能存在胰岛素抵抗。当恶液质进展时,体内肿瘤坏死因子(tumor necrosis factor,TNF)、白介素(interleukin,IL)-6以及IL-8水平显著增高。研究表明,血清TNF和IL-6通过增加瘦素水平降低食欲,减少对食物的摄取,葡萄糖生成增加,外周组织利用障碍,从而诱导机体产生胰岛素抵抗。通过抑制脂蛋白脂酶活性,造成脂肪组织丢失,血液循环中甘油三酯含量升高。而IGF-1可以下调瘦素水平,促进食欲,其作为一种促合成代谢类激素,可纠正机体高分解代谢状况。同时作为一种类胰岛素样生长因子,部分发挥胰岛素样作用降低血糖,这提示IGF-1可能具有拮抗TNF和IL-6的促肿瘤恶液质效应。恶液质机体中血清IGF-1可能发挥着促合成代谢和抑制癌性细胞因子的双重作用或者两者间本身存在交叉作用,从而抑制了恶液质状态的迅速恶化。国内外许多学者希望通过rhGH的代谢调理作用,改善肿瘤患者异常高分解代谢状态,促进蛋白质合成,纠正负氮平衡,提高机体的免疫功能。有研究表明,低能量肠外营养与rhGH联合使用7天,患者血清IGF-1明显高于对照组。IGF-1对骨骼肌有很强的合成代谢效应(图14-1-3),抑制蛋白质分解,增加氨基酸摄取和细胞增生,改善氮平衡,促进蛋白质合成及脂质氧化,从而减轻应激状态。但是,目前针对使用rhGH改善肿瘤恶液质的相关大型随机对照研究尚未见报道。
GH在危重症患者中的应用
GH有利于增强机体免疫功能,曾经有学者认为,GH可缩短危重患者的平均住院日,呼吸机通气时间和降低死亡率。同时也有学者建议在炎性肠病、短肠综合征、大手术围术期、严重创伤、感染、烧伤及肠道功能不全如长期应用全肠外营养(total parenteral nutrition,TPN)所致等方面应用GH。1999年发表在新英格兰杂志上的两个大型随机对照试验指出,重症患者应用GH可大大增加其死亡率,这种结果与重症患者可能存在GH的抵抗造成IGF-1的缺乏有关,也可能与大剂量使用GH (0.1mg/kg)造成IGF-1中毒或谷氨酰胺的缺乏有关,亦可能与GH所用的时间有关。目前,尚没有更新的大型随机临床试验来证实GH对重症患者的作用。国外学者最近发表的一篇综述指出,GH应用于危重患者的作用仍不明确,除非患者存在明确的GH分泌不足的指征(如血清IGF-1水平低等)。否则,不推荐给危重症患者使用rhGH。
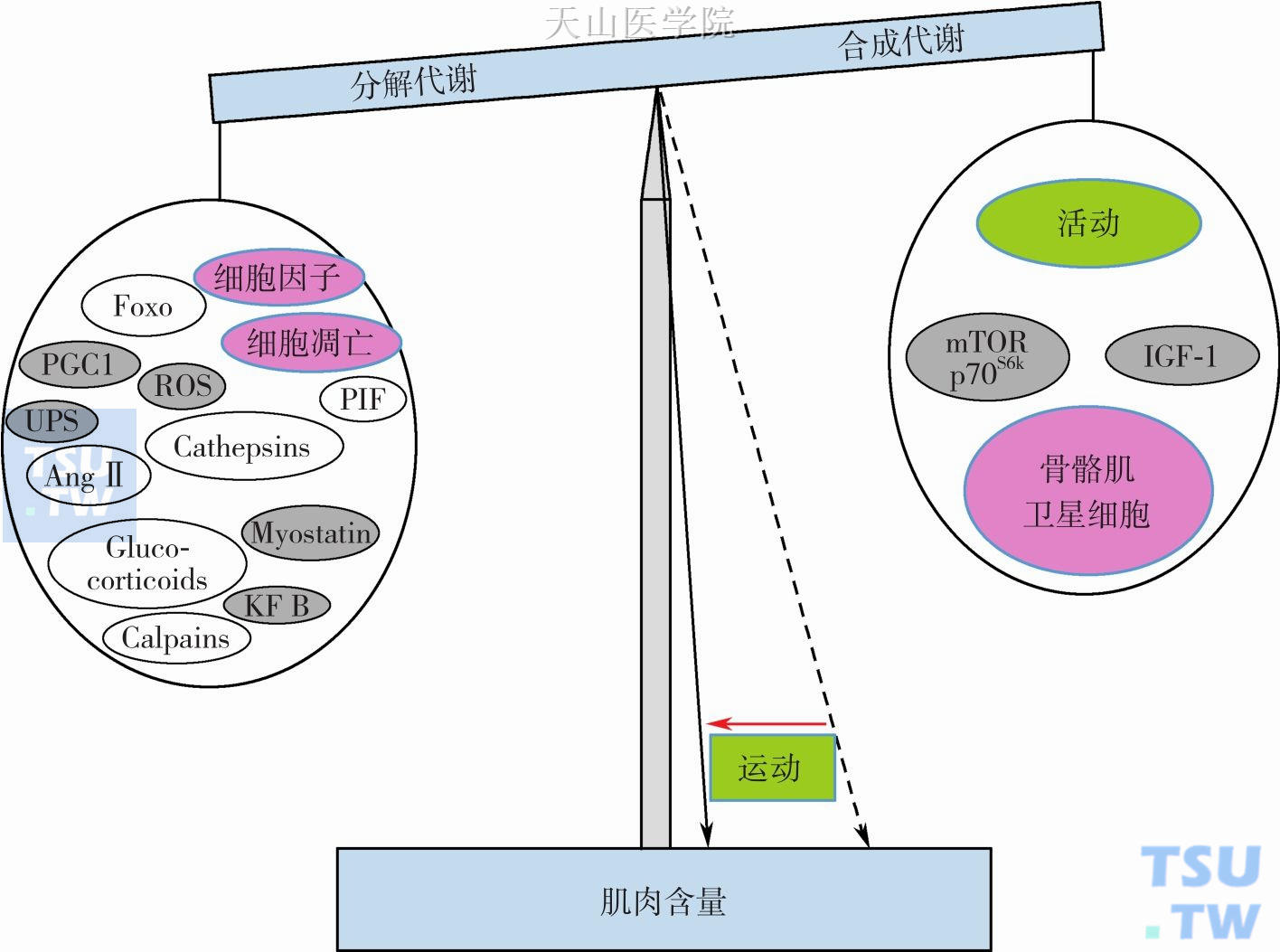
图14-1-3 IGF-1促进骨骼肌蛋白质的合成
一种理想的治疗恶液质的药物应该具备以下几点:①具有促进合成代谢;②抗炎;③促进食欲的作用。GH-IGF通过自分泌和旁分泌的机制对许多组织细胞的增殖、分化起调节作用。GH、IGF-1的信号通路,已经逐渐被医学界认为是改善恶液质的最具潜力的药物靶点。现有的研究肯定其具有改善氮平衡、增加体重、增加瘦体组织、增强免疫功能等作用。美国FDA已经批准临床将rhGH应用于艾滋病相关消耗综合征。而对于恶性肿瘤、心功能衰竭等慢性消耗性疾病引起的恶液质,目前尚未有明确的推荐,有待更多的研究提供依据。
(区俊文)
