对每一例撤机和拔管失败者,应积极查找失败的原因,并积极治疗导致SBT失败的可逆因素(图2-19)。在查找SBT失败的原因方面,近年加强了对撤机失败患者的病理生理学研究,取得了一些进展。撤机和拔管失败的病理生理学改变、失败原因、依据及其对策见表2-49。
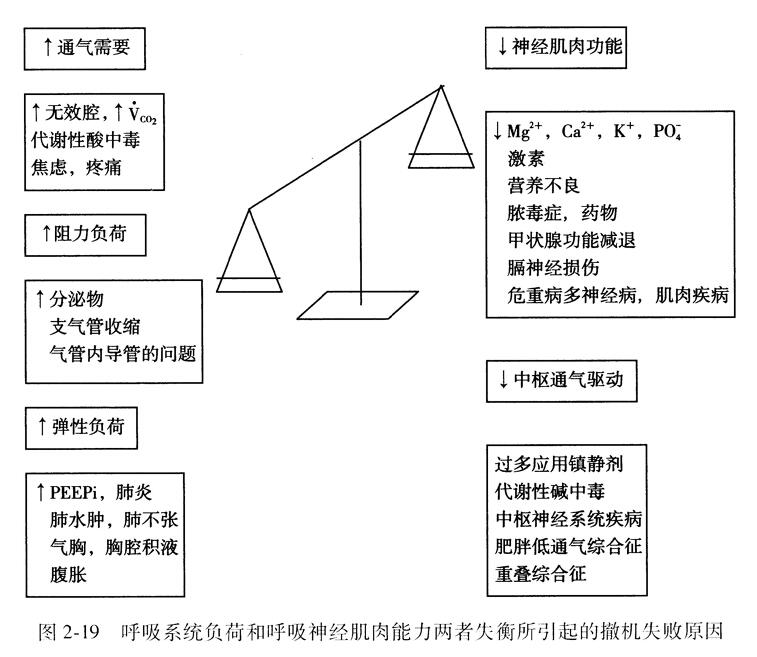
撤机失败的病理生理学分类为:呼吸负荷增加、心脏负荷增加、通气驱动降低、神经肌肉能力下降、神经精神因素、代谢紊乱、营养问题等。

呼吸负荷增加
是否决定让患者进行撤机尝试,取决于医生对患者的评估:患者的血流动力学稳定,清醒、疾病过程已适当治疗,微小的呼吸机依赖性是存在的[例如FiO2≤0.5,PEEP≤8cmH2O,PaO2/FiO2>150mmHg(20kPa),SaO2≥90%]。撤机的成功取决于呼吸肌泵的能力对其所承担负荷的耐受性。这种呼吸负荷是呼吸肌泵要克服的阻力和顺应性的功能。正常呼吸系统的阻力<5cmH2O/(L·S),正常呼吸系统静态顺应性是0.06~0.1L/cmH2O。静态肺顺应性的改善可提醒医生撤机的潜在可能,也已经把静态肺顺应性整合进计算机驱动的模式。那里VT≥8m/kg,平台压≤30cmH2O被包括在规则系统之内。最大吸气压被用于评估吸气肌强度,在用力呼气到残气量位以后维持负压1秒,或用单向呼气阀。最大吸气压≤-25~-20cmH2O被认为是预计成功撤机的指标。
肺顺应性的减低可能继发于肺炎、心源性或非心源性肺水肿、肺纤维化、肺出血或引起弥漫性肺浸润的其他疾病。在危重病患者中,肺炎是很常见的,可以是入院的主要诊断,也可以是继发性的呼吸机相关肺炎(vntiator-associaledpneumonia,VAP)。基础疾病的治疗和好转是拔除气管导管的先决条件。重新插管可使医院内肺炎的发生率增加4.5倍。治疗肺水肿,减少肺水,可增加肺顺应性。若肺胸顺应性减低是由肺纤维化或胸壁的病变(如脊柱后侧凸)引起,即是较难经治疗逆转的,肥胖、腹胀或腹水的夹板样作用也应考虑是降低顺应性的原因。此外,支气管痉挛、COPD患者的动态过度充气也增加呼吸负荷,应予相应治疗。
气道阻力增高:常因气道分泌物增加,气道分泌物潴留所致,并引起V/Q比例失调加重,徒增呼吸功,减少肺内气体交换。原因:①气道分泌物过多,常因肺感染未有效控制;②由于咳嗽无力,黏液纤毛廓清系统受损,气管吸引不经常或操作不当,使气道和肺内分泌物潴留。
治疗:给予有效抗生素,加强气道清洁处理技术的应用,包括气道适当湿化,让患者深呼吸和用力咳嗽,施行气管吸引,胸部理疗(叩背和体位引流)等增加气道分泌物郭清的方法。
上气道阻塞:发生的危险性随着插管创伤性和插管时间延长增加,另外,女性比男性更易发生危险性。原因:声门水肿,表现为吸气时喘鸣,通常在拔管后24小时内发生,声门下水肿或狭窄也产生类似表现。拔管前评估上气道通畅性的方法是:当将气管插管的气囊放气时,可听诊漏气情况(漏气试验)来发现。或应用辅助-控制通气,监测吸入和呼出潮气量差,如果气囊漏气量<110ml,或<输入潮气量的10%则提示拔管后喘鸣的危险性增加(定量气囊漏气试验阳性),但拔管后喘鸣常可有效的治疗而不一-定需要重新插管。此外,气管插管外周黏附分泌物可引起试验假阳性,或由于机械潮气量加上从导管周围自主吸入气体而使吸入潮气量隐性增加导致吸入潮气量增加。尽管有这些影响,但不少气道漏气处理专家仍推荐,当为患者拔管时气囊漏气试验仍有参考价值。随机对照研究并没有证明拔管前应用皮质激素可减少拔管后喘鸣的发生率。
治疗:如临床情况许可,可先试用肾上腺素(0.5ml肾上腺素稀释于3ml 0.9%氯化钠注射液)雾化吸入,常可在15~20分钟内缓解症状,如疗效明显,必要时可重复应用,每20~30分钟给另外1~2个剂量。应用肾上腺皮质激素因生效时间长,通常即时效果差。有条件可吸入氦氧混合气体,如用药后没有快速显著的效果,需重新气管插管,插管后留置导管48~72小时,以便在拔管前有足够时间让组织水肿改善。若反复发生水肿或严重上气道狭窄需气管切开。
过高的呼吸功也可以是不恰当的呼吸机条件引起(如不恰当的吸气流速或流量触发条件)导致人-机不协调,这种不协调的成分可包括吸气延迟,吸气初始的流量输送过快或过慢和吸-呼切换时的不同步,无效触发等,以及高PEEPi的作用(代表阈值负荷)。
心脏负荷增加
许多患者通常患有基础心血管疾病,如伴有缺血性心脏病(冠状动脉病变)、瓣膜性心脏病、收缩或舒张期的心功能不全,或为高龄老人。隐性和不易识别的心肌功能障碍,只有在承受撤机的负荷时才明显。在撤除正压通气,改由患者自主呼吸时,胸腔内压从正压转为负压,静脉血回流增加,回心血量增加,而引起左心室前负荷增加,同时,自主呼吸做功的增加,增加了心肌耗氧,导致心功能不全的发生和冠状动脉缺血的加重。这种不易识别的心肌功能障碍只有在开始撤机尝试时才表现明显。这在应用CPAP或心源性肺水肿应用NIV时获得明显的治疗效果,可获得证实。治疗可给予硝酸盐制剂、利尿剂等。
有一些增加心脏负荷的因素,如动态过度充气(存在PEEPi),可增加肺血管阻力,减少右室的充盈,减少心排出量。撤机过程的代谢需要也增加,如果基础性系统疾病(如脓毒症)没有完全解决,代谢增加就更明显。为适应撤机过程的代谢需要,心排出量必然要增加。可测定的指标,包括血清乳酸增加,混合静脉血氧饱和度(SpO2)降低,在SBT期间,测SpO2或胃黏膜pH可作为撤机失败的预计指标。在SBT时,心肌缺血可以变得明显,可引起左心室顺应性减低、肺水肿和增加呼吸功。
通气驱动降低(中枢驱动受抑制)
如果完全没有中枢驱动,患者就没有任何自主呼吸活动,即使存在高碳酸血症和低氧血症也如此。这种情况见于脑炎、脑干出血或缺血、神经外科并发症。要确定中枢驱动的减低即更具有难度,可用二氧化碳反应试验来评估之,但在危重病患者,尚未见有研究来评价其临床应用价值。在小样本的研究中,已显示可用P0.1(0.1秒时的口腔闭合压)来评价中枢驱动对二氧化碳的反应性。
中枢驱动可由于代谢性碱中毒,机械通气本身或应用镇静剂/催眠药而受损害,在这3种可能的原因中,有文献报道的是过度的镇静,延长了撤机和住ICU时间。
神经肌肉功能下降
要想撤机成功,需要有足够的神经肌肉能力来克服呼吸系统的阻力负荷和弹性负荷,以适应代谢的需要和维持CO2的平衡。这需要在中枢神经系统产生适当的信息,并完整地传输给脊髓呼吸运动神经、呼吸肌和神经肌肉接合,这种传输通路的任何一部分中断,都可引起撤机失败。
吸气肌疲劳是撤机失败的常见原因,引起吸气肌疲劳的原因很多:①基础肺疾病没有完全控制,呼吸肌疲劳没有完全恢复或呼吸功增加;②心排出量降低;③低氧血症;④机械通气时呼吸机与自主呼吸不协调,呼吸肌功能储备下降或撤机过程中发生呼吸肌的亚临床疲劳。
治疗:①治疗基础肺疾病以减少呼吸功耗和防止低氧血症;②纠正血流动力学异常(如心排出量降低等);③应用适当的撤机技术(如PSV),改善呼吸机与自主呼吸的协调性;④给予茶碱类药物,改善膈肌收缩力。
导致神经肌肉功能低下的原因中,危重病神经肌肉异常(criticalilnessneuromuscular abnormalities,CINMA)和呼吸机所致膈肌功能障碍(ventilator-induceddiaphragmaticdys-function,VIDD)问题尤其值得关注。CINMA是在ICU中很常见的周围神经肌肉疾病,常累及肌肉和神经。文献报道的CINMA发生率为50%~100%,其发生与疾病的严重性、多器官功能不全、应用皮质激素、高血糖,以及住ICU时间延长有关。应用“医学研究咨询评分”(he Medical Research Couneil Score)可在床旁对CIMA做出诊断,当评分<48时,与临床上显著的肌无力相关。有适当指征时,可用电生理试验和肌肉活检来证实。
VIDD:机械通气引起膈肌的功能障碍,导致膈肌肌力降低,膈肌萎缩,膈肌损伤,统称之为“VIDD”。动物实验研究证明:控制通气(CMV)导致横隔肌力的降低,引起跨膈压降低,在控制通气后不久即发生。并随着机械通气时间的延长而加重,在数日内产生跨膈压的能力下降至40%~50%。而且横膈的耐力也明显受损。
VIDD的治疗:积极的呼吸肌锻炼,增强呼吸肌的强度和耐力是防治VIDD的最有效方法。补充抗氧化剂可减轻氧化应激反应,因此可减轻VIDD。一些增强呼吸肌的药物,如氨茶碱、洋地黄类、β受体激动剂等是否对防治VIDD有确切疗效,尚缺乏研究。
心理学上的功能障碍
1)谵妄:谵妄或急性脑功能障碍,是识别和觉醒水平的紊乱,与许多可治疗的危险因素相关,包括应用精神作用药物、未治疗的疼痛、长期制动、低氧血症、贫血、脓毒症和睡眠剥夺。自2001年以来,已有在危重患者中发生谵妄的重要文章发表,文献中报道谵妄的发生为22%~80%,它与住ICU时间延长有关,在出ICU的6个月内,是高病死率的预计指标。目前发明的谵安筛选工具,已证明是有效的,但还没有建立一致的治疗意见,也没有证实谵妄与撤机困难直接相关,研究正在进行中。
2)焦虑和抑郁:在住ICU期间或在撤机过程中,许多患者发生焦虑,这些焦虑不安的,痛苦记忆可保持数年之久,文献报道ICU内焦虑的发生率为30%~75%。患者主诉引起焦虑的重要原因是呼吸困难,不能有效地进行语言交流,以及睡眠剥夺。
对患者睡眠进行的研究显示,患者不能休息或人睡,25%患者报告夜间失眠。而且,多导睡眠描记显示,ICU患者常发生觉醒和睡眠片断。睡眠紊乱可能与通气模式相关。最近也有证据显示,在ICU环境的噪声并不是如以前想象的那样是导致睡眠紊乱的明显原因。抑郁可作为单独的疾病发生或与ICU谵妄相关。
文献报道已有一些治疗策略可威轻机械通气期间的焦虑,这些策略包括,以增加吸气时间和PEEP或用双水平PSV通气来改善患者的语言交流;以减少噪声、光和夜间的护理干扰或应用松弛技术,如生物反馈法以改善睡眠,或生物反馈法与VT技术联合应用来减轻焦虑和减少撤机时间。
代谢和内分泌
1)代谢紊乱:低磷血症、低镁血症和低钾血症均可引起肌无力。甲状腺功能低下和肾上腺功能减退也会导致撤机困难。然而,特别评价这些代谢异常中的每种异常对机械通气撤机失败的相对作用的资料是缺乏的。
2)肾上腺皮质激素的作用:在撤机失败中,肾上腺皮质激素的相对缺乏或补充的重要性需要进-步分析。在当今的临床实践中,医生认为患者存在皮质激素的相对或绝对不足,而进行皮质激素的生理性替代治疗是常见的。来自对皮质激素研究的资料能有助于进一步确定皮质激素对危重病患者的作用。有一关于ARDS存活者的后果研究,补充肾上腺皮质激素的缺乏是和较好的功能后果相关的。药物剂量的作用需要进一步说明,应用比生理替代治疗推荐剂量更大的剂量是与严重肌病相关的。在住ICU期间,接触任何外源性皮质激素均可引起肌无力和可能对延长机械通气时间起作用。
皮质激素治疗损害血糖的控制。在外科手术患者人群,建立密切的血糖控制方案,可明显减少机械通气的时间,这已有文献报道。这种治疗是否应用于更广泛的内科危重病患者有待于分析。
营养问题及其他
1)体重过高:肥胖(过重的定义是体质指数>25)的机械性作用是减低呼吸顺应性,增高闭合容积/功能残气量比值以及呼吸功(WOB)的增加,可能会影响机械通气的时间。在ARDS小潮气量机械通气(6ml/kgVT对12ml/kgVT)网上研究的第2次资料分析中,过高体重和肥胖患者与正常体重者(18.5~24.9)比较,机械通气时间是类似的。另有研究调查肥胖对住ICU时间的影响是增加的,但机械通气的时间并没有增加。
2)营养不良:虽然已有文献报道,有高达40%的危重患者发生营养不良,但有关它与撤机困难之间的关系研究资料是有限的。例如在ARDS的网上研究中,4.7%的患者被确定低体重,低体重的定义是体质指数<20,这些患者常有通气驱动的抑制、肌肉质量的减低和撤机困难。
3)贫血:当考虑患者是否适合撤机时,理想的血红蛋白水平仍存在争议。原来的撤机指南规定血红蛋白目标值≥80g/L。在一大样本的前瞻性随机研究中,Hebert等报道,较积极地输注红细胞,维持血红蛋白浓度达100~120g/L,并没有减少危重病患者的机械通气时间。另有一组病例数较少的COPD患者研究,输血导致每分通气量和呼吸功(WOB)的明显减低,今后需要随机对照的研究以帮助确定不同患者人群所需要的血红蛋白目标值。在有选择的病例,应用红细胞生成素的作用需要进一步研究。
