妊娠后,血浆中类固醇激素水平远比非妊娠期高,并有大量类固醇类激素自尿中排出,但不只是由胎盘分泌的。胎儿或胎盘均缺乏单独合成类固醇类激素所必需的若干酶系,两者结合(即胎儿-胎盘单位)共同提供合成激素所需的酶,完成孕期所需激素的合成。所有胎盘类固醇类激素都是由母体或胎儿血中类固醇前身物质在胎盘中合成的,胎盘合体滋养层细胞合成类固醇类激素的能力比机体任何其他组织都强。
妊娠期产生大量雌三醇
在孕6周以前,雌酮及雌二醇(E2)由卵巢分泌;7周后,胎盘组织参与其合成和分泌,主要是利用母体内的脱氢异雄酮,经Δ4,Δ5异构酶及3β-脱氢酶作用生成雄烯二酮及睾酮,再转化成雌酮与E2。这样可保护胎儿不受雄激素的影响。进入母体后大部分与性激素结合球蛋白(SHBG)结合,小部分进入胎血循环,经16α-羟化酶作用生成E2,孕期雌激素分泌随妊娠月份持续增长,孕末期尿中雌酮和E2排泄量相当于月经周期黄体期的100倍,双胎和多胎妊娠时升高更明显。
胎儿-胎盘单位产生的雌三醇(E3)有80%来自胎儿肾上腺分泌的硫酸脱氢异雄酮(DHEAS),4%来自胎儿的E2,仅10%来自母体的DHEAS,DHEAS大部分在胎儿肝脏内经16α-羟化酶作用合成16α-硫酸脱氢异雄酮,再在胎盘内去硫酸及芳香化转化为E3。胎盘合成的E3大部分进入母血循环,在肝脏,与硫酸和醛糖酸结合成硫酸E3和醛糖酸E3,并以这两种结合形式从母体尿中排出。
妊娠期产生的雌激素主要是E3,孕妇尿中90%的雌激素是E3,非结合型E3从孕9~12周开始增加,显示此时胎儿肾上腺皮质分泌启动。孕16周尿E3水平大约为7μmol/24h,24周达35μmol/24h,35周后迅速增加,至37~39周达峰值,为123.5~175.5μmol/24h,相当于非孕期的1000倍,40周后逐渐下降(下图)。E3分泌有昼夜差别。孕期循环中E3的量很大,认为其在孕期具有重要作用,可能有抗E2的作用,与E2竞争胞膜受体,降低子宫对缩宫素的敏感性,抑制子宫自发收缩,与雌酮和E2协同维持子宫相对静止,参加脐血调节,降低脐带的血管张力,促进胎儿宫内发育。
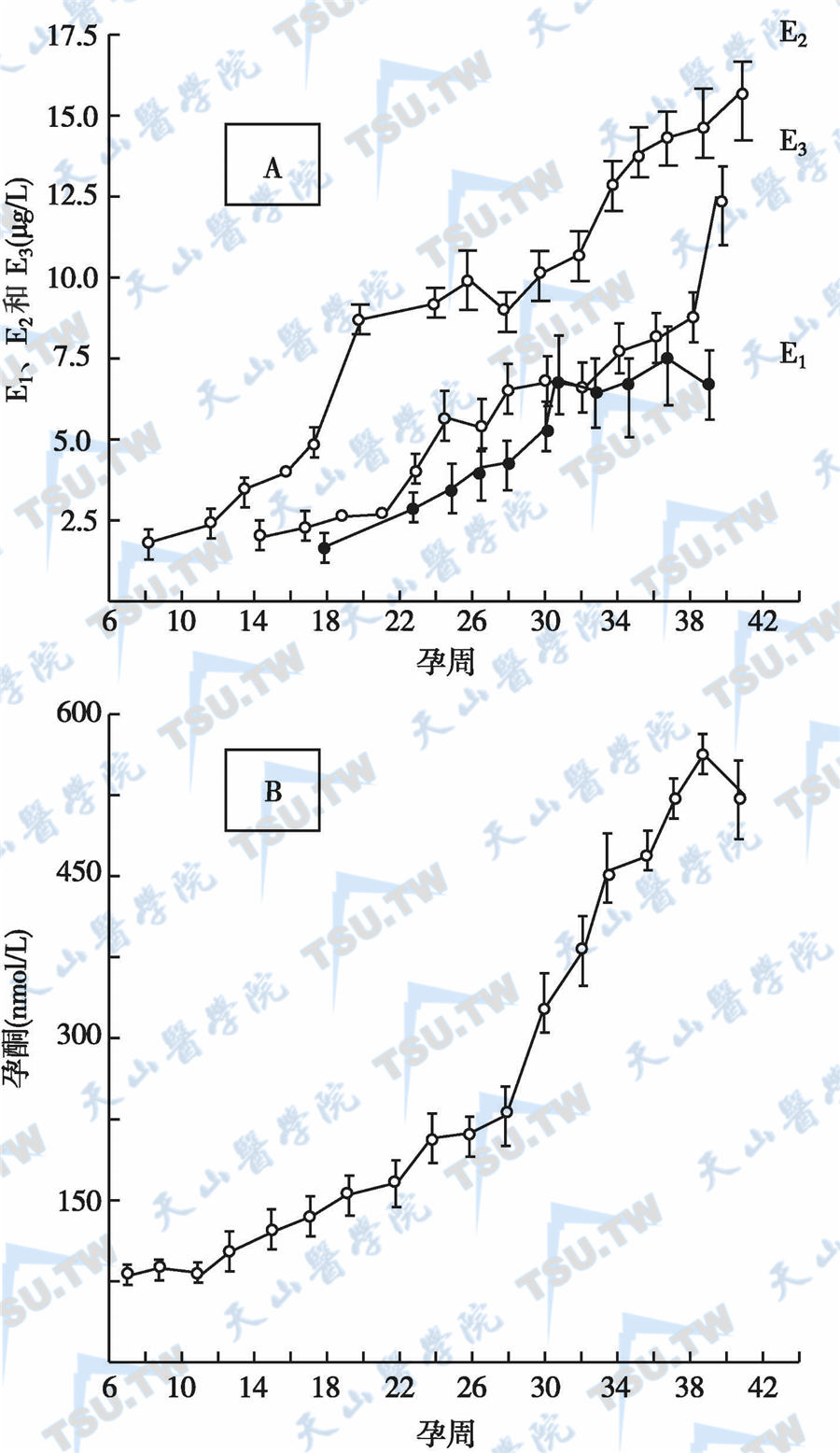
妊娠期血浆雌激素与孕酮的变化
测定母体血液及尿中E3的含量,可以反映胎儿健康状况及胎盘的功能状态。E3生成正常,提示胎儿循环、代谢以及胎盘功能正常。每日测定1次E3,若发现E3明显下降(超过50%),提示胎儿处于危险状态(如死胎、胎儿宫内发育迟缓或过期妊娠)。这项指标比胎儿心率的变化更为敏感。但在某些情况下,雌激素降低并不提示胎儿的危险性,而与胎儿先天性异常及药物的影响有关。如:胎盘硫酸酶缺陷或无脑胎儿,母体血清E3常维持低水平,其中,在无脑儿是由于缺乏ACTH,胎儿肾上腺皮质不能生成DHEAS,使E3的产生不足。若给予母亲糖皮质激素,则可抑制ACTH的分泌,同样使母体E3降低,此外,应用某些抗生素,由于阻碍E3的肠肝循环,可使母体E3降低。糖尿病胎儿肾上腺发育不全者的E3降低。
孕激素分泌随妊娠增高
孕5周前由妊娠黄体生成,以后胎盘滋养层合体细胞合成功能增强,孕9~10周其合成及分泌完全由胎盘代替,胎盘利用母体胆固醇合成孕烯醇酮,再转变为孕酮,90%进入母体,10%进入胎儿血循环供合成其他类固醇类激素使用。孕激素分泌随妊娠月份持续增长,孕23~24周达早孕的5倍,35~36周达峰值,为早孕期10倍并持续至足月。
