对恶液质的认识已进入一个全新的时代。很多慢性消耗性疾病发病初期可能就会伴随恶液质的病理生理改变,恶液质并不是指传统思想里的骨瘦如柴、病入膏肓,及时发现、愈早干预,治疗效果愈好。
对于恶液质名词的出现最早可追溯到古希腊时代,近当代医学逐步出现大量基于现代科学理念的研究。然而,直到2008年美国Evans教授带领的恶液质协作组推出的恶液质共识后,对恶液质领域的研究才真正在国际上被重视起来,并标准化。Evans教授领衔推出的指南是广义上的恶液质指南,是目前国际上较公认的。此后,多个地区、国家纷纷推出相应指南。在基本特点共识的基础上,不同的版本之间存在一些争议。此外,恶液质研究领域总体上仍存在很多未解的问题,包括发病机制、诊断的细化及分期节点等,干预措施亦不令人满意。
恶液质常伴发于慢性疾病,包括:肿瘤、慢性阻塞性肺病、慢性心衰、慢性肾衰、肝功能不全、艾滋病、风湿性关节炎等,共同特点是慢性炎症反应,其中每种疾病又有其特殊之处,尤其是肿瘤,当细胞发生不可遏制的自我复制时,细胞一方面分泌一些物质发挥特殊作用满足其不断增殖,另一方面激发机体产生一系列变化,这些现象基本都是在为肿瘤自身的无限增殖提供帮助。2011年,英国的Fearon教授带领的恶液质专家团队,推出肿瘤恶液质国际共识,该共识是目前国际上比较公认的肿瘤恶液质专家共识。以下四节详述几部重要的恶液质指南的制定及内容。
参与到此部肿瘤恶液质共识的专家是:从事肿瘤恶液质研究的内科肿瘤学家、外科肿瘤学家、姑息医学专家及营养学家,包括英国爱丁堡大学Fearon教授,以及来自瑞士、意大利、瑞典、美国、加拿大、葡萄牙、挪威的专家。参与的组织有:欧洲姑息治疗研究协作组、恶液质及消耗性疾病协会、英国国立癌症研究学会姑息治疗临床研究小组、欧洲临床营养与代谢学会特别兴趣小组。该共识于2011年正式发表,其主要内容包括:共识方法学、肿瘤恶液质定义、诊断标准、分期及评价。虽然在此之前,Evans带领的恶液质协作组提出了恶液质定义,但是该定义适用于所有慢性疾病并发的恶液质,不是针对肿瘤恶液质专属的。此外,2006年Fearon 教授带领的肿瘤恶液质研究组对恶液质的诊断指标曾提出过标准,2009年意大利肿瘤患者筛查工作组(SCRINIO)对恶液质的定义及分期也提出了标准,但均为单中心,未经过正式的共识形成过程。而2011年Fearon教授等提出的共识是在形成共识的标准程序基础上,制定了肿瘤恶液质定义、诊断标准及分期标准。
共识形成程序
该共识采用了标准的德菲法(Delphi)共识形成程序。先根据文献证据,提出观点,继之组织专家组(专家的选择是根据文献发表水平、恶液质临床研究参与程度及同行评议专家组来源)进行两轮匿名投票,决定共识内容。
肿瘤恶液质的定义
该共识的肿瘤恶液质定义是:以持续性骨骼肌丢失(伴有或不伴有脂肪组织丢失)为特征,不能被常规营养支持完全缓解,逐步导致功能损害的多因素综合征。病理生理学特征表现为低摄入量及代谢异常导致的蛋白及能量负平衡。
该定义指出了恶液质的三个最重要的特点:骨骼肌持续丢失、常规营养支持不能完全缓解、功能损害。其中骨骼肌丢失是恶液质的核心表现,蛋白(特别是肌肉蛋白)过度分解是其重要的病理生理改变。
肿瘤恶液质的分期
当患者出现恶性肿瘤广泛转移、持续分解代谢状态、肌肉丢失严重、低PS评分、对抗肿瘤治疗无反应时,通过综合治疗不大可能达到增加瘦体组织、改善体力状态等目的。而在恶液质刚开始发生时,给予积极的干预,就非常有机会迟滞恶液质的发生发展。因此,早期诊断恶液质便是一个非常迫切的需求。同时,缺乏诊断标准和分期标准也阻碍恶液质相关临床试验及临床实践的进行。
根据恶液质的发病特点,该共识首次将肿瘤恶液质分为三期恶液质:恶液质前期、恶液质期、恶液质难治期(图13-1-1),但值得注意的是并非所有的肿瘤患者都经历这三个阶段。
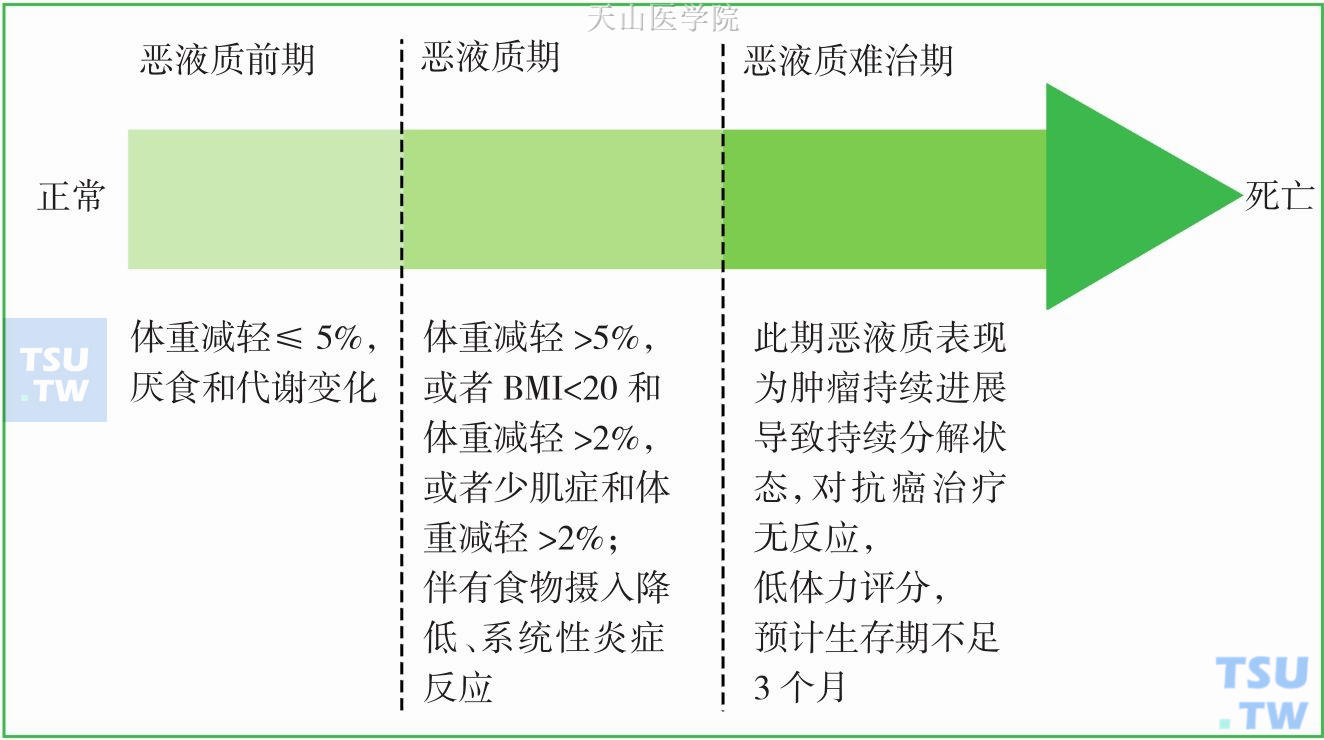
图13-1-1 恶液质分期
恶液质前期表现为早期的临床及代谢特征,如厌食、糖耐量受损发生早于体重丢失(体重丢失≤5%),进展风险取决于肿瘤类型和分期、系统性炎症的存在、低摄入量、对抗癌治疗的无反应。
恶液质期的诊断标准为:6个月内体重丢失大于5%(排除单纯饥饿),或者BMI小于20,同时体重丢失大于2%,或者四肢骨骼肌指数符合(男性<7.26kg/m2,女性 <5.45kg/m2),同时体重丢失大于2%。
恶液质难治期表现为肿瘤持续进展,对治疗无反应,活跃的分解代谢,体重持续丢失无法纠正。WHO体力评分3或4分,生存期预计不足3个月,营养支持措施的风险可能大于收益。
Vigano等对207例进展期非小细胞肺癌及胃肠道肿瘤患者的研究发现,共识的恶液质分期与患者症状、生活质量、化疗耐受性、体成分、住院时间、生存均相关。而Josep等认为目前的诊断标准及共识仍不能满足临床诊断、试验及治疗的需求,因此研究推出总分为100分的肿瘤恶液质评分系统,主要组成部分为:体重丢失(0~32)、瘦体组织丢失(0~8)、炎症/代谢紊乱/免疫抑制(0~20)、体力(0~15)、厌食(0~15)、生活质量(0~10)。各项得分相加得到总分,根据总分判断恶液质的进展情况,其中0~25分为轻度,25~50为中度,50~75为重度,75~100为终末期。
确定分期的重要性在于恶液质前期有利于更早的预防干预,较少程度的体重丢失是重要的线索,其他重要的生物学指标暂无相关研究。
分期是针对恶液质进展情况的划分,并不能代表恶液质的严重性。严重程度的分级相关研究有利于预测治疗毒性、生活质量、住院时间和生存期等结果。恶液质的严重性取决于体重丢失速度、能量储存及体蛋白量消耗程度(低的初始储备也相关)。例如:同样丢失5kg/m2,BMI为22的较BMI 为35的要严重。另外,同样的BMI和丢失程度,相比于肌肉蛋白群正常的患者,伴有肌肉丢失出现的患者风险要大。
肿瘤恶液质的评估
诊断恶液质后要评估如下四个方面:厌食或摄入量降低、分解代谢因素、肌肉量和力量、恶液质对患者影响,只有评估这些表型后,才能进行相应的针对性治疗。
摄入量降低要评估:摄食中枢、感觉异常、上消化道动力下降、下消化道运动障碍。另外还要评估是否存在口腔炎、肠梗阻、呼吸困难、疼痛、不良饮食习惯等。同时还要常规评价膳食摄入量,尤其是蛋白摄入量。
分解代谢驱动:分解代谢亢进是恶液质发生的一个重要但可变化的因素,促进分解代谢的原因可能来源于肿瘤代谢,系统性炎症,以及一些肿瘤介导的效应。其中,C反应蛋白(C-reaction protein,CRP)是系统性炎症公认的指标,而其他因素(如胰岛素抵抗,长期大剂量糖皮质激素应用,性腺功能低下,基础代谢升高),因为证据资料匮乏未达成共识。
肌肉量和力量:方法学未达成明确共识。肌肉量评价的方法推荐:CT、MRI、双能量X线成像、人体学测量(上臂肌面积)、生物电阻抗分析。力量测量推荐上肢握力。
功能和社会心理学影响:推荐常规评估生理功能及社会心理学影响。方法可以采用EORTC QLQ-C30或者ECOG问卷。
推荐从恶液质诊断到治疗决策按照管理流程进行(图13-1-2)。
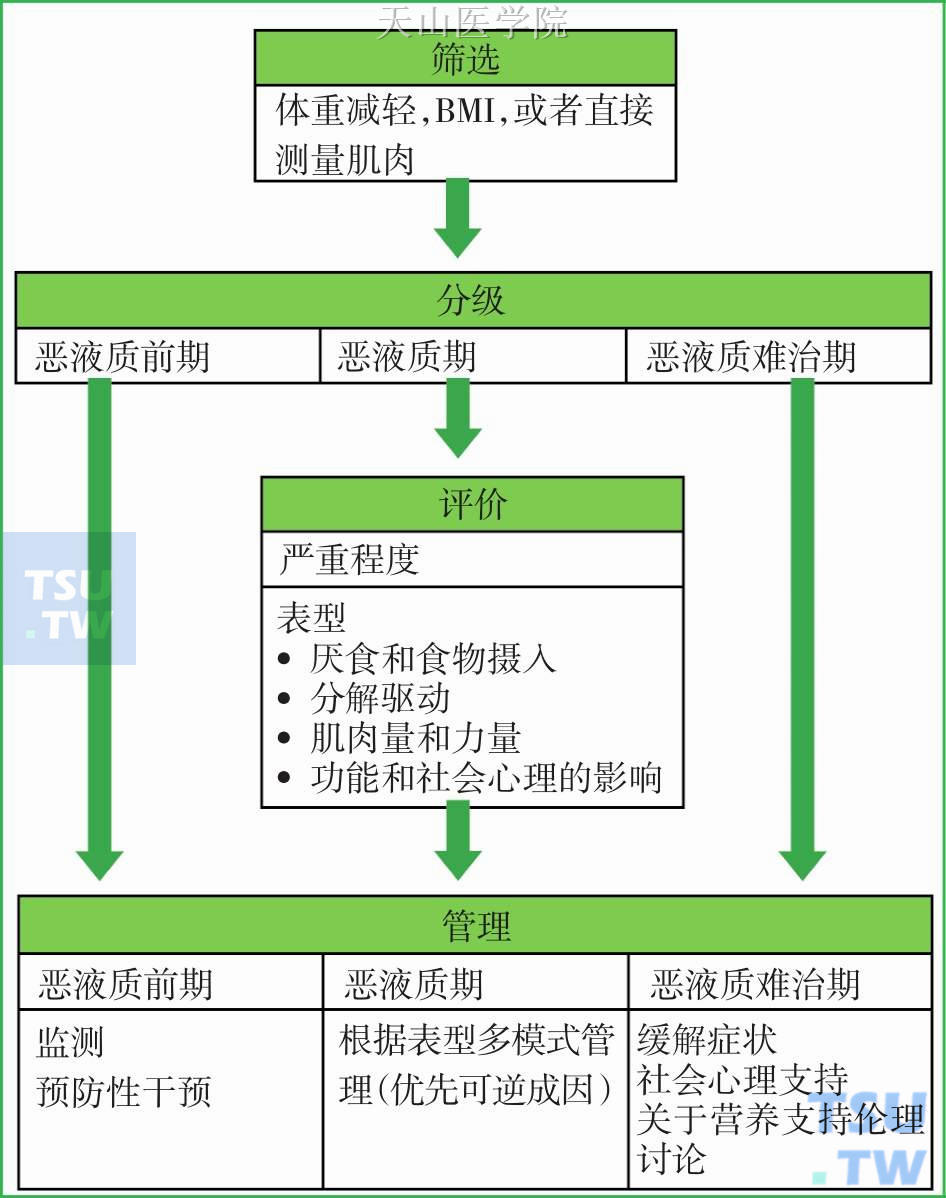
图13-1-2 恶液质管理流程进行
小结
这部共识主要强调低摄入量与代谢异常的相互作用,并明确指出骨骼肌丢失是患者功能受损的核心因素。肌肉丢失是恶液质的核心标志,也是治疗的靶点,因此定义更加强调肌肉的丢失,伴有或不伴有脂肪丢失。体重丢失比例尚无系统的临床研究证实,因此目前的标准有待进一步的研究提供更多循证医学证据。另外共识中指出,目前版本达不到临床指南的要求,其仅提出了恶液质的定义和分期,对分期的节点也不完全确定,有待更多的循证医学证据加以完善。
该共识的优点在于,是第一部遵循标准共识形成流程、集合国际上知名相关专家制定的肿瘤相关恶液质共识。不足在于体重丢失没有临床研究证据,且其他辅助诊断条件,如炎症指标等均无具体标准。虽然早在2006年Fearon教授带领的肿瘤恶液质研究组对恶液质的诊断指标研究表明:体重丢失大于10%,摄入量低于1500kcal/d,系统性炎症指标CRP 大于10mg/L三项同时存在时与患者的功能状况及预后相关,然而此共识中未采用这一标准。这部共识为肿瘤恶液质的研究打下了良好的基础。未来关于恶液质诊断及治疗的相关研究,均容易在同一诊断及分期标准下进行。
自2008年Evans等推出第一部恶液质共识,到2011年Fearon等推出的肿瘤恶液质共识,历时3年,期间一些地区和国家也根据这些共识推出相应地区和国家的共识。诊断的核心内容没有发生实质的变化,均强调肌肉的丢失是恶液质最显著的特征,其病理生理改变为过度蛋白分解,可能的机制为系统性炎症反应,涉及的调节部位主要为下丘脑。目前针对恶液质的治疗,尚无明确有效的方法,尤其是疾病持续进展的患者。那么早期发现恶液质,在体重轻度丢失,甚至体重未丢失,而如果通过体成分检测发现肌肉丢失的患者,予以早期营养咨询,或者积极的营养支持措施,可有效延迟或缓解恶液质的进展,对患者的预后产生积极的影响,改善预后。
(邓颖冰 丛明华)
