支持治疗/禁碘/戒烟是药物治疗的基础措施
应予适当休息。注意补充足够热量和营养,包括糖、蛋白质和B族维生素等。精神紧张、不安或失眠较重者可给予苯二氮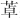 类镇静剂。抗氧化剂、营养支持和心理支持治疗对甲亢患者的恢复有益。在高代谢状态尚未改善以前,患者可采用高蛋白、高热量饮食。除糖类外,可使用牛奶、豆浆、瘦肉、鸡蛋、鱼、肝等食物,在两餐基本饮食之间可加牛奶、豆浆、甜食品。患者出汗多,丢失水分多,应保证足够的饮料,平时不宜喝浓茶、咖啡等刺激性饮料,禁食含碘食盐与食物和戒烟对Graves病,尤其是TAO的防治有积极意义。
类镇静剂。抗氧化剂、营养支持和心理支持治疗对甲亢患者的恢复有益。在高代谢状态尚未改善以前,患者可采用高蛋白、高热量饮食。除糖类外,可使用牛奶、豆浆、瘦肉、鸡蛋、鱼、肝等食物,在两餐基本饮食之间可加牛奶、豆浆、甜食品。患者出汗多,丢失水分多,应保证足够的饮料,平时不宜喝浓茶、咖啡等刺激性饮料,禁食含碘食盐与食物和戒烟对Graves病,尤其是TAO的防治有积极意义。
抗甲状腺药物控制甲亢
药物疗法应用最广,但仅能获得40%~60%治愈率;其优点是:①疗效较肯定;②不会导致永久性甲减;③方便、经济、使用较安全。其缺点是:①疗程长,一般需1~2年,有时长达数年;②停药后复发率较高,并存在原发性或继发性失败可能;③可伴发肝损害或粒细胞减少症等。
常用药物
常用的抗甲状腺药物分为硫脲类和咪唑类两类。硫脲类有甲硫氧嘧啶(methylthiouracil,MTU)及丙硫氧嘧啶(propylthiouracil,PTU),半衰期1.5小时;咪唑类有甲巯咪唑(thiamazole,MM,他巴唑)和卡比马唑(carbimazole,CMZ,甲亢平),半衰期6小时,所以轻~中度的Graves病患者每天服药1次即可。两类抗甲状腺药物的结构见图3-13-16。
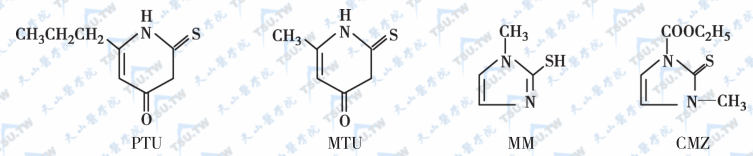
抗甲状腺药物的结构与名称;注:PTU:丙硫氧嘧啶;MTU:甲硫氧嘧啶;MM:甲巯咪唑;CMZ:卡比马唑
硫脲类和咪唑类抗甲状腺药物的作用机制基本相同,都可抑制TH合成,如抑制甲状腺过氧化物酶活性,抑制碘化物形成活性碘,影响酪氨酸残基碘化,抑制单碘酪氨酸碘化为二碘酪氨酸及碘化酪氨酸耦联形成各种碘甲腺原氨酸。近年发现,此组药物可轻度抑制免疫球蛋白生成,使甲状腺中淋巴细胞减少,血TSAb下降。但两类药物亦有一些差别(下表),其中PTU还在外周组织抑制5’-脱碘酶而阻抑T4转换成T3,故首选用于严重病例、甲亢危象、妊娠与哺乳妇女或对MM过敏者;而MM已经成为甲亢的一线用药,尤其适用于儿童Graves病、肝病患者和对PTU过敏者。此外,未经治疗的Graves病患者血清脂质过氧化活性增强,血浆巯基(thiol groups)和巯基裂解物水平下降,细胞内抗氧化酶活性增加,而细胞外的自由基清除系统活性不足。MM有助于逆转这些异常。
甲巯咪唑和丙硫氧嘧啶的比较
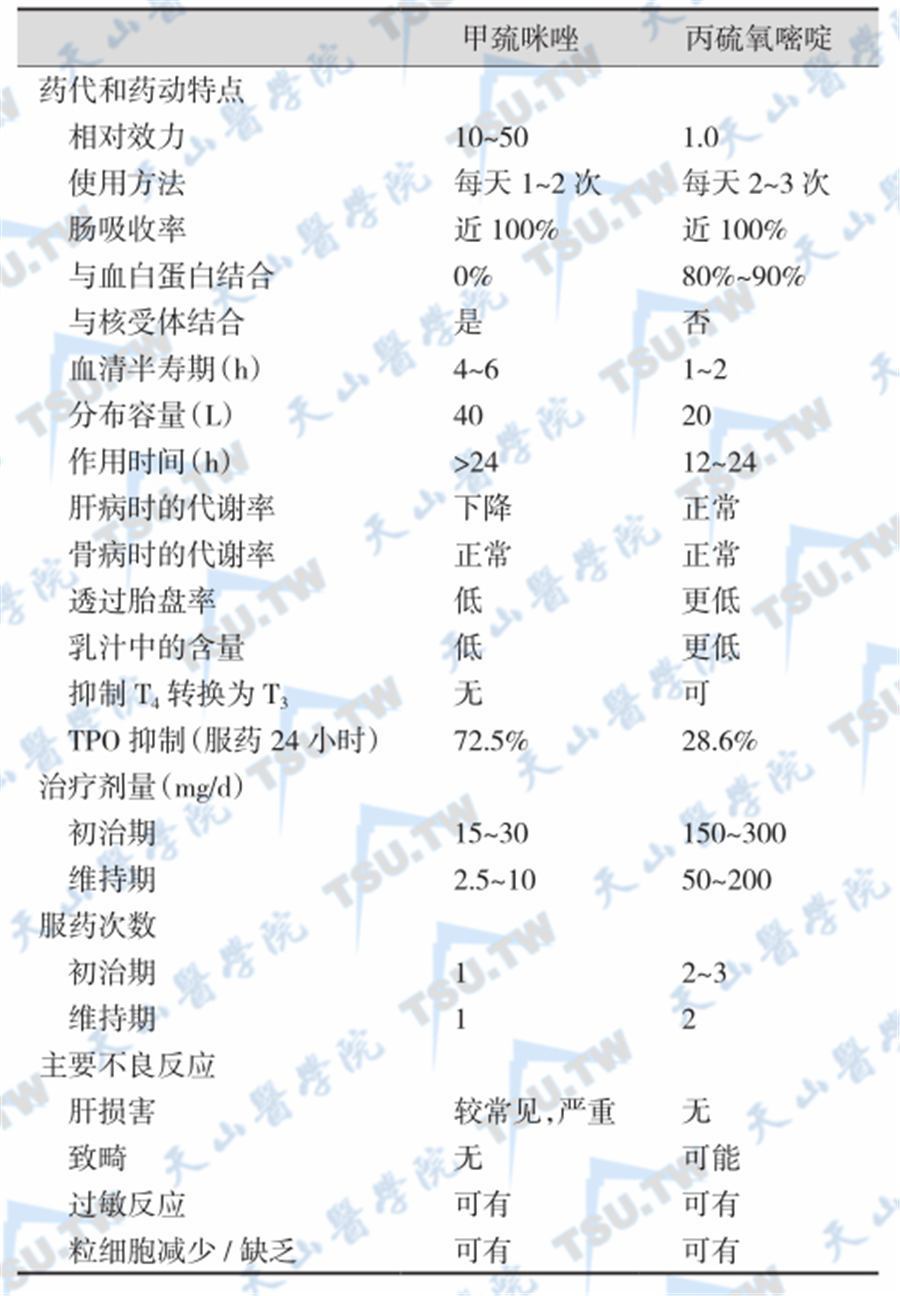
短期用MM治疗可使部分Graves病的病情得到长期缓解,而另一些患者即使长期使用药物治疗也很难达到这一目的。如果患者的血清IgE正常,易于用MM控制症状。Th淋巴细胞被激活后,合成过多IL-13,后者兴奋B细胞合成TSHR抗体和IgE,因而在用MM治疗时,如TSH封闭性Ig下降不明显,其缓解率低。
剂量与疗程
长程治疗分初治期、减量期及维持期。
- 初治期:MTU或PTU 300~450mg/d,或MM,或CMZ 30~40mg/d,分2~3次口服(初治期和应用大剂量时不主张使用每天单次疗法)。至症状缓解或血TH恢复正常时即可减量。
- 减量期:约每2~4周减量1次,MTU或PTU每次减50~100mg,MM或CMZ每次减5~10mg,待症状完全消除,体征明显好转后再减至最小维持量。
- 维持期:MTU或PTU 50~100mg/d,MM或CMZ 5~10mg/d(如必要可使用每天单次疗法),如此维持1.5~2年。必要时还可在停药前将维持量减半。
疗程中除非有较严重反应,一般不宜中断,并定期随访疗效。治疗中如症状缓解而甲状腺肿或突眼反而恶化时,抗甲状腺药物可酌情减量,有人建议加用L-T4 25~50μg/d或甲状腺粉20~60mg/d,但效果不明。长程(>1年半)治疗对轻、中度患者的治愈率约为60%;短程(<6个月)治疗的治愈率约为40%,但在停药后3个月~1年内易复发。
在Graves病的药物治疗过程中,一般可观察到血TSH的以下4种变化:
- 血TSH逐渐升至正常:约占治疗Graves病患者的50%;血TSH恢复至正常的时间不定,一般为3~6个月;血TSH迅速恢复正常说明药物治愈的可能性大。
- 血TSH持续降低:部分患者的T3和T4在药物治疗后数个月内达到正常,但血TSH长期≤0.1mU/L,这种情况提示药物治疗的疗效不满意,停药后复发的可能性大。
- 血TSH波动过大:有些Graves病患者的血TSH波动在0.1~10mU/L范围内,而临床不伴有甲亢或甲减表现,提示患者对抗甲状腺药物敏感,用药物治愈的可能性大,但需及时调整药物剂量;必要时可加用TH制剂(尤其是儿童患者)。
- 血TSH正常伴TgAb和(或)467TPOAb抗体明显升高:这种情况往往提示并发自身免疫性甲减的可能性大,不主张采用131I或手术治疗。
不良反应
抗甲状腺药物治疗的常见不良反应是粒细胞减少和药物性甲减,PTU容易发生肝脏或心肌损害;而粒细胞缺乏症与ANCA相关性小血管炎为抗甲状腺药物治疗的严重并发症,且预后较差。
(1)粒细胞减少和粒细胞缺乏症
一般为粒细胞减少(MTU多见,MM次之,PTU最少),严重时可致粒细胞缺乏症。前者多发生于用药后2~3个月内,也可见于任何时期。如外周血白细胞低于3×109/L或中性粒细胞低于1.5×109/L,应考虑停药,并应严密观察。Graves病用MM治疗后可出现贫血,血清中存在MM依赖性抗红细胞抗体,这些抗体可与Rh复合物蛋白结合,但与其他血细胞不结合,有些患者可合并粒细胞减少和血小板减少。有时也出现抗中性粒细胞特异性Fcr受体Ⅲb抗体和内皮细胞-血小板黏附分子-1(plateletendothelial cell adhesion molecule-1,PECAM-1,CD31),而导致中性粒细胞和血小板减少。MM还可引起皮疹、嗜酸性粒细胞增多、血管神经性水肿等。
粒细胞减少的处理原则和方法是:
- 试用一般性升白细胞药物,如维生素B4、鲨肝醇、利血生、脱氧核糖核酸、碳酸锂等。必要时,每日皮下注射重组的人粒细胞集落刺激因子(rhG-CSF)2~5mg/kg或重组的人粒细胞-巨噬细胞集落刺激因子(rhGM-CSF)3~10μg/kg。白细胞正常后停用;
- 必要时给予泼尼松30mg/d口服;
- 粒细胞减少合并药疹较常见,可用抗组胺药物控制,不必停药,但应严密观察,如皮疹加重,应立即停药,以免发生剥脱性皮炎;
- 粒细胞减少合并中毒性肝炎应立即停药抢救,其治疗方法有糖皮质激素、小剂量TH(甲亢已控制时)、溴隐亭和其他抗组胺药物、红细胞生成素、新鲜全血(少量多次)、骨髓移植。
(2)ANCA相关性小血管炎
多见于中青年女性,为PTU的较特异性不良反应。抗中性粒细胞胞浆抗体(antineutrophil cytoplasmic antibody,ANCA)相关小血管炎包括Wegener肉芽肿、显微镜下多血管炎和变应性肉芽肿性血管炎。ANCA以正常人中性粒细胞为底物检测到的自身抗体分为c-ANCA(胞浆型)和p-ANCA(核周型)两种。该抗体对血管炎的诊断极有帮助,尤其是c-ANCA对于Wegener肉芽肿(Wegener granulomatosis)具有较高特异性(98%),而p-ANCA对疾病诊断的特异性相对较差。这些药物偶可诱导产生ANCA血管炎。血清学检查结果与红斑狼疮改变一致,PTU与髓过氧化物酶发生反应形成反应中间产物,而反应中间产物促进自身免疫炎症反应。一般表现为间质性肺炎、肺出血、干咳和呼吸困难;肾血管炎表现为镜下血尿或肉眼血尿、蛋白尿、肾小球炎和肾功能减退(肺-肾血管综合征);少数侵犯多个脏器(肝、脾等),伴有发热、关节肌肉疼痛、皮疹、紫癜,多数于停用后恢复,个别危及生命。临床上呈全身多系统受累表现时应高度怀疑ANCA相关小血管炎可能,根据临床表现(至少存在三个以上的器官损害,如肾脏、肝脏、五官等),结合PR3-ANCA或MPO-ANCA阳性以及组织病理改变多能作出诊断。
少数重症患者需用大剂量糖皮质激素和免疫抑制剂治疗。有条件者在PTU治疗前测定ANCA抗体,并在治疗过程中监测尿常规及ANCA抗体有助于预防ANCA相关性小血管炎的发生和恶化。
(3)药物性甲减
多见于抗甲状腺药物用量过大或疗程过长者,但个体对抗甲状腺药物的敏感性差异很大。药物性甲减的最早表现是治疗过程中的甲状腺肿大与血TSH升高。处理的原则是减低抗甲状腺药物用量或暂时停用抗甲状腺药物(但不宜长期停用),在一般情况下,不补充TH(阻滞-替代治疗)。
(4)肝功能损害
抗甲状腺药物偶可引起胆汁郁积和肝细胞损害,以PTU多见,而MM一般对肝脏无损害。PTU相关性急性肝衰竭表现为痒疹、黄疸、白陶土样便、尿色加深、关节痛、腹痛腹胀、厌食、恶心或乏力等。30%患者有血清转氨酶升高,4%升高到3倍以上。美国FDA药物不良反应报告系统(AERS)指出,1969~2008年发生PTU相关性肝衰竭47例,其中成人33例,儿童14例。美国器官共享联合网络(UNOS)报告,从1990~2007年,23例患者因PTU相关的肝衰竭,接受了肝移植,其中成人16例,儿童7例。致急性肝衰竭的PTU总剂量为300mg,发生时间在服用PTU后的6~450天内,平均120天;儿童肝脏衰竭的发生机会大于成人,大约为1/1000。肝脏衰竭的预后(FDA-AERS报告):14例成人PTU相关性肝衰竭,9例死亡,5例接受肝移植,12例儿童PTU相关的肝衰竭,3例死亡,6例接受肝移植。
因而,凡对于Graves病合并肝脏疾病或已有肝功能异常者,建议选用MM治疗。轻度肝损害者停药后可恢复,重症可引起肝坏死。服用PTU期间要定期监测肝功能。如果血清转氨酶升高2~3倍,且经1周复查不见好转者需要停用PTU。
(5)QT间期延长
QT间期代表心肌从除极至复极的一段时间,QT间期明显延长容易诱发实行心动过速。抗甲状腺药物引起QT间期延长的情况少见,可引起QT间期延长的其他药物有口服降糖药、调脂药、生长抑素类似物和糖皮质激素等。一旦发生应及时处理。
停药指征
无论是否复发,抗甲状腺药物治疗1~2年后均需考虑停药(抗甲状腺药物治疗失败时必须停药),一般不主张患者接受抗甲状腺药物治疗的时间过长。完成抗甲状腺药物的长程治疗疗程,停药后Graves病不易复发的指征是:
- 血清TSAb转为阴性或抑制性抗体变为阳性(或滴度升高);
- 同时伴有自身免疫性甲状腺炎;
- 碘的摄入量正常或存在相对性碘缺乏;
- T3型Graves病;
- 甲状腺肿不明显或在治疗过程中逐渐缩小;
- 用小剂量的抗甲状腺药物能长期维持正常的甲状腺功能(血T3、T4和TSH正常);⑦TRH兴奋试验正常。
抗甲状腺药物治疗失败
抗甲状腺药物治疗失败可分为两种情况:①抗甲状腺药物治疗中失效:指在抗甲状腺药物治疗过程中所出现的抗甲状腺药物失效,甲亢病情加重,有的患者自治疗开始时仅部分有效或完全无效(原发性失效,少见);有的在治疗过程中逐渐无效(继发性失效,较多见)。原发性或继发性失效的原因很复杂,可能与家族遗传、碘过多、药物剂量不足、诊断错误(如甲状腺自主功能性结节、TSH瘤、自身免疫性甲亢等)有关。②停药后复发:复发系指甲亢完全缓解,停药半年后又有反复者。药物治疗的复发率较高,通过平均(46±33.1)个月的药物治疗观察,停药后1年、3年、5年及10年的复发率分别为42.9%、59.8%、67.9% 和78.9%。另有学者观察到,男性甲亢与女性甲亢的药物治疗缓解率分别为19.6%和40%,<40岁与>40岁的缓解率分别为32.6%和47.8%。为减少复发,要求除临床表现及T3、T4 和TSH正常外,TRH兴奋试验亦正常才停药则更为稳妥;血TSAb浓度明显下降或阴转提示复发的可能性较小。对药物严重过敏或经长期药物治疗仍疗效不佳者,应考虑改用其他方法治疗。
辅助药物与特殊方案治疗Graves病
β受体阻滞剂
β受体阻滞剂对减轻交感神经兴奋和由其引起的眼部症状有一定作用,但需较长期应用。除阻滞β受体外,还可抑制T4转换为T3,用于改善甲亢初治期的症状。如考虑使用β受体阻滞剂,宜首选普萘洛尔而非其他选择性β受体阻滞剂,因它们的作用较弱。一般给予普萘洛尔10~20mg,每日3~4次,其近期疗效显著。此药可与碘剂合用于术前准备,也可用于131I治疗前后、甲亢危象及甲亢周期性瘫痪时。支气管哮喘或喘息型支气管炎的患者禁用,此时可用选择性β受体阻滞剂,如阿替洛尔(atenolol)、美托洛尔(metoprolol)等。房室传导阻滞、严重心力衰竭和分娩者禁用β受体阻滞剂,必要时可加用钙通道阻滞剂,如地尔硫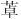 (diltiazem)。
(diltiazem)。
碘溶液
每滴卢戈(Lugol)液约含元素碘8μg,每滴饱和碘化钾液约含元素碘50μg。碘溶液仅用于术前准备和甲亢危象。其作用为减少甲状腺充血,阻抑TH释放,也抑制TH合成和外周T4向T3转换,但属暂时性,于给药后2~3周内症状渐减轻,继而又可使甲亢症状加重,并延长抗甲状腺药物控制甲亢症状所需的时间。
碳酸锂
为治疗躁狂症的药物,其抗甲亢的作用与锂离子分布在甲状腺中的浓度高,锂离子抑制TH释放有关。锂剂不作为抗甲亢的一线药物,当甲亢合并粒细胞减少、碘化物过敏或抗甲状腺药物不宜使用及严重甲亢或急需术前准备者,可应用碳酸锂,每日0.9~1.5g,分3次口服。锂盐口服吸收快而完全,抗甲亢所需药物浓度较高,易发生中毒。长期使用锂盐的其他不良反应有:
- 普通不良反应:主要有头晕、恶心、呕吐、腹痛、腹泻等,一般不影响继续用药。
- 锂盐相关性原发性甲旁亢(lithium-induced hyperparathyroidism):表现为无症状性高钙血症,但停用锂盐后,血钙不一定能恢复正常。
- 肾损害:夜尿增多,体重增加和水肿,长期使用锂盐可导致肾性尿崩症和慢性肾病。
- 甲状腺功能异常:以非毒性甲状腺肿常见,偶尔并发甲减。
- 锂盐中毒:早期表现为末梢白细胞数量增加和行为异常,严重时表现为意识模糊、震颤、反射亢进或癫痫等。
一旦出现锂盐中毒,应立即停药;同时补液,静推氨茶碱,促进锂的排泄。碳酸锂对伴有严重心肾病患者、电解质紊乱者、妇女妊娠前3个月及哺乳期者忌用。不宜同非甾体抗炎药物同时使用,老年患者应慎用。
阻滞-替代治疗
在应用抗甲状腺药物的同时加用TH制剂的治疗习惯(阻滞-替代治疗)已经持续多年。少数患者在使用抗甲状腺药物后,容易发生药物性甲减,加用TH制剂后可防止发生甲减,减少复诊频率。因此,该疗法用于儿童Graves病的治疗有一定理由。目前多用于儿童型Graves病的长程治疗,而不宜作为一般Graves病的常规治疗。阻滞-替代治疗对防治突眼的效果未定,且可干扰T3、T4和TSH测定,延长疗程。TH制剂的含碘量高(约占药物剂量的50%),对突眼和甲状腺免疫的作用亦未得到证实。
T3受体拮抗剂
理论上讲,应用T3受体拮抗剂(TR-antagonists)治疗Graves病可以达到治愈本病的目的。T3受体拮抗剂作为TH受体的一种配体,除了控制甲亢症状外,还可能对心肌病变有益,T3受体拮抗剂的设计主要是寻找受体类似物,干扰受体与配体的相互作用,既阻止了T3的作用,又消除受体的抗原性。
利妥昔单抗
利妥昔单抗(rituximab)是从淋巴细胞中提取的或经基因重组人工合成的)CD20单克隆抗体,该种单克隆抗体能嵌合到B淋巴细胞上,从而起到治疗作用。研究表明,利妥昔单抗能减少B淋巴细胞数目,阻止浆细胞发育,减少自身抗体的生成,降低细胞免疫反应。目前主要用于顽固性Graves病眼病的治疗,与此作用原理类似的肿瘤坏死因子α抑制剂(tumor necrosis factor-alpha inhibitors)亦可能有一定疗效,但目前仍缺乏足够的循证依据。
