支持细胞的成熟
支持细胞是胚胎性腺中第一个开始分化的体细胞,他的分化带动了精索的形成,并防止此时生精细胞进入减数分裂以及间质细胞的分化和功能。间质细胞分泌睾酮和胰岛素样因子3(insulin-like factor 3,INSL3),对男性性征的分化以及对睾丸下降至阴囊事件起重要作用。此外,支持细胞分泌抗苗勒激素(anti-Mullerian hormone,AMH)保证苗勒管的退化。到了青春期,支持细胞的功能转变为支持精子生成。没有支持细胞在结构和营养代谢上的维护支持,生精细胞的分化、减数分裂、精子变形和成熟都不可能发生。
支持细胞在性分化、睾丸形成和精子发生中都起重要作用,但在所作用的时间和功能上并不相同。支持细胞在成年期精子发生中的作用是胚胎期没有的。从胚胎向成年期的转变发生在青春期。大概在青春初期,支持细胞在形态和功能上发生根本变化,从幼稚、增殖的状态转为成熟、非增殖的状态。细胞核增大,核仁变得更明显。相邻的支持细胞之间形成紧密连接,把生精小管分成基底膜侧和管腔侧,使处于减数分裂中的生精细胞隔离在管腔侧,由于血-睾屏障的存在,无法直接从血-睾屏障外血液循环系统摄取营养物质,营养来源只能依赖于支持细胞。此时,支持细胞的主要功能就转变为从营养和结构上支持保护生精细胞。如果在幼稚期,支持细胞发生缺陷,将不可避免影响其成熟期的功能。目前认为,甲状腺激素T3与雄激素或与FSH相互作用,引起支持细胞成熟。新分化的生精细胞也是诱导支持细胞成熟的一个重要因素。
成熟支持细胞所表达的蛋白分子与未成熟支持细胞是不同的。观察分析支持细胞所表达的分子将有助于了解支持细胞的状态。如卵泡刺激素受体(FSHR)是一个G蛋白耦联的跨膜蛋白,他仅表达于支持细胞。在大鼠妊娠第14.5d时,胚胎性腺开始出现微弱表达,出生后FSHR表达增加了3倍,在出生后15dFSHR表达达到最高峰,之后逐渐下降至成年水平,相当于出生后2d的表达水平。FSHR的表达变化与支持细胞的增殖时间相吻合。表达雄激素受体(androgen receptor,AR)是支持细胞成熟的标志,尽管它的表达随着生精周期而变化。雄激素受体在支持细胞成熟前开始表达,他参与了支持细胞的成熟过程。Wilms肿瘤基因(Wilms,tumour gene,WT1)在胚胎性腺发育和成年期精子发生过程中是一个起关键作用的转录因子,他特异表达于支持细胞核。胚胎发育过程中,WT1首先在中胚层开始表达,胚胎发育早期,表达于生殖嵴和未发育性腺的体腔上皮及间叶细胞。之后体腔上皮发生迁移,分别形成雄性的支持细胞和雌性的颗粒细胞。支持细胞自此直至成年始终表达WT1。其他分子如AMH、角质纤维蛋白18 (cytokeratin 18,CK18)、芳香化酶(aromatase)、神经细胞黏附分子(neural cell adhesion molecule,NCAM)、抑制素βB亚单位(inhibin beta B-subunit)等表达于未成熟支持细胞,而转铁蛋白(transferrin)、白细胞介素1α(Interleukin-1α)、P27kip1、转录因子GATA-1、层粘连蛋白α5(laminin alpha 5)等表达于成熟支持细胞。
支持细胞在精子发生过程中的功能
支持细胞是生精小管内唯一与生殖细胞直接接触的体细胞,复杂而精密的精子发生主要依赖于支持细胞。不存在只有生精细胞而没有支持细胞的睾丸,体外培养时也只有将支持细胞和生精细胞共同培养才能维持生精细胞一定时期的存活,而且支持细胞的数量决定了生殖细胞的数量,所有这些现象说明支持细胞在雄性性腺中有非常重要的功能。支持细胞的功能大概包括:血-睾屏障形成、提供生精细胞结构支持、供给生殖细胞营养物质和吞噬作用。
血-睾屏障形成
青春期,相邻支持细胞之间在靠近基底膜附近会形成一个特殊的屏障——血-睾屏障(blood testis barrier,BTB)。血-睾屏障将生精小管分为基底室(basal compartment)和近腔室(adluminal compartment)。基底室存在不受血-睾屏障保护的精原细胞和前细线期精母细胞,近腔室内含细线期以后的各级生精细胞。
血-睾屏障主要有三方面功能:①为生精细胞的发育提供一个稳定的微环境。血浆和淋巴毛细血管中的物质可以直接进入到基底室,但由于血-睾屏障的存在,无法进入近腔室。这就保证近腔室内生精细胞进行减数分裂和变形的分化成熟过程能在一个相对稳定的微环境中进行,从而保证正常的精子发生过程和遗传基因的稳定;②封闭细胞间隙的通透性,选择性透过生物分子,调节营养物质和水份出入生精上皮,限制有害物质进入;③血-睾屏障也构造了一个免疫屏障,可以隐蔽生精细胞表面存在的抗原决定簇,同时他把血液循环中的免疫球蛋白和淋巴细胞隔绝在生精小管之外。
支持细胞之间形成的血-睾屏障是精子发生正常进行的物理保障,然而血-睾屏障紧密连接的周期性重建和形成机制还有待于阐明。在小鼠精子发生周期的第Ⅷ~Ⅸ期,血-睾屏障进行着活跃的解聚和重建过程。在这个阶段,位于早期精母细胞(主要是细线期精母细胞)之下相邻支持细胞间新的血-睾屏障形成是维持其屏障功能完整性的必要条件。研究发现,小鼠睾丸在43℃水浴30min后,在第10天早期精母细胞重新出现后能促进紧密连接分子ZO-1在生精小管中的正确定位。另外也观察到在缺失早期精母细胞的c-kit基因敲除小鼠中,血-睾屏障的完整性被破坏,ZO-1的分布也不正常。在支持细胞和精母细胞复合培养模型中,将早期精母细胞铺到已培养5d贴壁的支持细胞培养层上,结果发现,在48h内形成了新的紧密连接,同时还伴随着E-钙黏素(E-cadherin)和FRNK(FAK-related nonkinase)蛋白分子表达的上升。
在原代支持细胞中过表达FRNK能够诱导E-钙黏素表达及ZO-1在细胞膜上的聚集。加入ERK1/2磷酸化抑制剂能明显阻止早期精母细胞诱导的新紧密连接的形成及FRNK和E-钙黏素的升高。进一步的研究发现,早期精母细胞培养液中含有某(些)因子剌激紧密连接形成。这(些)因子相对分子质量在10 000~30 000之间,他(们)可通过ERK1/2MAPK信号通路促进新的紧密连接的形成。这些研究结果提示,精母细胞对紧密连接,即新的血-睾屏障的形成可能起重要作用,但早期精母细胞在新的血-睾屏障的形成过程中是如何起作用的还不清楚,而研究清楚这点不仅有助于完善血-睾屏障调控机制的理论体系,还可能发现新的调控紧密连接形成的细胞因子,可能为治疗男性不育药物的筛选提供新的理论基础。
结构支持功能
支持细胞具有高度发达的细胞骨架,能维持细胞外形、定位和转运细胞器,在细胞间和细胞-胞外基质的接触点固定细胞膜,帮助发育中的生殖细胞移动,参与成熟精子从生精上皮释放。
支持细胞不仅参与分泌基底膜(basement membrane)的组成成分,如laminin和collagenⅣ,还通过他的细胞骨架系统和细胞连接分子与各级生精细胞建立直接的联系。精子发生是一个包含细胞增殖、分化、移位和形态变化一系列复杂有序的精密变化过程。位于生精小管基底部的A型精原细胞经过数次有丝分裂生成B型精原细胞,接着染色质发生重构生成初级精母细胞,此时减数分裂开始,前细线期和细线期精母细胞脱离基底膜,越过血-睾屏障,随着生精细胞的分化逐渐向管腔迁移。最后,长形精子细胞脱离支持细胞释放到管腔,经过附睾,成为有受精能力的成熟精子。在这一系列高度复杂有序的变化中,迁移的生精细胞始终与围绕他的支持细胞紧密接触。各级生精细胞和支持细胞的这种相互作用对于成熟精子的产生是关键。因此,生精细胞在生精小管内成功迁移的前提是有一套精密完善的细胞连接系统。这个系统的典型特征是支持细胞与分化中的生精细胞之间的连接一直处于动态的分解和重建中。
上世纪70到80年代,对睾丸的形态学研究发现,睾丸中存在许多与其他上皮中相似的连接。这些连接基本可以分为三大类:闭锁连接(occludin junctions)、锚定连接(anchoring junctions)和通讯连接(communicating junctions)。睾丸中的闭锁连接和通讯连接均只有一种,分别为紧密连接(tight junctions,TJ)和缝隙连接(gap junctions,GJ)。这三种连接在睾丸生精小管中的分类和位置见下表。相邻支持细胞形成的紧密连接是血-睾屏障的有效成分。睾丸内的锚定连接按照所在部位、形态及与细胞内骨架的关系可分为四种类型:
- 黏合带(adhesion belt)或黏附连接(adherens junction,AJ);
- 黏着斑(focal adhesion)连接;
- 桥粒(desmosome)和半桥粒(hemidesmosome)连接。
黏附连接是锚定连接中研究最多的连接,他存在于支持细胞之间和支持细胞与各种生精细胞之间,生精细胞在小管内的成功迁移有赖于黏附连接的动态分解与重新构建。睾丸中除了常规的黏附连接外,还有两个独特的黏附连接结构,即胞外特化装置(ectoplasmic specializations,ES)和tubulobulbar复合物(tubulobulbar complexes,TBC)。前者分布于基底部支持细胞间或管腔部支持细胞与生精细胞间;后者分布于支持细胞与延长形精子细胞之间。
生精小管中细胞连接的分类和位置
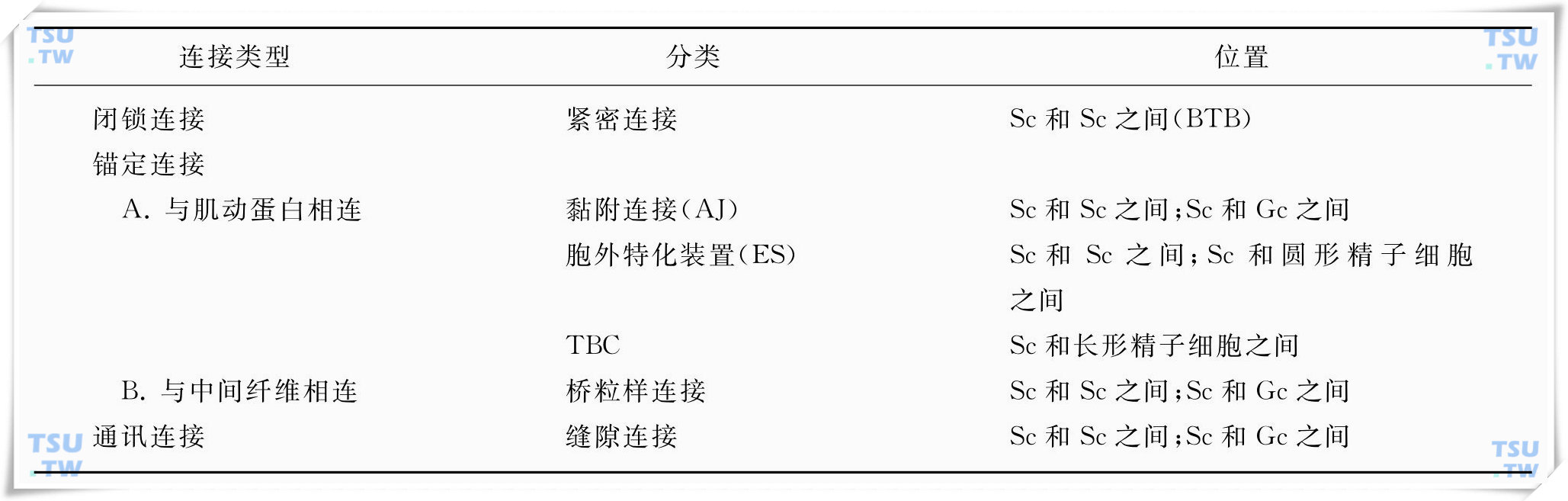
注:Sc:支持细胞;Gc:生精细胞。
营养和分泌功能
支持细胞是一类具有分泌功能的细胞,他能分泌蛋白酶及其抑制因子、激素、能量底物、生长因子、旁分泌因子以及细胞外基质成分等,这些蛋白对维持精子发生有重要作用。由于血-睾屏障的存在,血液循环中的大分子无法进入生精小管,生精细胞依赖包绕他的支持细胞提供营养物质和生物因子,包括氨基酸、碳水化合物、脂类、维生素、金属离子和多种细胞因子等,所以又被人称为“保姆细胞”(nursing cells)。而且对生精过程至关重要的两种激素,卵泡刺激素和睾酮也是通过支持细胞上各自的受体来发挥作用的。单独分离培养的生精细胞在体外存活时间不超过24h,表明生殖细胞的存活依赖于支持细胞。
吞噬作用
支持细胞在体内或体外培养中均有较强的吞噬能力。在体外生精小管培养中,退化的生精细胞能迅速被支持细胞所清除并伴随其胞质内包涵物增多。体内生精过程中,支持细胞吞噬从精子细胞脱落的残余小体和在精子发生过程中退化的各种生殖细胞。生精细胞因各种原因受到损害时,支持细胞吞噬活动显著增强。此外,在近腔室和基底室支持细胞有活跃的胞饮和受体介导的内吞作用。支持细胞的吞噬功能对维持生精小管管腔内环境的稳定有一定意义。
