英文:long QT syndrome,LQTS;
同义名:长QT间期综合征、QT间期延长综合征。
概述
长QT综合征(long QT syndrome, LQTS)是以静态心电图QT间期延长,多形性室性心动过速,心脏性晕厥和猝死为临床特征的一组综合征。
长QT综合征是一少见的疾病,是人类第一个发现的离子通道疾病,其重要性是对它的研究和防治,推动和带动了整个心血管疾病领域的遗传学-分子生物学、离子流-细胞电生理学、室速-室颤-心脏性猝死的电生理研究和临床预防治疗。目前将长QT综合征、Bruguda综合征和先天性传导系统疾病统称为遗传性离子通道疾病(inherited ion channel diseases)。
分类
长QT综合征可分为先天性或遗传性长QT综合征(congenital or inherited long QT syndrome,CLQTS)和后天获得性长QT综合征(acquired long QT syndrome,ALQTS)两大类。
- 先天遗传性长QT综合征:也是狭义的LQTS,是一遗传性疾病,按是否伴耳聋而区分为Jervell-Lange-Nielson综合征和Romano-Ward综合征,前者为常染色体隐性遗传,少见;后者为常染色体显性遗传,多见。按其遗传基因再分为LQT1型,LQT2型,LQT3型,LQT4型,LQT5型,LQT6型,LQT7型和LQT8型八个类型。
- 后天获得性长QT综合征:
- 缺血性心脏病;
- 高血压和左室肥厚;
- 代谢紊乱性疾病;
- 缓慢性心律失常;
- 抗心律失常药物:如奎尼丁,普鲁卡因酰胺,心律平,胺碘酮,索托洛尔;
- 抗微生物药:如红霉素等;
- 抗过敏药致QT间期延长;
- 治疗精神病的药物致QT间期延长;
- 其他药物:如血管扩张药、利尿药致QT间期延长;
- 其他:如二尖瓣脱垂、心肌病、心内膜疾病、带状疱疹病毒感染等致QT间期延长。
溯源与发展
早在1991年,著名电生理学家Zipes曾预言:如果说我们通过对预激综合征的研究,阐明了阵发性室上性心动过速的发病机制,并且解决了其诊治的话,那么有可能通过对LQTS的研究,解决室性心动过速和心脏性猝死的防治。
心脏性猝死(sudden cardiac death,SCD)是世界范围内的是一个防治难点和研究热点,每年有50多万人发生心脏性猝死,其中90%左右猝死病例为室速或室颤,少数为缓慢心率诱发。以长QT综合征(LQTS)为代表的分子遗传学的研究进展,为室速、室颤和心脏性猝死防治,及其发生机制的研究奠定了基础。
近十年来,LQTS的分子生物学研究取得了突破性进展,已阐明了8个基因上的300多个基因突变点与LQTS有关,其他的基因和突变点正在研究中,并可用相关的离子通道作用药物在实验室引出LQTS实验模型,进行其发病机制和干预治疗的研究。1993年,国际LQTS协作组制定了统一的诊断标准,此后对临床病史、特点、心电图诊断价值和治疗都有重要进展。随着大系列基因检测资料的积累,不同基因类型患者的临床心电图特点的对比观察研究取得了可喜进展,现在可依据患者心电图ST-T的特征性改变,从临床推断其致病基因类型,可靠性达64%以上(64%-100%)。以β受体阻滞剂为代表的药物治疗和以ICD和左侧颈胸交感神经切除为代表的非药物治疗已成为长QT综合征的有效治疗方法。
LQTS研究的历史:
- 1957年,Jervell和Lange-Nielsen首先报道了一个LQTS家系,该家系中四个小孩有QT间期延长和晕厥,并伴有耳聋,其中3个小孩猝死,日后被称为Jervell-Lange-Nielsen综合征(JLNS),呈常染色体隐性遗传型,较少见。
- 1963-1964年,Romano和Ward又分别报道了同样具有家族倾向的心脏性疾病,但不伴耳聋。后来被称为Romano-Ward综合征(RWS),为常染色体显性遗传型,较常见。
- 1966年,Yanowitz和Abildskov等报道了QT间期受左右侧交感神经的影响。
- 1974年,G.Michael Vincent和1975年Peter J. Schvrartz也分别报道了长QT综合征的病例,直到1985年正式统一命名为长QT综合征。
- 1991年,Vincent研究组Keating等人首先发现有关LQTS的第一个染色体突变位点。
- 1991-1996年,华裔学者Yan Ganxin和Antzelevitch,Sicourin等应用玻璃微电极技术定量测定犬心室肌从心外膜到心内膜AP时,发现心室肌中层肌细胞具有独特的电生理特性而将其命名为M细胞。M细胞的主要电生理特性包括:
- M细胞具有明显长的动作电位时程(APD)。其离子流基础为缓慢激活的延迟整流钾电流(IKS)小而晚期钠电流(late-INa或INa-L)大。
- M细胞的APD具有独特而显著的慢频率依赖性和对药物的特殊反应性,在缓慢心率下许多药物作用于M细胞容易发生后除极→触发活动→折返→室速(VT)、室颤(VF)。
- M细胞API相呈峰-切迹-圆顶形态,其离子流基础是M细胞复极早期较大的Ito,也是T波形成和ST段提高的基础。
- 1996年,Vincent研究组的华裔学者Wang Qing发现LQT1致病基因,为LQTS分子生物学遗传机制和遗传与临床的关系奠定了基础,使得LQTS的研究取得了突破性进展。
- 1993年,PJ Schwartz, AJ Moss, CM Vincent等代表国际长QT综合征协作组提出长QT综合征的诊断标准(Circulation 1993,88(2):782-784),为在国际范围内统一诊断标准奠定了基础。
- 2000年,华裔学者Li Zhang和Vincent研究组在10多年认真对比分析大量的常规12导联心电图和分子生物学遗传学资料基础上,研究出利用常规12导联心电图鉴别QT延长综合征的基因类型的创造性的结论:依据患者心电图ST-T的特征性改变,可从临床推断其致病基因类型,可靠性达64%以上,成为临床与分子生物学遗传联系的典范。
- 目前,已清楚地阐明了LQTS的8个致病基因,300多个突变点已被鉴别,基因突变类型包括错义突变、移码突变、无义突变、缺失突变、剪接点突变。然而这些发现并没有囊括所有的LQTS患者,研究发现一些LQTS家系不能用以上已知基因异常所解释,因此可以肯定LQTS至少还存在一种或多种基因突变类型有待于进一步发现研究。
我国的现状
我国人口众多,如果按每1/5000 -1/7000的患病率推算,全国LQTS患者达20万人左右,因此首先应引起国内心血管病学家和临床专家对该病的高度重视,凡是青少年有突发性或不明原因的晕厥或猝死者均应高度疑及LQTS的可能性。只有考虑到LQTS的可能性,才可能进一步询问有关的家族史,认真分析QT间期和ST-T形态学特征,按1993年的统一标准做出LQTS的临床诊断。因此所有医务人员对LQTS的认识、警惕和重视是防止漏诊、误诊的重要前提。
1999年,在北京、西安和武汉的部分专家倡议下,由中华医学会心电生理和起搏分会组织成立了LQTS协作组,先后在西安,北京等全国各大城市举办了LQTS专题学术研讨会,交流了国内外的研究进展,对国内LQTS的研究起到一定的推动作用。
我国LQTS临床研究和遗传学研究正在起步,应对发现的LQTS患者,进行认真系统的家系调查,包括其父、母、祖父母和曾祖父母,及其子女、孙子女和曾孙子女,以明确其家系遗传倾向和发现该家系成员中的新病例,并在有条件的单位开展分子遗传学和细胞电生理学研究。
LQTS的分子遗传学研究进展:从1991年Utah大学研究组MT Keating首先发现11号染色体p11.5位点突变与LQTS相关以来,至今已有8个基因300多个突变点被鉴别,是心血管疾病有关分子遗传学研究较为深入的一个疾病。目前可按各类突变基因作用机制在实验室复制出各LQTS的特征性电生理模型,进行深入的发病机制和诊治的研究。根据基因异常类型LQTS被分为以下几种类型。
| LQTS亚型 | 突变基因 | 染色体位置 | 离子通道蛋白质 |
|---|---|---|---|
| LQT1 | KVLQT1 | 11p15.5 | IKs(缓慢激活的延迟整流钾通道) |
| LQT2 | HERG | 7q35-36 | IKr(快速激活的延迟整流钾通道) |
| LQT3 | SCN5A | 3p21-24 | INa(纳通道) |
| LQT4 | Ankyrin-B | 4q25-27 | ICa2+(钙通道) |
| LQT5 | KCNE1 | 21q21.1-22.1 | IKsB(缓慢激活的延迟整流钾通道) |
| LQT6 | KCNE2 | 21q21.1-22.1 | IKrB(快速激活的延迟整流钾通道) |
| LQT7 | KCNJ2 | 17q23 | IKir(钾通道) |
| LQT8 | Cav1.2 | 12p13.3 | ICa-L(钙通道) |
| JLNS | KVLQT1或KCNE1 | 11或21 | IKs(缓慢激活的延迟整流钾通道) |
发生机制和电生理研究
LQTS动作电位延长的机制
动作电位平台期内向电流和外向电流大致平衡,故膜电位保持平台状。由于该期膜电位较高,任何离子成分的微小变化均有可能引起动作电位平台期时程和形态的显著改变。平台期外向电流主要包括延迟整流钾电流(IK)和内向整流钾电流(IKi)。IK为电压依从性电流,包括慢激活成分(IKs)和快激活成分(IKr),IK在除极到-50 nN左右激活,电流逐渐增强,IKr和IKs与心肌细胞复极有关,又称为复极化电流,是形成平台期和T波的主要外向电流,也是Ⅲ类抗心律失常药的主要作用部位,同时又是KCLQT1,HERC,KCNE1(包括LQTI、LQT2、LQT5和J,L-N)型LQTS的主要病变部位。IK1是电压依赖性的背景钾电流,不论兴奋状态还是静息状态其通道都开放,其大小取决于膜电位,与膜电位呈线性关系,表现内向整流作用。
KVLQT1或称KCNE1是一个定位于缓慢激活延迟整流钾电流IKs的亚单位的676氨基酸蛋白。IKs主要在3相,但也存在于2相后期的外向钾电流。该通道基因突变导致有功能的钾通道数量明显减少,K+外流减小,导致复极延长,APD延长产生EAD和触发活动。LQTS和其他病理状态的IKr和/或IKs可使ADD延长,AT间期延长,T波形态改变。
KCNE1-LQT5是定位于IKsβ亚单位的由130个氨基酸组成的复合体。该型基因突变改变通道的电压依赖性,并加速通道的失活,因而减少IKs电流,延迟复极,产生APD延长。
HERG-LQT2影响快速激活的延迟整流钾电流的IKr,该基因的错义突变和缺失可使有功能的通道减少50%左右,故IKr钾外流受阻,产生APD延长。
SCN5A-LQT3是一个心脏钠离子流基因,与以上钾离子基因不同的是该基因突变不引起通道功能的缺失和减退,而引起通道功能的增加,主要原因是该基因突变改变了通道的失活,使突变通道反复开放,这样就引起了前述的2位相背景内向电流的持续增加,使复极和APD延长。
TdP的发生机制
早期后除极(early after depolarization,EAD)和触发活动。LQTS患者的主要临床表现和致死原因是TdP,且TdP不能被程控期前刺激诱发和终止,说明TdP不由折返性机制引发。目前的实验及临床研究结果已明确,LQT2和LQT3患者动作电位时程(action potential duration,APD)延长,产生EAD及其触发活动并诱发TdP,而TdP持续可能是反复的EAD及其触发活动和折返激动共同参与。LQT1患者占全部LQTS患者的约50%,但因IKs减低而产生EAD并诱发TdP的实验及临床证据尚不充分,LQT1动物模型及TdP发生机制未完全统一。新近Antzelevitch应用LQT1动物模型研究显示,单独阻断IKs或同时给予β肾上腺素能刺激并不诱发EAD,但IKs阻断加β肾上腺素刺激引起延迟后除极(delayed after depolarization,DAD)增加APD离散度,LQT1患者TdP的发生机制待于进一步研究。
临床表现
症状
LQTS的典型临床症状是尖端扭转性室速(TdP)引起的反复短暂性晕厥和心性猝死,常无前驱症状,尽管有些LQTS患者晕厥和猝死的发生是在睡觉和休息时,但大多数患者是出现在运动(如跑步、游泳等)、情绪激动(如恐惧、害怕、生气和惊吓等)时,晕厥一般持续1-2 min。
以上症状与LQTS的基因类型有关,LQT1和LQT5大约90%的症状发生在运动和情绪激动时,LQT3约90%的猝死发生在睡觉时.LQT2患者症状的出现几乎均在运动、情绪激动、熟睡和唤醒之间。尖端扭转室速的诱发原因可能有两个,一是伴QT间期显著延长的心动过缓;二是窦性心动过速加上交感神经亢进,且后者常可自行终止,尖端扭转型室速转变成室颤是猝死的主要原因,但转变的机制仍不清楚。LQTS一家系谱如下。
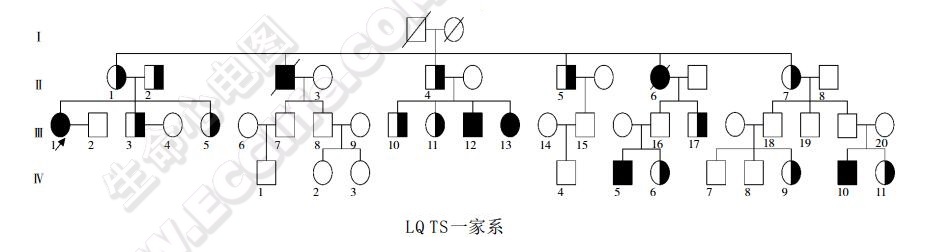
心电图类型和特点
心电图改变:QT间期延长是LQTS的主要特点,QT延长的程度有很大的差异,平均QTc为0.49s,范围是0.41到>0.60s,女性平均比男性长0.02s,LQT1(0.49s)和LQT2 (0.48s)的平均QT基本相等,LQT3的平均QTc较长,为0.52s(范围为0.43s到>0.60s)。
约12%的LQTS基因携带者QT正常,QTc≤0.44s,其中LQT2占17%,LQT1占12%,LQT3占5%,因此QTc正常并不意味不是LQTS,约30%的患者QTc在临界范围(0.45-0.46s),故约40%的患者不能用心电图诊断。
尖端扭转型室速可因心动过缓,RR长短交替加上交感神经亢进而引发,尖端扭转型室速转变成室颤是猝死的主要原因。
T波和U波异常也是LQTS的主要表现,且与基因型有关,T波宽大是LQT1的特点,T波双峰或低平是LQT2的特征,LQT3很少出现T波双峰,但却常表现出ST段延长和双相T波。
T波狭窄高耸:以上T波表现也常在各基因型间出现重叠,而且LQT1和LQT2的T波也可表现正常。根据既往资料ECC ST-T波形态可能与LQTS基因型有关,进一步对其进行研究探讨有益于简化LQTS致病基因的筛选步骤,节约时间和金钱,有着重要的临床意义。
典型的LQT1心电图图形(下图):
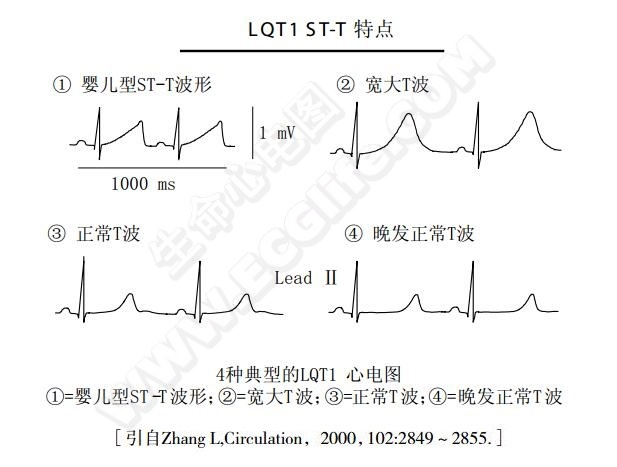
- 婴儿型ST-T波形:ST段短促,与T波上升支融合,后者呈直斜线状。双峰T波常见,在肢体和左胸导联上,第二峰常构成T波的顶端。大体上,T波基部较宽、顶部尖锐、T波的下降支陡立,呈非对称状。经Bazett公式校正后的QT间期可为临界值或明显延长(QTc(470+20)ms)。这种波形最常见于出生后2个月至2岁的婴儿患者,偶尔见于幼儿患者,所以常见存心率较快、右心主导等婴幼儿心电图特征。
- 宽大T波:T波呈单峰状,基部宽大,上升及下降支光滑。QT间期可为正常或明显延长(QTc(490±20)ms)。
- 正常T波:T波形态表现正常,QT间期可为正常或明显延长(QTc(460±20)ms)。
- 晚发正常T波:ST段延长,T波形态正常。QT间期多为明显延长(QTc(490±40)ms)。
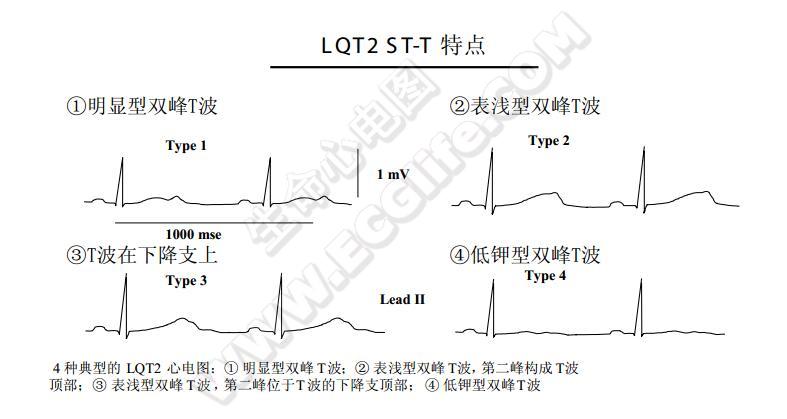
典型的LQT2心电图图形(上图)多导联双峰T波是LQT2的主要心电图特征。T波幅度常偏低。QT间期可为正常或明显延长(QTc(470±30)ms)。双峰T波可分为四种亚型:
- 明显型双峰T波:T波两峰分明,第二峰常位于T波下降支的早期;
- 表浅型双峰T波,T波双峰(或切迹)表浅,有两种形态:第二峰可位于T波顶部;
- T波在下降支上。由于双峰表浅,有时T波顶部可呈平台状。识别表浅型双峰T波,需要仔细观察,否则易被忽略;
- 低钾型双峰T波:T波低矮,两峰间距离较大,第二峰常与U波融合,类似于低钾时的心电图改变。
典型的LQT3心电图图形(下图):
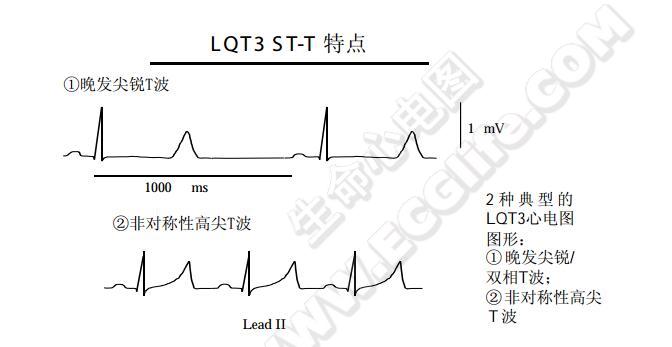
- 晚发尖锐/双相T波:LQT3心电图的主要特征表现为ST段平直或斜型延长,T波尖锐,起始和终止分明。双相T波常见。QT间期多为显著延长(QTc(530+40)ms)。
- 非对称高尖T波:T波高尖,下降支陡立,呈非对称型。QT间期正常或明显延长(QTc(490+20)ms)。
诊断与鉴别诊断
LQTS的典型临床症状是尖端扭转性室速引起的反复短暂性晕厥和心脏性猝死,常无前驱症状。尽管有些LQTS患者晕厥和猝死的发生是在睡觉和休息时,但大多数患者是出现在运动(如跑步、游泳等)、情绪激动(如恐惧、害怕、生气和惊吓等)时,晕厥一般持续1-2min。以上症状与LQTS的基因类型有关,LQT1和LQT5大约90%的症状发生在运动和情绪激动时,LQT3约90%的猝死发生在睡觉时,LQT2患者症状的出现几乎均在运动、情绪激动、熟睡和唤醒之间。LQT1、LQT2、LQT5大多于运动中发病,与其致病的离子流基础IKr、IKs对肾上腺和儿茶酚胺的反应有关,也为β受体阻断剂及左颈胸心交感神经切除治疗提供了依据。尖端扭转室速的诱发原因可能有两个,一是伴QT间期显著延长的心动过缓;二是窦性心动过速加上交感神经亢进,且后者常可自行终止。尖端扭转型室速转变成室颤是猝死的主要原因,但转变的机理仍不清楚(下图)。
不同基因型的心电图特点
QT间期延长是LQTS的主要特点,QT延长的程度有很大的差异,平均QTc为0.49s,范围是0.41-0.60s.女性平均比男性长0.02 s,LQT1(0.49s)和LQT2(0.48s)的平均QT基本相等,LQT3的平均QTc较长,为0.52s(范围为0.43-0.60s)。约12%的LQTS基因携带者QT正常,(QTc≤0.44s),其中LQT2占17%,LQT1占12%,LQT3占5%,因此QTe正常并不意味不是LQTS;约30%的患者QTc在临界范围(0.45-0.46s),故约40%左右的患者不能用心电图诊断。T波和U波异常也是LQTS的主要表现,且与基因型有关,T波宽大是LQT1的特点,T波双峰或低平是LQT2的特征,LQT3很少出现T波双峰,但却常表现出ST段延长和T波狭窄高耸。以上T波表现也常在各基因型间出现重叠,而且LQT1和LQT2的T波也可表现正常。新近,L.Zhang和GM.Vincent研究组的研究显示:常见LQT1、LQT2、LQT3的不同基因类型的患者,心电图有一定的特征性改变,其准确性达64%以上,因此根据ECG ST-T波形态可初步判断LQTS基因型,有利于简化LQTS致病基因的筛选步骤,节约时间和金钱,有着重要的临床意义。
LQTS的诊断
任何40岁以下的人出现发作性晕厥和意外性猝死均应怀疑LQTS,尤其是儿童和年轻人,运动、情绪激动诱发的晕厥和猝死更提示LQTS的可能。LQTS的晕厥常被误诊为神经源性晕厥,最易被误诊为癫痫。ECC诊断标准为,女性QT≥0.48s或男性≥0.47s即可作为独立的诊断标准,若女性QTc<0.43s或男性QTc<0.41s即可排除LQTS,若QTc介于0.41-0.46s应进一步结合病史、临床表现和ECC改变。基因诊断LQTS目前仍不能普及,主要被用作研究工具,大约50%-60%的临床LQTS可用现有的方法和知识检测出基因类型,因为目前还没有将所有的LQTS基因类型鉴别完,因此基因诊断阴性并不能排除LQTS,而且即使已知基因的突变检测也费时耗力,故基因普查检测仍不能应用于临床。根据1993年国际LQTS协作组的建议,目前的诊断标准如下图所示。

治疗
基因特异性治疗
长QT的综合征的病因的基因特异性治疗是:
- 根据病史和家系调查而初步诊断为先天性或者后天性,并且就其病因给予相应的基因特异性治疗;
- 长QT的病因治疗的重点是诊断和确定后天获得性长QT综合征的病因,并给予积极有效的相应病因治疗的基因特异性治疗。
发病的可能机制主要有两种
其一是交感神经学说,认为心脏交感神经张力不平衡,由于交感神经兴奋突然引发扭转性室性心动过速;其二是离子流学说认为由于钾离子流或钠离子流失衡而导致动作电位时程延长,QT时期延长而引发EAD和二位相拆返导致扭转型室性过速。而β受体阻断剂(B-RB)的应用和左侧颈交感神经节切除术就是根据此学说,并经临床实践证明具有良好的效果。2001年,欧洲心脏病协会推荐的LQT综合征的心脏性猝死的预防治疗指南,如下。

该预防治疗指南的重点是一级预防,第一,要对已诊断或待诊断的患者,不论无症状者、有症状者或隐性基因携带者,都应该避免应用引发QT延长和低钾的药物;第二,上述人群要避免竞争性剧烈运动和精神刺激;第三,要对上述人群应用以β受体阻断剂为主的药物或非药物治疗,
长QT综合征扭转型室速的急诊治疗,按2001年欧洲心脏病协会推荐的LQT综合征扭转型室速的治疗指南(上图)。
β受体阻滞剂的应用先天性长QT综合征的药物治疗主要有:β受体阻滞剂治疗,补钾补镁治疗和可能诱发因素的治疗。
β受体阻滞剂治疗LQT综合征指南及其选择有症状的长QT综合征的一级预防和二级预防均为I类适应证,而无症状的长QT综合征者为Ⅱa类适应证,β受体阻滞剂的作用机制是:
- 阻断和平衡交感神经活动,特别是减低左颈交感神经的活动;
- 缩短QT间期;
- 阻断扭转性室速的触发机制;
- 在动物实验表明β受体阻滞剂可以减低LQT1、LQT2和LQT3的扭转型室速的发生,但临床应用表明只对LQT1、LQT2有效,而对LQT3无效。β受体阻滞剂可分为:选择性和非选择性两类,目前,主张选择应用非选择性β受体阻滞剂,如普萘洛尔(心得安)30-200mg/d。也有人认为可选用选择性β受体阻滞剂,如美托洛尔(倍他乐克)(25-100mg/d)。
β受体阻滞剂的用法和剂量:β受体阻滞剂是治疗长QT综合征的最主要的药物,长期大量临床资料证明具有良好效果,病死率由每年20%降到9%以下(5年死亡率仅为9%)。应用的剂量相对比常规剂量要大一些。患者开始给予常规剂量治疗,如果心率没有明显减慢和/或无明显房室阻滞,患者可以耐受时,应逐渐加大剂量,以完全控制症状为目标。因此,普萘洛尔的常用剂量为30-60mg/d,最大剂量因人而异,波动在70-200mg/d。
注意事项:
- 最重要的是决定长QT综合征是否与交感神经失去平衡或交感神经刺激有关。
- 长QT综合征的类型:一般只用于长QT一型和二型,如明确诊断为三型则不用β受体阻滞剂。
- β受体阻滞剂应用后要严密监测心率变化和有无传导阻滞,如出现严重性心动过缓或房室阻滞,则应减量或者停药。
- β阻滞及应用后注意观察可能的和其他合并症,如血压过低、过敏反应、血糖变化和其他可能的负作用。
- 应用β受体阻滞剂以后,应定期随访并记录治疗效果,及时调整剂量。
- 如果β受体阻滞剂应用后,患者仍有频繁的晕厥发生,则应考虑ICD或者左侧心交感神经阻断术,如果仍有症状,而且心动过缓和出现停搏等或者用药前就有心动过缓和停搏等情况则应及时植入人工心脏起搏器。
补镁补钾治疗和注意事项:
补镁是治疗LQTS患者室速室颤的关键治疗之一。镁是细胞内外钾离子转移的主要辅酶,补镁可以增加钾离子转运,增加细胞内钾浓度,增加细胞膜和心电的稳定性,有利于治疗室速室颤。首次静脉补镁2-5g然后根据化验结果进一步补充。
先天性长QT综合征确诊后,即便没有低血钾的依据,目前也主张给予补钾补镁治疗,其原因是90%以上的患者为LQT1和LQT2,补钾补镁治疗有利于细胞膜钾离子运转,对缓解症状有效(Compton,SJ.Circulation. 1996. 94:1018)。
非药物治疗
左侧心脏交感神经阻断术或称为左侧颈胸交感神经切除术(left cervicothoracic sympathectomy. left cardiac sympathectomy,LCTS),左侧心脏交感神经阻断术(LCTS)治疗指南将LCTS列为二类b类适应证。其可能机制和解释为:
- 公认的解释为左侧交感神经对心脏的控制占优势,所以切除左侧,而且动物实验也证明了这一点。
- 多数作者认为左侧交感神经占优势,而右侧迷走神经占优势。
- 1998年Opine在《心脏生理学》一书中,曾提到左侧颈胸交感神经主要分布在心室肌,右侧颈胸交感神经则主要分布在心房肌、窦房结和房室结等传导传统。
左侧颈胸交感神经切除术是治疗LQT患者另一个有效方法,其适应证是长QT综合征患者应用β受体阻滞剂和补钾补镁治疗后,并且认真的进行了各种诱发因素的预防措施,患者仍有晕厥反复发生时且没有植入或者经济条件不允许植入ICD或心脏起搏器者,则应考虑进行LCTS治疗。
ICD适应证:治疗指南将ICD+β受体阻滞剂列为一类适应证,凡诊断为LQTS且有反复晕厥的患者,均为ICD的适应证。我国目前经济条件仍处于发展阶段,应积极对有经济条件的患者开展ICD治疗。
机制:ICD预防和治疗心脏性猝死的机制是:
- 通过起搏预防和治疗缓慢依赖性VT/VF;
- 当VT发作时,通过超速起搏终止VT;
- 当VF发生时,通过低能量和高能量的电复律或者电除颤进行治疗。
方法:同人工心脏起搏器和ICD常规植入技术。
效果:一组177例患者远期随访表明:存活率76%,ICD放电率68%,9例患者死亡(Circulation 1993,Mar,87(3:800-807)。
