IL-1家族配体包括IL-1α、IL-1β和IL-Ra。单核巨噬细胞、中性粒细胞、肝细胞均能产生IL-1α 和IL-1β。IL-1α和IL-1β均缺乏信号序列,故并非由经典的高尔基体-囊泡途径分泌出细胞外。IL-1α前体在细胞质合成后,可经细胞膜上的中性钙激活蛋白酶切割后释放出细胞外。但是另外一部分IL-1α前体可进入细胞核发挥自分泌因子的作用。IL-1β前体同样在细胞质合成,经过半胱天冬酶(caspase) -1切割后成为有活性的IL-1β分泌出细胞外。
IL-1总共有两种类型的受体:IL-1RⅠ和IL-1RⅡ。具有激活细胞功能的是IL-1RⅠ,IL-1RⅡ的胞内域很短,无法激活细胞,它主要的功能是与IL-1RⅠ竞争结合IL-1配体,起到负调节的作用。IL-1 与IL-1RⅠ结合后,IL-1受体辅助蛋白(IL-1 receptor accessory protein,IL-1RAcP)加入形成复合体,募集髓样分化蛋白(myeloid differentiation primary response protein,MYD) 88、白细胞介素受体相关激酶(interleukin receptor-associated kinase,IRAK)和TNF受体相关因子(TNF receptor-associated factor,TRAF)6等因子,然后激活NF-κB、核内激活蛋白(activator protein,AP) -1、氨基末端激酶(c-Jun N-terminal kinases,JNK)、p38 丝裂原激活的蛋白激酶(p38 Mitogen-activated protein kinase,p38 MAPK)等信号通路。IL-1α与IL-1β结构相似,却因为无法与IL-1RAcP结合而无法激活细胞。故主要发挥作用的细胞因子是IL-1β。早期的动物实验研究就发现IL-1与TNF-α均可以引起体重下降以及恶液质。在体外培养的脂肪细胞中,IL-1可以抑制脂蛋白酶的活性以及刺激脂肪分解。IL-1信号转导通路见图2-2-1。
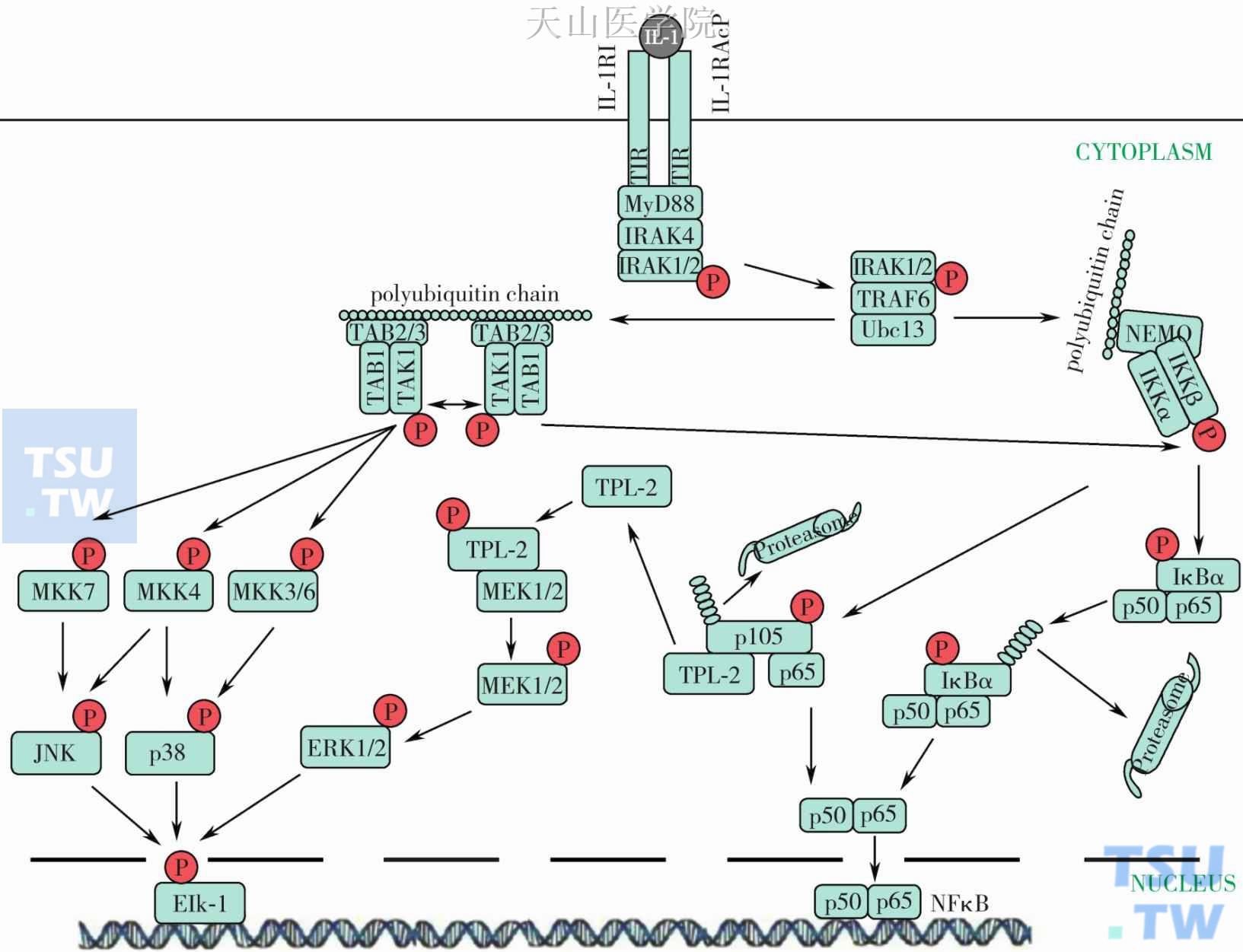
图2-2-1 简化的IL-1信号转导通路示意图
有研究者认为,IL-1在人体介导恶液质的机制中有特殊的地位:因为甲地孕酮的抗恶液质效应是通过减少单核细胞产生IL-1来生效的,而且该作用强于它对下丘脑神经肽Y浓度的影响。下丘脑钩状核具有恶液质效应的阿片-促黑素细胞皮质素原(pro-opiomelanocortin,POMC)和可卡因安非他命相关转录蛋白(cocaine-and amphetamineregulated transcript,CART)神经元均表达IL-1RⅠ,脑室内注射IL-1可以增加POMC和CART神经元动作电位的频率,刺激α-促黑激素(melanophore stimulating hormone,MSH)的释放,从而表现出恶液质效应。另一方面,有报道IL-1在中枢神经系统引起的恶液质效应是经过下丘脑-垂体-肾上腺轴发挥作用的,因为肾上腺切除术可以消除IL-1引起的中枢性恶液质。
