病例导读与思考
患者,女性,75岁,胰腺癌多发肝转移,腹腔转移。既往曾接受过3个疗程化疗,1个月前因病情进展,不能耐受抗肿瘤治疗,仅接受最佳支持治疗。近6个月体重下降约10kg,身高162cm,体重45kg。且6个月前开始出现上腹部及后腰部束状疼痛,未治疗,近1个月明显加重。臀部皮肤溃烂有烧灼样疼痛,且因严重便秘,还存在与排便有关的肛周痛。严重干扰睡眠。伴有多汗、腹胀、食欲下降、黄疸。每天进食极少,仅能进食少量流食,进食后常有呕吐,疲乏无力严重,几乎每天所有时间都卧床,但严重失眠,重度焦虑。几乎触不到脂肪和肌肉,眼窝凹陷,呈脱水貌。查体:消瘦、慢性病容,表情痛苦,坐位前倾。生命体征尚平稳。上腹部饱胀,压痛阳性,无反跳痛和肌紧张。腹部CT增强扫描提示:胰体尾占位,边界不清与包绕腹腔干、脾动脉、肠系膜上动脉。肝脏多发转移癌,肝门区,脊柱旁多发淋巴结肿大。
- 患者是否可诊断为恶液质,属于恶液质的哪个阶段?
- 患者疼痛的原因都包括哪些?
- 患者疼痛的机制如何分类?
恶液质可伴发或继发于多种疾病,包括肿瘤、严重创伤、大手术后、严重败血症等,其中肿瘤恶液质是恶液质最常见的临床表现形式,且肿瘤恶液质患者常常被疼痛、食欲缺乏、疲劳、衰弱等各种症状困扰。疼痛是最常见、也是最令肿瘤患者恐惧的症状之一。流行病学资料显示,晚期肿瘤患者中有70%~90%患者诉说疼痛。
通常来讲,恶性肿瘤、肿瘤相关性病变及抗癌治疗所致的疼痛都称之为肿瘤疼痛(cancer pain)。肿瘤患者疼痛,可以对机体的各个系统产生广泛影响,若得不到有效控制缓解,将引起或加重其焦虑、抑郁、乏力、失眠、食欲减退等相关症状,并相互之间形成恶性循环,不仅对恶液质的治疗造成诸多不利因素,还会对患者的功能情绪和生活质量等产生负面影响(图5-1-1)。因此,正确认识癌痛,重视癌痛患者,既是生物医学的需要,也是尊重人格和医者仁心的体现。
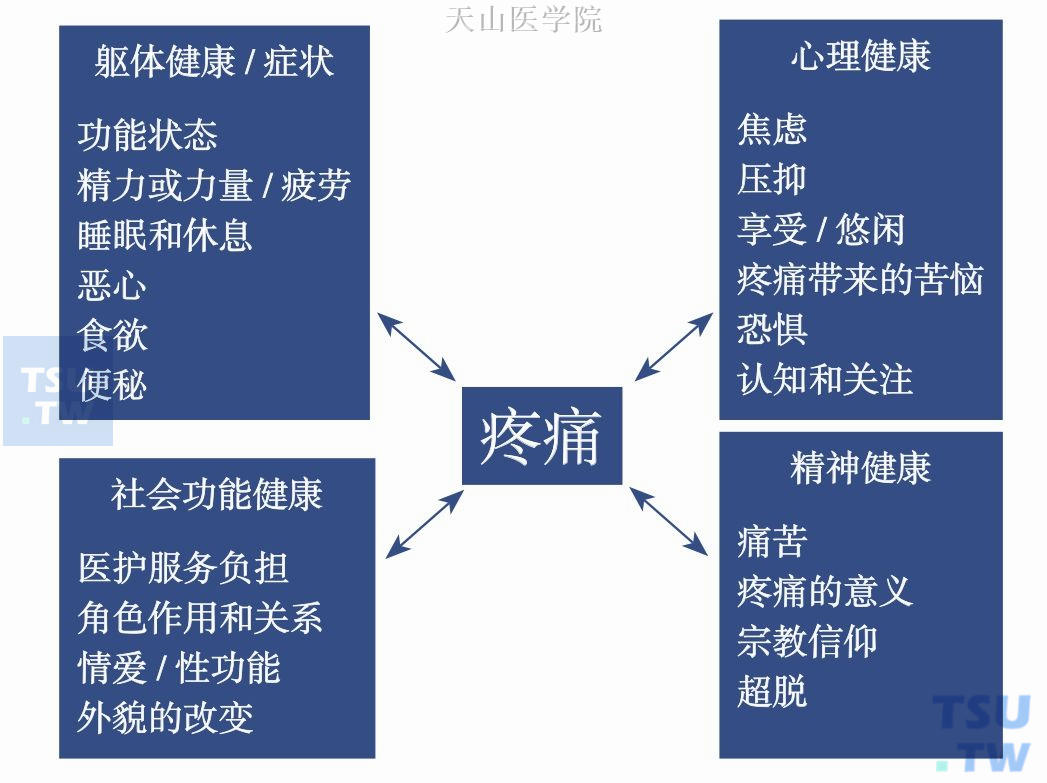
图5-1-1 疼痛与生活质量各方面的相互影响
肿瘤疼痛的病因
晚期肿瘤患者出现疼痛的原因是躯体因素及社会因素共同作用的结果,发病原因较复杂,尤其恶液质患者常常与其他相关症状同时出现,一定程度上更加重了病因的复杂性。导致肿瘤疼痛的心理因素主要包括疾病发生后的恐惧、焦虑、抑郁、愤怒、孤单等。而导致肿瘤患者出现疼痛的躯体因素大致可归纳为下列四类。
一、肿瘤直接侵犯所致的疼痛:肿瘤局部生长或远处转移的直接压迫、浸润、破坏及梗阻作用引起的疼痛。常见于骨转移、肿瘤压迫或浸润神经或神经节,肿瘤侵犯脑膜、硬脑膜、内脏、皮肤、黏膜,肿瘤导致空腔脏器梗阻,肿瘤阻塞血管、阻塞淋巴管等。
二、肿瘤相关并发症所致的疼痛:如虚弱、便秘、肌肉紧张/肌痉挛、卧床、压疮等并发症,均可能引起疼痛。
三、肿瘤诊断治疗的创伤及毒性所致的疼痛:创伤性诊疗操作或毒性治疗引起疼痛。如化疗相关的黏膜炎、栓塞性静脉炎、中毒性周围血管病、术后切口痛、神经损伤、四肢痛、放疗引起的神经损伤、放射性骨病等都可引起疼痛。
四、非肿瘤相关性合并症所致的疼痛:肿瘤患者因合并痛风、关节炎、强直性脊柱炎等非肿瘤因素所致的疼痛。如椎关节强直、骨关节炎等。
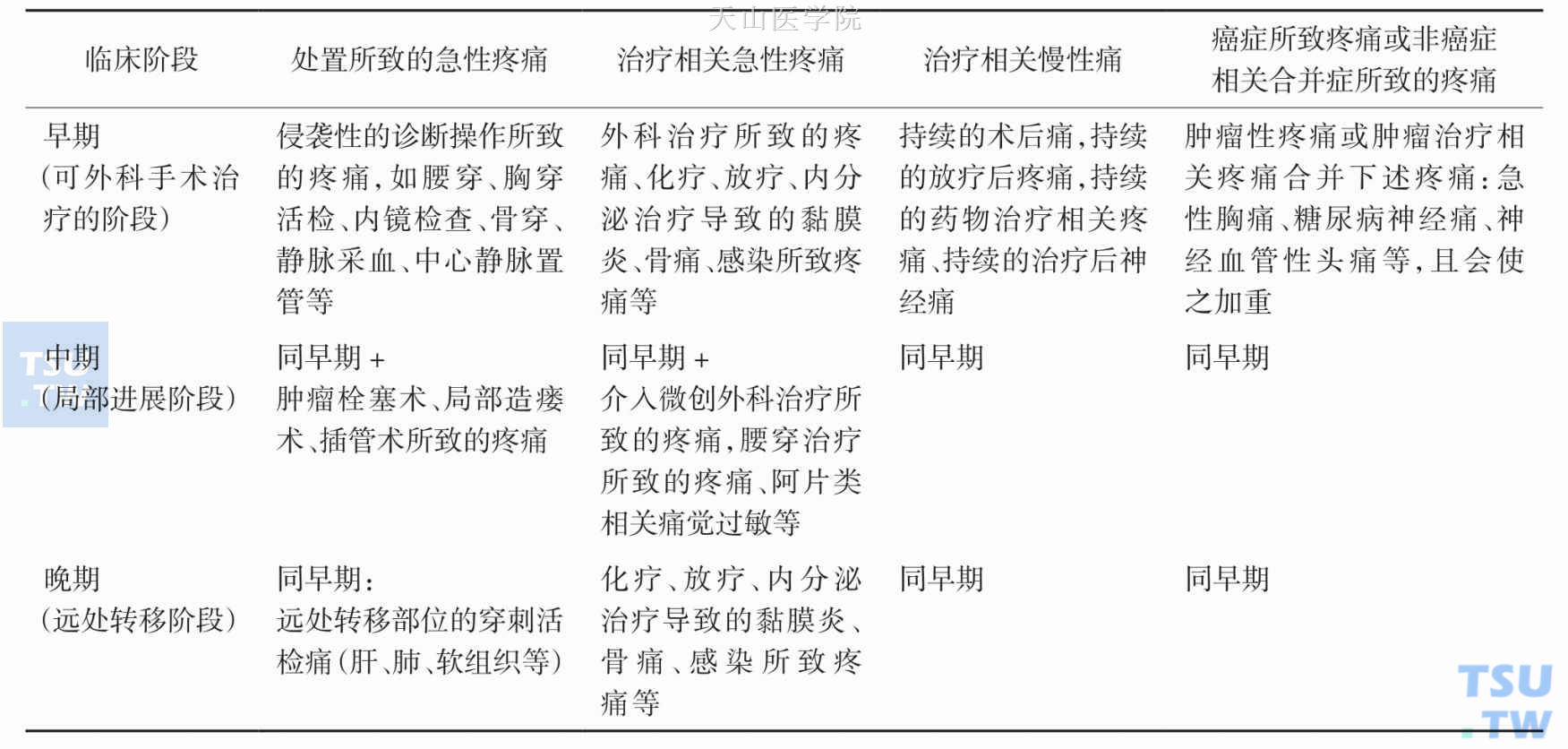
欧洲临床肿瘤协会的最新统计资料显示,除了肿瘤本身因素直接导致的疼痛之外,肿瘤患者在疾病过程中,治疗相关疼痛、并发症所致的疼痛及非肿瘤相关合并症所致的疼痛在肿瘤的任何阶段(无论早期还是晚期)均可出现,且常与肿瘤直接侵犯所致的疼痛并存,形成癌痛综合征。表5-1-1为对非肿瘤直接侵犯所致疼痛的其他病因的统计。
表5-1-1 肿瘤疼痛患者的病因
癌性疼痛的发病机制
急性疼痛的发生机制
恶液质患者的疼痛多是慢性疼痛,但其在疾病过程中也常常出现疾病本身或治疗相关的急性疼痛。急性疼痛常表现为伤害感受性疼痛。伤害感受性疼痛的发生机制是疼痛形成的神经传导基本过程。机体受到物理、化学或炎症刺激后,产生急性疼痛的痛觉信号,并通过神经传导及大脑的分析而感知。同时也伴有代谢、内分泌和免疫系统的变化。
1. 痛觉传感:任何外界或体内的伤害性刺激(物理、化学或生物毒素)均可导致局部组织破坏,释放各种内源性致痛因子如:①直接从损伤细胞中溢出的致痛因子5-羟色胺、乙酰胆碱、组胺、氢离子、钾离子等;②损伤细胞释放出有关的酶,在局部合成产生致痛因子缓激肽、前列腺素等;③由伤害性感觉器本身释放的致痛因子P物质。这些化学物质可以刺激疼痛感受器,使外源性刺激导致痛感。
2. 痛觉上行传递:伤害性刺激的信号由一级传入纤维传入脊髓背角,经过初步整合后,一方面作用于腹角运动细胞,引起局部的防御性反射;而另一方面则继续向上传递,组成上行束。疼痛信号通过这些上行束经过躯干和四肢的痛觉通路、头面部的痛觉通路和内脏痛觉通路由脊髓传递入大脑。致痛因子可激活多种疼痛信号传导受体,这些受体包括阿片类受体、外周神经中的兴奋性氨基酸受体、神经激肽受体等。它们也参与疼痛信号的传导,使疼痛信号的传递变得更加复杂。
3. 皮质和边缘系统的痛觉整合:脊髓丘脑束进入丘脑后形成二级神经元,发出纤维至白质的躯体感觉部位,与网状结构和丘脑核相连,延伸至边缘系统和扣带回,并与垂体和上行网状激活系统相连,整合多种感觉信号在大脑皮质形成痛觉,并引起相应的呼吸、循环及内分泌的变化。
4. 下行痛觉调控:在神经系统中不仅存在痛觉信号传递系统,而且存在痛觉信号调控系统。痛觉信号调控系统即内源性痛觉调制系统,主要有脊髓水平的调控、脑水平的调控、下行痛觉易化系统和调节因子等。
慢性疼痛的发生机制
恶液质患者罹患的疼痛几乎都有慢性肿瘤疼痛,这种慢性疼痛除伤害感受性疼痛的基本传导调制过程外,还表现出不同于急性疼痛的特殊发生机制。
1. 初级感觉神经元兴奋性异常增加:初级感觉神经元位于脊髓背根神经节(dorsal root ganglion,DRG),分布着感受不同刺激的多种受体,可将各种伤害性刺激转化为电化学信号传导至中枢神经系统。在持续的外周刺激下,DRG神经元发生可塑性变化,外周神经敏感性增加,表现出痛阈降低、痛觉过敏和诱发疼痛。以往的研究表明,肿瘤组织能释放一系列的生长因子、细胞因子和化学因子,如肿瘤坏死因子(tumor necrosis factor,TNF)-α、前列腺素E(prostaglandin E,PGE)、内皮素(endothelin,ET)、白细胞介素(interleukin,IL) -1、IL-6等,而初级神经元可以表达其中多种因子的受体,肿瘤组织分泌的这些因子可能作用于初级感觉神经元上各自的受体,激活和敏化感觉器,参与癌痛的发生。因此,严重的慢性疼痛患者甚至可能在无任何刺激的情况下也会感觉到疼痛(图5-1-2)。
2. 受损神经异位电活动慢性疼痛常表现为在:组织损伤愈合后的持续性疼痛,神经损伤导致神经元的异常电活动是痛觉异常的生理基础。神经损伤诱发异位电活动的发放形式与正常神经末梢受刺激产生的传入活动具有明显的差别,受损神经可以在无任何外部刺激的条件下产生高频放电,导致痛觉过敏和感觉异常。
3. 痛觉传导离子通道和受体异常:在慢性疼痛过程中,痛觉传导离子通道和受体发生异常变化,大量异位和自发的异常放电,导致神经细胞与其他不参与疼痛传导的细胞建立新的联系,从而引起疼痛感觉扩散,泛化以及痛觉皮肤分界紊乱,促使痛觉过敏和感觉异常。
4. 中枢神经系统重构:慢性疼痛的“疼痛记忆”表现为损伤治愈后疼痛信号依然持续存在。这种“疼痛记忆”并非心理性因素的结果,而具有中枢神经系统重构的病理基础。“疼痛记忆”将进一步加重慢性疼痛对患者认知行为和精神心理的损伤。
肿瘤疼痛的分类
肿瘤疼痛的分类有很多种方法:可分别按照疼痛的病理生理学机制、发作时间及强度进行分类。这些分类体现了疼痛的多维性,正确地划分疼痛类型,有助于了解疼痛发生的原因,对疼痛的评估及有效控制具有积极的临床意义。
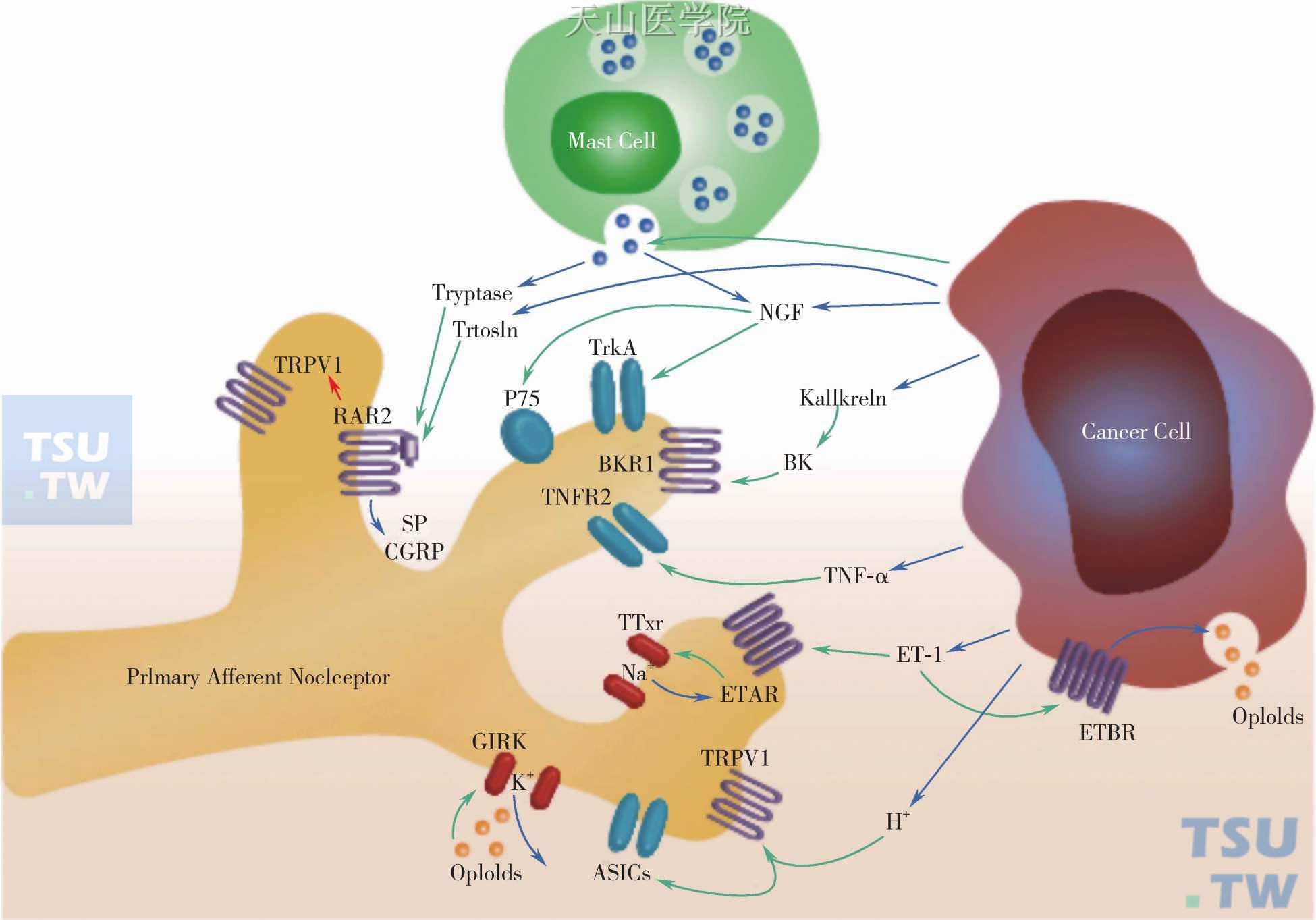
图5-1-2 肿瘤微环境主要细胞成分,包括肿瘤细胞、主要传入性伤害感受器及免疫细胞(如肥大细胞)
TNF-α:tumor necrosis factors α,肿瘤坏死因子-α;TNFR:tumor necrosis factors receptor,肿瘤坏死因子受体;ETAR:endothelin A receptor,内皮素A受体;ETBR:endothelinB receptor,内皮素B受体;Tryptase:类胰蛋白酶
按疼痛发病机制分类
1. 伤害感受性疼痛:因有害刺激作用于躯体或脏器组织,使该结构受损而导致的疼痛。伤害感受性疼痛与实际发生的组织损伤或潜在的损伤相关,是机体对损伤所表现出的生理性痛觉神经信息传导与应答的过程。伤害感受性疼痛包括躯体痛和内脏痛。躯体性疼痛常表现为钝痛、锐痛或者压迫性疼痛。内脏痛通常表现为定位不够准确的弥漫性疼痛和绞痛。
2. 神经病理性疼痛:外周神经或中枢神经受损,痛觉传递神经纤维或疼痛中枢产生异常神经冲动所致的疼痛。神经病理性疼痛常被表现为刺痛、烧灼样痛、放电样痛、枪击样疼痛、麻木痛、麻刺痛、幻觉痛、中枢性坠、胀痛,常合并自发性疼痛、触诱发痛、痛觉过敏和痛觉超敏。
按疼痛病程分类
1. 急性疼痛:指短期存在(<3个月)、通常发生于伤害性刺激之后的疼痛。且伤害性刺激消失,疼痛也随之消失,是一种机体的保护机制。
爆发痛(breakthrough pain),又称为突发性疼痛,是一种特殊类型的急性疼痛,是指在有效镇痛药物治疗期间,突然发作出现的短暂疼痛。50%~90%的癌痛患者在疾病过程中会遭受爆发性疼痛。
2. 慢性疼痛:持续时间长(常超过3个月),病因不明确,疼痛程度与组织损伤程度可呈分离现象,可伴有痛觉过敏、异常疼痛、常规止痛治疗疗效不佳等特点。慢性疼痛的发生,除伤害感受性疼痛的基本传导调制过程外,还可表现出不同于急性疼痛的神经病理性疼痛。肿瘤疼痛大多表现为慢性疼痛。
根据疼痛的强度分类
疼痛可依据疼痛程度不同而划分为轻度、中度、重度疼痛。该分类的划分依赖于临床常用的疼痛程度评估方法。详见疼痛的评估相关内容。按照疼痛程度对癌痛进行分类,也是制定癌痛综合治疗方案的重要依据。
肿瘤疼痛对恶液质患者的影响
肿瘤恶液质患者常常被多种生理及心理症状困扰。这些症状相互影响,影响患者的生活质量、对治疗的耐受性;同时也影响医生对患者的治疗决策,从而影响患者预后。而疼痛作为最常见的肿瘤恶液质患者相关症状之一,主要通过以下方面对恶液质患者产生影响。
疼痛本身对恶液质患者的影响
1. 疼痛对恶液质患者其他伴随症状的影响
如消化道肿瘤局部浸润导致的疼痛常常引起或加重患者食欲下降、恶心、呕吐、吞咽困难、疲乏无力、便秘等,从而进一步加重患者的恶液质状态。而疼痛引起的焦虑、抑制等不良心理因素同样也是引起或加重患者乏力、食欲下降等恶液质相关症状。图5-1-3为恶液质患者疲乏症状的各种病因,其中疼痛为多种原因之一。
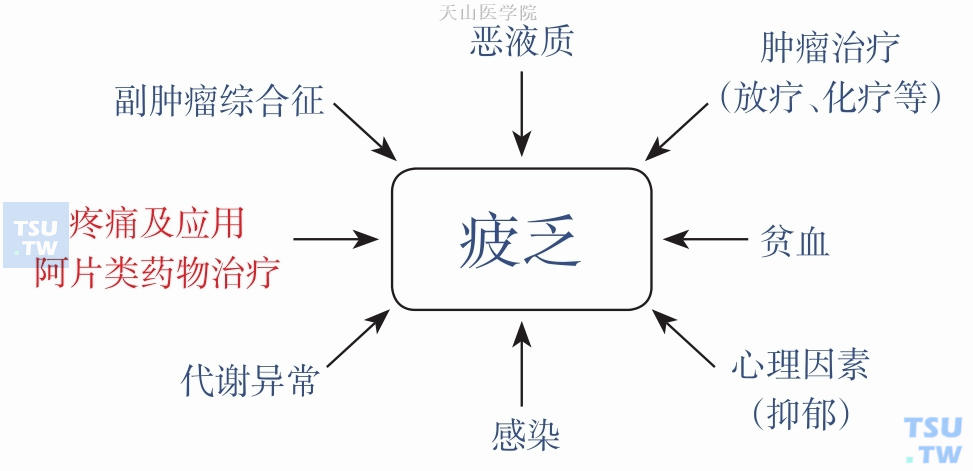
图5-1-3 引起晚期癌症患者疲乏的原因,疼痛及阿片类药物治疗为原因之一
2. 疼痛对恶液质患者体内炎症因子的影响
慢性癌痛的持续存在常常导致神经损伤,进而引起或加重神经病理性疼痛。而各种炎症细胞因子在神经病理性疼痛中发挥着重要作用。研究显示,各种炎症因子的分泌增加,如TNF、IL-1β、IL-15 和IL-6等不仅能提高机体对疼痛的敏感性,还产生对镇痛药物的抵抗性。而恶液质患者本身体内就存在各种炎症介质的紊乱状态,疼痛存在进一步加重了这种状态,也导致药物治疗效果下降。
镇痛药物对恶液质患者的影响
阿片类药物是晚期肿瘤患者镇痛治疗的主要药物。阿片类药物引起恶心、呕吐、便秘、神经精神症状等副作用,若处理不及时,则将进一步影响患者进食,加重患者的营养不良、乏力、贫血等相关症状,从而加重恶液质状态,使患者病情进一步恶化。图5-1-4为肿瘤患者呕吐症状常见的病因。
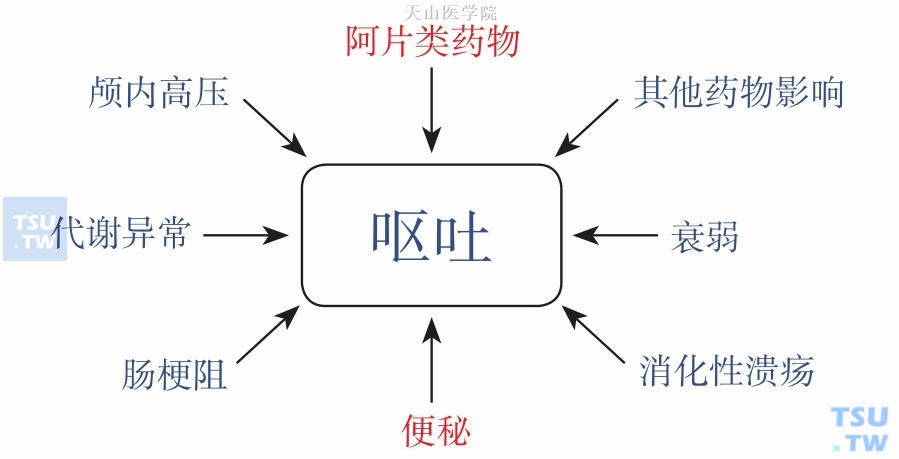
图5-1-4 引起晚期癌症患者呕吐的原因,疼痛治疗药物为原因之一
小结
晚期肿瘤患者中有70%~90%患者发生疼痛,疼痛的原因是躯体因素和社会因素共同作用的结果。根据疼痛发生的病理生理学机制将疼痛分为伤害感受性疼痛和神经病理性疼痛,根据发作的时间分为急性疼痛、慢性疼痛,根据疼痛的强度分为轻度、中度、重度疼痛等。急性疼痛的发生机制就是疼痛形成的神经传导基本过程。而慢性疼痛的机制包括初级感觉神经元兴奋性异常增加、受损神经异位电活动、痛觉传导离子通道和受体异常、中枢神经系统重构。且疼痛对恶液质患者的其他相关伴随症状、体内炎症因子的分泌具有相互影响。同时疼痛治疗的阿片类药物也会对恶液质患者产生影响。
思考题答案
1. 患者近6个月体重下降10kg,目前体重仅为45kg,6个月内体重下降为18.2%,超过5%的体重下降标准。且目前体质指数为17.14,小于中国人18.5的低限,故其恶液质诊断是明确的。且患者目前几乎全部时间卧床,KPS评分为20分,进食极少,预期生存期小于3个月,故为恶液质难治期。
2. 患者的疼痛病因较复杂,从躯体因素讲,局部胰体尾肿瘤和肝门区,脊柱旁多发的淋巴结肿大浸润周围胃壁、肝门、胆管和腹腔神经丛。还有多发肝转移引起的右上腹胀痛。此为肿瘤直接侵犯导致的疼痛。还有长期卧床,臀部压疮、严重便秘导致的排便痛,此均为肿瘤相关合并症导致的疼痛。而心理因素包括患者长期病痛引起焦虑,严重失眠均会加重上述疼痛。
3. 患者的疼痛从机制上进行分类,考虑一方面为局部肿瘤压迫浸润所致的伤害感受性疼痛和侵犯腹腔神经丛导致的神经病理性疼痛。同时压疮的疼痛和排便痛均为伤害感受性疼痛。从时间上讲患者疼痛超过3个月,属于慢性疼痛。从强度上讲,已经严重影响睡眠为重度痛,当然具体的疼痛程度评估要依赖于第九章详细讲述的疼痛的治疗。
(王楠娅 李薇)
