从骨质疏松高风险对象中筛查骨质疏松症
PMOP的流行特点是:
- 发病风险与发病率随增龄而增加;
- 女性(尤其是老年女性)的发病率明显高于男性(3~6倍);
- 患病率存在明显的种族差异和家族差异;
- 腰椎骨质疏松最多见,而髋部骨质疏松导致的骨折后果最严重;
- 发病率与经济社会地位无明确关系。
出现下列临床情况时,提示PMOP可能:
- 绝经后和双侧卵巢切除后或合并性激素缺乏;
- 不明原因的慢性腰背疼痛;
- 低体重或过度肥胖;
- 身材变矮或脊椎畸形;
- 长期应用某些药物(抗惊厥药、抗酸药、驱钙性利尿剂、糖皮质激素等);
- 脆性骨折个人史或脆性骨折家族史。
根据WHO标准确立骨质疏松诊断
BMD测定
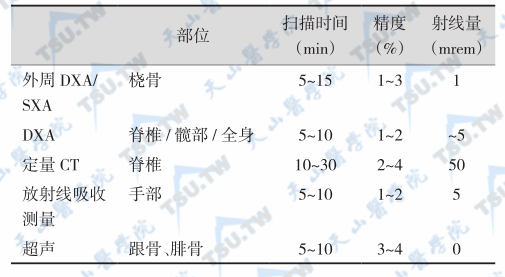
测量骨密度的方法较多,应根据需要和条件选择合适的测定方法,一般推荐使用双能X线骨吸收法(DXA)测量,各种方法的技术参数见下表。
BMD测定技术参数
我国的骨质疏松防治指南建议的DXA骨密度测量人群对象是:
- 女性65岁以上和男性70岁以上者;或女性65岁以下和男性70岁以下且有一个或多个骨质疏松危险因素者;
- 有脆性骨折史或(和)脆性骨折家族史的成年人;
- 各种原因引起的性激素水平低下的成年人;
- X线摄片已有骨质疏松改变者;
- 接受骨质疏松治疗和进行疗效监测者;
- 存在影响骨代谢疾病或使用影响骨代谢药物史;
- IOF骨质疏松一分钟测试题结果阳性者;
- OSTA≤-1者。
骨质疏松的诊断需根据BMD测定结果,首先确定属于低骨量(osteopenia,低于同性别正常人群的峰值骨量的1~2.5SD)、骨质疏松(osteoporosis,低于峰值骨量的2.5SD以上)或严重骨质疏松(骨质疏松伴1处或多处自发性骨折);然后,再明确是原发性骨质疏松或继发性骨质疏松,继发性者应找到原发病因(1个或数个)。诊断为低骨量或骨质疏松后,还应对发生骨折的概率作出判断和预测。用WHO专家组的标准诊断骨质疏松时,需注意以下几点:
一、T值和骨折阈值应用
T值=(测得的BMD-正常人群峰值BMD)/(正常人群峰值BMD的标准差),主要用于评价围绝经期、绝经后妇女和50岁以上男性BMD与正常人群的差异。
用T值(T-Score)表示骨量时,T在-1.0以上为正常,-2.5<T<-1.0为低骨量,T在-2.5以下为骨质疏松。测定部位的BMD对预测该部位的骨折风险价值最大,如腰部的骨折危险性用腰部BMD预测最有意义。用DXA仪测定的BMD受骨组织退变、损伤、软组织异位钙化和成分变化以及体位差异等的影响,使其产生一定偏差,而且还受仪器的精确度及操作规范程度影响。因此,应用DXA要严格按照质量控制要求[参考国际临床骨密度学会(ISCD)共识意见]。临床上常用的推荐测量部位是腰椎1~4和股骨颈,诊断时要结合临床情况进行分析。通过T值切点能够诊断出具有较高骨质疏松风险的患者。
也可用“骨折阈值”(fracture threshold)来判断。一般用峰值骨量或正常成人BMD的2SD作为骨折阈值。但骨折阈值主要是用来预测某个体发生骨折的概率大小,因为作为诊断标准时,正常与非正常值的重叠程度高、误差大。而且已有脆性骨折者的BMD和T值不能作为诊断标准,骨质疏松的诊断标准要适当放宽,或者凭骨折即可诊断。
Z值=(测得的BMD-同年龄正常人群BMD)/(同年龄正常人群BMD的标准差),主要用于评价50岁以下男性和绝经前女性BMD与正常人群的差异。此外,骨量减少或骨质疏松者是否发生骨折还与其他许多因素有关,这些因素可统称为“骨的生物质量”因素。最近,WHO将T值定为≤峰值骨量的2.5标准差,以期与骨质疏松的诊断吻合。
二、建立BMD参考值范围
近年来,国际骨质疏松基金会(IOF)建议采用DXA测得的髋部BMD作为诊断标准,其中T值的参考值范围应以NHANES Ⅲ(National Health and Nutrition Examination Survey)为基础。一般东方人群的BMD低于西方人群,但在用身高和骨面积校正后,两类人群的BMD几乎相同。因而,建议采用体积BMD(vBMD)来代替通常的面积BMD(aBMD)。aBMD是目前诊断的主要工具,ISCD指出,aBMD难以反映骨的三维结构,而外周定量CT(peripheral quantitative computed tomography,pQCT)可非创伤性检测骨的三维结构,男性的骨小梁厚度、骨小梁容量和骨组织容量(TBV/TV)高于女性。由于高转换和基本多细胞单位的骨吸收增加,女性的小梁骨容量随增龄而减少。
诊断骨质疏松应该选用能较好反映小梁骨BMD的部位,如脊椎正位或侧位。为了追踪病情或需了解外周的BMD情况,可选用价廉的SPA、QUS等方法;如要重点了解骨的微结构可选用QCT或QMR;如要了解骨强度可选用QUS。但SPA、QUS、QCT或QMR不用于骨质疏松的常规诊断。
三、测量部位
各部位的BMD变化存在明显的不一致性,如脊椎以腰部最易发生骨量减少或骨质疏松,其次为股骨Ward三角区和桡骨。跟骨骨密度除了随年龄变化外,也受身高、体重及体重指数的影响。当这些部位已有骨质疏松时,其他部位可仍正常或仅有轻度异常。而且,在同一个体左、右侧的改变亦不一致,这说明诊断骨量减少或骨质疏松时要注明部位和程度,某一部位的BMD难以代表全身的整体骨量情况。我们发现,60~64岁组各部位骨量比峰值骨量平均减少(28.3±7.4)%,Ward区和腰椎侧位中间区的减少最多(分别减少46%)。70岁以前的老年妇女腰椎侧位是诊断骨质疏松的敏感部位,随年龄增长股骨和桡骨的骨质疏松检出率迅速增高。因此,老年妇女不同骨骼部位骨丢失方式和丢失率存在明显差别。
腰椎侧位测量可排除脊椎后棘突/横突/椎弓根的干扰。测量腰椎侧位BMD的优点是:①排除腹主动脉钙化、腰椎小关节退行性变、椎间盘钙化、Schmorl结节及骨刺等的干扰;②椎体是发生骨质疏松性压缩骨折的好发部位;③椎体侧位BMD测量更能反映骨松质及椎体骨量的实际变化。
四、不同DXA仪的数据换算
经线性回归方程进行数据换算的公式分别为:BMD:Hologic值=0.802×Lunar值+ 0.318(r=0.991;P<0.001;SEE=0.03g/cm2);BMC:Hologic值=1.20× Lunar值+1.685(r=0.984;P<0.001;SEE=0.816g);BA:Hologic值= 1.414×Lunar值-1.647(r=0.972;P<0.001;SEE=0.520cm2)。因此,在临床应用中不同DXA仪之间存在灵敏度、精密度、准确度以及测量结果绝对值方面的差异,两仪器之间的数据不能互用,但可用回归方程进行数据校正,从而得出骨质疏松诊断的标准化骨密度参考值。
五、DXA仪测量的缺点
DXA的主要缺点是不能测得真实的骨密度,而且无法将皮质骨和小梁骨区别开来;另外,椎体压缩性骨折后,用DXA仪所测定的BMD呈假性升高,掩盖骨质疏松真相。用pQCT测量桡骨超远端BMD,可得到总体骨密度(BD)、小梁骨骨密度(TBD)、总体的骨矿含量(BC)、小梁骨骨矿含量(TBC)、皮质骨骨密度(CBD)、皮质骨骨矿含量(CBC)。当BMD测量与临床诊断不符时,为了明确骨病变性质,应进一步做骨扫描、骨活检组织形态计量及QCT、μCT、QMR等检查。
骨质疏松分类和鉴别
根据影像特征,可将BMD降低分为单纯性骨质疏松、单纯性骨质软化、混合型骨质疏松(骨质疏松合并骨质软化、骨质疏松合并骨质软化和骨质硬化)。
一、X线摄片
可观察骨组织的形态结构,是对骨质疏松所致骨折进行定性和定位诊断的较好方法,也是骨质疏松与其他疾病进行鉴别的主要途径。常用摄片部位包括椎体、腕部、掌骨、跟骨和管状骨等。因受多种技术因素影响,用X线摄片法诊断的敏感性和准确性较低,只有当骨量下降30%以上才可以在X线摄片显现出来,故对早期骨质疏松诊断的意义不大。
早期骨质疏松表现为非应力部位的骨小梁变细、减少、稀疏,一般以椎体、股骨颈、股骨髁及其他骨端关节面下的骨小梁更明显。非应力骨小梁在上述部位一般与关节面平行,而承力骨小梁多与关节面垂直。随着非应力骨小梁吸收,承力骨小梁呈代偿性增粗。正常骨松质由于多方向交织骨小梁形成的网状结构消失,使与关节面垂直的承力纵向骨小梁在照片上显示得特别清晰而明显。随后,承力骨小梁亦受累,表现为纵向骨小梁数量减少、稀疏,部分区域的骨小梁完全消失,骨密度减低犹如软组织。如骨小梁呈非均匀性吸收,其中可见散在分布的1至数毫米大小的点状透光区。在椎体,骨小梁减少多开始于椎体的中央区域,随后向椎体四周扩展。表现为椎体中央区的透光区逐步扩大。严重者,椎体内骨小梁可完全消失,残存的椎体轮廓呈“画框样”。骨皮质变化往往晚于骨小梁,表现为厚度变薄、分层、疏松化,最终可呈细线状,但其边缘仍清晰,骨的轮廓类似铅笔勾画状。同时获取口腔与颌面骨的X线片,能明显提高骨质疏松的早期诊断率。
二、其他影像检查
CT/MRI可确定骨折部位、类型、移位的方向和程度,对骨折诊断和治疗有重要价值。合理的CT 和MRI检查对椎体骨折、微细骨折显示,尤其在鉴别诊断方面有较大价值;CT三维成像能清晰显示关节内或关节周围骨折;MRI检查对鉴别新鲜和陈旧性骨质疏松性椎体骨折具有较大意义。
由于骨折本身和骨折后治疗的疗效评价很困难,目前定量评估宏观骨脆性的方法主要是DXA和容积QCT(volumetric QCT),应用高分辨CT(high-resolution CT)、微CT(microCT)、高分辨MRI(high-resolution MR)和高分辨微MRI(high-resolution microMR)评估微结构。
骨髓内水肿或出血导致骨髓信号异常,需要与其他原因所致的病理压缩骨折鉴别。骨质疏松性椎体压缩骨折后,其压缩的椎体后上角呈尖角状突入椎管内,T1WI椎体终板下呈带状低信号或除椎体后角外全椎体低信号。肿瘤所致的压缩骨折椎体形态不规则,椎体前、后径变长,椎管内、外常见到软组织肿块,异常信号为局限结节状、不规则形或全椎体受累并累及椎弓根。此时应首选MRI,以鉴别肿瘤脊椎转移或肿瘤相关性骨质疏松性脊椎骨折。
三、骨显像
主要用于轻微椎体压缩和嵌顿骨折与不移位肋骨骨折的诊断。骨显像对轻微的椎体压缩、嵌顿骨折和不移位肋骨骨折较敏感,表现为骨折局部的线性、卵圆形或梭形放射性浓集。骨显像对平片难以确认的骨折也有鉴别意义。骨质疏松患者伴急性或慢性背痛时,特别是X线平片示椎体呈楔形变者,如骨显像正常,可排除近期骨折。
辅助检查鉴别骨质疏松的病因与并发症
通常采用排他法鉴别各种类型的原发性与继发性骨质疏松,诊断流程见下图。
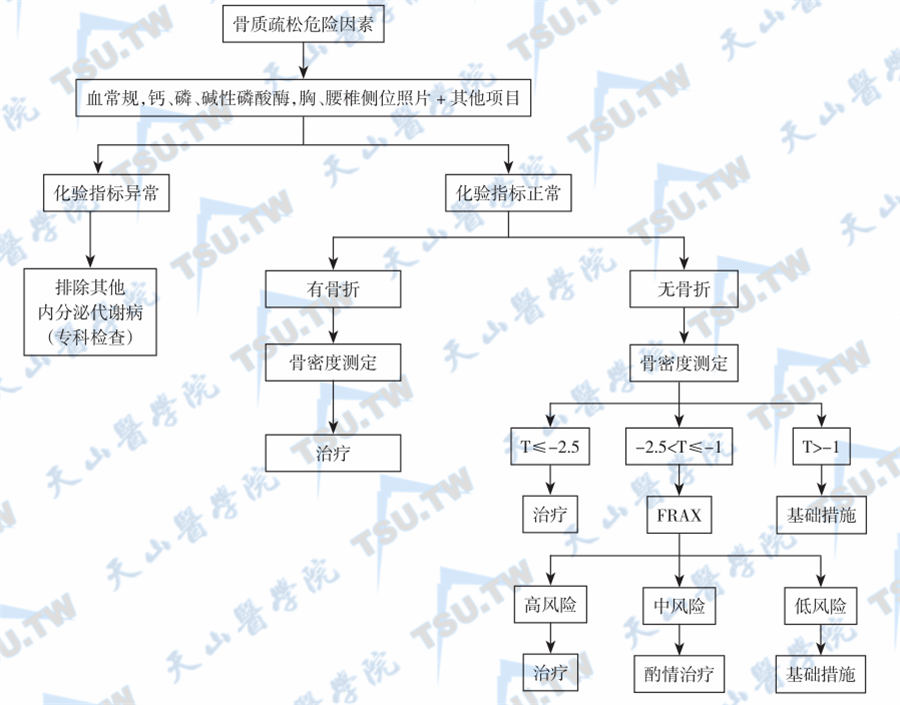
骨质疏松的诊断流程
在排除非骨质疏松性代谢性骨病后才能根据BMD测定结果诊断PMOP,而其他代谢性骨病的排除方法主要是从3种临床情况着手,它们是高钙血症、低钙血症和骨密度减低。绝大多数情况下,血钙正常的代谢性骨病主要表现为骨密度降低,极少数表现为骨密度增高。尿钙、磷、镁,血磷、镁和其他生化标志物(biochemical markers)异常均应与高钙血症、低钙血症或骨密度减低结合起来分析,以便进行诊断和鉴别诊断。为了进一步鉴别诊断的需要,可酌情选择以下检查:血沉、性腺激素、25-(OH)D、1,25-(OH)2D、甲状旁腺素、尿钙、磷、甲状腺功能、皮质醇、血气分析、血和尿轻链、肿瘤标志物、甚至放射性核素骨扫描、骨髓穿刺或骨活检等。
如果患者存在高钙血症(hypercalcemia),可以排除原发性骨质疏松的可能性。高钙血症是一种临床代谢紊乱综合征,其发病原因多种多样,且易被原发疾病所掩盖。另一方面,有的患者仅有血钙升高而缺乏原发病表现,发现和确定无症状性高钙血症是临床诊疗工作的重点与难点。高钙血症的主要病因为原发性甲旁亢和非甲状旁腺恶性肿瘤,而结节病、淋巴瘤、急性胰腺炎、器官移植后常引起轻至中度高钙血症。血钙升高时,要首先排除非疾病因素,最好同时测定血总钙、离子钙、血磷和PTH(或PTH1-84/PTH-C比值);有条件时加测PTHrP,然后进行进一步检查与鉴别。
引起低钙血症(hypocalcemia)的病因以甲旁减、严重缺镁、VD缺乏、使用某些抗肿瘤药物常见,低钙血症主要分为甲状旁腺相关性、VD相关性、钙沉积过多、螯合钙作用类型。
骨密度降低分为代谢性BMD降低和破坏性BMD降低两种,前者属全身性改变,主要包括骨质疏松(osteoporosis,OP)和骨质软化;后者为局部表现,其主要原因为骨质破坏(如肿瘤、血管瘤、囊肿、血肿)或骨组织炎症(坏死/纤维化)。虽然80%以上的全身性BMD降低是由原发性骨质疏松症引起的,但BMD降低亦可见于许多其他疾病或疾病阶段。因而,BMD降低是一种临床表象,不等于骨质疏松诊断中的低骨量(osteopenia)术语。
PMOP并骨质软化
PMOP合并骨质软化的情况并不少见,这可能是我国PMOP的特点之一。骨质软化的原因主要是VD不足或缺乏,个别病例可能与肾功能障碍有关,因为血清25-(OH)D或1,25-(OH)2D往往降低。PMOP合并骨质软化的临床特点是:①存在引起VD不足(独居、户外活动少、饮食不当、慢性肝病等)或慢性肾病(肾炎、肾病综合征药物性肾损害等)病史;②BMD降低更明显;③血清25-(OH)D 或1,25-(OH)2D降低;④血清总钙正常或轻度降低,血清离子钙降低;⑤抗骨质疏松药物治疗的效果较差。
内分泌与代谢疾病
主要包括:①甲旁亢;②Cushing综合征;③甲亢;④性腺功能减退症;⑤高PRL血症;⑥糖尿病;⑦GH瘤;⑧妊娠。甲旁亢者的骨骼改变主要为纤维囊性骨炎,早期仅有骨质疏松表现,测定血PTH1-84/PTH-C比值、血钙、血离子钙和血磷一般可予排除。仍有困难者应行特殊影像检查或动态试验。其他内分泌疾病因原发病表现较明显,鉴别不难。
血液系统疾病
主要见于血液系统肿瘤,如多发性骨髓瘤、淋巴瘤等。
一、浆细胞病
多发性骨髓瘤是一种以骨髓中单克隆浆细胞大量增生为特征的恶性疾病。临床症状以贫血、骨骼疼痛或溶骨性骨质破坏、高钙血症和肾功能不全为特征,多发于中、老年人,中位发病年龄约为65岁。男、女发病比例为3∶2。大部分患者慢性起病,早期可无症状,随着疾病进展,骨髓瘤细胞负荷或(和)M蛋白水平逐渐增加,出现骨骼破坏、贫血、肾功能不全、高钙血症、发热与感染、出血倾向、骨髓外浸润、淀粉样变性、多发性周围神经病变和高黏滞综合征等表现。骨髓象的最明显特征是浆细胞数量和质量异常。骨髓瘤细胞形态不一,成堆出现。典型的瘤细胞为未成熟、分化较差的浆细胞,其形态为多核,核圆形或不规则,核膜内陷,核内可见空泡,染色质稍疏松,不呈车轮状排列,核仁大而明显。少数病例可见浆母细胞,称为浆母细胞骨髓瘤。流式细胞术(flow cytometer,FCM)可以检测浆细胞标记指数(plasma cell labeling index,PCLI),即测定处于S期的单克隆浆细胞占所有单克隆浆细胞的百分比。80%的患者有骨骼损害,脊柱、肋骨、头颅、肩胛、骨盆和长骨近端最常被累及。X线摄片表现为骨质疏松、溶骨性损害和病理性骨折;典型的圆形或卵圆形穿凿样透亮缺损,边缘清晰,一般不伴新骨形成。病理性骨折常发生于肋骨和脊柱。对于临床上高度怀疑有骨病的患者,如果常规X线检查不能确定或为阴性,可选择CT平扫,MRI或PET/CT或99mTc-骨扫描检查。
二、其他血液系统疾病
主要包括系统性肥大细胞增多症、白血病、淋巴瘤、Gaucher病等。局限性骨病变伴骨吸收指标明显升高时,要想到血液系统疾病可能。有时,血液系统肿瘤的骨损害类似于甲旁亢,需要用血PTH及其组分和PTHrP、肿瘤特异标志物鉴别。
肿瘤相关性骨质疏松的诊断主要依靠骨髓穿刺和骨活检,非血液系统肿瘤骨转移时,除了确认原发肿瘤(如肺癌、乳腺癌、前列腺癌、肠癌等)病灶外,骨骼转移往往是引起骨质疏松的另一个重要原因,因此需要寻找和肿瘤骨转移的证据。常用的影像检查见下表,其中皮质骨和松质骨的X线照片与CT检查主要是确定骨骼病灶,CT与MRI可发现骨髓与骨肿瘤,骨扫描和SPECT可了解骨代谢变化而PET主要用于评价肿瘤的糖代谢状况。旁癌综合征、肿瘤骨转移与化疗所致骨质疏松的鉴别见下表。
肿瘤相关性骨质疏松的影像诊断方法
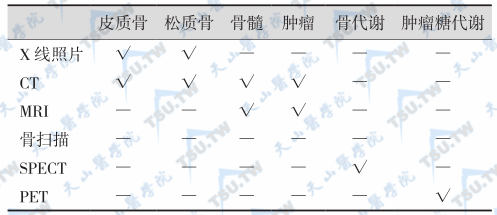
注:√表示有意义;—表示无意义或意义有限
三种肿瘤性BMD降低的鉴别

结缔组织疾病
主要包括:①成骨不全;②Ehlers-Danlos综合征;③Marfan综合征;④同型半胱氨酸血症和赖氨酸血症;⑤Menkes综合征。成骨不全的骨损害特征是骨脆性增加,多数是由于Ⅰ型胶原基因缺陷所致,其临床表现依缺陷的类型和程度而异。轻者可仅表现为骨质疏松而无明显骨折,必要时要借助生化或分子生物学方法鉴别。此外,蓝色巩膜有重要鉴别意义。另一方面,当患者应用糖皮质激素后可合并皮质激素性骨质疏松,应注意鉴别。
局限性游走性骨质疏松
局限性游走性骨质疏松(regional migratory osteoporosis,RMO)是下肢负重关节的一种游走性关节痛,属于痛性营养障碍综合征(algodystrophy syndromes)的范畴。RMO的病因未明,与全身性骨质疏松相关。有一部分髋部暂时性骨质疏松(transient osteoporosis of the hip,TOH)患者同时伴全身性骨质疏松,TOH与RMO密切相关,近来两者被归入暂时性骨质疏松(transient osteoporosis)一类。TOH被认为是无血管性髋关节坏死(avascular necrosis of the hip,AVN)前的一种可逆阶段。TOH在妇女妊娠的后3个月常见,其X线征象和MRI征象类似于RMO。RMO常以急性或逐渐加重的关节痛起病,该疼痛与创伤无关;随负重而加重,起病2个月时达到高峰,不能行走。3~9个月后症状消失,但症状可在邻近关节,有时甚至在同一关节再现。体查可有关节渗出伴局部发热、触痛广泛而程度中等,同时有肌肉萎缩。中等活动受限,有时伴肢端疼痛。功能损害和有限的临床表现之间的差异具有特异性。症状发生3~6周时,传统X线照片显示中等至严重关节周围骨质疏松,关节间隙存在,在受累关节X线照片上出现骨质疏松,骨显像有放射线吸收增加,该征象可预测受检关节是否会发生RMO。骨活检显示局部骨质疏松,关节滑液组织学检查提示慢性非特异性炎症反应。实验室检查改变常不显著。
肝素所致的骨质疏松
低分子量肝素(low-molecularweight heparin,LMWH)是从未分离肝素(unfractionated heparin,UFH)中提取的单组分肝素,分子量3600~6500Da,其目的是克服UFH的多聚体现象,更有利于疾病治疗。LMWH是预防和治疗血栓栓塞性疾病的最佳药物,尤其适合于妊娠期妇女,因为LMWH还有较良好的抗补体和防治抗磷脂综合征(antiphospholipid syndrome,APS)作用。应用肝素抗凝的其他情况有复发性妊娠失败(recurrent pregnancy loss,RPL)、变态反应、维生素K拮抗剂所致的出血倾向、肿瘤、急性冠脉综合征等。
UFH和LMWH降低骨形成率,增加骨吸收。但目前LMWH对骨代谢的影响机制仍不明了,甚至对LMWH能否引起骨质疏松仍存在不同看法,但LMWH对骨形成的不利影响是事实。
女运动员三联症
女运动员三联症(female athlete triad,FAT)包括节食、闭经和骨质疏松。FAT可发生于从事任何形式运动的运动员,但以需要瘦身和体形的运动员最常见,这些运动包括体操、芭蕾、跳水和运动型演员等。一般表现为青春期发育延迟,黄体功能缺乏,月经稀少或无排卵,与运动过度有关,称为运动相关性女性生殖功能紊乱(exercise-related female reproductive dysfunction,ERFRD),其病因未明确。
幼年型透明性纤维瘤病
幼年型透明性纤维瘤病(juvenile hyaline fibromatosis,JHF)少见,常染色体隐性遗传。儿童和青少年发病,其特点是皮肤与其他组织的非结晶性透明样物质沉积,常伴有低骨量/骨质疏松。
其他继发性骨质疏松
肾疾病主要包括:①慢性肾炎;②慢性肾病;③慢性肾衰;④肾移植。药物引起的骨质疏松主要包括:①糖皮质激素;②肝素;③抗惊厥药物;④环孢素;⑤GnRH类;⑥抗肿瘤药物。制动和失用性骨质疏松主要包括:①肢体瘫痪;②手术后长期制动;③关节功能障碍。营养不良和胃肠疾病主要包括:①吸收不良综合征;②不经肠营养;③胃切除;④肝胆疾病。
几种易与PMOP混淆的继发性骨质疏松的鉴别要点见下表。在临床上,有时原发性与继发性骨质疏松也可同时或先后存在。
原发性与数种继发性骨质疏松的鉴别

注:↓:下降;↑:升高;↑↑明显升高;↓↓:明显下降;→:正常;括号内表示较少发生的变化
根据年龄鉴别不同类型的原发性骨质疏松症
原发性骨质疏松症分为特发性青少年OP、绝经后OP、老年女性OP和老年男性OP四类。在临床上,该四种类型的骨质疏松症凭年龄即可区分,一般不存在鉴别诊断问题。但是,有下列三点值得特别关注。
各型原发性骨质疏松的重叠
特发性青少年OP和绝经后OP与老年性OP有时存在重叠现象。例如,65岁以上的女性骨质疏松患者应了解既往有无特发性青少年OP或绝经后OP及其治疗预后情况;如果以前的骨质疏松已经治愈,则患者仅可诊断为老年性骨质疏松症。又如,65岁以上的男性骨质疏松患者应了解既往有无特发性青少年OP及其治疗预后情况;如果以前的骨质疏松已经治愈,则患者仅可诊断为老年性骨质疏松症。
各型原发性骨质疏松症的临床特征
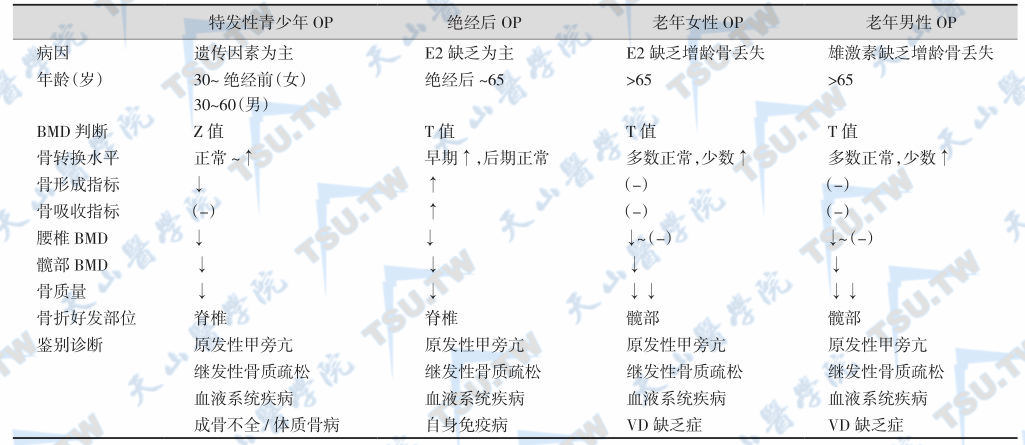
不同类型原发性骨质疏松症的病理生理、临床特征和治疗是不完全相同的。
四种原发OP的鉴别要点
原发性骨质疏松合并继发性骨质疏松症或其他骨代谢异常
原发性骨质疏松症患者常可合并有多种代谢性骨病,其中常见的合并症是维生素D缺乏/不足、继发性骨质疏松症和肾性骨病,不少绝经后骨质疏松症患者的预防和治疗没有达到控制疾病发展的目的,进入老年期后,往往在原有骨质疏松的基础上,因增龄性骨丢失而使病情加重。原发性OP常见合并症的鉴别见下表。

根据BMD/遗传因素/生化标志物评估骨折风险
用危险因素模型的斜率(gradient β)拟合骨折研究资料,模型显示,骨折风险随着Z值下降而呈指数上升,其结果通常用相对危险度(relative risk,RR)表示;RR是指Z值每降低1个单位所增加的骨折风险。RR的最重要意义是预测骨折风险。在大样本人群中,正常人的Z值分布近似于高斯曲线(Gaussian curve),发生骨折者的Z值分布组成另一条高斯曲线,两条曲线的标准差相同,两线的最大偏离度即是与斜率β相等的ΔZ,即RR的自然对数;这种现象可用数学式表示为:ΔZ=β=ln(RR)。
骨质疏松是一种多因素疾病综合征,每个人的易感性不同,因此对个体进行骨质疏松和骨折风险评估能为防治提供依据。临床上评估骨质疏松风险的方法较多,这里推荐以下几种方法:
国际骨质疏松症基金会(IOF)骨质疏松症风险1分钟测试
测试内容有:
- 是否曾经因为轻微的碰撞或者跌倒就会伤到自己的骨骼?
- 父母有无轻微碰撞或跌倒就发生髋部骨折的情况?
- 经常连续3个月以上服用“可的松、强的松”等糖皮质激素类药品吗?
- 身高是否比年轻时降低了(超过3cm)?
- 经常大量饮酒吗?
- 每天吸烟超过20支吗?
- 经常患腹泻吗?(由于消化道疾病或者肠炎而引起)
- 您是否在45岁之前就绝经了?
- 是否曾经有过连续12个月以上的闭经(怀孕期除外)?是否患有阳痿或者缺乏性欲这些症状?如果有一题的回答结果为“是”,即为阳性。
亚洲人骨质疏松自测指数
亚洲人骨质疏松自测指数(osteoporosis risk assessment tool for Asians,OSTA)基于亚洲8个国家和地区绝经后妇女的研究,在收集多项骨质疏松危险因素并进行骨密度测定的基础上,从中筛选出11个与骨密度具有显著相关的风险因素,再经多变量回归模型分析,得出年龄和体重两项简易筛查指标,其计算方法是:(体重-年龄)×0.2。如患者的体重为50kg,年龄为70岁,则其骨质疏松风险=(50-70)×0.2=-4;评价的标准是:<-1为低度风险;<-1~-4为中度风险;<-4为高度风险。此外,也可以通过图表,根据年龄和体重进行快速评估。
由OSTA指数可知,“瘦老太太”的骨质疏松风险肯定很高。在临床上,衰老多病者的确是如此,但是这等于所有的“瘦老太太”都很容易发生骨质疏松,肌肉发达、精力充沛、无骨折家族史而青壮年期健康者的BMD可能较低,但骨折风险要比衰老多病者低得多。另一方面,因为肥胖并非骨健康的保护因素,肥胖者不等于没有OP,而过度肥胖同样导致骨折而BMD正常,所以“胖老太太”亦是骨质疏松性骨折的高风险对象。此外,男性和女性老年人的BMD降低速度并不一致,女性明显快于男性,男性80岁时降低约30%,女性在50%以上。男、女性70~80岁后的BMD下降可能并不明显,而骨折发生率与年龄呈级数负相关,这主要是骨质量显著下降所致,因而,单凭BMD难以或不能预测骨折风险和药物疗效。
骨折风险评估算法
为了实施对骨质疏松骨折风险的分层干预,WHO提出了骨折风险评估(fracture riskassessment calculator,FRAX)系统,使用风险因素计分法评估10年内的髋部与其他部位骨折概率。骨折风险预测简易工具FRAX®可以通过以下网址(http://www. shef. ac. uk/FRAX/)获得,见下表。FRAX是一种由单纯BMD扩展到综合因素评估,由群体评估扩展到个体评估和将相对风险扩展到个体绝对风险的较好评估体系,其应用广泛。患者可以在网上下载,根据父母骨折史、年龄、性别、体重指数、种族、吸烟、饮酒、糖皮质激素应用、类风湿关节炎和继发性骨质疏松(有人建议加入“经常摔倒”1项)进行自我测算,该系统适用于未治疗的绝经后妇女和40~90岁的男性。实践证明,FRAX具有简便和易于推广的优点,但忽视了个体差异、遗传因素、PBM、抗骨吸收药物和环境因素的影响,有条件者应尽量进行BMD检查和骨代谢生化标志物测定。
FRAX评估指标

该工具的计算参数包括股骨颈骨密度和临床危险因素。在不能获得股骨颈骨密度数据时,可以由全髋部骨密度取代,然而,在这种计算方法中,不建议使用非髋部部位BMD。在没有骨密度测定条件时,FRAX®也提供了仅用体重指数(BMI)和临床危险因素进行评估的计算方法。
在FRAX®中,明确的骨折危险因素是:①年龄(骨折风险随年龄而增加);②性别;③低骨密度值;④低体重指数(≤19kg/m2者);⑤既往脆性骨折史(尤其是髋部、尺桡骨远端及椎体骨折史)和父母髋骨骨折病史(65岁前的骨折史更有意义);⑥糖皮质激素治疗者;⑦吸烟或过量饮酒;⑧合并引起继发性骨质疏松的其他疾病;⑨类风湿关节炎。由于我国目前还缺乏系统的药物经济学研究,所以尚缺乏根据FRAX结果计算的治疗阈值。如果FRAX®工具计算出的髋部骨折概率≥3%或任何重要部位的骨折概率≥20%(美国),应视为骨折高危患者,而欧洲一些国家的髋部骨折概率≥5%为治疗阈值。
FRAX的适用人群是没有发生过骨折又有低骨量者(T值>-2.5),因临床难以作出治疗决策,使用FRAX工具可快捷计算出骨折绝对风险;或者,根据年龄或BMD测量结果查对骨折风险。适用人群为40~90岁男性和女性,40岁以下和90岁以上的个体可分别按40岁或90岁计算。FRAX的不适用人群是临床上已诊断骨质疏松,即骨密度(T值)低于-2.5或已发生脆性骨折者不必再用FRAX评估。
FRAX中骨折相关危险因素的确定基于来自全球(包括北美、欧洲、亚洲、澳洲等多个独立)的大样本前瞻性人群研究和大样本荟萃分析,因此具有共性特征。但FRAX的计算模型中还需要相应国家人群的骨折发生率和人群死亡率流行病学资料验证。由于我国缺乏骨折发生率的流行病学资料,普遍应用时会出现小的偏差,一般这种偏差不会显著影响评估结果。
但是,FRAX工具的缺陷也不少。首先,FRAX的“糖皮质激素使用”不能定量,而糖皮质激素的制剂、人群对象、性别、年龄、使用的途径和方法及疗程均与骨质疏松风险程度相关,大剂量使用还容易合并骨坏死。第二,“父母骨折史”的本意是想反映遗传因素的强度,但FRAX不能排除后天因素的影响;骨折部位也很重要,因为较年轻时发生髋部骨折往往与遗传素质密切相关,而老年期的脊椎压缩性骨折与遗传没有明确关联,可惜FRAX没有涉及。第三,吸烟和饮酒亦缺乏定量概念。既然这些指标缺少定量参数,那么所得出的判断就必然带有主观与客观偏差。第四,FRAX没有包括影响骨质疏松和骨折的其他重要因素,如跌倒、维生素D营养状态、骨转换生化标志物(骨形成指标和骨吸收指标)、骨代谢调节指标(如PTH、血钙、血磷、维生素D、FGF23等),因而FRAX不具备骨质疏松病因鉴别功能。跌倒是发生骨折的重要危险因素,FRAX计算中没有包括跌倒,原因是用来开发这一工具的队列研究数据对跌倒的报告形式不一,难以标准化;而药物干预没有表明减少跌倒可降低骨折危险性,但在临床上避免跌倒显然是预防骨折的有效措施之一。第五,FRAX仅适合于未经治疗的患者,难以反映长骨骨量的股骨颈BMD虽然可代表女性髋部的总体骨量,但男性例外;股骨颈BMD更无法反映骨质量,而高龄患者的脆性骨折与BMD常是分离的,BMD的T值正常或轻度降低的老年人常在不经意中发生脆性骨折,原因是骨质量显著下降。第六,FRAX不能指导治疗,不能提供降低10年内骨折风险的干预途径或具体方案。
椎体骨折评价
椎体骨折评价(vertebral fracture assessment,VFA)可以预测脊椎和其他部位再发骨折的风险(wwww.iscd.org)。
BMD
如BMD低于骨峰值平均值1个标准差以上,即可列为高危人群。髋部BMD预测髋部骨折危险的强度最高,而年龄增强其预测性。同样,亦可根据年龄和髋部BMD 的T值评估5年内的骨折风险。
骨转换生化标志物
骨转换生化标志物(biochemical markers of bone turnover)是骨组织本身的代谢(分解与合成)产物。骨转换标志物分为骨形成标志物和骨吸收标志物两类,前者代表成骨细胞活动及骨形成时的代谢产物,后者代表破骨细胞活动及骨吸收时的代谢产物,特别是骨基质降解产物。在正常人的不同年龄段以及各种代谢性骨病时,骨转换标志物在血循环或尿液中的水平发生不同变化,反映了全身骨骼代谢的动态状况。这些指标的测定有助于判断骨转换类型、骨丢失速率与骨折风险、对了解病情进展、干预措施的选择以及疗效监测等很有帮助。有条件的单位可选择性做骨转换生化标志物以指导临床决策。
常用的骨形成标志物有血清骨源性碱性磷酸酶(B-ALP)、骨钙素(OC)、Ⅰ型原胶原C-端前肽(PⅠCP)和Ⅰ型原胶原N-端前肽(PⅠNP);常用的骨吸收标志物有空腹2小时尿钙/肌酐比值、血清抗酒石酸酸性磷酸酶(TRAP)、血清Ⅰ型胶原交联C-末端肽(S-CTX)、尿吡啶啉(Pyr)、尿脱氧吡啶啉(D-Pyr)、尿Ⅰ型胶原交联C-末端肽(U-CTX)和尿Ⅰ型胶原交联C-末端肽(U-NTX)。在以上诸多指标中,IOF认为Ⅰ型原胶原N-端前肽(PⅠNP)和血清Ⅰ型胶原交联C-末端肽(S-CTX)的敏感性较高。
根据鉴别诊断需要,可检测血、尿常规,肝、肾功能,血糖、钙、磷、碱性磷酸酶、性激素、25-(OH)D和PTH等。但是,这些指标对疾病病因的诊断与鉴别诊断意义不大。骨代谢转换生化标志物测定不能用于骨质疏松诊断,但对骨转换率的评价十分重要。同时,BTM可提供诊断、鉴别诊断和治疗的重要信息。一般在血清25-(OH)D正常前提下,要求将BTM降至正常值的1/2水平。
随着增龄,骨代谢生化标志物与BMD的相关性越来越明显。一般在绝经30年后,骨转换率对BMD的贡献率达50%,骨转换率增加是预测骨折的主要指标。用骨代谢生化标志物来预测骨折风险时,不能用骨折后的测量值来判断,因骨折后制动、骨痂形成和骨折部位的骨转换率增强等可干扰测量结果。OFELY研究发现,骨源性ALP升高和脊柱骨折及非脊柱骨折相关,反映骨吸收的标志物一般均可预测骨折风险。
选择骨代谢生化标志物时不宜单用1个指标来判断骨代谢转换率,一般可选择1~2项分别反映骨形成和骨吸收的标志物。而且,要尽量选择那些较特异而敏感的标志物。例如,血清中存在两种抗酒石酸酸性磷酸酶(TRAP5a和5b)。因TRAP5b来源于破骨细胞,而5a来源于其他细胞,肝素可抑制5a活性而对5b无作用,血清TRAP5b与血、尿中的Ⅰ型C末端前肽、N末端前肽、尿中的游离脱氧吡啶酚有良好的相关性,TRAP5b与BMD呈负相关。因此,血清TRAP5b是反映骨吸收率的较好标志物。又如,确立骨质疏松诊断及治疗前检测骨代谢标志物基础值,一般选用β-CrossLaps或其他骨吸收指标监测抗骨吸收治疗疗效,而用总PⅠNP监测促合成代谢治疗的疗效。治疗3个月后复查上述指标,如果抗骨吸收治疗后,β-CrossLaps明显下降(大于35%~55%)或促合成代谢治疗后总PⅠNP明显上升(大于40%),可继续维持原来治疗,并每6~12个月监控1次;如果抗骨吸收治疗后β-CrossLaps无明显降低,应该重新评价患者的服药依从性和胃肠副作用,调整治疗方案。骨代谢转换标志物的缺点是指标变异较大,季节和昼夜节律变化(最大骨吸收发生在夜间)较明显,骨转换标志物水平在骨折后增加等。
PMOP者的骨吸收指标提示骨转换率轻度升高,而老年患者多为低转换型或正常转换型。但如病因复杂且有多种因素参与发病时,单凭临床资料很难确定其骨转换率类型。高和低的骨转换型骨质疏松的生化特点见下表。但在临床上,一般应结合临床风险因素、BMD和骨转换指标综合评价10年的髋部骨折风险。
高转换型和低转换型骨质疏松的生化特点
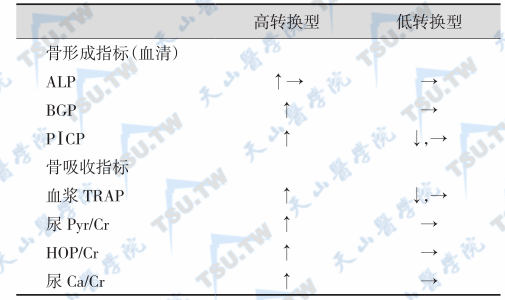
注:ALP:碱性磷酸酶;BGP:骨钙素(osteocalcin);PⅠCP:Ⅰ型前胶原羧基端前肽;TRAP:抗酒石酸酸性磷酸酶;HOP:羟脯氨酸;Cr:肌酐;Pyr:胶原吡啶啉;Ca:钙;↑:增高;↓:降低;→:正常。
高转换型PMOP患者多见于绝经后妇女早期,临床表现隐匿,一般无不适,但实验室检查可发现异常。如果血钙升高(游离钙升高为主),PTH和ALP升高伴骨吸收指标的明显变化,在排除原发性甲旁亢后,这类患者可诊断为“绝经后原发性甲旁亢”(postmenopausal PHPT,PPHPT)。
影像检查与特殊检查协助骨质疏松诊断
X线摄片法
依据X线平片定量诊断骨质疏松的敏感性和准确性较低,X线影像表现骨质疏松时,其骨量丢失可达30%以上,早期诊断的意义不大。但在无任何骨密度和骨测量方法的情况下,X线平片也应视为一种有帮助的评估手段。脊椎侧位X线片是诊断椎体骨折及判定骨折程度的必要方法。X线平片也是鉴别骨质疏松与其他骨代谢疾病及骨肿瘤的必要方法。
长期以来,人们用Genant半定量诊断脊椎骨折,其判断标准是:①1度:椎体高度下降20%~25%;②2度:椎体高度下降25%~40%;③3度:椎体高度下降40%以上。但判断时的主观因素干扰结果,CT/MRI诊断非典型脊椎骨折有独到优点。
定量超声
定量超声(quantitative ultrasound,QUS)是一种利用声波检测BMD的非电离技术,具有简便、无辐射损伤、重复精度较高、价格便宜、便于搬动等优点。通过QUS主要获得两个参数:宽幅衰减系数(broadband ultrasound attenuation,BUA)和超声速度(speed of sound,SOS)。在理论上,QUS不仅能评价BMD,还能提供骨小梁结构,胶原纤维等方面的信息,但是目前并不清楚其对BUA和SOS影响的程度,也没有超声诊断骨质疏松症的统一标准,套用WHO的T≤-2.5SD诊断标准并不合适,其敏感性和特异性均不理想。此外,QUS参数改变还可用于抗骨质疏松治疗疗效评估。
CT与磁共振
定量CT是检测BMD的可选新方法。因为诊断其他疾病的需要,定量计算机断层扫描(quantitative computer tomography,QCT)的应用较多,如能同时观察骨骼变化,对骨质疏松的诊断有很大帮助,可以成为检测BMD的又一可选手段。QCT的原理和DXA一致,即利用数学重建公式分析X线透过目标部位后的衰减程度来获得BMD值。值得注意的是,WHO规定的T≤-2.5SD诊断标准对于腰椎BMD/QCT并不合适,因为成年人BMD/QCT较BMD/DXA随增龄降低更快。QCT相对于DXA或QUS的最大优势是其三维空间分辨率,能测量容积骨密度(volumetric BMD,vBMD)和骨的大体几何结构,并能分别测量皮质骨和松质骨BMD。股骨几何形态复杂,且密度分布不均匀,QCT可以分别对股骨颈、转子间、Wards三角区等区域进行测量,同时获得松质骨及皮质骨BMD。临床实验表明,皮质骨和松质骨BMD对于药物干预有着不同的反应,而且股骨近端皮质骨和松质骨BMD均是预测股骨骨折风险的独立因素。此外,QCT还能排除其他结构(动脉硬化、周围软组织等)对BMD的影响。
容积定量CT(volumetric QCT,vQCT)是QCT的一种,其空间分辨率达到0.5mm,可沿多个方向进行成像。目前,有应用vQCT评价骨质疏松症治疗疗效的研究报道。周围骨定量CT(peripheral QCT,pQCT)是另一种QCT,主要用于周围骨(如桡骨远端和胫骨远端)的骨密度测量。但是,桡骨远端pQCT与股骨或者椎体BMD的关联性不强。平板容量CT系统(flat-panel volume CT systems)结合了CT和数字平板成像技术的长处,类似于螺旋多排CT,却应用了数字平板成像探测器,能提供松质骨的结构信息。
QCT测量BMD最大的局限是部分容积效应。因为其分辨率达不到骨小梁的数量级,所以其测定值是骨骼、红骨髓、骨髓脂肪的总体反映,使得测定的BMD低于实际BMD。双能QCT能消除红骨髓和骨髓脂肪对BMD测定的影响。pQCT与微CT及有限元分析(FEA)结合已经应用于临床病例的诊断,老年人脊椎微CT显示的骨质疏松并不显著时,有限元分析发现其压力变形所需应力显著降低,并用不同的颜色显现,直观而具有定量特征。数字拓扑分析(digital topological analysis,DTA)和容量拓扑分析(volumetric topological analysis,VTA)也得到了迅速发展,但离临床应用还需时日。
在X线片上,当非典型骨折表现为局限性骨皮质增厚而无骨折线时,难以作出诊断,而CT、MRI和99mTc-MDP延迟扫描可见骨膜下水肿、骨皮质增厚或局部摄取增加,有助于早期诊断。
磁共振(magnetic resonance,MR)技术利用强磁场和电磁脉冲序列获取三维影像。松质骨由棒状和层状骨小梁相互连接而成,其周围充满着富含水和脂肪的骨髓组织,从而导致骨和骨髓的磁化率明显不同,在骨-骨髓界面存在着明显的敏感梯度。当前,实验研究和临床研究的热点是通过改变磁场强度、磁场范围、信噪比(signal-to-noise ratio,SNR)、扫描时间、脉冲序列等而获得不同的骨结构信息,实现了MR对活体近端股骨的扫描。更高磁场强度(7-Tesla)系统可对全身进行扫描,有望成为皮质骨多孔性的替代指标。
骨组织形态计量和微结构分析评价骨质量
临床上,说明骨质量(bone quality)的典型例子是骨硬化和成骨不全,虽然BMD正常或升高,但因骨质量差而容易发生骨折。许多研究证实,在女性骨质疏松合并骨折患者中,超过1/2的BMD都高于WHO骨质疏松诊断标准中的BMD参考值(-2.5≤T值≤-1);Kanis等发现,与同样BMD的青年人群相比,老年骨质疏松性骨折的发生率高出10倍以上。同样,在抗骨质疏松的药物治疗中,抗骨吸收药物降低骨折风险的程度与BMD增加没有相关,即少量提高BMD就能大幅降低骨折发生率。这些事实说明,骨质量(尤其是老年人群的骨质量)是决定抗骨折性能的关键因素。骨质量可用骨强度表示,即骨强度=骨质量+BMD。但是,骨质量的多数评价指标仍处于研究阶段。
微结构分析分为离体和在体两种。离体微结构分析的方法主要有骨组织病理形态、骨组织形态计量分析和激光扫描共聚焦测量;在体微结构分析主要有QCT、QMR和QUS等。除进行微结构和生物力学分析外,这些分析仪器亦可直接或间接测出BMD值。
骨组织形态定量分析
当临床怀疑为骨质软化、骨质疏松-骨质软化症(osteoporomalacia)、骨质硬化佝偻病(osteopetrorckets)、变形性骨炎或血液系统疾病时,应尽量进行此项检查,以详细了解骨组织的超微结构和组织化学特征,得到静态与动态的组织形态计量学资料。老年性骨质疏松的骨小梁数目减少、骨小梁平均宽度下降、骨小梁彼此分离,平均骨壁厚度下降,骨髓中细胞数减少,脂肪组织增多;但是,骨矿沉积率和类骨质沉积速率一致,且骨细胞周围矿物质无明显减少。PMOP者的骨形态计量根据其类型不同而有明显差别。
在体骨微结构测量
用高分辨影像技术可以间接地分析骨的微结构变化,对指导临床治疗有一定价值。但在病例和测量方法选择上要慎重。
