肿瘤对宿主的作用
肿瘤对宿主的作用表现在多个方面,如肿瘤细胞直接消耗能源物质,肿瘤的机械作用压迫相邻器官组织或堵塞消化道,肿瘤分泌相关肿瘤因子影响宿主,前两个内容已经在第一章讨论,本节主要讨论肿瘤因子。图4-2-1简述了肿瘤对宿主的作用。
肿瘤细胞产生的因子大致分为两类:细胞因子及代谢因子。细胞因子又分为致炎细胞因子(proinflammatory)、抑炎细胞因子(antiinflammatory);代谢因子又称致恶液质因子(procachectic factors)。致炎细胞因子如IL-1β、IL-6、TNF-α,诱导炎症反应,抗御外来损伤,但是过激的炎症反应同时损伤了机体(宿主);抑炎细胞因子如IL-4、IL-10,抑制过激的炎症反应,保护机体免受炎症反应损伤,但是,客观上保护了肿瘤细胞免受损伤,使肿瘤细胞逃避了宿主的免疫杀灭作用。生理条件下,致炎细胞因子与抑炎细胞因子处于平衡状态,构成机体的正常防御功能。肿瘤条件下,二者的平衡被破坏。代谢因子主要是指蛋白水解诱导因子(proteolysis-inducing factor,PIF)及脂肪动员因子(Lipid-mobilising factors,LMF),它们是导致机体体重下降及肌肉消耗的主要原因。目前,已经从体重下降的胰腺癌、结肠癌、肺癌、卵巢肿瘤、乳腺癌及肝癌患者尿液中检测到PIF,动物实验发现PIF通过NF-κB及STAT3途径发挥作用,刺激NF-κB 及STAT3途径,诱导骨骼肌蛋白水解(通过UPP系统),诱导肝细胞产生IL-6、IL-8 及CRP。肿瘤细胞还可以分泌一种循环因子——甲状旁腺激素相关肽(parathyroid hormone-related peptide,PTHrP),它与可溶性TNF受体水平升高有关,与白蛋白及转铁蛋白降低有关。体重丢失的肿瘤患者LMF升高,而体重稳定的患者LMF无变化,提示LMF与体重丢失有关。LMF通过增加cAMP产物,致敏脂肪细胞,使其对脂肪分解刺激更加敏感。LMF与β肾上腺素能受体结合,引起β肾上腺素能受体数量或G蛋白表达增加。
宿主对肿瘤的作用
机体遭遇创伤、感染、炎症、肿瘤后,机体会发生一系列急性改变,这种变化统称为急性期反应(acute phase response,APR)。狭义的APR是机体遭遇创伤、感染、炎症、肿瘤后,肝脏蛋白质合成发生的一系列变化的总称,表现为肝脏白蛋白合成转向合成急性期蛋白(acute phase proteins,APP),如C反应蛋白(C-reactiveProtein,CRP)、纤维蛋白原、血清淀粉样蛋白A、α2巨球蛋白、α-抗胰蛋白酶,所以,又称为急性期蛋白反应(acute phase protein response,APPR)。研究发现,APR与胃肠道肿瘤、非小细胞肺癌(non-smallcelllung cancer,NSCLC)患者的体重丢失有关,血浆IL-6水平与CRP浓度有关,这也是肿瘤患者体重丢失与单纯饥饿体重丢失的差异所在。胰腺癌患者APP升高,生存时间缩短。
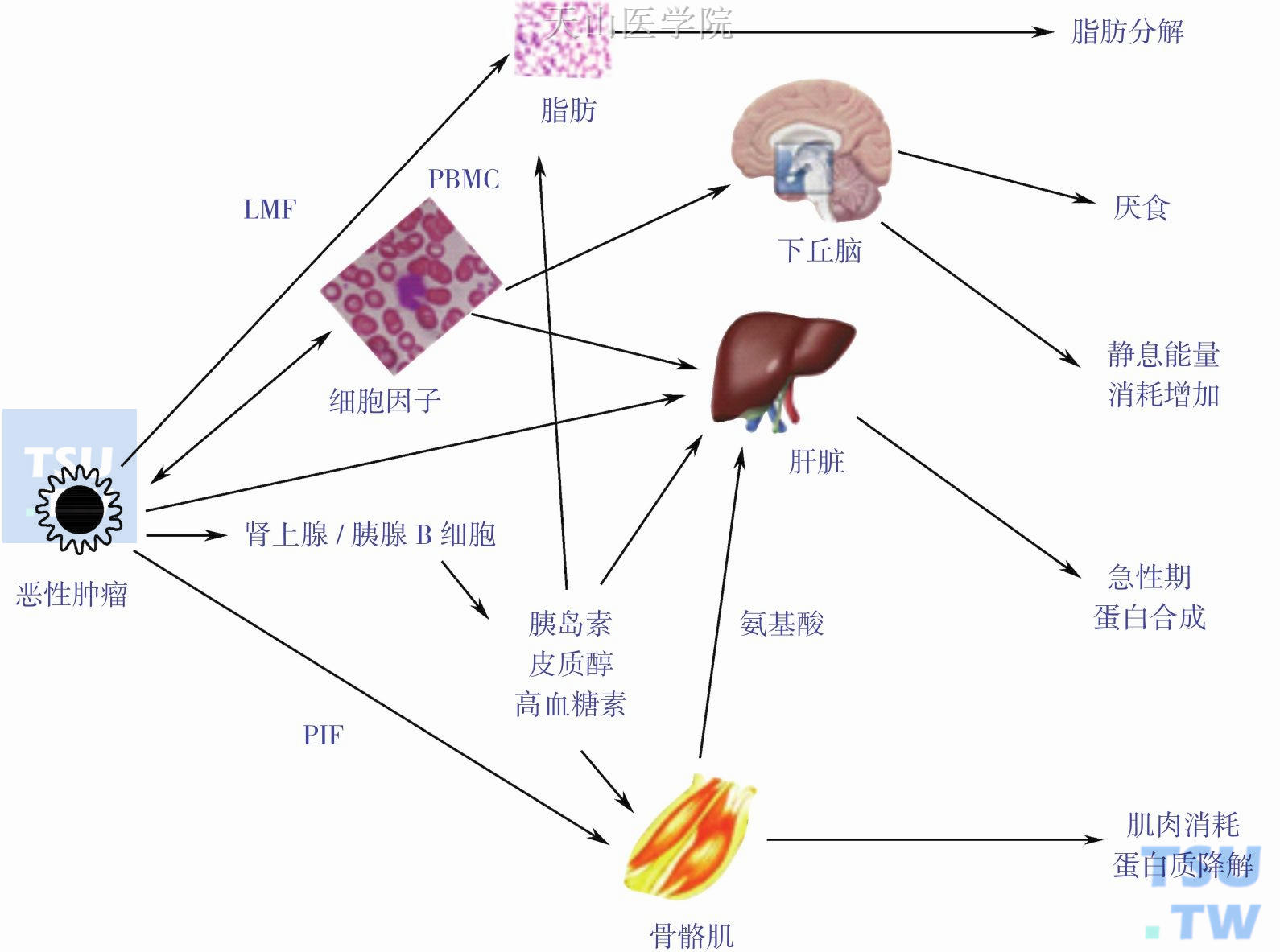
图4-2-1 肿瘤对宿主的代谢影响
LMF,lipid mobilizing factor,脂肪动员因子;PIF,proteolysis-inducing factor,蛋白水解诱导因子;PBMC,peripheral blood mononuclear cell,外周血单核细胞
宿主对肿瘤的反应同样是一种炎症反应,即急性期反应。宿主对炎症反应会导致一系列改变,这些变化构成APR。研究发现50%以上的实体上皮肿瘤(即癌症)存在APPR升高。APPR与高代谢相关,胰腺癌患者APPR升高与静息能量消耗(restingenergyexpenditure,REE)增加及能量摄入减少有关。时间纵向研究发现凡是出现APPR的患者,其预后较差。这种预后不良独立于体重丢失(与体重丢失无关) 。
CRP检测是评价这种全身炎症反应(systemic inflammatory response,SIR)严重程度的最常用方法。改良格拉斯哥预后评分(The modified Glasgow prognostic score,mGPS) 将CRP及白蛋白浓度结合起来,从而建立了一个更加简单的评分系统,表4-2-1。
表4-2-1 改良格拉斯哥预后评分(mGPS)

注:mGPS,the modified Glasgow prognostic score,改良格拉斯哥预后评分;CRP,C-reactive protein,C反应蛋白;Alb,albumin,白蛋白
研究发现这个评分系统(mGPS)可以独立预测生存情况,不依赖分期及治疗情况。患者入院时CRP升高预示患者全因死亡率(all-cause mortality)风险升高,患者CRP升高(>80mg/L),则肿瘤患者的死亡风险增加22.8倍。一个研究发现,108例不可手术切除的非小细胞肺癌(NSCLC),80%的患者CRP升高,40%患者体重丢失>5%。一组无体重丢失的患者中,出现APPR的患者更加感到疲劳。一组胃食管癌患者,体重丢失率与血浆CRP浓度相关。肿瘤诊断时CRP升高是胰腺癌、肺癌、黑色素瘤、多发骨髓瘤、淋巴瘤、卵巢肿瘤、肾癌、胃肠道肿瘤预后不良的预测因素。APPR与恶液质不良预后的机制不清,可能与APPR消耗骨骼肌、分解的游离氨基酸有关。系统炎症反应使骨骼肌水解产生的游离氨基酸更多地转向合成急性期反应蛋白,而不是机体机构蛋白质的合成。APPR需要大量必需氨基酸:产生1g纤维蛋白原必需分解2.6g肌肉蛋白质。
