环氧化酶(cyclooxygenase,COX)是催化花生四烯酸(arachidonic acid,AA)转化为前列腺素(prostaglandins,PGs)过程中重要的限速酶。迄今为止共发现三种COX同工酶:即COX-1、COX-2与COX-3。COX-1为结构性酶,在几乎所有组织中有表达,具有保护胃黏膜,促进血小板聚集和止血等生理功能;COX-2是诱导性酶,当细胞受到内外因素的刺激时表达上调,并参与炎症及肿瘤的发生与发展;COX-3目前对其功能知之甚少。非甾体抗炎药(nonsteroidal anti-inflammation drugs,NSAIDs)主要通过抑制COX,从而减少前列腺素类的合成而发挥其解热、镇痛、抗炎作用。传统的NSAIDs对COX-1、COX-2的作用缺乏选择性,常导致胃肠道不良反应,近年来更多研究对COX-2抑制剂寄予很大希望。
COX-2的生物学特征
人类COX-2基因于1995年被克隆,长约8.3kb,位于染色体的1q25.2~q25.3,包含10个外显子。与COX-1在几乎所有的细胞类型中有一个比较稳定的表达水平不同,COX-2在正常组织细胞中极少甚至不表达。但在许多病理条件刺激下,COX-2可能呈过度表达。大多数刺激COX-2表达的因素与炎症有关:如LPS、致炎细胞因子如IL-1、IL-2、IL-6、TNF-α等,而抗炎细胞因子如IL-4、IL-10、IL-13等以及皮质类固醇则降低COX-2的表达。除炎症外,在一些病理条件下,如阿尔茨海默病、多种肿瘤、心肌梗死等COX-2表达上调,提示COX-2可能在多种疾病中发挥作用。
COX-2在肿瘤发生发展中的作用及分类
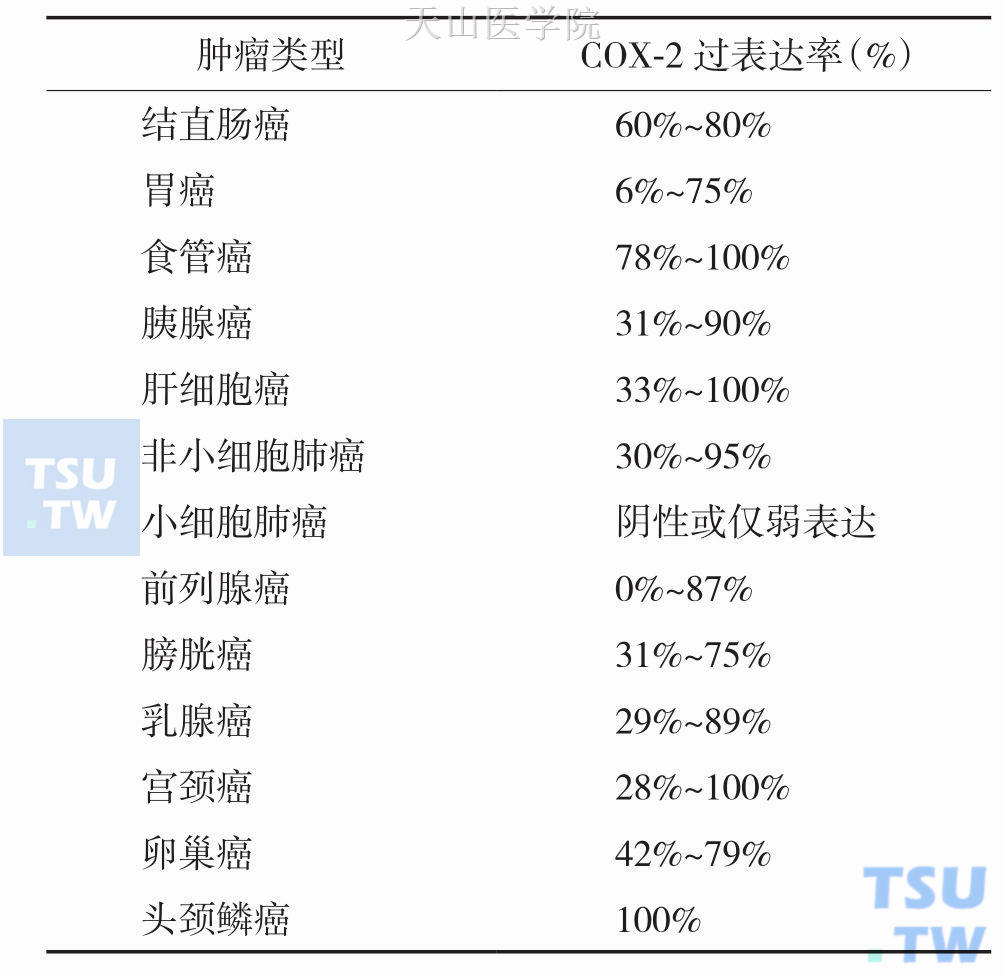
临床研究发现,COX-2基因或蛋白在多种肿瘤中存在过度表达情况,并与肿瘤的发生、发展有密切的关系,其表达水平与肿瘤患者的预后呈负相关。Hak Choy总结了不同临床文献报道的COX-2在不同实体瘤中的过表达情况(表10-13-1)。研究发现多数实体瘤COX-2过表达往往与肿瘤细胞分化差、浸润、转移、肿瘤新生血管生长等临床病理特征相关,预后往往较差。
COX先催化花生四烯酸生成前列腺素G2,再催化后者生成不稳定的中间产物前列腺素H2,再经特异性的前列腺素酶类将前列腺素H2代谢为至少5种结构相关的类脂类分子,包括PGE2、PGD2、PGF2、PGI2、TXA2,这些分子的作用各异(图10-13-1)。其中PGE2为其主要代谢产物,可诱导细胞增殖,促进细胞黏附,抑制具有免疫调节功能的淋巴细胞因子的产生,抑制T细胞和B细胞增殖,抑制宿主对肿瘤细胞的局部免疫反应。
表10-13-1 各种肿瘤组织细胞COX-2表达情况
依据对作用靶点的选择性不同,可将COX-2抑制剂分为两大类:第一类为非选择性COX-2抑制剂。主要指传统意义上的NSAIDs,典型的代表阿司匹林、舒林酸等,它们对COX-2和COX-1均有抑制作用,副作用以胃肠道出血最常见,其次为间质性肾炎和哮喘等。第二类为选择性COX-2抑制剂,主要包括塞来昔布、罗非昔布等。选择性COX-2抑制剂对COX-2具有显著的抑制作用,对COX-1的抑制作用较小,可避免传统NSAIDs类药物的胃肠道出血等不良反应的发生。
COX-2在肿瘤防治中的作用
COX-2抑制剂主要是通过不可逆的乙酰化和竞争性抑制作用来抑制COX-2,减少了PG生成或使其前体AA浓度增加,刺激神经鞘脂转化为促进细胞凋亡的神经酰胺。其确切抗肿瘤机制尚未完全清楚,可能涉及以下环节:①抑制癌基因的启动,使细胞内以及细胞间信息传递受阻断,从而阻断癌细胞的增殖;②诱导癌细胞凋亡;③促进细胞的免疫监视及肿瘤杀伤功能;④促进抗体的产生;⑤减少转移及抑制肿瘤新生血管生成等多个方面。
COX-2抑制剂对消化道肿瘤的防治作用
研究发现NSAIDs降低了消化道恶性肿瘤的发病风险,包括结直肠癌、胃癌、食管癌、胰腺癌、肝癌等。其中对结直肠癌的研究是最广泛,也是最深入的。结直肠癌肿瘤组织中COX-2表达增加,在细胞系研究中也发现通过COX-2途径调节PGE2表达增加而使肿瘤细胞凋亡受到抑制。结直肠癌患者肿瘤细胞COX-2高表达与肿瘤的侵袭性、新生血管以及远处转移能力呈正相关。20世纪90年代多项大规模回顾性研究显示,长期服用阿司匹林能显著降低患结直肠癌的风险,阿司匹林对结直肠癌的预防作用逐渐受到重视。然而随后开展的多项随机对照临床研究观察不同剂量的阿司匹林对结直肠癌的预防作用的结果并不一致。2010年,牛津大学Rethwell教授系统评价了5项大型临床研究结果认为,每天低剂量阿司匹林(81mg/d)能显著降低近端结直肠癌的发病风险,而常规剂量(325mg/d)则没有显示相似的作用。选择性COX-2抑制剂如塞来昔布也被发现能降低结直肠癌的发病风险,但是这类药物在心血管方面的毒副作用值得关注。临床研究也评估了COX-2抑制剂对结直肠癌患者生存期的作用。前瞻性队列研究显示肿瘤组织COX-2高表达的患者规律服用阿司匹林能显著减少肿瘤特异性死亡率及总的死亡率,尤其是存在PI3kCA基因(蛋白能活化COX-2)突变的患者。总之,临床研究结果显示规律服用NSAIDs,特别是低剂量阿司匹林(每天80~100mg),持续4年以上能显著降低结直肠癌的患病风险。但是,获益的优势人群、最佳剂量及剂量暴露的最佳时间有待进一步研究。
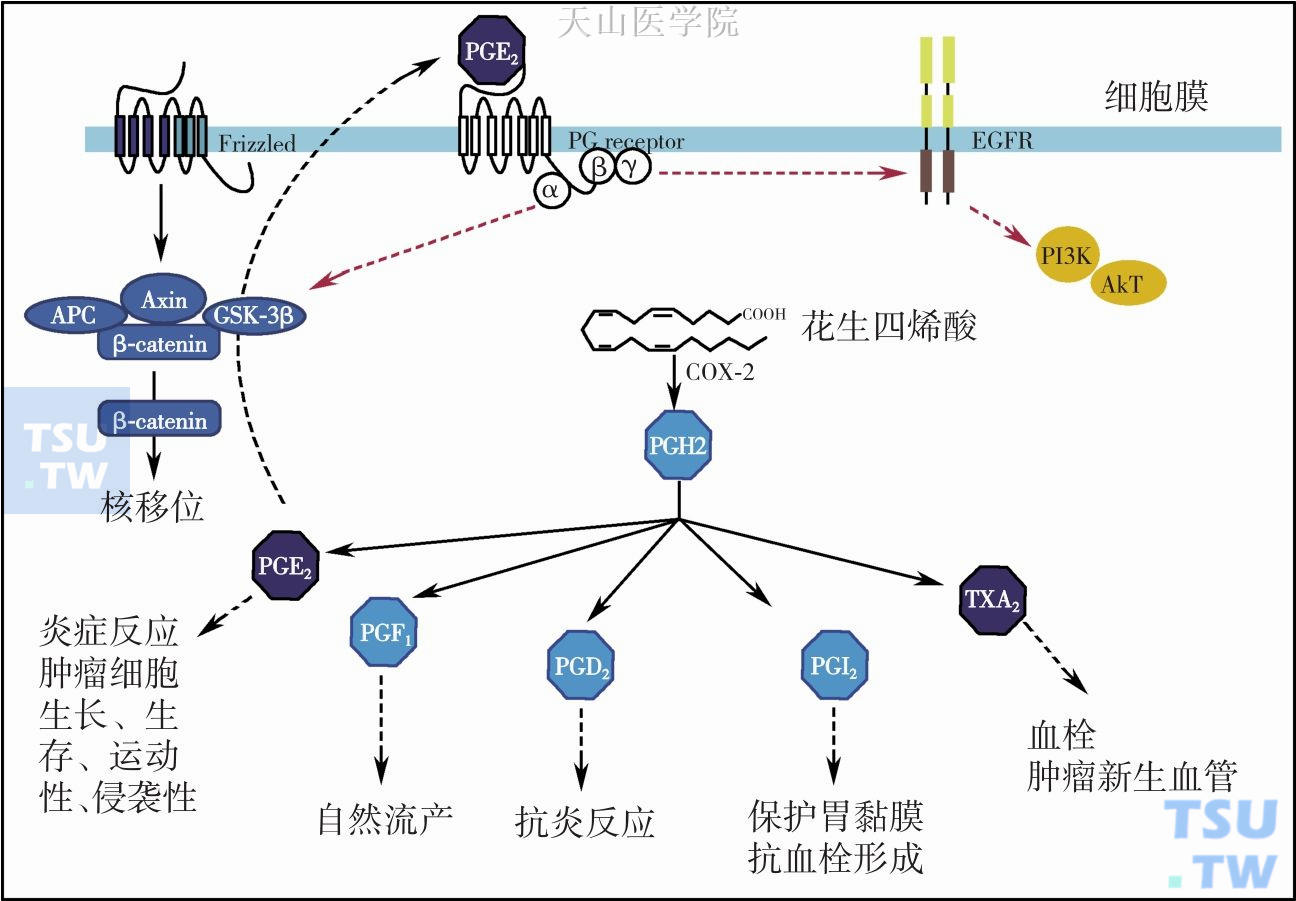
图10-13-1 COX-2催化花生四烯酸产生的产物及其作用
Barrett食管是食管腺癌的一个好发因素,在一项前瞻性研究中观察了NSAIDs对350例Barrett食管的影响,结果显示与不用NSAIDs的Barrett食管患者比较,服用NSAIDs能显著降低食管癌的发病率。对多项临床研究的荟萃分析也显示无论服用阿司匹林,还是非阿司匹林的NSAIDs均能显著降低食管腺癌的发病率,这两类药物之间并没有显著统计学差异。说明COX-2抑制剂能抑制致癌因素对癌基因的活化,使食管癌的发病率降低。幽门螺旋菌(Helicobacter Pylori,HP)感染引起胃溃疡及慢性萎缩性胃炎是诱发胃癌的高危因素之一,研究显示HP感染的慢性胃炎患者中,COX-2表达明显增高。流行病学研究也观察到与不服用阿司匹林的人比较,每月至少服用阿司匹林16次以上持续1年的人死于胃癌的风险显著下降。在一项回顾性研究中发现服用阿司匹林能降低非贲门癌的发病率,对贲门癌的发病率则没有作用。一项纳入了15个临床研究的Meta分析报道了服用阿司匹林频率与持续时间对胃癌发病的影响,作者认为每周服用1~4.5次,平均持续4年以上,能显著降低胃癌的发病风险。
另一项Meta分析纳入了21项流行病学研究,最终分析认为服用NSAIDs能降低包括贲门及非贲门癌的发病率。中国台湾的一项研究报道,胃溃疡患者规律地服用NSAIDs可以显著性降低胃癌发病率,与不服用NSAIDs的胃溃疡患者差异显著。获益人群为HP感染胃溃疡患者,无HP感染的胃溃疡患者无明显获益。NSAIDs除了能化学预防胃癌的发生外,其对胃癌的癌前病变及胃癌的作用也进行了研究。患有胃癌前病变的患者,在常规HP根除性治疗的同时分别给予塞来昔布或安慰剂,发现塞来昔布与安慰剂相比能显著逆转胃癌的癌前病变。总之,从上述研究我们可以发现,服用NSAIDs能显著降低胃癌的发病风险。但是需要前瞻性的、随机的双盲临床研究进一步阐明二者之间的关系,包括服用药物的类型、剂量及服用时间等。
COX-2在胰腺癌组织中表达也较高,对于COX-2抑制剂对胰腺癌的防治作用也开展了较多的研究。在两项比较阿司匹林与非阿司匹林类NSAIDs作用的前瞻性队列研究中发现,阿司匹林能显著降低胰腺癌的发病率,且与阿司匹林的服用频率呈正相关。有意思的是该项研究中非阿司匹林NSAIDs没有显示相同的作用。在近期一项对照研究中发现服用NSAIDs超过2年的患者患胰腺癌的风险显著下降。然而,在另一项前瞻性研究中发现长期规律服用阿司匹林却增加了妇女患胰腺癌的风险。一个纳入13项研究的Meta分析结果也显示不能证实服用阿司匹林或非阿司匹林NSAIDs与降低胰腺癌发病率之间的联系。总之,虽然临床前研究显示COX-2抑制剂有潜在的抑制肿瘤的作用,但是与预防其他消化道肿瘤的作用相比,COX-2在胰腺癌的预防作用是有限的。
原发性肝细胞癌组织中COX-2表达越高的患者,其生存时间越短,提示COX-2可能在以肝炎及肝硬化为基础的肝癌的形成中发挥作用。在一项观察阿司匹林与非阿司匹林NSAIDs对肝细胞癌形成风险及慢性肝病的作用的前瞻性队列研究中发现,服用阿司匹林的患者能显著降低患肝细胞癌的风险及慢性肝病相关的死亡率。但另一些临床研究则未显示COX-2抑制剂能降低原发性肝癌的发病风险。COX-2抑制剂对肝癌的防治作用的资料有限,而且结果并不一致,需要进一步的前瞻性随机对照研究明确其在肝癌发生过程中的作用。
COX-2抑制剂对非小细胞肺癌的防治作用
COX-2在小细胞肺癌中几乎不表达,因此COX-2抑制剂对肺癌的防治作用研究主要针对非小细胞肺癌。COX-2往往在进展期非小细胞肺癌患者中表达增高,与低表达患者相比,COX-2高表达的患者生存期更短。在动物实验中发现COX-2选择性抑制剂塞来昔布能抑制非小细胞肺癌的生长,在Ⅱ期临床研究中也显示塞来昔布能延长非小细胞肺癌患者的生存时间,然而在随后开展的两项随机对照双盲的Ⅲ期临床研究发现标准的化疗方案联合塞来昔布与安慰剂对比不能延长非小细胞肺癌患者的生存时间。小分子酪氨酸激酶受体抑制剂联合COX-2抑制剂对非小细胞肺癌的作用也不理想。一项Ⅱ期临床研究显示吉非替尼联合塞来昔布治疗初治的未经选择的非小细胞肺癌的效果相比传统化疗没有优势。因此,COX-2抑制剂对非小细胞肺癌的防治效果还不能确定。所以,未来应该通过分子标记等方法筛选COX-2抑制剂的优势人群进行临床研究。
COX-2抑制剂对乳腺癌的防治作用
对乳腺癌的预后有重要影响的分子标志物除了雌孕激素受体、HER-2受体外,近来认为COX-2也是判断预后的重要指标。乳腺癌组织中COX-2表达增高预后更差。COX-2抑制剂不仅能抑制肿瘤细胞迁移、浸润及新生血管生长,COX-2与雌激素的代谢有协同作用,同时抑制COX-2和雌激素受体是一种理想的抗肿瘤策略。在多项Ⅱ期临床研究中也发现依西美坦联合塞来昔布可提高治疗效果。然而,德国乳腺肿瘤协作组开展的一项随机对照的Ⅲ期临床试验最终结果显示依西美坦联合塞来昔布作为辅助性抗乳腺癌治疗与依西美坦组比较没有差异。另外一项Ⅱ期临床研究中比较了塞来昔布联合卡培他滨治疗晚期乳腺癌的作用显示临床获益率47.5%。尽管临床前资料显示COX-2抑制剂对乳腺癌有良好的作用,但是COX-2抑制剂对乳腺癌的作用还需要更多的临床研究。
COX-2抑制剂对卵巢癌的防治作用
COX-2在上皮性卵巢癌组织中表达增高意味着对化疗耐药几率增加、预后更差等。Meta分析结果显示卵巢癌中COX-2表达越高生存期越短,是一个独立的预后不良因素。一项卡铂联合塞来昔布治疗化疗耐药的卵巢癌的Ⅱ期临床研究中发现有效率为28.9%,而且患者耐受性良好。然而在另外一项塞来昔布联合标准化疗一线治疗晚期卵巢癌的Ⅱ期临床研究结果却是阴性的。因此,COX-2抑制剂对卵巢癌,尤其是对化疗耐药的卵巢癌的作用还不确定,需要开展随机对照的临床研究。
总结
COX-2在许多恶性肿瘤中有表达,表达水平愈高预后愈差。COX-2抑制剂对多个肿瘤如结直肠癌、胃癌、乳腺癌等显示出一定的防治效用,但是与这些药物相关的毒副作用需引起足够的重视。还需要临床研究不断进行探索,尤其是在COX-2抑制剂获益优势人群选择方面未来应该投入更多的精力,以期取得更多突破,让患者能真正在COX-2抑制剂治疗中获得好处。基于此,我们正在国家肿瘤新药临床评价技术研究平台(重大新药创制)项目的支持下开展阿司匹林联合标准化疗对PI3KCA突变结直肠癌的作用,以及选择性COX-2抑制剂塞来昔布对晚期肿瘤恶液质的作用的临床研究。相信在大家的共同努力下,会不断出现新的研究成果为肿瘤患者提供更多的帮助。
(李鸿立 巴一)
