甲状腺肿瘤患者常常以颈部肿块或结节而就诊,不少甲状腺癌与甲状腺良性疾病的临床表现相似。就甲状腺结节或肿块而言,绝大多数属于良性疾病,因此,对每一例甲状腺结节或甲状腺肿块患者来说,几乎均存在排除恶性病变的问题。故甲状腺肿瘤的诊断实际上是甲状腺良、恶性肿块(或结节)的鉴别诊断问题。
无痛性颈部肿块和甲状腺结节是甲状腺癌的常见表现
甲状腺癌患者的主诉常常为“颈部肿块”或“甲状腺结节”。在病史询问中,要特别注意肿块或结节发生的部位、时间、生长速度,是否短期内迅速增大,是否伴有吞咽困难、声音嘶哑或呼吸困难,是否伴有面容潮红、心动过速及顽固性腹泻等表现。是否因患其他疾病进行过头颈部、上纵隔放射治疗及有无131I治疗史等。有否暴露于核辐射污染的环境史。从事的职业是否有重要放射源以及个人的防护情况等。髓样癌有家族遗传倾向性,家族中有类似患者,可提供诊断线索。
通过现病史调查,要对患者的甲状腺功能状态有个总体评估,应详细了解有无食量增加、易饥饿、体重减轻、失眠、兴奋、多汗、心悸等症状。此外,还应注意询问有无肿瘤转移的系统症状(如头痛、视力下降、咳嗽、咯血、胸痛、腹痛、黄疸、骨痛等)。既往是否有甲状腺疾病(如慢性淋巴细胞性甲状腺炎、甲亢、硬化性甲状腺炎)、垂体瘤、嗜铬细胞瘤等病史及非甲状腺肿瘤的MEN有关病史。
单一实性冷结节的恶性风险高于囊性结节/多发性结节/热结节
在临床上,遇有下列情况时,提示恶性甲状腺结节的可能性较大:①成年人和老年人;②男性;③单结节、囊性结节或钙化性结节;④质地硬,活动度差;⑤结节迅速增大或伴局部淋巴结肿大;⑥既往有头颈部、上纵隔放射治疗或核暴露史,甲状腺癌或MEN家族史。
甲状腺的良性或恶性肿瘤均表现为可扪及的“甲状腺结节”。一般认为,除多数“热”结节外,其他类型的大小结节或经影像学检查发现的“意外结节(意外瘤)”均要想到甲状腺肿瘤的可能;有些甲状腺癌亦可自主分泌TH,故亦可表现为“热”结节,所以事实上凡发现甲状腺结节均要首先排除甲状腺肿瘤(有时,甲状腺癌仅在镜下才可诊断)。甲状腺结节可分为一般性结节、多发性结节和放射性结节等类型。甲状腺癌多为单个结节,可为圆形或椭圆形,有些结节形态不规则,质硬而无明显压痛,常与周围组织粘连而致活动受限或固定。若发生淋巴结转移,常伴有颈中下部、胸锁乳突肌旁肿大的淋巴结。一般来说,甲状腺单个结节比多个结节、小的实质性结节比囊性结节、男性比女性的甲状腺癌可能性大,但多发性结节、囊性结节也不能排除甲状腺癌的可能性。家族型甲状腺髓样癌常为双侧肿块,可有压痛。
甲状腺癌较大时可压迫和侵袭周围组织与器官,常有呼吸困难、吞咽困难及声音嘶哑等症状。远处转移时,可出现相应的临床表现。甲状腺髓样癌可有肠鸣音亢进、气促、面颈部阵发性皮肤潮红、血压下降及心力衰竭等类癌综合征体征。
临床转归与肿瘤类型及手术时期有关
甲状腺癌的预后依肿瘤性质和治疗方法而异。一般可用Mayo医院的MACIS计分系统进行评判。在这一评判体系中,用Cox模型分析和逐步回归分析(n=1779)得到5个影响预后的独立变量MACIS:转移(M)、年龄(A)、完全切除程度(C)、侵犯情况(I)和肿瘤大小(S)。即:MACIS=3.1[(年龄≤39岁)或0.08(年龄≥40岁)]+0.3(肿瘤大小,cm)+1(完全切除时)+1(不完全切除时)+1(有局部侵犯)+3(有远处转移)。用这一方程得到的20年存活率与相应MACIS计分值分别为:MACIS<6者,20年存活率为99%;6~6.99者为89%;7~7.99者为56%;≥8者为24%。经多年验证,MACIS预后评判已被绝大多数人所接受和应用。对RET基因突变者行预防性甲状腺切除可预防甲状腺髓样癌的发生,其效果良好。
- 乳头状癌:其预后好,常通过近全部甲状腺切除、长期TH的抑制治疗及131I治疗具有摄碘功能的转移灶,可降低甲状腺癌的复发率,延长生存时间,其术后生存期常在10~20年以上。
- 滤泡状癌:多先向下,继而向纵隔及下颈部淋巴结转移;后期因气管前、气管旁淋巴管被肿瘤堵塞而向颈深上淋巴结转移;血液转移至肺和骨,较乳头状癌恶性程度高、侵袭力大,预后较差。因此对其治疗措施应比乳头状癌更有力。除监测血清Tg外,定期的X线追踪检查是必要的。
- 未分化癌:其恶性程度高,治疗往往是姑息性的。手术治疗的预后与清除可疑的甲状腺组织是否完全有关,一般均在术后加用131I治疗,并在放疗前用rhTSH提高甲状腺的摄碘率,以期获得最佳疗效。
- 甲状腺髓样癌:其恶性程度仅次于未分化癌,约2/3患者的生存期为10年左右,对于得到早期诊断、早期治疗的患者有望获得痊愈。
实验室检查和动态试验监测甲状腺功能和术后复发
实验室检查
一般应测定血清TT4、FT4、TT3、FT3和TSH。必要时还应检测抗Tg抗体和TPOAb或TSAb等。如均正常,一般不考虑有甲状腺功能异常。如TSH<0.5mU/L,FT4(或FT3)正常或稍升高,即应考虑有亚临床型甲亢可能。甲状腺癌患者的甲状腺功能一般正常,少数可因肿瘤细胞能合成和分泌T3、T4而出现甲亢症状,较轻者可仅有TSH下降和FT3、FT4的升高。肿瘤出血、坏死时,有时也可出现一过性甲亢。
血清Tg测定主要用于分化良好的甲状腺癌的复发判断。血清Tg浓度主要由3个因素决定:①甲状腺容量,体积越大,分泌的Tg越多;②TSH受体的活化程度,TSH受体被刺激时,分泌的Tg较多;③滤泡细胞或肿瘤细胞合成和分泌Tg的能力,一般分化良好的甲状腺癌可保存Tg的合成和分泌功能。
动态试验主要用于确定甲状腺髓样癌和甲状腺癌有无转移
一、重组的人TSH兴奋试验
当血TSH很低时,一般测不到Tg,使用重组的rhTSH后,Tg分泌增多,血Tg一般升高10倍以上;分化程度差的肿瘤患者升高<3倍。但分化较好的甲状腺癌患者(约20%)血清中存在Tg自身抗体,用免疫化学和RIA法测定Tg时可使Tg呈假性升高或降低,故分析结果时必须引起注意。接受L-T4治疗的甲状腺癌患者,如血清Tg正常或测不出,提示复发的可能性小,5年存活率高;如血清Tg高于正常,提示肿瘤已复发。在临床上,甲状腺癌(尤其是分化较好者)术后患者均常规应用L-T4抑制TSH,维持甲状腺功能。可先测定基础血清Tg浓度(不停用L-T4)、继用rhTSH滴注,连续2天后再测定血Tg和抗Tg抗体,必要时可加作131I扫描。如经rhTSH刺激后,血Tg仍较低,或131I扫描未发现新的病灶,可认为患者尚未复发,其预后良好。
二、血清CT测定及五肽胃泌素兴奋试验
血清CT升高是甲状腺髓样癌的较特异标志物。髓样癌患者在滴注钙剂后,血CT进一步升高,而正常人无此反应。因此,血清CT测定及钙滴注兴奋试验可作为本病的诊断依据,同时可作为家族型甲状腺髓样癌患者家族成员的筛选与追踪方法之一。血清CT测定还可用于筛选非家族型甲状腺髓样癌和甲状腺C细胞增生症病例。Kotzmann等对150例行血液透析的慢性肾衰竭患者和800例肾移植患者用血CT测定筛选甲状髓样癌,29%的血液透析患者和6%的肾移植患者的血CT>10pg/ml。这些患者经五肽胃泌素兴奋后,其中有4例血透患者和7例肾移植患者的血CT>100pg/ml,在这11例患者中,有8例行甲状腺切除术(6例为C细胞增生症,2例为髓样癌),而6例C细胞增生症中有2例的病理改变酷似C细胞癌或C细胞微小癌。这说明,如果患者经五肽胃泌素兴奋后,血CT浓度≥100pg/ml,必须考虑C细胞增生和(或)C细胞癌的诊断,应行甲状腺切除。在甲状腺肿瘤的术前诊断中,血CT测定和五肽胃泌素兴奋试验已经成为继细针活检、B超及放射核素扫描等的另一项诊断方法。对结节性甲状腺疾病常规用血CT测定、五肽胃泌素兴奋及ret基因突变分析可望早期诊断甲状腺C细胞增生及C细胞癌。一经发现,即可行预防性手术。据报道,其预防效果为100%。
值得注意的是,由于测定方法和所用抗体的差异,因此各地必须规范标准、建立正常参考值(基础值和五肽胃泌素兴奋后的兴奋值)。此外,高CT血症还可见于甲状腺C细胞增生症(可伴淋巴细胞性甲状腺炎或滤泡性癌)、慢性肾衰行透析治疗者及多种神经内分泌肿瘤。血清中的CT存在不均一性,在高CT血症时更为明显。由于CT基因的差异与突变及CT的组织来源不同,可存在数种结构类型的CT(包括糖化型CT原)。甲状腺髓样癌细胞以表达Ⅰ型CT基因为主,如能测定CT的各组分值对诊断更有价值。Grauer等报告,用一种化学发光-双位点免疫测定法(chemiluminescent twosite immunoassay)测定人血CT,较以前的RIA法有很大进步,此法的可测范围为0.7~2500pg/ml(RIA法为2.0~1000pg/ml),正常均值(95%可信限)为6.55pg/ml(男性)和4.13pg/ml(女性)。五肽胃泌素兴奋后,正常均值为43.0pg/ml(男性)和36.8pg/ ml(女性)。可将C细胞癌、C细胞增生和其他非特异性高CT血症较好地分开。
影像检查提供良恶性鉴别依据
超声检查
随着高频探头的使用,超声分辨率得以提高。可以借超声来分析肿块或结节的位置、大小和性质,帮助鉴别良、恶性肿块。甲状腺腺瘤常为圆形、边界清楚的实体性肿块,而囊肿或肿块囊性变可显示囊内液性暗区,甲状腺癌则可呈边界不清、回声不均匀图像。
高分辨率B超在甲状腺疾病中主要有以下用途:①B超较SPECT、CT、MRI等均有其独到的优越性,尤其在了解血流情况方面其优点突出。②了解甲状腺结节的大小、位置,可发现“意外结节”,明确甲状腺后部的结节位置以及与附近组织的关系;③作为结节穿刺、活检的引导,甲状腺B超检查已成为甲状腺肿瘤术前诊断和术后追踪的重要手段。在高分辨B超系统中,加入立体定位系统(3D扫描B超),可进一步提高其敏感性和诊断效率。3D B超实际上相当于超声体层扫描,使图像更为清晰,定位具三维特征。在甲状腺肿瘤的诊断方面,可作为放射治疗的靶向定位和血管图像重建等。在治疗方面可用于精确评价结节经131I、乙醇、化学抗癌药物及放射介入栓塞治疗等的坏死程度。但超声显像对于单发结节性甲状腺肿与单发腺瘤常难以区别。
近年发展起来的以能量方式显示血管内血流的彩色多普勒技术[彩色血管能量成像(CPA)]能敏感地显示肿瘤内的细小血管。甲状腺癌的周边及内部均见丰富血供尤其内部血供丰富,CPA大多以Ⅲ级血流为主,且血管走行迂曲,管径可见不规则的扩张,缺乏远端的逐渐变细的正常形态。而甲状腺腺瘤CPA多为周边型血流,大多以Ⅰ级血流为主,少数表现为肿瘤内部及周边未见血流信号,这可能由于甲状腺腺瘤的新生血管的能力小于甲状腺癌。应用CPA可帮助在我们术前、术后评估甲状腺肿瘤的血管生成情况,为临床早期诊断和评估预后提供有价值的信息,并为临床治疗方案的制订提供依据。
甲状腺核素扫描
临床上应用核素扫描显像检查的另一目的是确定甲状腺结节(包括肿瘤)的功能性(摄取碘、合成和分泌TH等)。与131I或123I比较,99mTc(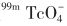 )的特异性和敏感性更高,而且不会导致碘甲亢。
)的特异性和敏感性更高,而且不会导致碘甲亢。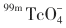 摄取与123I摄取有极佳的相关性,故前者同样可用于甲状腺功能的评价。但必须注意的是,放射性锝的清除率也包括了非肿瘤的正常甲状腺组织,故仅在抑制试验阴性时才能确定结节的功能状态。采用131I或99mTc作为示踪剂对甲状腺进行扫描,可显示甲状腺肿块的大小、位置、形态、数目及功能状态,有助于甲状腺肿块的性质及异位甲状腺肿块的鉴别与定位,“热”结节和“温”结节多为良性甲状腺腺癌(但也有例外),而“凉”结节和“冷”结节提示为无功能甲状腺腺癌、甲状腺囊肿或伴有出血坏死及甲状腺癌肿。特别是男性患者,出现边界不清的单个冷结节时,要高度考虑甲状腺癌的可能。
摄取与123I摄取有极佳的相关性,故前者同样可用于甲状腺功能的评价。但必须注意的是,放射性锝的清除率也包括了非肿瘤的正常甲状腺组织,故仅在抑制试验阴性时才能确定结节的功能状态。采用131I或99mTc作为示踪剂对甲状腺进行扫描,可显示甲状腺肿块的大小、位置、形态、数目及功能状态,有助于甲状腺肿块的性质及异位甲状腺肿块的鉴别与定位,“热”结节和“温”结节多为良性甲状腺腺癌(但也有例外),而“凉”结节和“冷”结节提示为无功能甲状腺腺癌、甲状腺囊肿或伴有出血坏死及甲状腺癌肿。特别是男性患者,出现边界不清的单个冷结节时,要高度考虑甲状腺癌的可能。
甲状腺恶性病变行甲状腺全切后,可用诊断性131I检查来判断是否有病灶复发和转移,一般进行的是131I全身性扫描,该项检查的结果取决于甲状腺恶性病变组织在高浓度TSH刺激下摄取131I的能力。131I全身性扫描前,女性要排除妊娠。患者必须禁用碘制剂和含碘药物(包括TH制剂)。对于已经应用了TH制剂的患者,131I全身性扫描前的准备有3种方法:①一般在停用TH 4~6周后进行。②难以耐受停药后出现的甲减者,可在进行131I全身性扫描前改用代谢更快的L-T3,这样可将停用L-T3的时间缩减至2周。③仍不能耐受者可将L-T3减量50%。④必要时,在不停药情况下,肌肉注射rhTSH,0.9mg/d,共2天,使血TSH>25~30mU/L后扫描。131I的常规诊断用量为2~5mCi(74~185MBq)。如患者已经接受了大剂量131I治疗(或扫描检查或血Tg升高),在再次做131I全身性扫描复查时,要间隔7天以上,且131I剂量要大。分化性甲状腺癌常采用131I或123I扫描。但是,如患者已经接受多次131I治疗,肿瘤细胞的摄碘功能下降甚至丧失,可使扫描阴性,而肿瘤的恶性程度又在此时增强(尤其多见于老年患者)。此时应选用PET或PET-CT 检查,以提高阳性发现率。
CT/MRI
甲状腺组织因含碘高,血供丰富,与周围组织自然对比度好,而甲状腺病变无论是弥漫性病变或是结节性病变常常导致组织含碘量发生改变,从而使甲状腺的整体或局部的密度减低,易被CT扫描发现。CT扫描对甲状腺肿瘤压迫气管、食管以及向胸骨后延伸情况和有无颈部淋巴结肿大优于同位素扫描及超声检查。新近的螺旋CT扫描还可明显提高对微小肿瘤病灶的检出率。甲状腺良性肿瘤常为实质性的1~4cm孤立结节,边缘光滑锐利,其内密度均匀。甲状腺癌常为不规则或分叶状软组织密度不均匀肿块,与周围组织分界不清,增强扫描呈不规则钙化,可有局部转移,或向气管、喉和食管浸润现象。如高度怀疑甲状腺癌肺转移灶,宜选用肺部CT检查。甲状腺区CT扫描可用于肿瘤的分级,如CT显示的病变欠满意,宜用MRI检查。注意,在CT片上发现任何多发性淋巴结存在钙化、血供增多、增大、出血、形态不规则,或在MRI图上发现结节呈低至中等T1和 T2信号强度(提示含多量Tg),不论甲状腺内有无病灶,都要考虑甲状腺癌转移灶的可能。
欲重点了解病变与毗邻组织的关系时首选MRI检查。MRI能清楚地显示甲状腺位置、大小、肿块与腺体及与周围组织的关系。甲状腺良性肿瘤常为边界清楚、局限性长T1与长T2信号肿块。甲状腺癌常表现长T1及不均匀长T2异常肿块。肿块可向上下蔓延,左右浸润,常伴有颈部淋巴结肿大。
PET扫描
血清Tg升高往往提示甲状腺癌复发或转移,一般选用131I全身扫描或CT扫描进行定位。如131I全身性扫描复查为阴性而高度怀疑甲状腺癌转移灶时,用18FDG PET扫描可发现隐性病灶,尤其是颈部淋巴结转移灶。
甲状腺针吸活检鉴别病变性质
凡有甲状腺结节(尤其是迅速增大的单个的甲状腺结节)患者都要想到甲状腺癌的可能。细针穿刺活检(FNA)是诊断甲状腺结节的金标准,在判断结节良恶性和决定下一步治疗方案上起着至关重要的作用,国外已将其作为基本的常规检查,美国国立综合癌症网(NCCN)指南中把FNA作为甲状腺结节的首选检查。目前,接受FNA指征主要有:临床评估中被视为高危患者;血清降钙素水平明显升高;直径大于1cm的实性结节,超声提示低回声,合并钙化或血流丰富;超声提示包膜外生长或颈部转移性淋巴结肿大;18FDC-PET/甲氧基异丁基异氰(MIBI)显像发现的甲状腺偶发瘤。其具体方法为:选用22~27号针头套在10ml或25ml针筒上,颈部常规消毒后,将针头刺入甲状腺肿块抽吸,也可将针头转换几个不同的角度进行抽吸,抽吸的标本涂片作细胞学检查。目前认为该技术对区别甲状腺肿块性质敏感性大于80%,特异性大于70%。但限于技术因素和组织细胞类型不同等问题,仍有16%~20%左右的病例难以作出诊断。如区别滤泡细胞癌的良、恶性可能需要血管、包膜浸润的证据,因此没有病理组织学的发现是难以诊断的,同时也可出现假阳性或假阴性。但细针穿刺仍然是大多数病例首选的诊断方法。如果细针穿刺失败,或所得结果不能确诊,换用粗针抽吸活检可提高诊断率,筛选手术病例。穿刺获得的细胞也可作细胞遗传学和分子生物学(如癌基因与抑癌基因突变等)分析,协助诊断。
通过细针(或粗针)穿刺或活检获取甲状腺病变组织标本作病理检查时,除常规细胞涂片、冰冻、石蜡切片光镜检查外,还可作免疫组化染色和癌基因/抑癌基因表达检测来协助诊断。高度怀疑为家族型甲状腺髓样癌者,除可测定血清CT浓度外,尚可用RET基因突变分析来协助诊断。并对其家庭成员进行筛选。
当转移性甲状腺肿瘤的原发灶不明时,其与原发性甲状腺肿瘤的鉴别十分困难,而甲状腺针吸活检可能是两者鉴别的唯一方法。
