高分辨超声提供诊断信息
检查前禁食8~10小时,肠气较多者,可用轻泻剂或口服活性炭减少肠气。怀疑为嗜铬细胞瘤者,应常规先行降压处理,以免诱发高血压危象。检查中尽量用高频探头,以提高分辨力。
凡怀疑有肾上腺病变者均可作此项检查,可确定病变的大小、范围和基本性质,可发现“意外瘤”,了解肾上腺的血流情况,并为进一步的检查提供线索,在超声引导下还可进行肾上腺活检,或行肾上腺肿瘤的腔镜下切除术,在开腹手术中,可于术中协助微小病变的定位或作局部的引导性化疗或栓塞等介入性治疗。于产前,可用超声发现肾上腺的先天性增生,或在产后,在为肾上腺性两性畸形患儿决定手术方式时,超声可精确了解阴道、尿生殖窦的解剖情况,为手术提供决策和可靠资料。B型超声无创伤性,但敏感性低于CT或MRI(尤其是严重肥胖者),不过对肾上腺外如腹腔、盆腔、膀胱等部位的嗜铬细胞瘤进行初步筛选有较大价值,在儿童中因其腹膜后脂肪较少而实用价值更大。但超声波探头的加压可能引起发作。在嗜铬细胞瘤的诊断被排除前不应进行肾上腺肿块的穿刺活检,以免引起高血压危象。
CT/MRI/核素扫描提供诊断依据
一些肾上腺病变在CT或MRI图上有特殊表现,故可为诊断提供特有的依据如肾上腺出血、钙化、囊肿、髓脂瘤(myelolipoma)等。CT在Addison病伴肾上腺肉芽肿性病变时较MRI优越。在腺瘤和非腺瘤的鉴别方面,增强对照有重要意义,尤其是延迟增强CT(delayed-enhanced CT)可明显提高鉴别的敏感性和特异性。肾上腺恶性肿瘤术后的随访和转移性癌的追踪观察也主要依赖于CT检查。由于PET具有显示体内生化过程的优点(生化显像技术),显然在肾上腺疾病的诊断和鉴别诊断中会越来越受到重视。用稳定核素标记技术可测定激素(如睾酮)的生成率和代谢清除率,或用123I-MIBG (metaiodobenzylguanidine,可被浓集在肾上腺)协助嗜铬细胞瘤或神经母细胞瘤的定位。
经肾上腺影像学检查,有时意外发现存在结节性病变(肾上腺“意外瘤”),和垂体意外瘤一样,患者无任何临床表现,或因表现轻微,患者并无诉说。当发现这种意外瘤后,应引起医师和患者重视,尽管无症状也要排除肿瘤可能,在临床上可根据下图的处理程序明确意外瘤的性质。在地塞米松抑制(避免肾上腺束状带和网状带摄取碘)条件下,Np-59扫描亦可用于两者的鉴别,但单侧显影或双侧显影决定于肿瘤的大小,当肿瘤的体积很小时,可呈双侧显影而误为特发性双侧增生,为了防止甲状腺显影,在试验前应先口服碘剂5~7天。
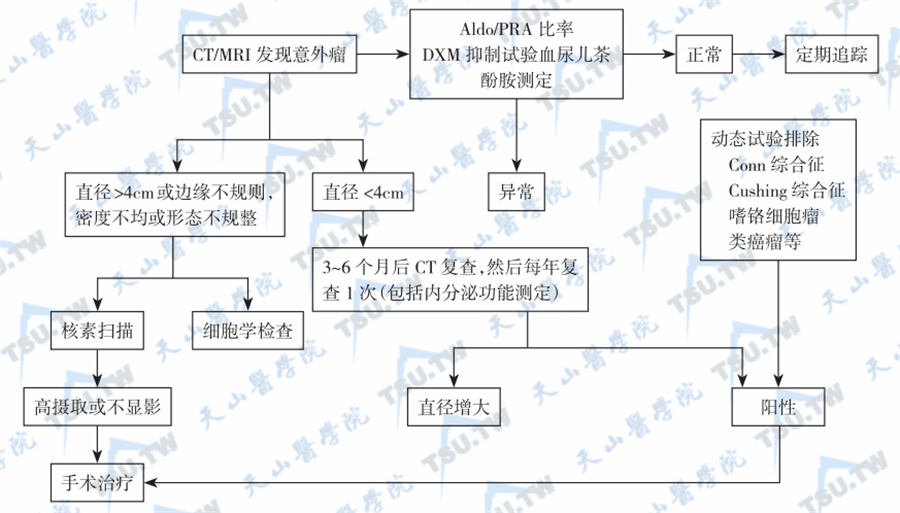
肾上腺意外瘤的处理
肿瘤定位常在生化检测确诊有嗜铬细胞瘤后进行,但对于临床表现不典型的患者可以先做定位检查。目前用于定位的方法有CT扫描、MRI、123I-间碘苄胍闪烁扫描(123I-MIGB)、生长抑素受体闪烁扫描和18F-DOPA正电子发射体层扫描(PET)等。动脉造影和静脉造影(结合或不结合静脉血浆儿茶酚胺测定)可用于肿瘤定位诊断,但目前基本上已被无创性方法替代。定位诊断首选CT,对于肾上腺和肾上腺外的肿瘤,CT和MRI均可以获得肿瘤所在部位的解剖细节而有利于手术,MRI优于CT,特别是对于心脏和血管旁的肿瘤,MRI可以显示胸腔内和心包肿瘤对心脏和血管的侵犯情况,所以如CT发现肿瘤并准备手术时,应再做MRI。MIBG用于生化检查提示有嗜铬细胞瘤的患者,特别是CT和MRI未发现肿瘤的患者,但MIBG有10%的假阴性,如MIBG阴性,但仍高度怀疑嗜铬细胞瘤,则应做胸腔、腹腔及盆腔的CT和MRI。18F-DOPA-PET由于其高的空间分辨率与特异性选择的示踪剂结合,对于原发于肾上腺内或外及转移灶均有良好的显像,将来有希望取代MIBG。
增强对照CT显示病灶特征
嗜铬细胞瘤瘤体在CT片上呈圆形或类圆形软组织块影,密度常不均匀,10%的肿瘤可有散在的实质钙化;恶性者一般瘤体较大,外形不规则且密度不均匀,可有周围组织浸润和远处转移;在多发性内分泌肿瘤综合征的患者,肿块往往较小。由于CT可以快速获得高分辨率的图像,可用于嗜铬细胞瘤的初筛,使用螺旋型CT可以发现直径小于0.5cm的肿块;薄层CT使用16mm×0.75mm的平行光管进行最大强度投影(MIP)和多平面成形(MPR)可以达到1mm的薄层切面。较厚的平行光管的敏感性较低,对于较小的病灶难于发现,可以使用增强剂使其与正常肾上腺区分开来,并可估计肿块的血供情况。如果使用离子型增强对照剂,应先使用α和β肾上腺能阻滞剂,以免诱发儿茶酚胺释放而导致危象发作;而使用非离子型增强对照剂则不一定使用阻滞剂。一般使用增强剂后诊断更可靠。由于肠袢和肿瘤都是透X线的,对于腹膜后主动脉旁的肿瘤可以使用口服不透X线的造影剂使消化道不透X线;心包内肿瘤较难发现,可使用慢速动态CT扫描,使肿瘤与相连的心血管结构的密度比增大而较易发现。对于膀胱内的嗜铬细胞肿瘤,不需任何增强,因为肿瘤在充满尿液的膀胱内是高密度的。CT对原发于肾上腺内的嗜铬细胞瘤诊断定位的敏感性为76%~100%;特异性约70%,其对于鉴别嗜铬细胞瘤、肾上腺皮质瘤、肾上腺类脂瘤较为困难。对于手术后再发的嗜铬细胞瘤CT的敏感性降至73%,对于肾上腺外或多发的肿瘤因其较大的放射性,常不推荐使用。
多维成像MRI显示病变与周围组织的关系
MRI成像应包括冠状面和中轴面连续 T1W(自旋-点阵弛缓时间)自旋回波扫描,和中轴面T2(自旋-自旋弛缓时间)自旋回波脂肪饱和扫描。冠状面和矢状面的成像可以显示大的病灶对邻近组织的侵犯,顺磁的对比剂可以将实质性肿块从囊性肿块中区别出来,并且评估肿块的血供情况。正常的肾上腺在T1成像中为中间强度信号,在T2成像中为低脂肪信号;嗜铬细胞瘤在T1显像中呈低强度或等强度,在T2显像中呈高强度表现,然而有35%的嗜铬细胞瘤在T2成像中的强度信号不典型;化学移位(chemical shift)MRI优于T2定性分析。肿瘤有出血时MRI表现为典型的出血征象;反过来由于有出血,在T1显像时肿块内可有增强的信号。用钇-DTPA增强显像可见到肿块内血管增多,并且肿块变得更清晰。对于肾上腺内的嗜铬细胞瘤MRI敏感性85%~100%,特异性约67%;在与肾上腺转移癌鉴别时有一定的困难。对于异位的和多病灶的嗜铬细胞瘤,其敏感性下降。磁共振血管造影术可以显示肿瘤的血流动力学。在一般情况下,MRI的多维成像比CT更精确,特别是在妊娠妇女和疑肾上腺外嗜铬细胞瘤时,因无X线的影响而更加适用可靠。
MIBG扫描显示嗜铬细胞瘤分泌功能
间碘苄胍(metaiodobenzylguanidine,MIBG)是胍乙啶的芳烷基衍生物,其结构与去甲肾上腺素相似,是去甲肾上腺素运载体的基质,能被分泌儿茶酚胺的细胞或肿瘤组织的小囊泡摄取并储存。对于有功能的嗜铬细胞瘤,用123I标记后静脉注射,可有阳性显像,故能对嗜铬细胞瘤同时进行定性和定位诊断,尤其适合于肾上腺外嗜铬细胞瘤的定位诊断。此外,也可用于所有能摄取胺前体和含脱羧酶系统的其他肿瘤(特别是神经母细胞瘤)。MIBG扫描的敏感性在90%以上,而特异性几乎达到了100%。123I标记的MIBG扫描的敏感性高于131I,因为前者的γ颗粒散射(particulate emission)更小。方法:停用对儿茶酚胺释放和扫描检查有影响的药物至少3天,并在检查前3天和扫描后7天服用卢戈碘溶液或高氯酸钠阻止甲状腺对游离123I的摄取,缓慢静脉注射185~370MBq 123I标记的MIBG(成人剂量,儿童剂量应通过计算获得),用计算机内低能量(123I)平行光管获得γ-照像显影。在患者进行123I-MIBG时可同时获得单光子发射CT(SPECT)扫描显影(注射后12小时)。在注射后24小时、48小时和72小时进行扫描,可获得全身嗜铬细胞瘤的显影。对于胸腔内邻近心脏的病灶可用1.5mCi的 201T1或15mCi的Tc标记红细胞注射来显示心脏的位置与结构。
使用低浓度MIBG时,细胞通过钠和能量依赖性的胺摄取机制主动摄取MIBG,而细胞质内的MIBG通过ATP酶依赖性质子泵主动转运至细胞内儿茶酚胺储存颗粒中。但在某些肿瘤,囊泡外的储存也可导致MIBG的滞留。与儿茶酚胺不同,放射标记的MIBG不能很好地与突触后受体结合,且较少代谢。放射性碘标记的MIBG静脉注射后,快速从血管内清除,仅有少量保留在血池中,主要存在于血小板内。大部分的MIBG原型从尿中排出。某些药物如钙通道阻滞剂、三环类抗抑郁药、拟交感神经药物、利舍平、可卡因和拉贝洛尔等可影响MIBG的摄取和(或)潴留。
123I-MIBG由于有更高的光子流和较短的半衰期,而具有较好的显像质量和敏感性,及较低的放射性暴露。为避免假阴性结果,在操作前48~72小时前应停用对MIBG积聚有影响的药物。如必须控制高血压,可用通常剂量的酚苄明和普萘洛尔。正常肾上腺髓质可摄取123I-MIBG。MIBG发现嗜铬细胞瘤的敏感性为78%~95%,特异性为90%~100%。Tshii等报道的果是:在48例患者(嗜铬细胞瘤16例、神经母细胞瘤23例、甲状腺髓样癌7例、Sipple综合征2例)140个病灶中,123I-MIBG的真阳性率51/140,真阴性率79/140,假阳性率1/140,假阴性率2/140,无诊断价值率7/140,总敏感率96.2%,总特异性98.8%,精确率97.7%,以注射药物后4小时和24小时摄片的诊断效果较好。MIBG诊断嗜铬细胞瘤的假阴性率极低,阳性率高,故是目前(尤其是在用生化检查不能确诊时)肿瘤术前定位和术后追踪的首选方法。因为它能使整个机体的嗜铬组织显像,故其对肾上腺外的肿瘤和恶性嗜铬细胞瘤的转移病灶的发现有重要的价值,对于肾上腺内的肿瘤,其准确性与MRI基本相同。但其缺点是空间分辨率较低,某些肿瘤对MIBG缺乏摄取能力。
生长抑素类似物扫描诊断肾上腺外嗜铬细胞瘤
生长抑素是14肽神经递质,含14个氨基酸,生物半衰期约2~4分钟。大部分神经内分泌细胞表达生长抑素受体,肾上腺髓质和副神经节的生长抑素受体表达水平较高,而嗜铬细胞瘤的生长抑素受体密度最高,故某些合成的稳定的生长抑素类似物如奥曲肽(octreotide)或喷曲肽(pentetreotide)等能进行放射性核素显像,可用于嗜铬细胞瘤的定位诊断,特别适用于肾上腺外嗜铬细胞瘤和恶性嗜铬细胞瘤的诊断。111In(铟)标记的DTPA(二乙烯三胺五乙酸)-D-Phe-奥曲肽(111In-喷曲肽)广泛用于神经内分泌肿瘤的检查。不像MIBG,111In-喷曲肽对于神经节肿瘤是非特异性的,在很多其他肿瘤、肉芽肿性疾病及自身免疫性疾病也为阳性。对于成人111In-喷曲肽的推荐剂量是90~110MBq,儿童剂量应通过计算而得。使用111In(铟)标记的示踪剂不需要对甲状腺进行阻滞,111In-喷曲肽几乎全部经肾脏排泄。在注射后24小时和48小时扫描可得到全身的二维显像,24小时后可作SPECT显像。111In-喷曲肽正常可由垂体、甲状腺、肾脏、肝脏、脾脏及膀胱摄取,在乳腺、胆囊、消化道也有部分摄取。影响111In-喷曲肽与神经内分泌肿瘤结合的因素有:不同亚类生长抑素受体的亲和力不同,肿瘤不同的分化程度对生长抑素受体表达的影响,非标记的生长抑素产生增多等。在扫描前1周,应停用治疗使用的生长抑素类似物。在嗜铬细胞瘤和副神经节瘤的诊断中,生长抑素受体闪烁扫描的敏感性为88%,准确性低于MIBG或MRI;由于111In-喷曲肽与神经内分泌肿瘤的结合率不同,其特异性也低于MIBG;但也有MIBG阴性而奥曲肽阳性的报道。
18F-DOPA-PET具有更高解剖分辨率
多数副神经节瘤不分泌儿茶酚胺,而仅仅分泌多巴胺,但是这些肿瘤细胞的细胞膜或细胞内存在去甲肾上腺素转运体囊泡。另外,肿瘤细胞的凋亡、缺氧、酸中毒、无氧酵解和血管生成等均为定量影像检查,尤其是PET提供了方便。选择PET核素标记物的原则是:①肾上腺PGL(即嗜铬细胞瘤)首选18F-FDA或18F-FDOPA-PET,亦可考虑123I-MIBG扫描,但效果较差;②肾上腺外PGL首选18F-FDOPA-PET,但SDHB突变者的显像效果较差,此时可选用18F-FDG-PET(18F-FDAPET的效果一般);③转移性PGL者宜首选68Ga-DOTATOC/ DOTANOC-PET(新一代生长抑素类似物标记PET),其次可选111In-喷曲肽扫描,而123I-MIBG的效果一般。
用18F标记的多巴(18F-DOPA)进行正电子体层扫描是基于神经内分泌肿瘤对氨基酸如多巴及其生物胺的摄取、脱羧及储存能力。在成人18F-DOPA的推荐剂量是200~300MBq,在静脉注射后约45~90分钟开始PET扫描。18F-DOPA的生理性摄取发生在纹状体、胰腺、胆囊及泌尿系,在某些患者也可见到结肠及退行性骨病的非特异性摄取。与MIBG及生长抑素类似物闪烁扫描比较,18F-DOPA-PET有更高的解剖分辨率。18F-DOPA聚集的低背景能使嗜铬细胞瘤及副神经节瘤与周围组织形成对比,并且容易进行图像分析。其高的空间分辨率与特异性选择的示踪剂结合,在4小时内能得到质量极高的全身显像。而MIBG及生长抑素类似物闪烁扫描在示踪剂注射后24小时才能获得最早的显像。
18F-FDG-PET用于良恶性嗜铬细胞瘤的鉴别优于CT或MRI(下图)。18氟标记的脱氧葡萄糖(fluorodeoxy-D-glucose,FDG)是多种恶性肿瘤诊断和分类的重要临床工具。葡萄糖的类似物FDG进入细胞的方式与葡萄糖相同,与葡萄糖不同的是其被细胞捕获后进行磷酸化后不再代谢,因此细胞内FDG浓度反映了细胞内葡萄糖的代谢状况,而在多种肿瘤细胞中葡萄糖的代谢是显著增加的。有报道在肾上腺恶性肿瘤和转移癌中,18F-FDG-PET的敏感性可达100%;另外初步结果显示,18F-FDG-PET可以用于鉴别良性的皮质腺瘤和肾上腺癌,其作用可能优于CT或MRI。
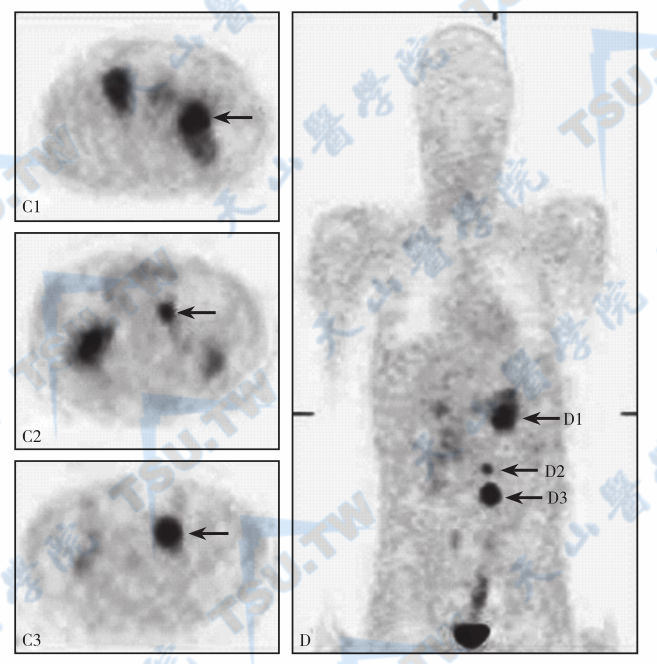
18F-DOPA-PET阳性的肾上腺肿瘤
注:C:矢状面显像。C1:左肾上腺嗜铬细胞瘤、胆囊;C2、C3:腹腔淋巴结转移灶。D:冠状面显像。D1:左肾上腺嗜铬细胞瘤;D2、D3:腹腔淋巴结转移灶
11C-甲咪酯(metomidate)核素-PET鉴别病变性质
如能判断肾上腺素和去甲肾上腺素的分泌比例,对定位诊断有帮助,除肾上腺内或Zuckerkandl体的肿瘤外,其他部位的嗜铬细胞瘤均以分泌去甲肾上腺素为主。肾上腺皮质肿瘤与髓质肿瘤的鉴别相当困难,一般的影像检查几乎无法鉴别两类肿瘤;另一方面,有时又可发生皮质-髓质同时增生或混合瘤,除了临床表现和实验室检查外,较好的鉴别手段是11C-甲咪酯核素PET扫描检查。11C-甲咪酯为肾上腺皮质细胞11β-羟化酶的示踪剂,故用此法能较好地将肾上腺皮质和髓质病灶分开。根据Bergstrom等的经验,可将皮质瘤、皮质癌、皮质结节性增生、嗜铬细胞瘤和髓质髓脂瘤、囊肿等较好地鉴别开,不过,11C-甲咪酯扫描的最大优点是鉴定皮质病变。
下腔静脉插管定位嗜铬细胞瘤
当定性诊断确诊为嗜铬细胞瘤而上述定位检查未能发现肿瘤时,可采用此方法。如果一侧肾上腺静脉中去甲肾上腺素明显增高或去甲肾上腺素/甲肾上腺素比值(正常者<1)>1须考虑诊断嗜铬细胞瘤。但应注意右肾上腺静脉较短,易被下腔静脉血稀释,故最好同时测定血浆皮质醇作为对照以判断有无稀释。应注意在操作时有诱发高血压危象发作的可能,必须准备酚妥拉明并建立静脉通道。
病理检查鉴定嗜铬细胞瘤生物学行为
肾上腺皮质的组织病理学检查缺乏特异性。例如,先天性酶缺陷所致的肾上腺皮质增生与CRH/ACTH依赖性CS所致的皮质增生在细胞形态学上并无本质差异,异位CRH/ ACTH分泌综合征所致的或原因未明的肾上腺皮质增生均很难用一般病理形态学方法鉴别。
基因突变检测遗传病因
一些肾上腺皮质的恶性肿瘤可伴有癌基因表达的异常,但这些异常一般在血液中并无特异性标志物。先天性肾上腺皮质增生和一些肾上腺皮质功能不全与合成类固醇激素的酶基因异常有关,对酶(如11-、17-和21-羟化酶)基因进行分析可明确病因诊断,例如可用单链构象多态性(single strand conformation polymorphism,SSCP)分析来诊断CYP11B1或其他致病候选基因的突变(如G267R、G267D、Q356X、R427H、C494F等)或CYP11B1/CYP11B2嵌合基因。此外,ACTH过敏综合征、糖皮质激素抵抗综合征、遗传性Cushing1综合征、醛固酮不敏感综合征、表观盐皮质激素过多(apparent mineralocorticoid excess,AME)综合征、遗传性副神经节瘤等有赖于相关基因的分子生物学鉴定,才能做出最后的病因诊断。
遗传性嗜铬细胞瘤需根据家族史和风险度确定候选基因筛选和追踪。一般情况下,有家族史的腹部分泌儿茶酚胺的副神经节瘤患者按顺序对SDHB、SDHD、VHL基因测序,发现突变即终止下一步筛选;患者存在双侧肾上腺嗜铬细胞瘤,但无甲状腺髓样癌或甲状腺肿,则先对VHL基因测序,如VHL无突变,再检测RET;发病年龄<20岁的单侧肾上腺嗜铬细胞瘤者则按顺序对VHL、RET、SDHB、SDHD基因测序,发现突变即终止下一步筛选;而年龄>20岁的单侧肾上腺嗜铬细胞瘤者按顺序对SDHB、SDHD基因测序。如果在追踪过程中筛选到了任何一种致病基因的种系(胚系,germline)突变,就应该对相应的遗传性肿瘤进行全面检查,但单侧和双侧遗传性嗜铬细胞瘤患者的遗传病因筛选和追踪是有区别的。(方团育 伍西羽 廖二元)
