支链氨基酸(branched chain amino acids,BCAAs),特别是亮氨酸(leucine)或者其代谢产物β-羟基-β-甲基丁酸(beta-hydroxy-beta-methyl butyrate,HMB)均被证实有一定拮抗恶液质疗效。其机制在于一方面能够抑制双链RNA依赖的蛋白激酶(doublestranded RNA-dependent protein kinase,PKR)的磷酸化,同时激活PI3K/Akt,抑制Foxo的活化,减少MuRF-1和Atrogin-1的表达,从而阻断恶液质的发生。二十碳五烯酸(eicosapentaenoic acid,EPA)能够抑制AA释放,稳定IκB/NF-κB复合体,起到抑制UPS激活的作用。已有试验表明胰腺癌患者使用富含EPA营养剂(1.09g/d)7周后,体重增加2kg。但是最近大样本随机双盲试验证实与安慰剂组相比,EPA(2g/d或4g/d)单药治疗组的恶液质患者体重增加并未取得显著差异。而肿瘤恶液质患者使用蛋白酶体抑制剂后并未获益,提示相比泛素蛋白酶本身,针对UPS上游信号通路的调节在恶液质的治疗中可能发挥更重要的作用。
如最近Zhou X等研究发现ActRⅡB,一种活化素(activin)Ⅱ型受体,可能成为新的治疗靶点。该受体可以介导转化生长因子(transforming growth factor,TGF) -β超家族成员Myostatin、activin等信号通路,促进MuRF-1 和Atrogin-1的表达,导致骨骼肌的降解。但是给予恶液质小鼠(C26结肠细胞种植、inhibin-α敲除) sActRⅡB,即一种重组activin受体诱饵分子后,不仅可以阻止肌肉分解,肌肉块质量增加,还可以逆转骨骼肌和心肌萎缩。其机制与sActRⅡB降低MuRF-1和Atrogin-1过表达有关。TRAF6也同样有可能成为恶液质治疗靶点(图2-8-4)。
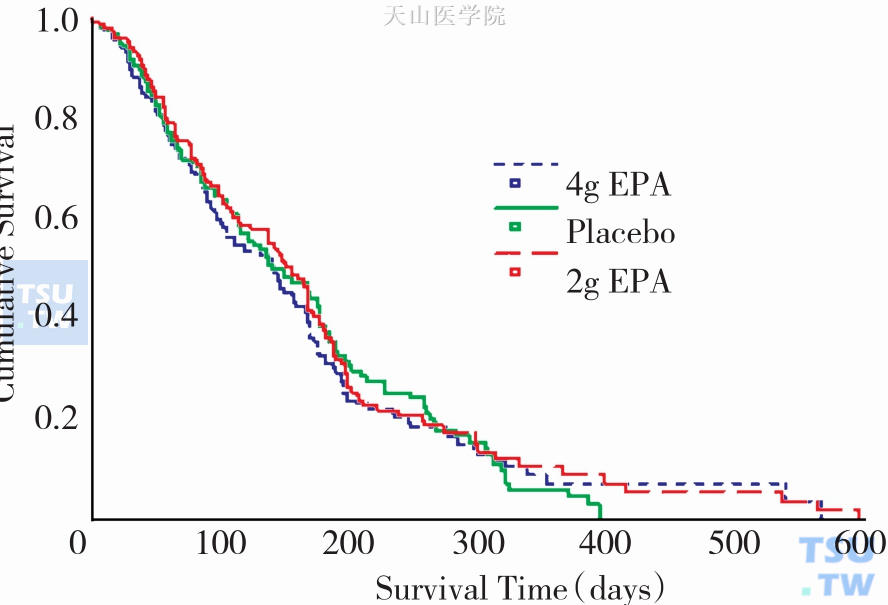
图2-8-4 恶液质患者口服EPA或者安慰剂生存分析(″=0.75)
