继发性甲旁亢的治疗包括内科治疗和手术治疗。内科治疗的目的是纠正代谢紊乱,使血钙、磷和PTH浓度保持在正常范围内。在发生严重继发性甲旁亢症状前,给予适当治疗可使多数患者避免手术,一般当肌酐清除率降至40ml/min时,即应预防继发性甲旁亢的发生。对于有手术指征的患者,在条件和时机不成熟时,可以先行药物治疗和对症处理,为手术治疗创造条件。
原发病的治疗措施包括抗感染、维持电解质平衡、避免应用对肾毒性药物,必要时采用血液透析及肾移植。卧床者要增加户外活动,尽可能减少糖皮质激素的用量,并缩短用药时间。减少含磷和蛋白质较高的肉类及奶制品摄入,使每日的磷摄取量保持在0.6~0.9g。避免使用磷结合剂(如氢氧化铝胶),因其可致铝性骨病,而不含钙的磷结合剂(如无钙无铝无磷结合剂RenaGel)具有许多优点。ABD治疗的核心问题是使用低钙透析液和低剂量VD,以恢复PTH活性,停用含钙的磷结合剂和补钙治疗。盐酸司维拉姆、镧(lanthanum)盐和低盐透析液是目前预防ABD的主要方法。
根据需要补充钙剂和维生素D
钙剂
一般低磷饮食的含钙量低,所以需补充钙剂。补钙除了纠正体内缺钙状态外,尚有助于抑制PTH的过度分泌,降低血磷水平。元素钙摄入量应达到1.0~1.2g/d,首选碳酸钙。补钙过程中,每2周测定1次血钙和血磷,保持血钙磷乘积(血钙浓度mg/dl,血磷浓度mg/dl)低于55,以防止发生软组织钙化。
普通VD
补钙需同时补充VD制剂,以促进肠道钙吸收。低剂量VD抑制血管钙化,并促进骨形成,刺激骨的微重建(mini-modelling,即独立于局部骨吸收的骨小梁骨生成)。慢性肾病患者补充VD除治疗继发性甲旁亢,还有多种益处。一般推荐对慢性肾病患者进行常规PTH测定,并按照肾病分期,确定治疗的目标PTH值(如第5期慢性肾病者的血PTH值应控制在150~300pg/ml)。如果PTH高于目标值,应该使用VD或拟钙制剂(calcimimetic agents);相反,如果PTH低于目标值,应该停用任何抑制PTH分泌的药物,以免引起ABD和软组织钙化。3~4期慢性肾病如PTH>70pg/ ml,建议首先使用VD使血25-(OH)D恢复正常。在多数情况下,可使用25-(OH)D,因为价廉,并极少出现中毒或过量现象。如果血清25-(OH)D低于30ng/ml,每月补充25 000U是安全有效的。
活性维生素D
活性维生素D可部分逆转骨病变,1,25-(OH)2D的剂量一般为0.5~1.0μg/d;但长期用骨化三醇治疗有可能引起高钙血症和异位钙化。慢性肾病患者VD和钙制剂的治疗方案见下表。
慢性肾病并继发性甲旁亢的治疗方案

VD受体激活剂和钙受体激动剂降低PTH分泌
VD受体激活剂
如果血清PTH≥300pg/ml,应选择性VD受体激活剂(selective VD receptor activator),抑制炎症、血栓栓塞和血管平滑肌细胞增殖与钙化,并可降调节肾素-血管紧张素-醛固酮系统,有助于高血压和水肿的治疗。维生素D受体(VDR)激动剂分为非选择性VDR激动剂(nonselective VDRAs)和选择性VDR激动剂(selective VDRAs,如paricalcitol)两类。选择性VDR激动剂对肠钙吸收和骨钙代谢无明确作用,而对心血管钙化和相关并发症有防治意义。VD受体激活剂对血管钙化的影响属于双相剂量反应(biphasic-dosage-response)性的。低剂量时表现为抑制作用而高剂量时表现为兴奋效应,而paracalcitol在降低血PTH方面与1,25-(OH)2D差不多,但引起高钙血症和异位钙化的不良反应明显减少。paricalcitol治疗12周可使PTH降低60%,不过血钙和血磷有上升趋势。副作用包括口干、消化道出血、恶心、呕吐、水肿等。继发性甲旁亢治疗中的骨代谢状况监测主要依靠骨组织病理检查和骨代谢生化标志物测定。由于前者不是临床常规检查项目,因此有人提出,主动脉钙化指数>8/24提示为ABD。当PTH降低时,药理剂量的VD即成为促进动脉钙化和无动力性骨病的危险因素。
钙受体激动剂
盐酸西那卡塞特(cinacalcet hydrochloride)是苯乙胺Ⅱ型拟钙类似物家族的成员,属于拟钙类似物的盐酸盐,作用于甲状旁腺钙受体(CaR),使PTH分泌降低。如果患者没有VD缺乏,可用西那卡塞特替代1,25-(OH)2D。西那卡塞特与paracalcitol合用可更好地控制继发性甲旁亢。因部分继发性甲旁亢是由于甲状旁腺钙受体表达降低所致。paricalcitol的用量可从6μg/周开始,并根据需要增加用量,最大剂量180mg/d。2004 年起,临床使用西那卡塞特治疗透析的继发性甲旁亢患者,使用6 个月后可使部分患者的血钙磷有所纠正,PTH下降约30%;但对多数病例的效果不佳,甚至引起更为严重的高PTH血症或高磷血症。本药亦可同时降低血PTH和血钙,主要用于慢性肾病并继发性甲旁亢和甲状旁腺癌伴高钙血症的治疗。口服后的血浓度高峰见于2~6小时,绝对生物可用度20%~25%。该药与碳酸钙或磷酸盐结合剂(司维拉姆,sevelamer)不存在相互作用,半衰期30~40小时,7天内达到血清稳态浓度,分布容量1000L,常用量50~100mg/d。当血钙升高时,激活CaR而使PTH的分泌迅速下降;相反,当血钙降低时,CaR被抑制而促进PTH的分泌;因而既可降低血钙又可抑制甲状旁腺细胞增生。
根据病情确定和调整透析液钙浓度
近数十年来,终末期骨病主要表现为ABD,这主要与糖尿病、高龄、含钙的磷结合剂、VD和高钙透析液的使用有关。特别是含钙的磷结合剂与VD联合应用时,可引起严重的PTH抑制并进一步导致ABD。长期的血液透析治疗可维持肾功能正常,但并不能完全纠正骨代谢紊乱,亦难以降低心血管病并发症。透析液中的钙浓度是决定性因素,钙浓度不能一成不变,一般应根据个体的具体情况进行调整,钙浓度过高或过低都是有害的。调整的具体方案应主要由体内的钙量和血钙、血磷确定,其主要目的是降低心血管钙化和由此引起的并发症。
低钙透析液
低钙透析液(1.25~1.3mmol/L)可提高骨的代谢转换率,最适合于ABD患者,并可减少高钙血症和异位钙化的发生率,但应同时给予VD制剂和磷结合剂。低钙透析液的缺点是容易诱发心血管功能紊乱和透析期低血压(intradialytic hypotension)。
高钙透析液
高钙透析液(1.75mmol/L)有利于提高血钙浓度和降低血磷,适合于用磷结合剂或经补钙治疗后血钙仍降低的患者,高钙透析液抑制PTH的分泌,但易导致高钙血症、异位钙化和甲状旁腺功能过度抑制,引起ABD。在慢性肾病患者中,血管钙化和异位钙化与骨形成呈反变关系,尿毒症毒素(如硫酸吲哚酚,indoxyl sulphate)增多和骨形成蛋白减少可能是继发性甲旁亢的适应性反应,而VD受体激活剂引起的PTH过度抑制可被拟钙类似物抵消。因此需要应用拟钙类似物预防。
最佳透析液
应用广泛,对于大多数患者来说,透析液钙浓度1.5mmol/L可能为最佳透析液,因为它既对骨组织有一定的保护作用,又可降低心血管危险性。但是,长期透析、每日透析或夜间透析者究竟以何种浓度为最佳,则需根据个体的具体情况而定,因为每一例患者的病情都是不同的,而且时刻在变化。
甲状旁腺切除治疗特殊病例
手术适应证
如经3~4个月治疗后PTH仍不下降,骨病变无好转,应次全切除增生的甲状旁腺。继发性甲旁亢的手术适应证为:
- 慢性肾病及继发性甲旁亢有症状及并发症(严重瘙痒、广泛软组织钙化、骨痛、病理性骨折、精神异常等),或血钙磷乘积持续>70,或血钙>2.75mmol/L者;
- 经B超、核素扫描及CT等检查证实甲状旁腺明显增大及PTH明显增高(>800pg/ml)者;
- 肾移植后持续性高钙血症(血钙>2.87mmol/L)6个月以上,特别是肾功能损害加重者;
- 三发性甲旁亢;
- 血PTH正常,但伴有高钙血症者。继发性甲旁亢手术治疗筛选和手术指征见下图。
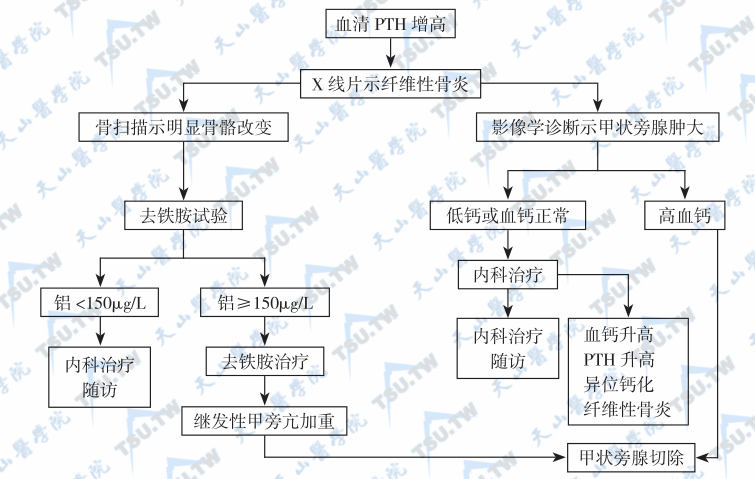
继发性甲旁亢患者手术治疗对象的筛选
术前准备
肾性骨营养不良症血液透析者及严重继发性甲旁亢的术前准备包括控制血钾和高血容量,治疗高血压及冠心病。宜于甲状旁腺手术前连续2日血液透析,可避免手术后次日作血液透析及应用抗凝药。因为无论局部或全身应用肝素都存在出血可能,故手术后的血液透析时间应推迟2~3天。腹膜透析持续术前,术后4~6小时(麻醉清醒后)即可重新透析。围术期应定期测定血PTH水平,并监测病情变化。
手术方式和病情监测
继发性甲旁亢的病理基础是甲状旁腺增生,手术采取甲状旁腺次全切除或全切除后自体移植。原发性、继发性和三发性甲旁亢手术应常规进行术中PTH(intraoperative PTH,IOPTH)监测,但继发性与三发性甲旁亢手术时的IOPTH结果分析有所不同,需要特别考虑肾功能和测定方法的影响。如果IOPTH降至基础值的50%以下,可认为切除的甲状旁腺组织已经充分,因为切除的甲旁腺腺体多而且PTH在肾脏的清除缓慢,观察IOPTH下降的时间应由原发性甲旁亢的10~30分钟延长至继发性甲旁亢的1小时以上。三发性甲旁亢的IOPTH判断标准仍未统一,建议适当提高治愈阈值(65~200pg/ml),以防发生永久性甲旁减(原发性甲旁亢的PTH下降时间为10分钟,<35pg/ml或下降90%为治愈)。
1、甲状旁腺次全切除术
选择该种手术方式的根据是:①手术后若能接受适当的内科治疗,残存的甲状旁腺并不会导致甲旁亢复发;②术后甲旁减较甲状旁腺全切除少,持续时间较短;③移植甲状旁腺组织的长期功能未确定;④手术时间较短;⑤有的甲状旁腺全切除者虽移植物的功能良好,但容易发生骨质软化症。
2、甲状旁腺全切加自体移植
其根据是:①继发性甲旁亢作次全切除术后,若患者不合作,未能适当用药而引起继发性甲旁亢复发,而全切的效果可靠;②全切时可确切了解甲状旁腺数目,明确有无异位甲状旁腺,移植后的腺体组织若功能过高,易于处理,在局部麻醉下即可清除部分腺体组织。移植时,将其中1个甲状旁腺切成1mm×1mm×3mm的小片,在一侧前臂屈肌内植入15~20小片,切开肌膜后置于肌袋中,黑丝线缝合肌膜并作为移植标记。荧光素氨基乙酰丙酸(aminolevulinic acid,ALA)可清楚地显示甲状旁腺,而甲状腺和其他组织不显影,有助于定位。
术后低钙血症处理
1、甲状旁腺次全/全切后低钙血症
需立即进行如下治疗:①若血钙1.62~2.00mmol/L,可口服钙剂,每4小时 2.5g;②明显低钙血症应给予10%葡萄糖酸钙10~20ml加等量葡萄糖注射液,稀释后缓慢静脉注射,每5~10分钟 1次,直至手足抽搦停止。然后以10%氯葡萄糖酸钙10~50ml加于5%葡萄糖液1000ml中静脉滴注,控制滴速,保持血清钙在1.75mmol/L以上。③首选1,25-(OH)2D,最初剂量0.25~0.5μg,每天2次,因其反应快而半衰期短,即使患者已无低血钙症状,仍需继续补充;④血清磷增高时限制磷摄入,必要时应用磷结合剂;⑤血液透析应推迟到手术后的第2天,增加透析液中的钙浓度,纠正低钙血症和低镁血症。
2、甲状旁腺次全切除-前臂自体移植后血PTH升高
其可能原因包括:①移植物分泌过多PTH;②残余有甲状旁腺组织或前纵隔甲状旁腺组织;③怀疑为甲状旁腺癌时,用止血带扎紧移植侧前臂,然后再测血PTH,如果快速下降,证明是移植物分泌过多,反之要做扫描、超声、CT/ MRI检查,寻找其他部位的甲状旁腺组织;④移植甲状旁腺致甲旁亢的复发率约10%,第5年约20%,术后第7年约30%。因此,甲状旁腺移植者的血清PTH监测频度应随时间而提高。
综合治疗CAP
血清PTH明显升高并计划做甲状旁腺切除术的患者应该首先使用钙受体调节剂(盐酸西那卡塞特)治疗,如果患者对西那卡塞特的反应差,要考虑尽早甲状旁腺切除。甲状旁腺切除加或不加自体甲状旁腺移植是治疗顽固性继发性甲旁亢的有效方法,有时亦适合于药物治疗失败者。二膦酸盐具有抗炎作用,可抑制破骨细胞活性,降低局部巨细胞的活性。一般认为,二膦酸盐的益处来源于其抗炎活性而对非矿物质的代谢作用。抗血栓治疗有一定效果,当其他治疗无效时可慎重使用,一般用低剂量的纤溶酶原活化剂,但应注意内脏出血可能。许多CAP患者的闭塞性血栓形成反复发作,因此抗氧化治疗是合理的选择。
硫代硫酸钠具有较强的抗氧化作用,可通过各种硫醇反应抗氧化,分子中的2个非配对电子可淬灭ROS的氧化应激,使eNOS复活。研究发现,本药可减轻疼痛和炎症,溶解钙盐,逆转内皮细胞功能紊乱,并有一定的扩张血管作用。该药主要用于CAP所致的组织坏死、反复发作的尿钙结石、肾钙盐沉着症、肿瘤性钙盐沉着症等。主要不良反应是升高阴离子间隙水平,故可引起轻度代谢性酸中毒。
近年发现,钙受体变构辅活化因子(allosteric coactivators)是血管钙化的抑制剂,通过血管钙受体和甲状旁腺钙受体抑制高PTH血症、高钙血症和高磷血症,而具有防治血管钙化作用。
其他的治疗措施包括:①伤口处理;②高压氧治疗;③避免局部创伤;④缓解疼痛;⑤纠正血清PTH和钙磷异常。外科处理包括溃疡清创和肢体血管重建等。(廖二元)
