引起糖皮质激素抵抗的临床疾病有家族性/散发性糖皮质激素抵抗综合征、类风湿关节炎、骨关节炎、SLE、Crohn病、溃疡性结肠炎、脓毒败血症、呼吸窘迫综合征、支气管哮喘、Cushing病等。在这些疾病(如慢性阻塞性肺病和呼吸窘迫综合征)的治疗过程中,糖皮质激素抵抗患者表现为糖皮质激素治疗抵抗,而对非糖皮质激素抗炎药物,如钙神经素抑制剂(calcineurin inhibitors)、免疫调节剂(immunomodulators)或磷酸二酯酶-4抑制剂(inhibitors of phosphodiesterase-4)及核因子κB(nuclear factor kappaB)抑制剂的效果良好。
继发性糖皮质激素抵抗导致治疗失败
糖皮质激素和盐皮质激素通过它们的受体,两者的作用是相互配合的。类固醇类药物同时作用于两种受体,长期应用可导致糖皮质激素受体-α的表达下调,糖皮质激素受体的半衰期明显下降,引起糖皮质激素抵抗。另一方面,盐皮质激素的代谢酶11β-HSD2的改变也与糖皮质激素抵抗有关。当11β-HSD存在缺陷,而糖皮质激素明显升高时,MR被激活,而糖皮质激素受体的正常活性被抑制,出现糖皮质激素抵抗(肾和结肠为主)。
躯体疾病引起继发性糖皮质激素抵抗
继发性糖皮质激素抵抗可见于某些对糖皮质激素治疗无反应的淋巴细胞性白血病、神经性厌食、获得性免疫缺陷综合征(AIDS)、肾功能不全、某些类风湿关节炎、支气管哮喘、ACTH瘤等疾病。糖皮质激素IS的临床表现一般不明显,且可被原发性疾病的临床表现所掩盖,直到行实验室检查才被发现。AIDS患者伴随的GCIS,其临床表现与Addison病类似,包括皮肤色素沉着、软弱乏力和低钠血症等,实验室有血皮质醇和尿游离皮质醇明显增高,且不被小剂量的外源性DXM抑制,ACTH正常或升高,糖皮质激素受体亲和力降低。但少数患者糖皮质激素受体数目增加,对此尚无满意解释。终末期肾衰竭患者不管是否需要作透析治疗,均有血皮质醇明显升高,且不被外源性DXM抑制,患者垂体-肾上腺轴功能关系异常是由于存在糖皮质激素抵抗,而不是由于ACTH分泌增多所致。
获得性免疫缺陷综合征
在AIDS患者中,有血皮质醇和尿游离皮质醇升高,有些患者的血ACTH亦升高,血皮质醇不受外源性DXM抑制,患者血中单核细胞结合3HDXM的亲和力降低,且DXM抑制3H-胸腺嘧啶结合只有对照组的一半(23% vs 50%),但糖皮质激素受体数目比正常组织增加[(16.21±9.41)fmol/106细胞对(3.15±2.33)fmol/106细胞]。
肾衰竭
患者在接受透析治疗时,血皮质醇升高且不能被DXM抑制,但对CRH刺激有正常反应。至于慢性淋巴细胞性白血病和神经性厌食患者,则往往有糖皮质激素受体数目减少。此外,米非司酮(mifepristone,RU486)为糖皮质激素受体阻滞剂,长期服用可引起与糖皮质激素IS极为相似的临床表现。
其他疾病
对糖皮质激素治疗无反应的少数慢性淋巴细胞性白血病、神经性厌食、酒精中毒和重症抑郁性精神病患者均有血皮质醇升高,垂体-肾上腺皮质轴关系也不正常,可能存在GCIS。Feller等报道1例转移性肾上腺皮质癌患者,分泌大量的糖皮质激素和盐皮质激素,而雄性类固醇很低,尿中排出大量的类固醇激素代谢产物,肿瘤组织分泌大量的P-糖蛋白(P-glycoprotein,Pgp)和肺抵抗相关蛋白(lung resistance-related protein)。肿瘤细胞对各种抗癌药物存在显著抵抗现象是因为肿瘤细胞表达了大量的突变型P53蛋白,致使抗癌药物不能诱导肿瘤细胞的凋亡,不过神经性厌食患者常伴有糖皮质激素受体数目减少。
继发性糖皮质激素IS的基本缺陷见下表。
继发性GCIS的基本缺陷
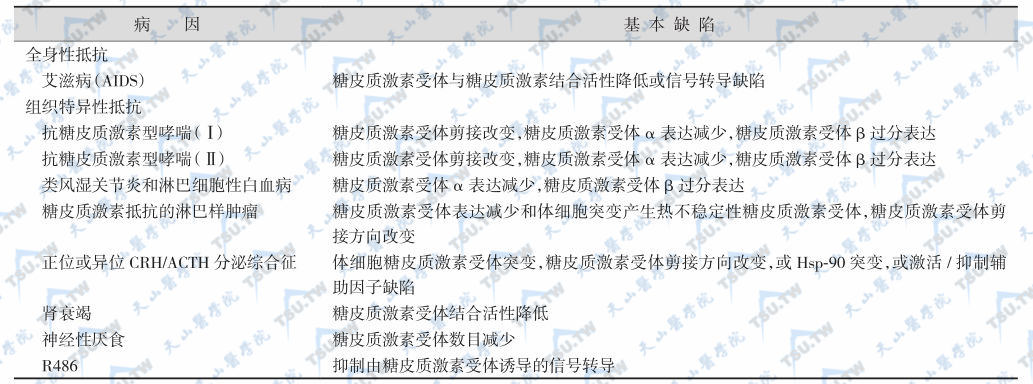
注:GCIS:糖皮质激素不敏感综合征;GC:糖皮质激素;GR:糖皮质激素受体
Cushing综合病患者的垂体ACTH细胞常发生糖皮质激素受体基因点突变,但这并非引起糖皮质激素抵抗的原因,但该受体基因的杂合性丢失(loss of heterozygosity,LOH)可产生相对性糖皮质激素抵抗,这些患者似乎更容易表现为ACTH分泌的自主性。由于垂体对糖皮质激素不敏感,垂体分泌ACTH不受糖皮质激素的反馈抑制,ACTH分泌增多,以致肾上腺皮质3种激素的生成和分泌均增多。但由于靶细胞对糖皮质激素不敏感,故无CS的临床表现,而只有皮质酮和肾上腺皮质雄激素增加的相应表现。
