睾丸(testis)是男性的性腺(gonad),主要具有两种功能,一是性类固醇激素和其他睾丸激素的合成与分泌功能,主要由Leydig细胞和Sertoli细胞分泌睾酮(testosterone)、雌激素(estrogen)、抑制素(inhibin)、活化素(activin)、抗苗勒管素(anti-Müllerian hormone,AMH)、胰岛素样因子3(insulin-like factor 3,INSL3)及许多细胞因子;二是生殖功能,主要由曲细精管的上皮细胞生成精子(spermatozoa)。两种功能是相互配合,密切联系的,任何一种功能障碍必然导致另一种功能异常。
睾丸体积主要由曲细精管决定
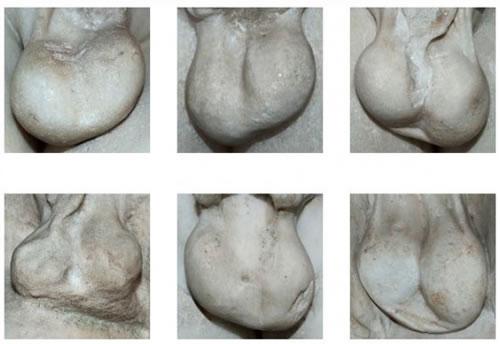
睾丸是一对略扁的卵圆形组织,分别位于阴囊隔两侧的阴囊(scrotum)内,其纵轴由上前外方斜向下后方。正常成年男子每侧睾丸重20~30g,长径4~5cm,容积15~25ml。后缘的睾丸白膜增厚而形成睾丸纵隔,由纵隔伸出结缔组织隔将睾丸分隔成约250个锥形小叶,每一小叶有1~3条曲细精管,每个睾丸共有600~1200条曲细精管(seminiferous tubules),总长度约250m。曲细精管在小叶内迂曲前进,相互吻合,接近睾丸纵隔时融合为输精管(seminiferous tubules,tubuli seminiferi recti)。输精管进入纵隔后反复分支吻合,形成睾丸网(rete testis)。睾丸网从后上部发出8~12条输出小管,构成附睾(epididymis)头,然后融合成附睾管。附睾管沿睾丸后缘迂曲下行,形成附睾的体部和尾部。睾丸的体积主要由曲细精管决定,并受FSH的调节。
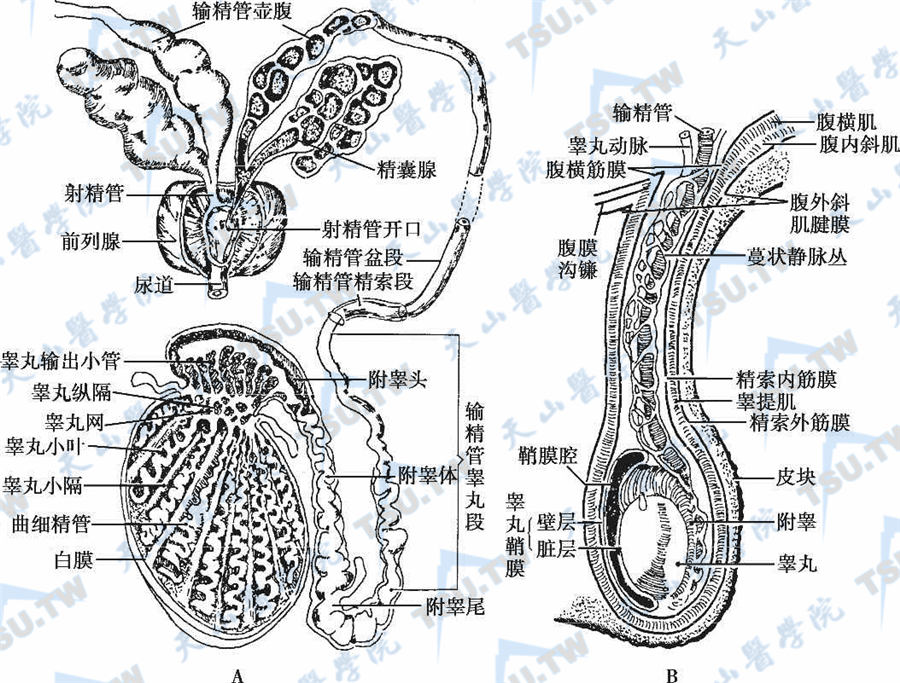
睾丸及其附属器官;注:A:睾丸的结构与排精系统;B:睾丸、附睾与精索
精液含有充分的能源和营养
在男性的生殖道内,精子悬浮于液体之中,射出体外时,与附睾、精囊、前列腺和尿道球腺分泌的液体混合(精浆,seminal plasma)。精浆和精子混合物为精液(semen)。精子只占精液容积的5%。如果分段收集精液,即可发现前部的精子密度、精子运动力和生存率都显著高于后部,前一部分的精浆成分主要为附睾液、前列腺液和尿道球腺液,后一部分主要为精囊液。精浆中某些电解质、蛋白质、氨基酸、脂肪和糖类的含量与血浆相同,另有一些成分为精浆所特有。精浆含有钠、钾、枸橼酸盐和碳酸氢盐(维持精浆pH的稳定)、多种蛋白水解酶(精液液化)、精胺(防止顶体酶原过早转化为顶体酶)、灭能因子(调节精子的能量转化)以及果糖、酸性磷酸酶(acid phosphatase,ACP)、锌、镁和前列腺素等。作为精子在女性生殖道转移和运动的载体,精浆含有可供精子直接利用的能源(果糖、山梨醇等),亦可缓冲阴道酸度。
精液射出后立即凝固,然后在20分钟内自然液化。这一过程受酶的催化,引起精液凝固的酶来自精囊腺,而液化酶来自前列腺和尿道球腺,至少有3种蛋白水解酶系(胃蛋白酶、纤维蛋白溶酶和糜蛋白酶样酶)参与了液化过程。分段收集精液时,前部通常不凝固,立即液化;后部迅速凝固而液化较慢。精液凝固时,精子被稽留在凝块内,直至完全液化后才能自由运动。这种延缓运动现象可能对精子的活动有保护作用。精液的液化与pH有关,只有在pH 6.8~8.8时才会液化,这是因为pH影响了与液化有关的蛋白水解酶降解的活性。附件器官炎症是精液凝固和液化异常的主要原因。
附睾是维持男性生殖功能的重要组织
附睾管(epididymal ducts)全长5~6m,卷曲于结缔组织鞘中,鞘再分出间隔进入管腔间隙,形成组织学上相同的若干区段,各段的上皮细胞有或无纤毛,细胞之间在靠近管腔侧形成紧密连接复合体(tight junctional complex,TJC),此即睾丸屏障(testicular barrier)。附睾尾连接输精管(vas deferens),折返向上,经腹股沟管进入盆腔,输精管末端膨大成输精管壶腹,长3~4cm,再次变细,在精囊末端汇合成射精管(ejaculatory ducts),进入前列腺(prostate),在精阜(colliculus seminalis)处开口于尿道的前列腺部。迂曲小管构成的精囊(约5cm×2cm)位于膀胱底与直肠之间和输精管的外侧。
附睾头是附睾上端的膨大部分,位于睾丸上端,主要由睾丸网发出10~15条输出小管盘曲而成,再由输出小管汇合成一条附睾管。附睾管是输出小管与输精管之间的管道,长4~6m、直径0.33mm,构成极度蟠曲的附睾体部和尾部,附睾尾部的附睾管内有一层平滑肌。附睾为精子成熟(sperm maturation)提供特殊内环境,与精子授精(sperm insemination)和运动能力的获得有关,作为精子成熟和贮存的部位,附睾在男性生殖中起重要作用。
Sertoli细胞/Leydig细胞/管周细胞是睾丸的功能细胞
Sertoli细胞
又称支持细胞(supporting cells),位于曲细精管表层。Sertoli细胞是一种高柱状非增殖性细胞,底部与曲细精管基底膜相连。顶部游离于管腔,胞质伸出突起并形成许多陷窝,生精细胞在该陷窝中完成发育过程。Sertoli细胞的主要功能是:①支持和营养作用:如果没有Sertoli细胞,生精上皮细胞不能成熟。②合成及分泌活性物质:包括FSH、活化素(activin)、卵泡抑素(follistatin)、Sertoli细胞刺激睾酮分泌因子(SCF)、促性腺激素释放激素(GnRH)、二氢睾酮、睾酮、雄烯二酮(Δ4-A)和雌二醇(E2)等激素类物质以及数十种蛋白质如细胞外基质胶原(如板层蛋白、Ⅰ和Ⅳ型胶原)、铜蓝蛋白、转铁蛋白(transferrin,TF)、胰岛素样生长因子(IGF)、白细胞介素(IL)、纤溶酶原激活物(PAS)、纤溶酶原抑制物(PAI)、转化生长因子(TGF)和硫化糖蛋白(SGP-1、SGP-2)等。在胚胎早期,Sertoli细胞分泌副中肾管抑制素(抗苗勒管素,anti-müllerian hormone,AMH),参与胚胎早期性别分化的调节。分泌的雄激素结合蛋白(androgen binding protein,ABP)可维持曲细精管内的高雄激素水平,为生精上皮细胞利用。分泌的抑制素(inhibin)能选择性抑制FSH分泌,对下丘脑-垂体-睾丸轴起调节作用。支持细胞产生的转铁蛋白将血中的铁离子(Fe3+)转到生精细胞内,促进其发育与成熟。粗线期精母细胞较其他细胞具有更多的转铁蛋白受体,反映其代谢活跃及对转铁蛋白的依赖性。③血-睾屏障(blood-testis barrier)作用:在睾丸生精小管中构成血-睾屏障,阻止外来抗原进入睾丸,防止自身抗原(生精细胞)引发的免疫应答。④吞噬作用:释放精子进入管腔,吞噬残余或凋亡的精细胞。
Leydig细胞
又称间质细胞(interstitial cells),位于曲细精管外的间质中,约占睾丸体积的5%~12%。细胞形态较大,直径15~20μm,呈圆形或多边形。胞质嗜酸性,细颗粒状,核圆形或卵圆形,核仁明显。超微结构显示胞质含丰富的滑面内质网、线粒体、脂滴和溶酶体。组织化学显示胞质含胆固醇、琥珀酸脱氢酶、3β-脱氢酶和酯酶等。Leydig细胞的主要功能是合成和分泌睾酮(testosterone),促进男性生殖器官的分化与发育,维持第二性征和促进精子生成。
管周细胞(peritubular cell)
管周细胞位于曲细精管管壁的最外层,具有成纤维细胞和平滑肌细胞的形态特性。过去认为管周细胞只有收缩功能,以促使不同发育阶段的生殖细胞在曲细精管内行进和排放。现发现,管周细胞表达丰富的雄激素受体(androgen receptor,AR),可在睾酮的作用下合成和分泌Ⅰ型胶原、纤维连结蛋白和管周支持细胞功能调节因子(peritubular factor that modulates Sertoli cell function,PModS)。PModS蛋白作用于Sertoli细胞,刺激其合成和分泌多种活性物质,参与精子发生的调节。因此,管周细胞是生殖调节网络中的重要细胞。
生精细胞经历多次发育演变为成熟精子
在生精细胞演变为精子的过程中,共经历5代发育过程,分别称为精原细胞、初级精母细胞、次级精母细胞、精子细胞和精子。
精子生成
睾丸的生精上皮细胞每天约产生123× 106个精子。精子生成(spermatogenesis)包括精原细胞增殖,初级精母细胞经过减数分裂由双倍体变成单倍体,形成次级精母细胞;再经过第2次减数分裂形成精子细胞,最后发育成精子(spermatozoa)。在这一过程中,至少有13种不同的细胞,即暗核A型精原细胞(Ad)、淡核A型精原细胞(Ap)、B型精原细胞(B)、前细线期初级精母细胞(PL)、细线期初级精母细胞(L)、偶线期初级精母细胞(Z)、粗线期初级精母细胞(P)、次级精母细胞(II)以及Sa、Sb1、Sb2、Sc、Sd1和Sd2精细胞,见下表。
人精子的发生周期
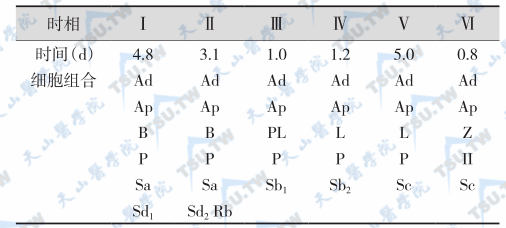
注:Ad:暗核A型精原细胞;Ap:淡核A型精原细胞;PL:前细线期初级精母细胞;L:细线期初级精母细胞;II:次级精母细胞;P:粗线期初级精母细胞;Sa~Sb2:早期精子细胞;Sc~Sd2:后期精子细胞;Rb:残余体
精原细胞从A型到B型分化,细胞核完成分裂后胞质并不完全分离,相邻两个细胞之间有胞质桥相连,这种现象称为克隆或同源群现象。胞质桥对细胞增殖的同步以及单倍体细胞基因的控制有重要意义。从曲细精管的某一固定点观察,可发现细胞的组合有固定规律,人类的生精上皮细胞可分为6个时相。其特征是:Ⅰ时相有圆形精子细胞,时相长约4.8天;Ⅱ时相有胞质残余体,时相长约3.1天;Ⅲ时相无精子,全部精子细胞核圆而淡染,时相长约1天;Ⅳ时相亦无精子,精子细胞核圆而浓染,时相长约1.2天;Ⅴ和Ⅵ时相均无幼稚精细胞,时相长分别为5.0天和0.8天,Ⅵ时相的另一个特点是终变期核分裂象。人类同一时相细胞的循环需要(16±1.0)天,称为1个生精上皮周期。从精原细胞到释放精子需要4个周期的时间。生精上皮周期各个时相在曲细精管上的分布在某些种属(如鼠、豚鼠和兔等)是连续性的,各期所占长度不同,但界限分明,某一横切面上是同一时相的细胞,这种现象称为生精上皮波。人类无生精上皮波现象,各时相只占曲细精管管壁的一部分,呈镶嵌式不规则排列,在一个横切面上可见到3~5个时相的细胞组合。
精子是精细胞发育演变而成,其过程分为4期:①高尔基复合体期:颗粒聚合形成顶体泡,附着于核膜上,附着点是以后精子核的尖顶。②顶体帽期:顶体泡沿核膜扩展,覆盖核的前半部,中心粒向相反方向转移,并突出于细胞表面,形成鞭毛雏形。③顶体期:顶体物质重新分布,核浆浓缩,精子变长,尾部进一步分化为中段、主段和末段。④成熟期:核浆均匀,不能分辨其内在结构。
精子形态和结构
人类精子形似蝌蚪,长约60μm。光镜下分头部和尾部,尾部又称鞭毛,头和尾间是短的颈部。头部正面观呈卵圆形,侧面呈梨形,长4.5μm,宽3μm,厚1.0μm,主要由细胞核、顶体及后顶体鞘组成。细胞核含高度致密而均匀的染色质。顶体覆盖头部的前2/3,含有透明质酸酶和顶体酶等多种水解酶,是精子赖以穿透卵细胞膜的物质基础。精子尾部与精子运动有关。电镜下,尾部可分为颈段、中段、主段和尾段。精子颈段起连接作用,由连接段和近中心粒组成。中段长5~6μm,有螺旋状包绕轴索的线粒体鞘,线粒体含有氧代谢和ATP形成所需的酶,是精子能量的主要来源。轴索的核心是轴丝,由一对中央纤丝和9对周边纤丝组成,轴丝外环绕着9条纵行的致密粗纤丝,外层粗纤丝是收缩运动的主要成分,能使局部收缩沿长轴传递。每对周边纤丝的内纤丝有一对达宁臂(dynein arm),即内臂和外臂,含ATP酶。轴丝可迅速传递冲动,引起颈部的节律性运动和协调外层粗纤丝的局部收缩运动。主段约长45μm,是尾部的最长部分,直径比中段小。主段和中段的分界线是终环,外层粗纤丝在主段远端逐渐变细消失。末端长5~6μm,直径更小,尾段只有轴丝而无外层粗纤丝。
精子获能
曲细精管释放的精子不具有自主运动和使卵子受精的能力,这些能力是精子通过附睾后获得的(获能,capacitation)。年龄和性活动影响精子通过附睾的时间。20岁时,通过的时间最短,约2.7天;性活动频繁者,通过时间显著缩短。附睾内储存精子的数目与年龄、精子发生速度和性活动有关。20~30岁男子附睾储存的精子为209×106,约60%在尾部。精子在附睾尾部能储存多长时间以及不被排出的精子在附睾内的转归尚未明了。
附睾头部的精子不能运动或只有高幅度低频率的尾部“抽打”,引起头部颤动,不能前进。50%以上的附睾尾部的精子有前向运动,精子的生殖能力通过附睾后获得。用人精子与地鼠无透明带卵子作用的实验证明,取自附睾头部的精子不能穿入卵子,而附睾尾部的精子则可以。通过附睾时,精子膜内成分和代谢发生变化,附睾头部的精子膜不能吸附带正电荷的氧化铁,而尾部的精子具有这种能力。此外,精子膜的植物血凝素结合特性、糖蛋白组成、免疫反应性和碘化特性都有改变,这些特性可能与附着于卵子透明带的能力有关。同时尾部的精子代谢率增高,在有氧条件下,抑制糖酵解的作用增强,氧的摄取利用以及能量底物的利用亦增高。
