欧洲姑息治疗研究协作委员会(EPCRC)已经发展了基于临床证据推荐的恶液质分类和治疗用于晚期肿瘤患者,并且作为临床指南工作。其中营养状态的评估是非常重要的环节,即对治疗方案的制定起到指导价值,同时也为治疗方案的效果提供客观的指标和评价。很多研究者和营养协会开发了各种各样的营养不良评估工具,包括营养筛查目的,以及综合评价营养状态。营养评估工具的内容应比营养风险筛查更深入、更复杂,包括疾病史、饮食摄入情况、人体学测量、生化检查、体格检查等。恶液质本身没有专门的评估工具提供临床使用,大多数专家认为可以采用目前临床使用的营养不良评估工具用于恶液质的评价。但最近有学者提出了恶液质评分系统(CASCO),通过对体重和瘦体组织的下降、厌食、炎症、免疫和代谢紊乱、体力状况及生活质量等5个方面的问题评分,根据分数的结果对恶液质分期。下面就临床最为常用的几种评估工具分别描述。
患者主观整体评估
患者主观整体评估(patient-generated subjective global assessment,PG-SGA)PG-SGA是1994年Ottery在多伦多小组设计的主观全面评价的基础上,专门为肿瘤患者制订的营养筛查工具。美国膳食协会认定PG-SGA可作为肿瘤患者营养评价的标准,澳大利亚营养师协会也推荐将PG-SGA用于肿瘤放疗后患者的营养评价。此表优点是使用简便,在门诊或病房内数分钟即可完成,由患者作答四项问题:体重变化、饮食情况、体能活动能力以及有无影响患者进食的一些不良症状,如疼痛、便秘、腹泻、恶心、呕吐、焦急和紧张等。由医师判定两项,包括有无高分解和高代谢状态,体检有无肌肉和脂肪大量消耗状态。
目前PG-SGA已广泛用于头颈部肿瘤、肺癌、妇科肿瘤、胃肠道及晚期恶性肿瘤患者的营养筛查与评估。Bauer等将PG-SGA应用于住院肿瘤患者,以SGA为近似金标准,测得较高的敏感性(98%)和特异性(82%);PG-SGA与SGA一致程度高,PGSGA对预测肿瘤患者的住院时间有积极意义。Hill等发现,PG-SGA筛检出的营养不良程度越严重的胃肠肿瘤患者,放疗后不良反应越重,营养良好者的耐受力明显优于营养不良者。Isenring等将PGSGA用于头颈部、腹部放疗后的门诊肿瘤患者,发现PG-SGA评分与6个月内体重减轻、生活质量低下呈线性关系,营养状况评分可客观反映患者生活质量的变化。PG-SGA适合筛查不同年龄阶段的成年肿瘤患者,操作前需要进行专门训练。
PG-SGA评估过程需要经过专业和统一的培训才能规范有效的在临床应用,有许多细节的评价决定最后的评分,而评分的结果是指导营养治疗介入的依据,也是营养治疗效果评价标准。因此,在应用此量表进行临床研究和应用前需要统一标准的培训,建议参考《PG-SGA肿瘤患者营养状况评估操作手册》(见本书网络增值服务)。该手册囊括了评估表填写注意事项和要点,对于容易出现差异结果的体格检查项目(脂肪、肌肉丢失情况评价)通过图示给予了展示,具有准确的统一评估标准的作用。
主观整体评估
主观整体评估(subjective global assessmennt,SGA)SGA是1984年由Detsky等基于外科住院患者建立的营养评估表,被美国肠外肠内营养学会、ESPEN推荐使用。SGA包括两个方面,共8项内容,病史方面包括体重改变、饮食状况、胃肠道症状、活动能力、应激反应,体格检查方面包括皮下脂肪厚度和肌肉的测量、水肿情况的检查。分为营养状况好(SGA-A)、轻-中度营养不良(SGA-B)和重度营养不良(SGA-C)。SGA具有无创性、易操作性,在住院患者中敏感性(82%)和特异性(72%)均较高。SGA已广泛用于外科手术、慢性疾病、危重患者等,也应用于妇科肿瘤、乳腺癌、肺癌、消化系统肿瘤患者的营养风险筛查和评估,且适用性均较好。Montoya等用SGA评估肿瘤患者化疗后的营养状况,结果表明,患者的营养不良程度与肿瘤分期、卡氏评分密切相关。
已经有研究证实了SGA的可信性和有效性。通过SGA评估发现的营养不足患者并发症的发生率是营养良好者的3~4倍。针对不同住院患者前瞻性研究显示SGA能够很好预测并发症,包括透析、肝移植和HIV感染的患者。
SGA作为营养风险筛查工具也具有一定的局限性。有学者指出SGA反映的主要是疾病状况,而非营养状况。SGA侧重于筛查出慢性的或已经存在的营养不足,而不能很好地体现急性的营养状况的变化。同时由于此筛查方法没有将观察项目与患者分类直接联系起来,使该工具使用不够简便,无法用于快速的临床筛查。另外,Reilly指出,SGA对使用者要求较高,更适合接受过专门训练的专业人员使用,不适合作为综合大医院常规的营养风险筛查工具。SGA作为主观的评估工具,需要评估者在使用前接受专业的培训才能够保证评估的敏感性和特异性。
营养风险筛查2002
营养风险筛查2002(nutritional risk screening,NRS2002)NRS2002由丹麦肠外肠内营养协会于2003年发表,为ESPEN 推荐,适用于住院患者营养风险筛查。主要包括三个方面的内容:①营养状况受损评分(0~3分);②疾病的严重程度评分(0~3分);③年龄评分,在以上评分基础上年龄≥70岁者加1分。总分为0~7分。根据对128个关于营养治疗与临床结局的随机对照试验(randomized controlled trial,RCT)的分析发现,在NRS评分≥3分的情况下,大部分研究显示营养治疗有效(能够改善临床结局),而在NRS评分<3分的情况下,大部分研究显示营养治疗无效。因此,将是否具有营养风险的评分切割点定为3分,即NRS评分≥3分为具有营养风险,需要根据患者的临床情况,制订基于个体化的营养计划,给予营养干预;而NRS<3分者虽然没有营养风险,但应在其住院期间每周筛查1次。NRS2002是基于128项随机临床研究,循证医学证据充分,通过综合分析患者的营养状况、疾病严重程度以及年龄因素的干扰,减少了评价时因主观因素引发的误差,较为客观地反映被测者的营养风险,同时简便易行、易于推广。
NRS2002突出的优点在于能预测营养不良的风险,并能前瞻性地动态判断患者营养状态变化,便于及时反馈患者的营养状况,并为调整营养支持方案提供证据。这是其他方法所缺乏的。有研究显示,应用NRS2002能发现存在营养风险的患者,给予营养支持后,临床预后优于无营养风险的患者,改善临床结局,如缩短患者住院时间等。而且NRS2002简便、易行,能进行医患沟通,通过问诊的简便测量,即可在3分钟内迅速完成。因无创、无医疗耗费,故患者易于接受。目前作为综合医院营养筛查工具使用,对于肿瘤患者的营养评估不如PG-SGA针对性更强。
微营养评价法
微营养评价法 (mini nutrition assessment,MNA)。MNA是一种简单、快速,适用于评价患者(特别是老年人,目前也有多项相关肿瘤患者的临床研究)营养状况的方法。应用该方法10分钟内即可完成营养状况的评定,已获得国外诸多学者的认可和推广。最初由Guigoz等在20世纪90年代提出,主要用于老年患者,近年来也有许多学者用于肿瘤患者的研究报告。内容包括人体测量、整体评价、膳食问卷及主观评价等4部分18项组成。各项评分相加即得 MNA总分。
MNA的不足之处:①在量表组成上存在一些有待改进的问题:有些患者不能给出明确答案,由此造成假阳性;询问有关每日是否进食蛋白质及水果、蔬菜,只为定性,没有定量。②未进行适用对象的研究,MNA是否均能应用于各年龄组、是否适用于各种疾病及病情程度不同的患者还没有相应的研究来确定。③护理质量的优劣与患者(尤其是卧床、饮食依赖的患者)的营养状况息息相关,但MNA中未涉及该方面。④未考虑性别差异,男、女性上臂肌围、腓肠肌围标准不同,不能用同一张调查表。因此在以后的使用中,仍应不断地改进和完善。
营养不良通用筛查工具
营养不良通用筛查工具(malnutrition universal screening tool,MUST)。MUST是2003年英国肠外肠内营养协会开发的营养风险筛查工具,该工具主要用于蛋白质-能量营养不良及其风险的筛查,包括三方面评估内容:①BMI;②体重减轻者;③疾病导致进食量减少的患者。通过三部分评分得出总分,将营养不良程度分为3个等级:0分为低风险、1分为中等风险、≥2分为高风险。营养不良高风险者需给予相应的营养支持。操作MUST时一般只需3~5分钟,它适用于筛查所有住院患者的营养状况。MUST是基于社区人群发展起来的,在社区及住院老年患者中的应用较常见,近年来也逐渐用于肿瘤患者的营养风险筛查。Amaral等筛检130例肿瘤患者的营养不良,与临床上应用较多的NRS2002比较,测得MUST的敏感性为97.3%,特异性为77.4%,内部一致性83.1%,还发现MUST在肿瘤患者的住院天数上有较高的预测效度。Stratton等研究显示,MUST可预测老年住院患者的病死率和住院时间,即使是无法测量体重的卧床老年患者,MUST 也可进行筛查,并预测临床结局。将MUST与其他7个目前被使用的营养风险筛查工具进行比较的研究显示,MUST与SGA和NRS2002有较高的一致性。
恶液质评分系统
恶液质评分系统(cachexia score,CASCO)。由于肿瘤恶液质患者往往在体重减少的同时存在肌肉和脂肪组织的丢失,因此,对于评价与瘦体组织相关的体重变化也是很重要的。从这个角度来看,肿瘤恶液质患者瘦体组织的下降意味着体力状况和生活质量的下降,因此,体重的变化可能意味着患者的存活时间变化。事实上,一些作者认为脂肪变化与患者的生存有关,而骨骼肌质量的减少与生活质量的下降有关。在CASCO评价系统中,瘦体组织体重下降在该评分系统中的比例高达40% (表7-2-4)。
表7-2-4 CASCO:一种新的肿瘤恶液质分期方法
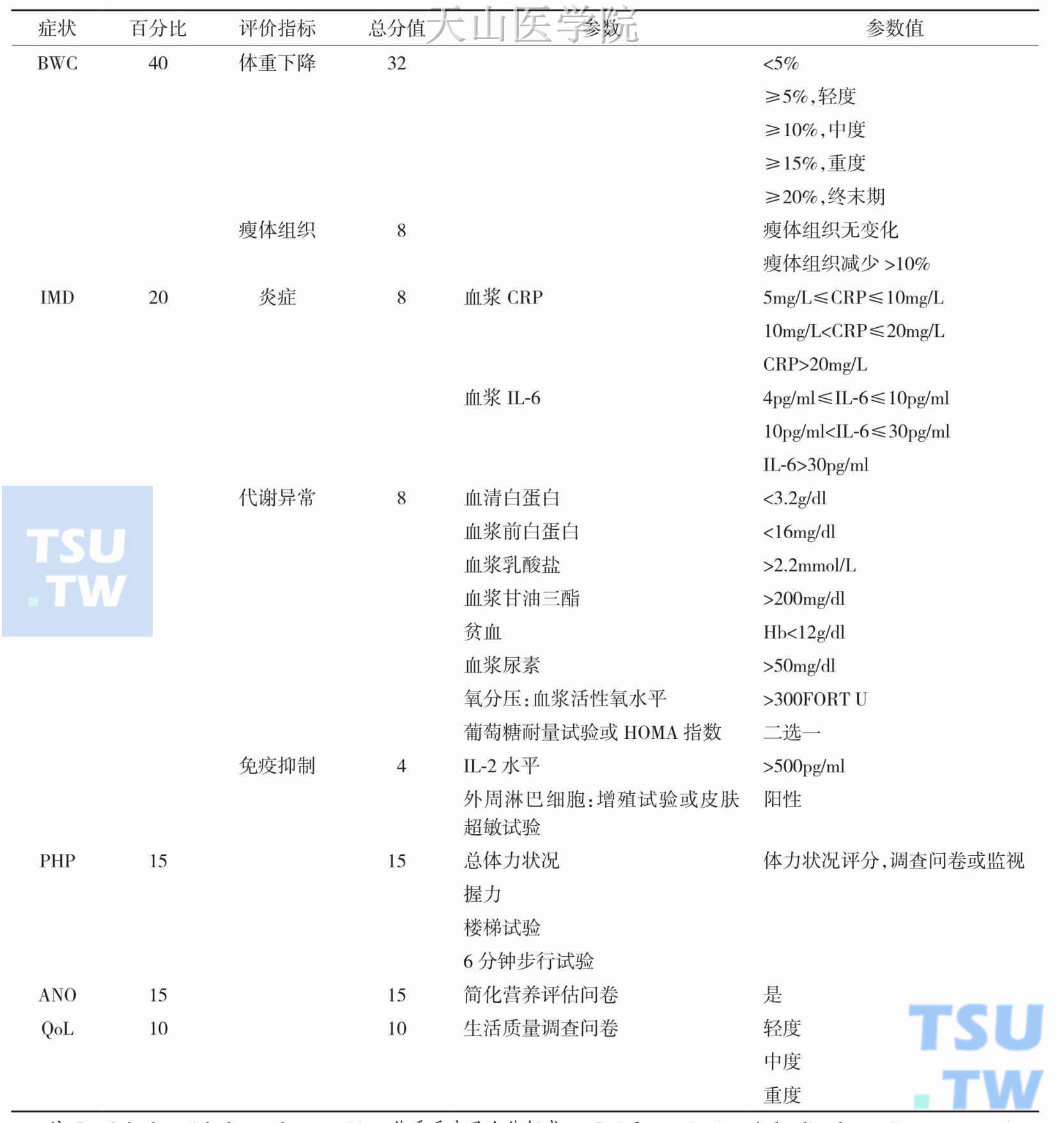
注:BWC,body weight loss and composition,体重丢失及人体组成;IMD,inflammation/metabolic disturbances/immunosupression,炎症/代谢紊乱/免疫抑制;PHP,physical performance,体能;ANO anorexia,厌食;QoL,quality of life,生活质量。
CASCO总分=BWC(0~40)+IMD(0~20)+PHP(0~15)+ANO(0~15)+QoL(0~10)
- 0<CASCO总分≤25,轻度恶液质
- 25<CASCO总分≤50,中度恶液质
- 50<CASCO总分≤75,重度恶液质
- 75<CASCO总分≤100,终末期恶液质
这是一种肿瘤恶液质的定量试探性(尚未证实)分期评分方法。它是辨别恶液质前期患者的工具,也是根据体重下降和体重构成、炎症/代谢紊乱/免疫抑制、体力状况、厌食及生活质量对恶液质综合征进行分类并分期的工具。一经证实,新的CASCO评价系统与其他分期方法相似,将成为肿瘤恶液质患者治疗和营养建议的有用工具。未来努力的方向将集中于在多中心临床中验证该评分标准。
肿瘤恶液质是肿瘤终末期的特殊状态,以目前的营养筛查和评估工具而言尚没有适合的方法来特异性的表达患者的具体状态来指导临床的治疗。无论何种评价方法,其主旨是为了临床制订合理化、个体化治疗提供一个依据性的平台。而我们上述这些评估工具的最初目的不是为恶液质评估所设计,因此,在临床上使用难免出现不合理之处,这也是我们今后需要努力的目标。作为探讨性的工作,所列出的评估方法是以营养不良为评估主体,而恶液质是营养不良的一种极端状态,部分内容应也对临床有参考价值。
