虽然许多来自于唾液腺导管的肿瘤可出现乳头状结构,但局限在导管内的唾液腺导管原发性乳头状肿瘤即导管乳头状瘤(ductal papilloma)很少见。WHO分类中将导管乳头状瘤分为三种类型:内翻性导管乳头状瘤(inverter ductal papilloma)、导管内乳头状瘤(intraductal papilloma)及乳头状唾液腺瘤(sialadenoma papilliferum)。它们共同的特点是多见于小唾液腺、有乳头状结构、其解剖部位与排泄管关系密切,而且是单灶性病变,它们彼此之间的组织学结构又有所不同。由于导管乳头状瘤报道较少,其发病情况难以确定。可能有很多已发表的研究并没有认识这些良性的乳头状肿瘤,或者将它们用一般性词语描述,如其他腺瘤或单形性腺瘤。Regezi等1985年报道的238例小唾液腺肿瘤中有4例内翻性乳头状瘤,未见导管内乳头状瘤。Waldron等的425例中则未有乳头状瘤。美国陆军病理研究所复习3100例唾液腺肿瘤,其中只有4例导管内乳头状瘤。另一项380例小唾液腺肿瘤的研究中,有17例导管乳头状瘤,其中导管内乳头状瘤3例(0. 8%)。国内的侯之艳等报道的1878例唾液腺肿瘤中无乳头状瘤。四川大学华西口腔医院的3461例唾液腺上皮性肿瘤中只有1例导管乳头状瘤。上海的6982例唾液腺肿瘤中有10例导管乳头状瘤。
内翻性导管乳头状瘤
内翻性导管乳头状瘤(inverted ductal papilloma)。唾液腺排泄管的基底样、表皮样细胞和柱状细胞向管腔内乳头状增生形成的肿瘤,位于和口腔黏膜表面交界处。1981年Batsakis等对大唾液腺单形性腺瘤的研究中,描述了3例表皮样乳头状腺瘤。这可能是最初的对内翻性乳头状瘤的描述,尽管他们称这些肿瘤为表皮样乳头状腺瘤。内翻性乳头状瘤的名称是White等在1982年首先应用。该瘤的组织发生不详,可能来自于排泄管储备细胞、排泄管细胞,也有人对储备细胞理论持怀疑态度。
临床特点
内翻性乳头状瘤在3种导管乳头状瘤中最少见,目前有35例报道。该瘤发生在成人小唾液腺,平均年龄50岁(28~77岁)。男性稍多见或性别分布无差别。唇、特别是下唇多见、其次见于颊、腭、前庭沟、口底。临床上内翻性乳头状瘤为无症状、实性黏膜下结节,个别的表现为乳头状、皱褶样、息肉样。病程数月至29年。直径通常小于1. 5cm。与乳头状唾液腺瘤一样,通常位于唾液腺导管的开口附近,黏膜表面常常有小的凹陷或扩张的小孔。文献报道一例内翻性乳头状瘤与义齿引起的纤维性增生有关。
病理特点
肉眼见界清、实性或囊性肿物,位于黏膜上皮下方。囊性时与表面相通。肿瘤直径0. 5~1. 5cm,平均0. 9cm。
组织学:位于黏膜浅固有层的界清的肿物,与表面上皮相联通,位于排泄管与口腔黏膜的交界处,与周围的固有层分界明显。如果切面较正,可见肿瘤腔通过一个狭窄的孔与表面上皮相通,此联通处的口腔黏膜往往位于肿瘤表面的中心处,有一个凹陷或弹坑样下陷,在此处口腔上皮反转并且与肿瘤上皮延续。也可见直接位于黏膜上皮以下。内翻性乳头状瘤表现为排泄管内的腺管上皮和鳞状上皮呈球根样、乳头状向管腔内增生,并且向黏膜固有层膨胀,与间质有较宽的界面。肿瘤上皮由多层基底样或鳞状细胞(类似于正常上皮的基底层和其邻近的棘层细胞)组成,通常无角化。这些上皮自腔面围绕纤维血管性中轴,形成球根样乳头结构,充斥于腔内。柱状导管细胞一般被覆在增生的鳞状上皮的腔面侧。黏液细胞可以散在于导管细胞和邻近的鳞状细胞之间(图7-83)。乳头间常常可见裂隙样间隙。肿瘤细胞大小一致,即使有细胞的非典型性也很轻微。核分裂通常不明显。
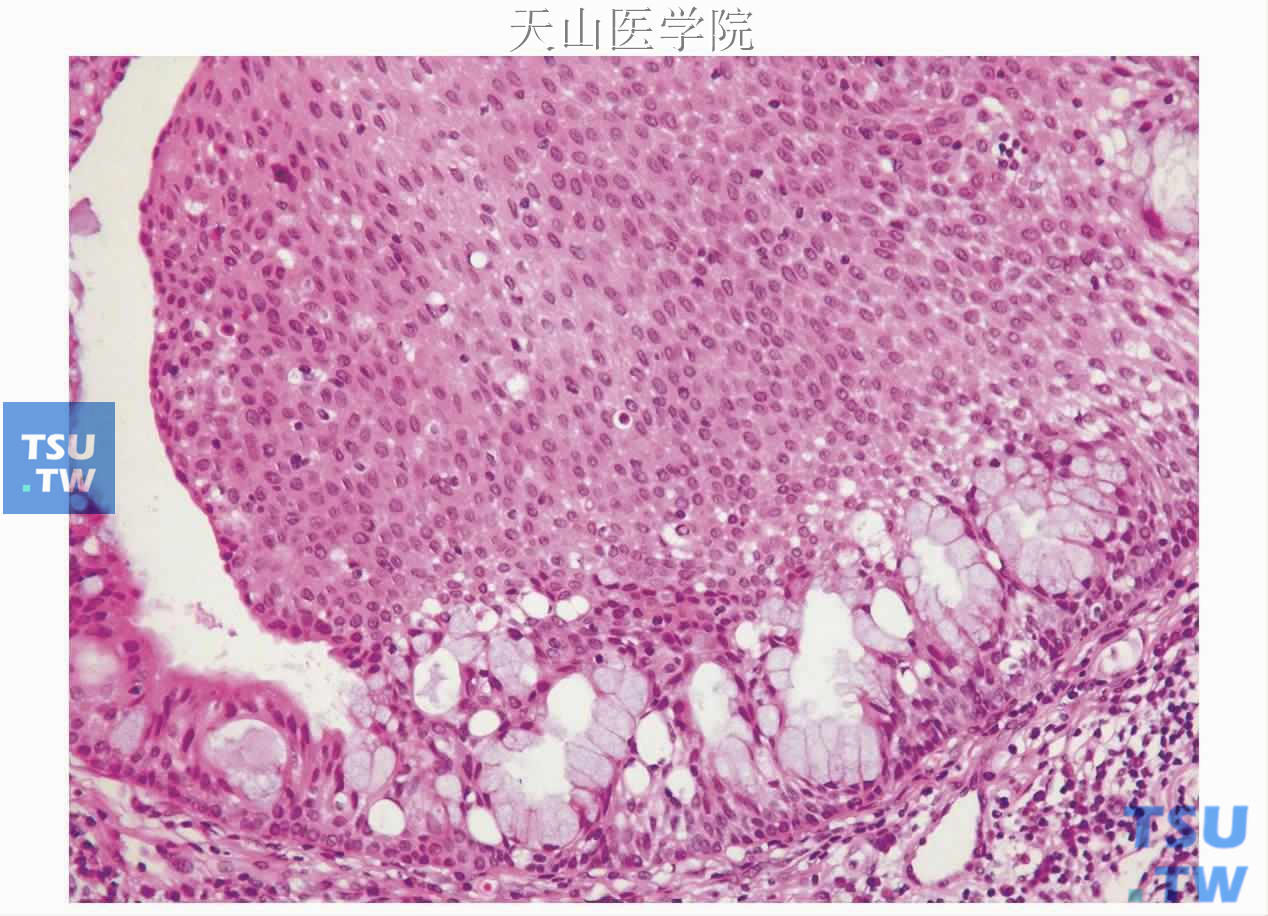
图7-83 内翻性导管乳头状瘤:鳞状上皮呈乳头状增生突入管腔内,局部见黏液细胞
免疫组化
内翻性乳头状瘤的免疫组化特点类似于排泄管上皮。肿瘤细胞表达CK (AE1/AE3),CK8在面向腔面的细胞阳性,高分子量CK34 βE12在基底处的鳞状细胞阳性、EMA阳性,Ki67见少许基底细胞阳性。平滑肌标志物阴性。关于该瘤是否伴人乳头状瘤病毒感染的研究有不同的结果。有的原位杂交和PCR未发现伴乳头状瘤病毒感染的证据,有的研究报道部分病例的肿瘤细胞含人乳头状瘤病毒DNA。最近有报道1例女性HIV阳性患者,患唇内翻性乳头状瘤合并尖锐湿疣,HPV11 DNA PCR检测阳性。
鉴别诊断
黏液表皮样癌有鳞状上皮和黏液细胞分化,但为多囊性、多结节、浸润性生长,乳头状生长少见。鼻腔鼻窦道的内翻性乳头状瘤虽然与唾液腺内翻性乳头状瘤有相似之处,但它们通常是多结节的,累及黏膜较广泛的区域,而且其上皮常常有纤毛。乳头状唾液腺瘤有外生性和内生性部分,内生性部分为腺管结构而不是内翻性乳头状瘤的鳞状上皮和基底样上皮。
治疗和预后
切除可治愈,不复发。虽然该瘤与鼻腔鼻窦内翻性乳头状瘤有相似之处,但不像鼻的肿瘤那样,无恶变危险。
导管内乳头状瘤
导管内乳头状瘤(intraductal papilloma)导管内乳头状瘤是排泄管内衬上皮向腔内的乳头状增生形成的肿瘤,肿瘤导致管腔单囊性扩张。可能是Castigliano和Gold于1954年首先在英文文献中报道。关于此瘤的组织发生多数同意来自导管上皮,最可能为排泄管。关于其性质有争论,多数认为是肿瘤性,有人认为是单形性腺瘤或Warthin瘤的亚型,也有人认为其为增生性病变。
临床特点
少见报道,目前大约有50例。该瘤的性别分布均等,几乎所有患者均大于30岁,常见于40~60岁,平均54岁(8~77岁)。Tomonao等总结的47例中,发生在大唾液腺14例(腮腺9例、下颌下腺3例、舌下腺2例,常发生在主导管)、其余的发生在小唾液腺,其中唇14例,颊8例,腭6例,舌、舌下区、口腔前庭各1例,1例部位不详,另外还有1例鼻腔的报道。在美国陆军病理研究所的45例唾液腺导管乳头状瘤中,导管内乳头状瘤占50%多一点。
导管内乳头状瘤的发生位于排泄管距离口腔上皮较远的水平。临床表现为小而无症状的黏膜下肿块,无症状,病程数月至数年,最大直径可达2cm。
病理特点
界限清楚或有包膜的单囊性肿物,腔内有乳头状突起,完全或部分充填于扩张的排泄管或小叶间导管。单囊性的囊腔含有碎的颗粒样组织和黏液。
组织病理
乳头状瘤起源于扩张的唾液腺导管的表面,偶尔可见排泄管与该囊腔相通。导管内乳头状瘤为单囊性,通常有许多分支的乳头突起,自囊壁延伸至囊腔内。乳头状突起一般有细的纤维血管轴,乳头表面衬覆1~2层大小一致、温和的立方或柱状细胞,细胞核位于细胞的基底部(图7-84、7-85)。偶尔有黏液性上皮和灶性皮脂腺化生。增生的乳头并不扩展出唾液腺导管外。肿瘤细胞通常无非典型性和核分裂。病变的外侧有厚的纤维组织围绕。纤维性囊壁常常见炎症细胞浸润。如果有明显的细胞的非典型性或明显的分裂活性,应该考虑乳头状囊腺癌的可能。如果病变累及一个以上的导管,最好归为囊腺瘤。
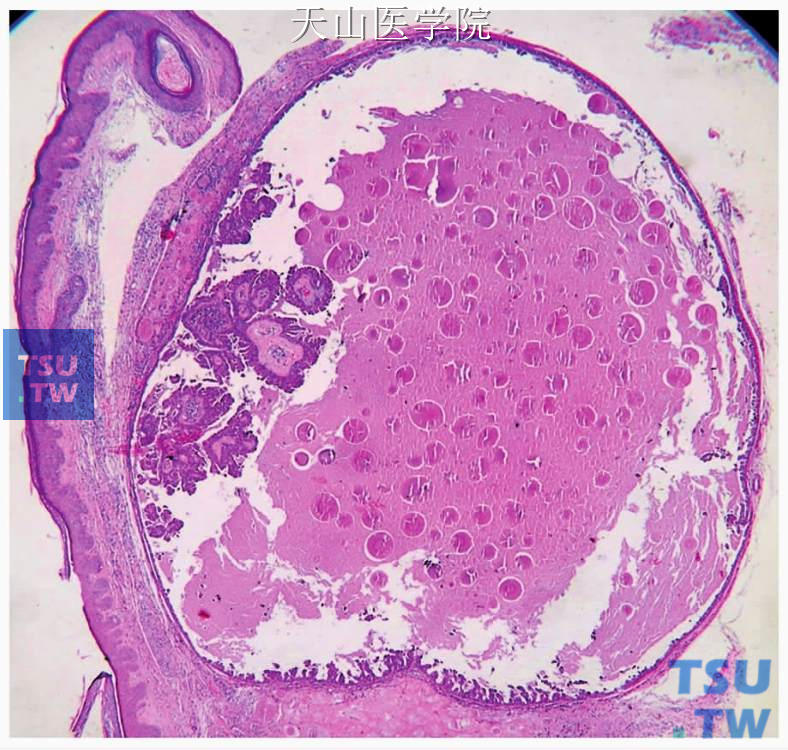
图7-84 导管内乳头状瘤:导管扩张呈囊性,内含乳头结构
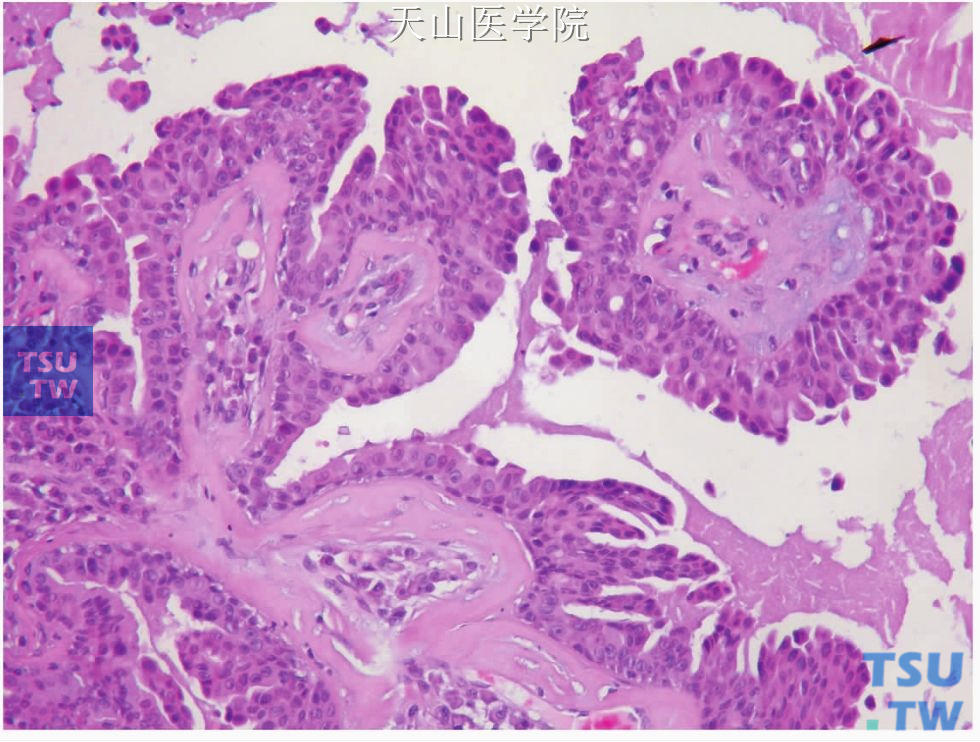
图7-85 导管内乳头状瘤:乳头含结缔组织轴,表面衬覆2层以上的立方状细胞
免疫组化
肿瘤细胞的免疫组化特点类似于导管的腔面细胞。肿瘤细胞表达CK(AE1/3、CAM5. 2)、EMA、S-100蛋白,淀粉酶、乳铁蛋白阳性,肌上皮抗原SMA、p63、和CK14阴性。有研究显示Ki67指数为1. 1%。
超微结构
对少数病例的电镜研究见导管内乳头状瘤由单层、双层或多层柱状至立方细胞构成。肿瘤细胞的腔面部分胞质内含很多分泌颗粒。腔面细胞常常有纤细的微绒毛或顶浆分泌的特点。细胞内含粗面内质网、高尔基体和线粒体也提示其分泌功能。肿瘤细胞内还见环状板(annulate lamellae),可能与细胞增生有关。有人认为该瘤有腺泡细胞分化倾向。
鉴别诊断
包括乳头状囊腺瘤、导管阻塞导致的乳头状变化、内翻性乳头状瘤、低级别乳头状囊性型腺泡细胞癌和黏液表皮样癌。
关于导管内乳头状瘤与乳头状囊腺瘤是各自独立的疾病、还是导管内乳头状瘤是囊腺瘤的亚型尚存争论。乳头状囊腺瘤在定义上是多囊性的,而导管内乳头状瘤始终是单囊性的。乳头状囊腺瘤不累及腺体本身的导管,而导管内乳头状瘤发生在囊性扩张的导管内,并不在导管以外的部位形成囊性结构。乳头状囊腺瘤常常含非乳头性的微囊和筛状区,导管内乳头状瘤无此特点。
低级别筛状囊腺癌可能与导管内乳头状瘤难以鉴别。但该瘤形成多灶性导管内病变,含微乳头、丛状或斑块样的突起,不含明确的纤维血管轴。而导管内乳头状瘤为真性纤维血管轴乳头、单个扩张的导管。S100弥漫阳性有助于确定低级别筛状囊腺癌。
多形性低度恶性腺癌可有乳头状结构,但混杂有管状、筛状、梁状和靶心样的浸润性生长。
甲状腺转移性乳头状癌甲状腺球蛋白阳性。
在导管阻塞附近的一段导管常常伴有导管扩张和上皮增生。但是这种上皮增生的程度不广泛,不如导管内乳头状瘤中的那样复杂。
内翻性乳头状瘤常常含有鳞状上皮成分,不见于导管内乳头状瘤。内翻性乳头状瘤开口于表面上皮,而导管内乳头状瘤在黏膜的深面,与黏膜表面无直接交通。
腺泡细胞癌很少形成明显的乳头状囊性结构,主要是类似于闰管的细胞增生,至少有些细胞类似于腺泡细胞样(含抗淀粉酶消化的PAS阳性颗粒)。乳头状囊性型腺泡细胞癌通常有更纤细的纤维血管轴并且混杂有微囊或滤泡样结构,这些表现不见于导管内乳头状瘤。
黏液表皮样癌罕见情况下可表现为单囊性肿瘤,但有鳞状细胞、透明细胞和含黏液细胞可以帮助鉴别。
治疗和预后:单纯切除,切除彻底一般不复发。发生在小唾液腺者未见恶变的报道。但有2例发生在大唾液腺的恶变病例报道。
乳头状唾液腺瘤
乳头状唾液腺瘤(sialadenoma papilliferum)由黏膜表面的复层鳞状上皮外生性乳头状增生、深部唾液腺导管内生性腺瘤样增生而构成的肿瘤。Abrams和Finck根据该肿瘤与皮肤附属器来源的乳头状汗腺瘤(syringocystadenoma papilliferum)在组织学上的相似性,在1969年将其命名为乳头状唾液腺瘤,至今在唾液腺约有60例报道。关于此瘤的组织来源和性质有争议,多数人同意该瘤是来自于排泄管上皮细胞(储备细胞)的肿瘤,也有人根据电镜的表现提出可能来自于闰管细胞,或者是一种非肿瘤性增生性病变。还有人认为该瘤来自于多潜能肌上皮细胞。
临床特点
该瘤少见,文献报道占唾液腺良性肿瘤的0. 6%~2%。美国陆军病理研究所的1000例小唾液腺肿瘤中只有2例,其他2个大样本中分别为0. 8%和1. 2%。Kubota等总结的48例中,患者年龄18~87岁,平均56. 8岁。男女之比为1. 6∶1。虽然乳头状唾液腺瘤有发生在腮腺的报道,但最常见的还是在小唾液腺,特别是腭部,约占70%,其中2/3在硬腭,其他部位有颊、唇、磨牙后区、舌、口底等。目前发生在大唾液腺者只有4例报道,3例发生在腮腺、1例舌下腺。发生在小唾液腺的肿瘤直径0. 3~2cm,(美国陆军病理研究所有一例腮腺的7. 5cm)。病程1~12年。其他部位如鼻腔、鼻咽部、食管和支气管也有类似肿瘤的报道。
该瘤发生在唾液腺排泄管开口邻近,界限清楚、生长缓慢,表现为黏膜表面的无痛性、外生性、乳头状肿块。临床上常常误诊为鳞状上皮乳头状瘤。
病理特点
大体:界限清楚,外生性或疣状病变,0. 3~2cm,平均0. 7cm。
低倍镜下,肿瘤往往位于唾液腺导管在口腔黏膜的开口附近,有外生性和内生性成分。外生性部分为典型的乳头状瘤表现,基底宽,呈指状突起,内含纤细的纤维结缔组织轴。乳头状伸展至高出邻近黏膜表面,可高达1cm。乳头表面覆盖的复层鳞状上皮,可有过度角化或不全角化,颗粒层明显,分化好。此部分病变常常见淋巴细胞、浆细胞和中性粒细胞浸润。外生性部分的深部为内生性部分,无包膜,由腺管或分支状、偶尔迂曲的导管构成。这些导管可呈囊性,与外生性部分的乳头间的裂隙相联通。有些导管可扩张并在导管内形成乳头状突起。衬覆导管的上皮通常为双层细胞,腔面细胞呈高柱状,基底部的细胞为立方或扁平状。由于导管结构常有皱褶和乳头,导管的腔面的外形常常不规则,呈分支的裂隙样。导管的腔面细胞和基底细胞均呈弱嗜酸性,与小叶间或排泄管的上皮相似(图7-86、7-87)。偶尔可见黏液细胞混杂在导管细胞间和表面的乳头状上皮细胞间,间质常见炎症细胞浸润。
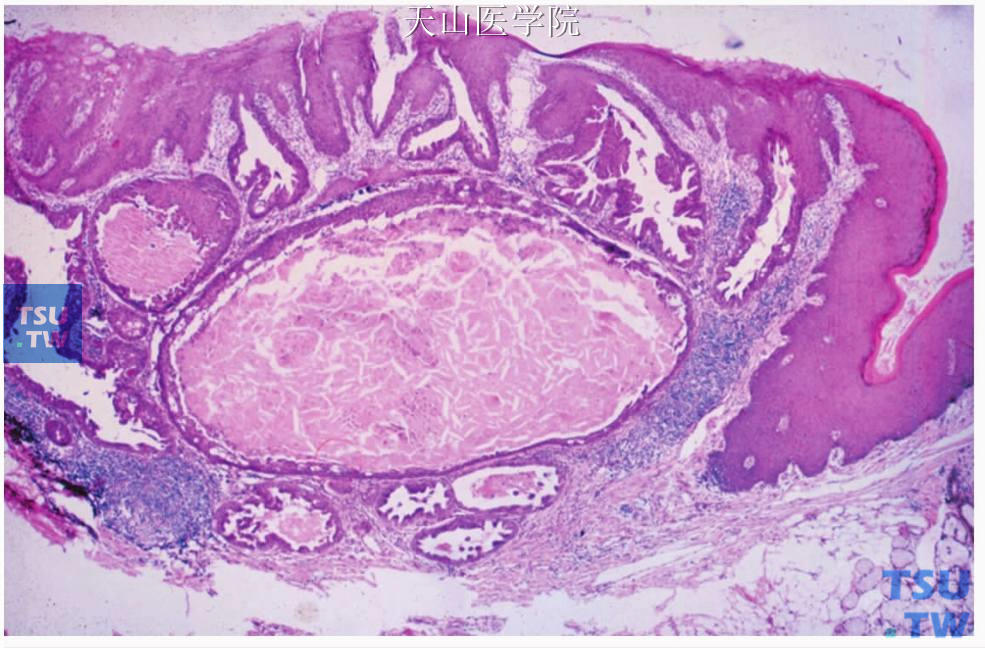
图7-86 乳头状唾液腺瘤
黏膜表面形成突起性肿物,鳞状上皮轻度增生,深部见裂隙样导管结构,导管局部扩张
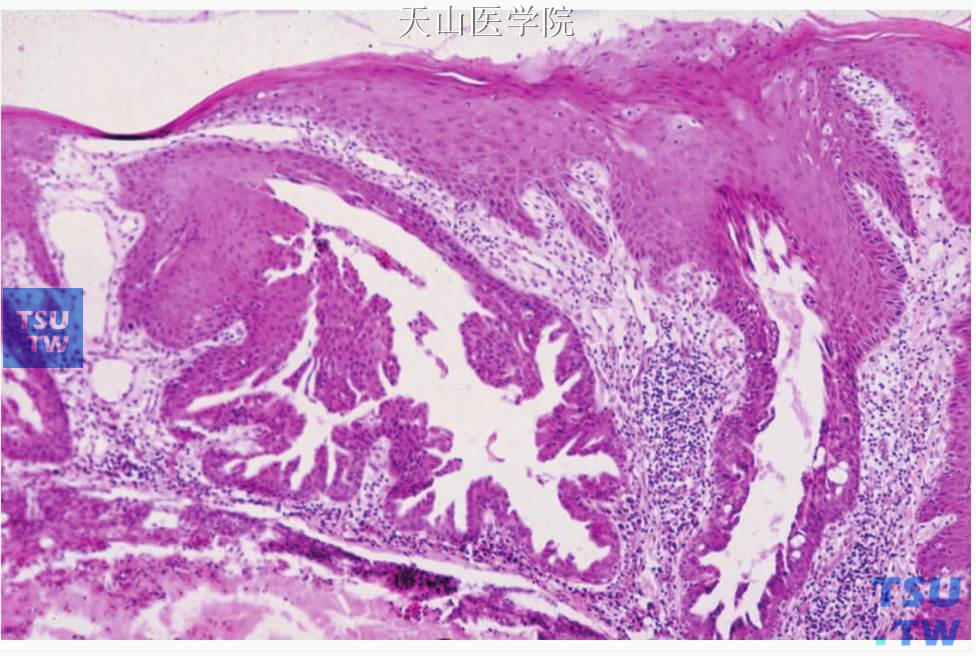
图7-87 乳头状唾液腺瘤:导管中含有乳头,呈裂隙样
免疫组化
外生性鳞状部分表达CK7、AE1/3、CEA和EMA。导管的腔面细胞表达CK7、CAM5. 2、AE1/3、CK8、CK18、CK19、CEA、EMA和S-100蛋白。非腔面基底细胞为波形蛋白、CK14和SMA阳性,也表达CK7、S100、GFAP和CK13,说明乳头状唾液腺瘤有导管上皮和肌上皮分化。分子生物学检查无乳头状瘤病毒感染的证据。
鉴别诊断
包括鳞状细胞乳头状瘤、尖锐湿疣、疣状癌、乳头状囊腺瘤和黏液表皮样癌。前3者无乳头状唾液腺瘤的深部腺体或导管成分,而后2个肿瘤无乳头状唾液腺瘤的表面部分。
治疗和预后
治疗应为完整切除,因为本肿瘤有较高的复发倾向(10%~15%)。虽然有复发的报道,一般认为此瘤为良性。与其他2种不复发的乳头状瘤不同,文献上有4例该肿瘤发生恶变的报道,如恶变为上皮肌上皮癌和高级别微乳头状侵袭性癌、外生性的部分出现异常增生和原位癌等。虽然对上述恶变的病例还有不同看法,但必要的随诊还是应该的。文献上有3例恶性乳头状唾液腺瘤的报道。
