黏液表皮样癌(mucoepidermoid carcinoma,MEC)是由不同比例的黏液细胞、中间细胞、表皮样细胞构成的恶性肿瘤。有时含有柱状细胞、透明细胞偶尔还有嗜酸细胞,常呈囊性生长。黏液表皮样癌又称黏液表皮样瘤(mucoepidermoid tumor),由Stewart在1945年首先提出,1953年Foots等研究认为此瘤有恶性性质。目前已趋于统一称为黏液表皮样癌。
黏液表皮样癌相关的最常见的病因是辐射,电离辐射可潜在增加患黏液表皮样癌的危险。由于潜伏期长,需要长期随访。Land等复习广岛和长崎原子弹爆炸幸存者大小唾液腺肿瘤145例,其中11例黏液表皮样癌患者接受的辐射剂量与患黏液表皮样癌的相对危险性相关,平均危险性在9. 3,黏液表皮样癌发生与辐射计量呈正相关。最近的研究报道了12例接受化疗和放疗的儿童癌症患者发生了唾液腺肿瘤,其中10例为黏液表皮样癌。
一般认为黏液表皮样癌来源于排泄管的储备细胞或闰管-腺泡的储备细胞。腭部或口腔他处黏膜发生者,除来自小唾液腺外,也可能来源于口腔黏膜上皮。发生于颌骨中央者,可来自陷入下颌骨中的磨牙后腺组织、下颌骨内异位腺体及颌骨内含牙囊肿上皮衬里中的黏液细胞。
临床表现
此瘤为最常见的唾液腺恶性上皮性肿瘤之一,我国6所医学院校统计的23 010例唾液腺上皮性肿瘤中有2214例,占9. 6%。占8478例唾液腺癌的26. 1%,在唾液腺癌中是第二位最常见的,仅次于腺样囊性癌。上海的一项研究中,黏液表皮样癌占6982例唾液腺上皮性肿瘤的9. 64%,占2239例唾液腺癌的30. 06%,其数量也是位于腺样囊性癌之后的第二位最常见的唾液腺癌。以上的2个大样本统计中,黏液表皮样癌的发病情况在大小唾液腺均列在腺样囊性癌之后,与早期的研究结果稍有不同。俞光岩报告的405例唾液腺癌中,黏液表皮样癌有120例,占29. 6%,其发病率在唾液腺癌中占首位。在小唾液腺的恶性肿瘤中,也以此瘤最常见,孙开华等统计的327例中有98例,占小唾液腺恶性肿瘤的30%。在多数西方国家,黏液表皮样癌是大、小唾液腺最常见的恶性肿瘤,占所有唾液腺恶性肿瘤的30%左右,但有一些人口统计学的差异。
国内数据显示黏液表皮样癌在大唾液腺约占1/3,发生在小唾液腺者约占2/3。发生在大唾液腺者约80%以上发生于腮腺,下颌下腺及舌下腺少见。小唾液腺中以腭部多见,约占50%,其次为颊、舌、颌骨、磨牙后、唇、鼻窦等。发生于磨牙后腺的肿瘤绝大多数为此瘤,颌骨中枢性唾液腺肿瘤的大部分均为黏液表皮样癌,还可以发生在腮腺的淋巴结内、副腮腺和其他易位腺体如颈部易位的黏液腺。有报道该瘤发生于腮腺主导管。身体其他部位可发生黏液表皮样癌的有:泪腺、鼻腔、鼻窦、鼻咽部、喉、气管、肺、胸腺、乳腺、肝、皮肤和子宫颈等部位。有时黏液表皮样癌作为多原发肿瘤之一,如唾液腺泪腺同时发生黏液表皮样癌、黏液表皮样癌与其他肿瘤如腺样囊性癌、多形性腺瘤、Warthin瘤等同时发生。个别情况下见良性肿瘤如Warthin瘤、乳头状唾液腺瘤恶变为黏液表皮样癌。
黏液表皮样癌在女性比男性多见,男女之比约为2∶3。而美国的一项1554例黏液表皮样癌的统计中男性为775例、女性为779例,大致相等。黏液表皮样癌患者年龄分布广泛,任何年龄均可发生,最小者1岁,国内有1例先天性腮腺黏液表皮样癌报道。中年或中年以上为发病高峰,也有人报道20~70岁之间大致发病相等。黏液表皮样癌也是儿童最常见的唾液腺恶性肿瘤,但10岁以下儿童少见。
黏液表皮样癌的临床表现与肿瘤的分化程度密切相关。高分化者(低级别)与多形性腺瘤表现相似,为无痛性肿块,生长缓慢,病程从数月至数十年,平均1. 5年。肿物较小,直径多为2~4cm,肿瘤形态不规则,活动度较差。肿物较硬,部分区域有囊性感,很少出现面瘫。发生在小唾液腺者肿瘤表现为蓝色至紫红色、实性至波动、表面光滑或呈乳头状,有时有液体溢出。症状有吞咽困难、疼痛、感觉异常等,最常见于小唾液腺黏液表皮样癌。发生于磨牙后腺者,常为囊性且黏膜呈浅蓝色,易误诊为囊肿;低分化者(高级别)为恶性肿瘤的表现,肿瘤生长迅速,病期短,平均病期1~5年。瘤体较大,平均直径3. 5cm,活动度差,与周围组织之间缺乏清楚界限,常出现疼痛及面瘫。颌骨中枢性黏液表皮样癌多发生在下颌骨,位于下颌角或升支。肿胀、疼痛、开口困难是常见症状。X线表现为颌骨低密度透射性影像,极个别的病例也可表现为透射阻射混合表现。
大体病理:肉眼见低度恶性者与多形性腺瘤相似,但常无包膜,或见假性包膜,肿瘤一般较小,直径不超过5cm。剖面为灰白色或浅粉红色,有散在的小囊腔,腔内有淡黄色黏液,偶见血液,还可见半透明区。个别病例类似于囊肿。高度恶性者与癌相似,肿瘤无包膜,与周围组织之间无清楚界限,剖面灰白色,实性,囊腔极少。
组织病理
光镜下黏液表皮样癌主要由三种细胞即黏液样细胞、表皮样细胞和中间型细胞以不同比例构成。黏液样细胞体积大,为立方、柱状或杯状,胞质呈泡沫状或网状,染色浅,不同程度地嗜碱性,黏液卡红和奥辛兰阳性,有清楚的胞膜,胞核小,位于基部;表皮样细胞为多边形,可见细胞间桥,有丰富的嗜酸性胞质和泡状核(图7-114)。表皮样细胞很少发生角化,只是偶尔有单个细胞角化或角化珠形成。罕见情况下角化可很明显,但常见在有手术史者,可能是一种化生反应。中间型细胞似基底细胞,为多边形,体积小,胞质少,核为圆形,大小一致(图7-115)。此外,尚可见透明细胞和嗜酸细胞。透明细胞体积大,圆形或多边形,胞界清楚,胞质透明,细胞核位于中心或靠边(图7-116)。许多透明细胞含糖原,只是偶尔含黏液或二者均有;嗜酸性细胞呈不规则圆形,胞核圆或卵圆形,胞质内含嗜酸颗粒(图7-117)。
黏液表皮样癌的细胞分化和构成上的变异很大。不同细胞和组织结构在不同肿瘤和同一肿瘤内部均有不同。细胞的多形性和非典型性可能从轻微到严重。坏死(图7-118)、显著的细胞分裂(图7-119)、神经侵犯(图7-120)、类似于淋巴结侵犯的显著的淋巴样反应均可见到。
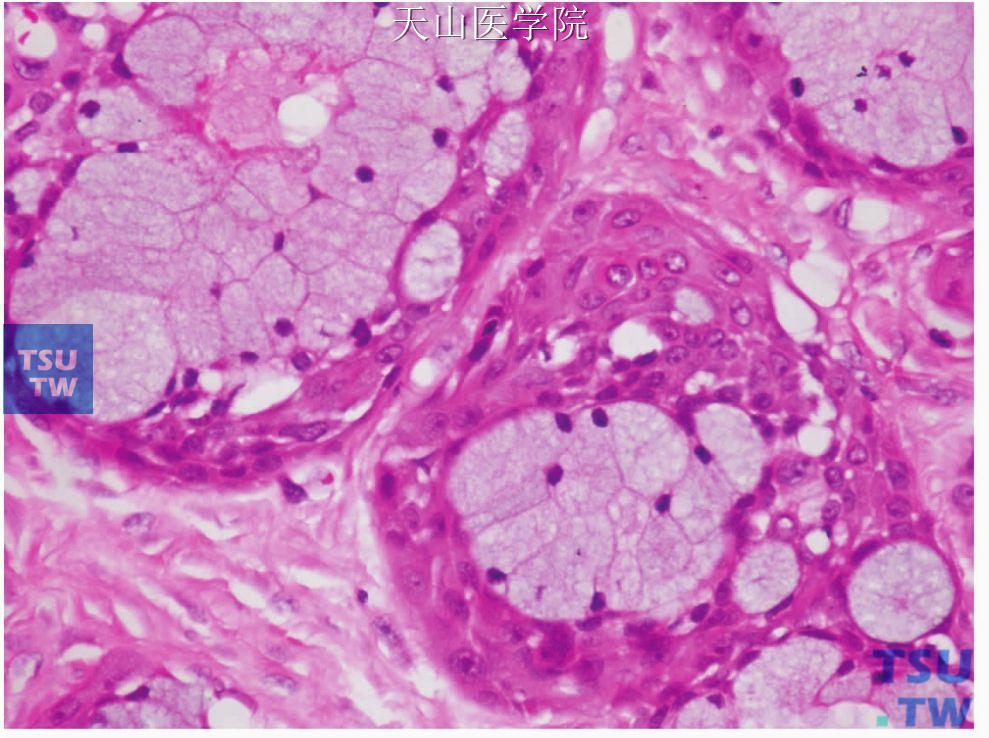
图7-114 黏液表皮样癌:黏液样细胞和表皮样细胞
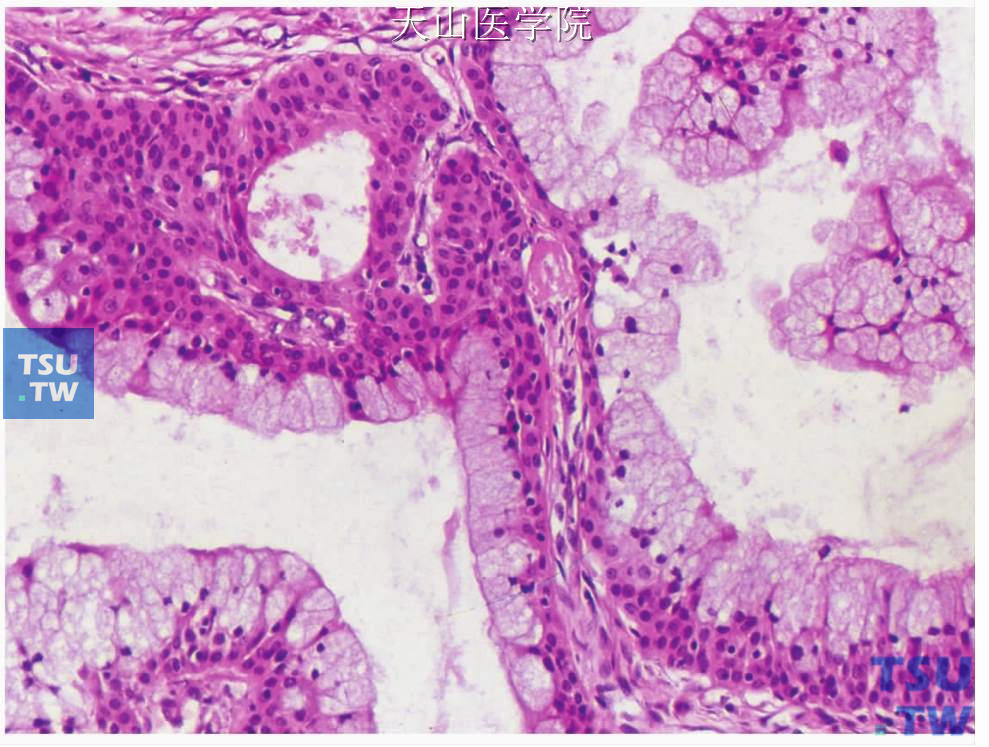
图7-115 黏液表皮样癌:黏液样细胞和中间细胞(类似于表皮的基底细胞)
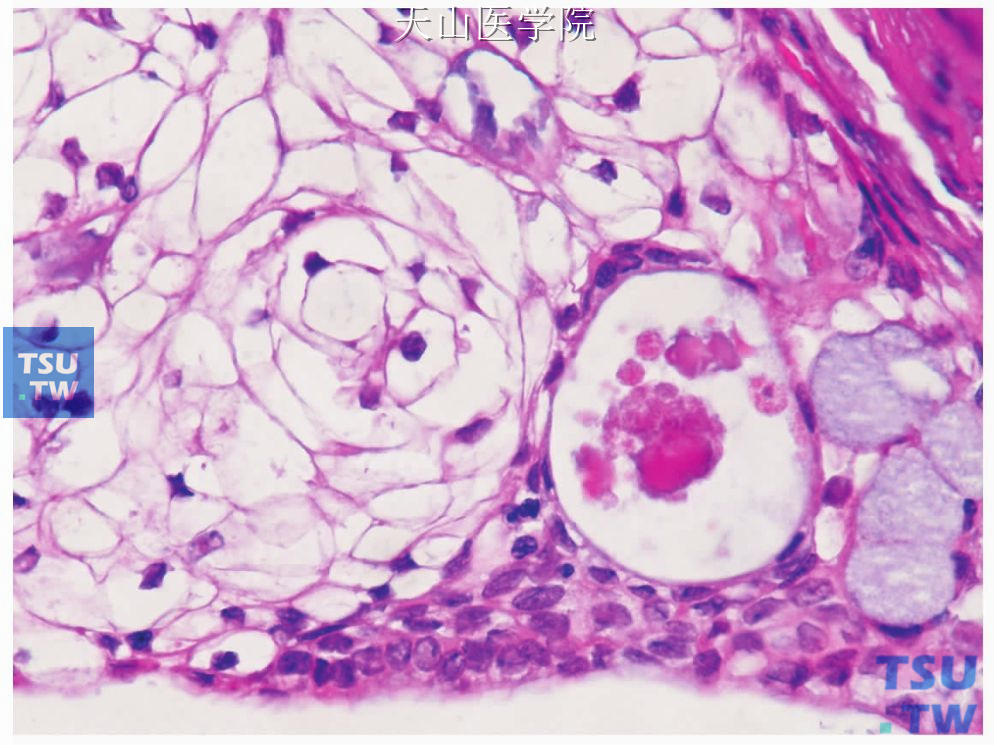
图7-116 黏液表皮样癌:透明细胞(左侧)和黏液细胞右下角
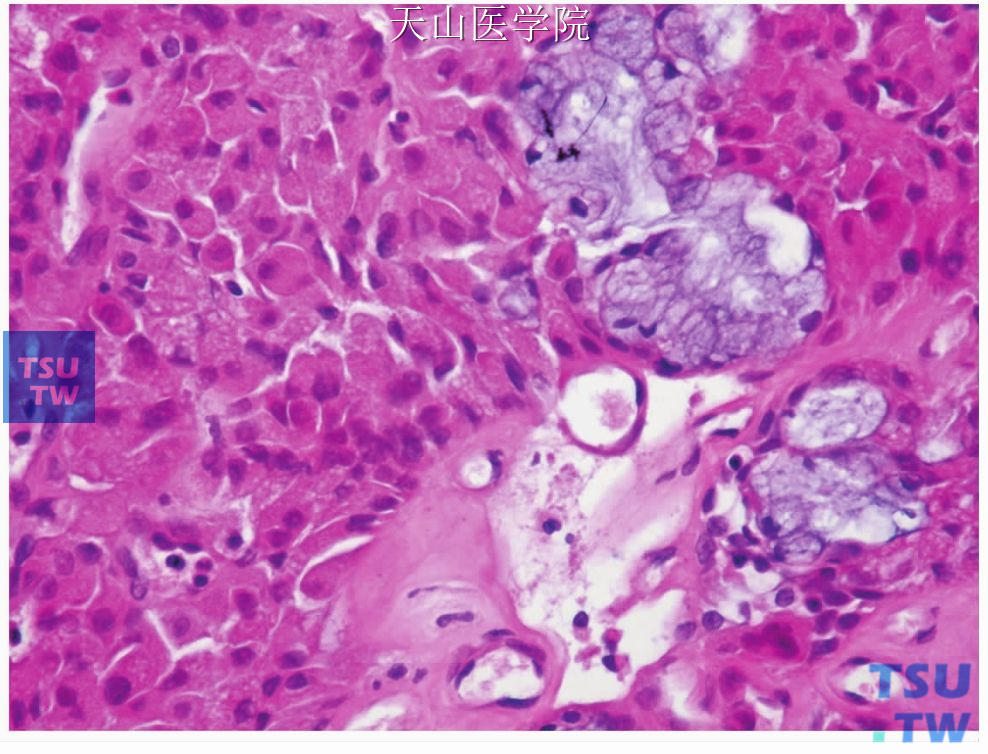
图7-117 黏液表皮样癌:嗜酸细胞和黏液样细胞
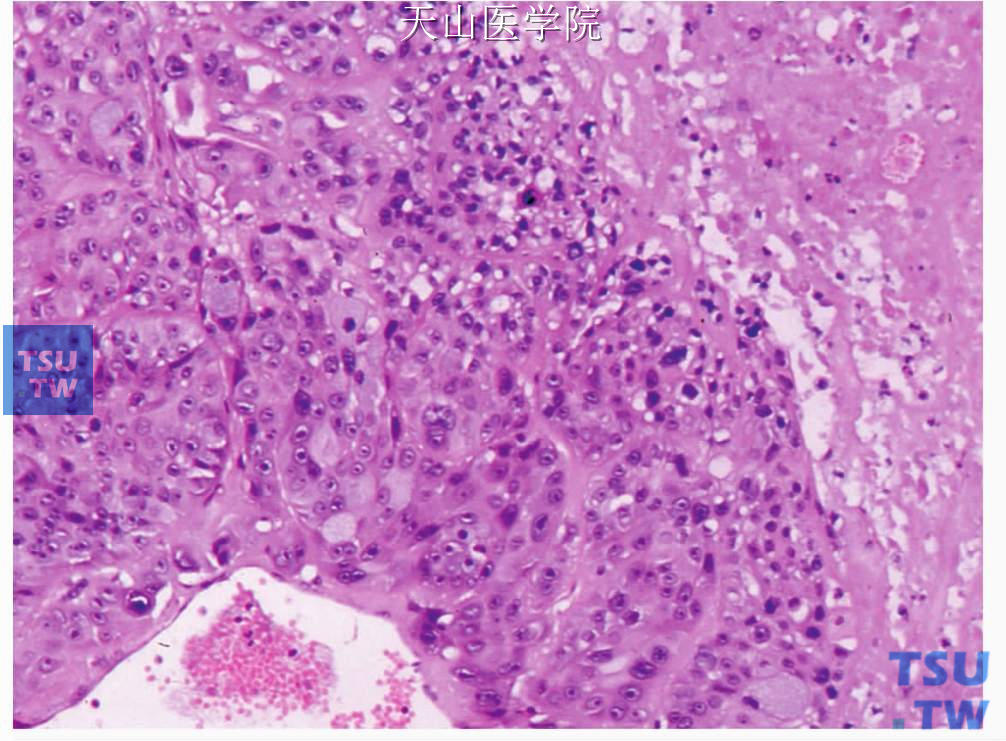
图7-118 黏液表皮样癌:肿瘤细胞坏死(右上角)
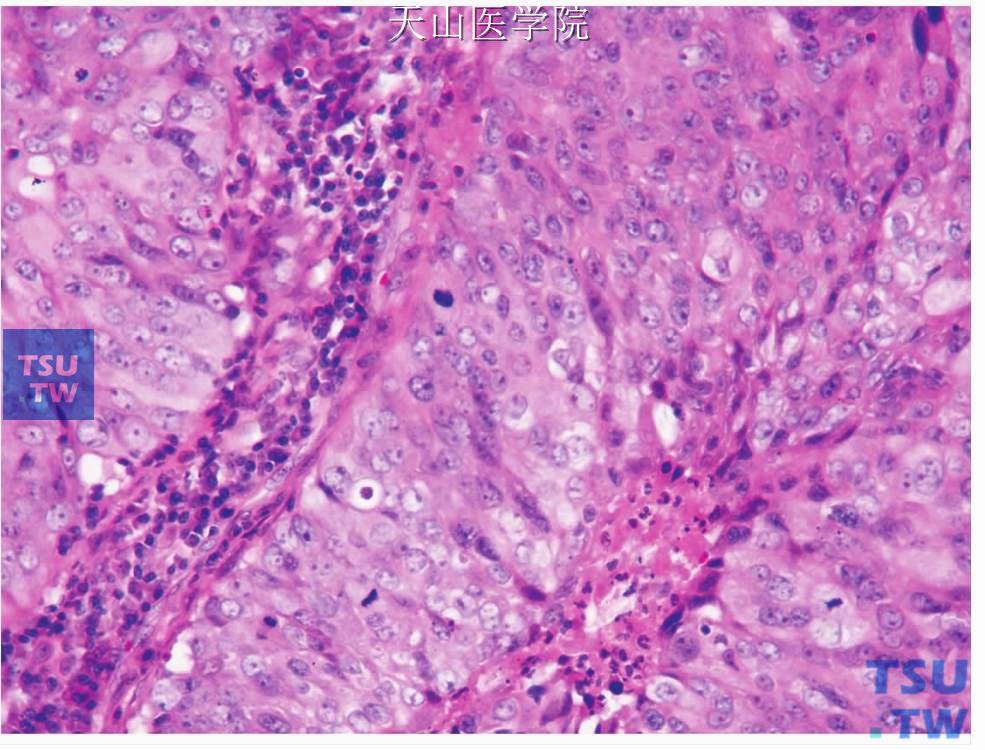
图7-119 黏液表皮样癌:显著的核分裂
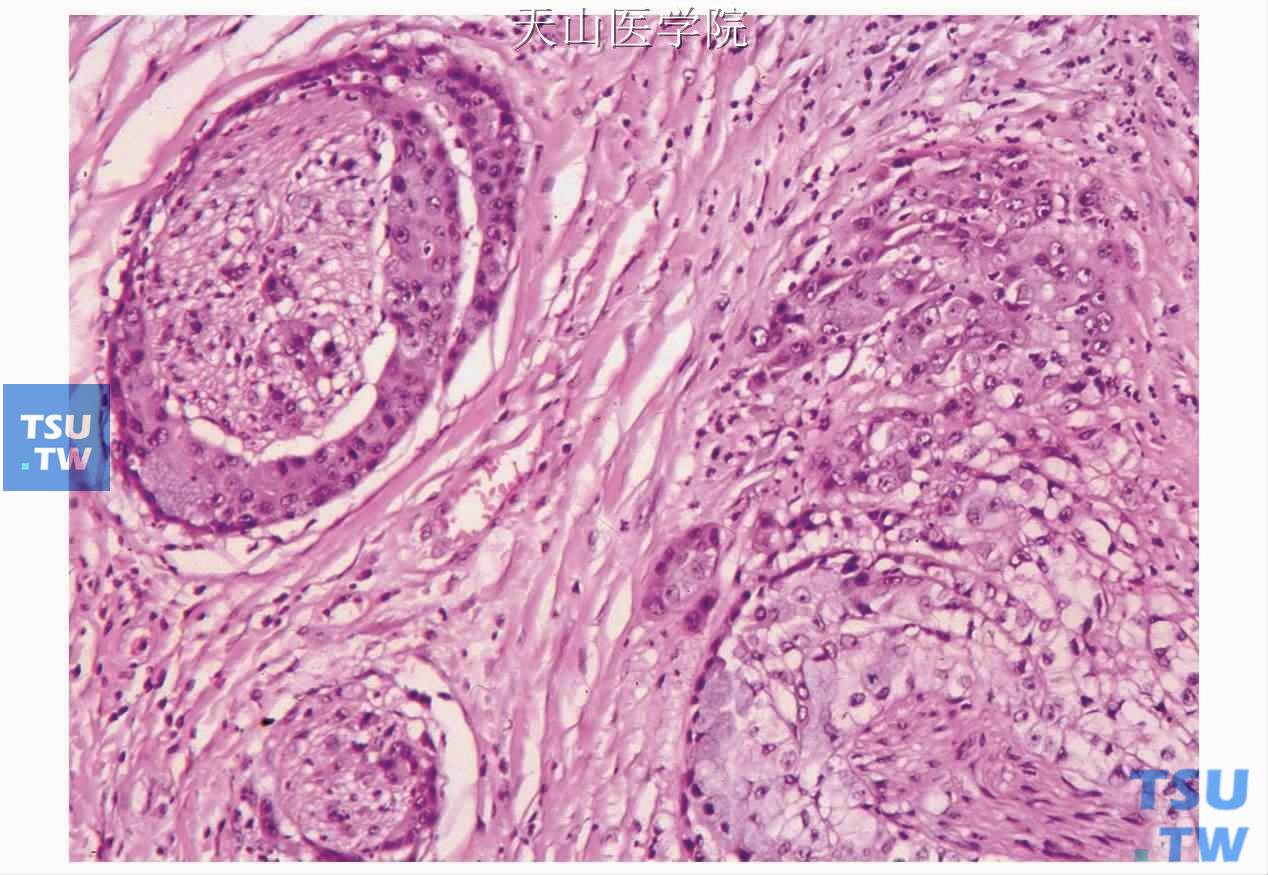
图7-120 黏液表皮样癌:肿瘤组织的神经周浸润
在唾液腺肿瘤中可能只有黏液表皮样癌的组织学分级对肿瘤预后判断和治疗都显得非常重要。报道的低级别黏液表皮样癌的5年生存率为92%~100%,而中级别和高级别者分别为62%~92%和0~43%。最近的研究还显示黏液表皮样癌的组织学分级对肿瘤的处理有价值。低级别黏液表皮样癌只需手术治疗,而高级别黏液表皮样癌需辅助放疗和颈清扫。对中级别的处理则有争论,恐怕争论的根源还在于所应用的组织学分级。目前的黏液表皮样癌分级是主观性的,采用的标准不同,没有被一致接受的分级系统。Stewart等早在1945年就描述了良性和恶性两种黏液表皮样肿瘤,相当于如今的低级别和高级别黏液表皮样癌。稍后不久出现了中级别。目前多数人采用低、中、高级别三层分级方法。三个最常用的分级是美国陆军病理研究所分级系统、改良的Healey系统和Brandwein系统。所有这些分级都采用相似的细胞形态学和组织结构评级参数,还可能包括神经周和血管淋巴管侵犯。美国陆军病理研究所和Brandwein用评分制,对每个不良的组织学参数指定分值,较高的分值代表较高的级别。改良的Healey系统可被认为是最佳匹配式的分级系统,某些组织学参数代表一个特定的级别,对一个肿瘤的分级基于其占主导的形态学特点。然而临床分期似乎较组织学分级是更好的预后指标。WHO分类中建议使用美国陆军病理研究所的分级。
表7-8 黏液表皮样癌的组织学特点,分级的记分方式和评分方法
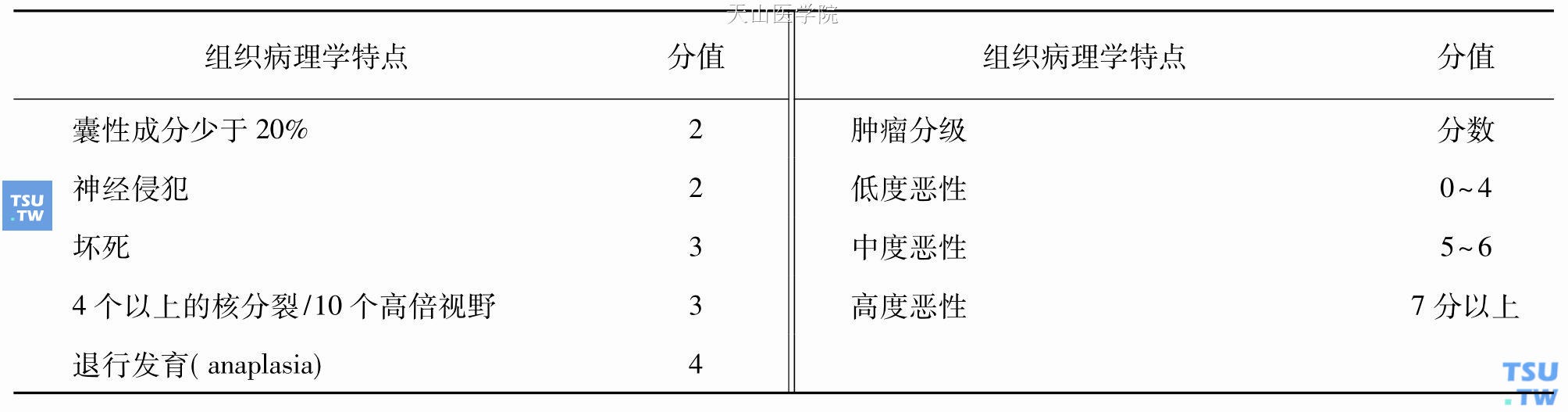
根据三种主要细胞类型的相对比例、囊性腔隙相对于实性成分的比例、肿瘤侵袭程度、细胞间变程度、侵袭方式、细胞分化程度、细胞分裂情况、有无坏死及神经、血管侵犯等将分为高分化、低分化及中分化三种类型。
一、高分化(低级别)型:以黏液细胞和表皮样细胞为主,占50%以上,中间型细胞较少。肿瘤通常界限清楚,细胞排列成巢状或片状,常形成大小不等的囊腔,衬里上皮细胞为黏液细胞,这些黏液细胞有时呈柱状。囊性结构的内衬黏液细胞可连同结缔组织形成乳头突入囊腔,腔内有粉染的黏液(图7-121、7-122)。一些微囊的衬里黏液细胞的外层可见基底样中间细胞。中间细胞的外侧为表皮样细胞。中间细胞和表皮样细胞的层数不定。大部分实性成分倾向于形成多个界限清楚的、含有许多透明细胞的表皮样细胞巢,其中一些透明细胞内含黏液。大的囊腔可出现囊壁破裂,黏液溢入间充质中,形成大片黏液湖,引起炎症反应。此型间充质成分较多,常见结缔组织玻璃样变性,并有淋巴细胞聚集,有时形成淋巴滤泡。偶尔肿瘤表现为单个囊腔,肿瘤位于增厚的囊壁部位。低级别黏液表皮样癌核分裂少,一般无神经侵犯、坏死和细胞非典型性。
二、低分化(高级别)型:以表皮样细胞和中间型细胞为主,排列成片或实性上皮团,黏液细胞较少,低于10%,散在于成片的表皮样细胞之间,有时易误诊为鳞状细胞癌,需通过黏液染色才能鉴别。高级别黏液表皮样癌肿瘤细胞大小不一,可见核浓染及核分裂像,并有核异型性及多核巨细胞。间充质中“黏液湖”较少,缺乏淋巴细胞。肿瘤明显向周围组织浸润(图7-123、7-124)。
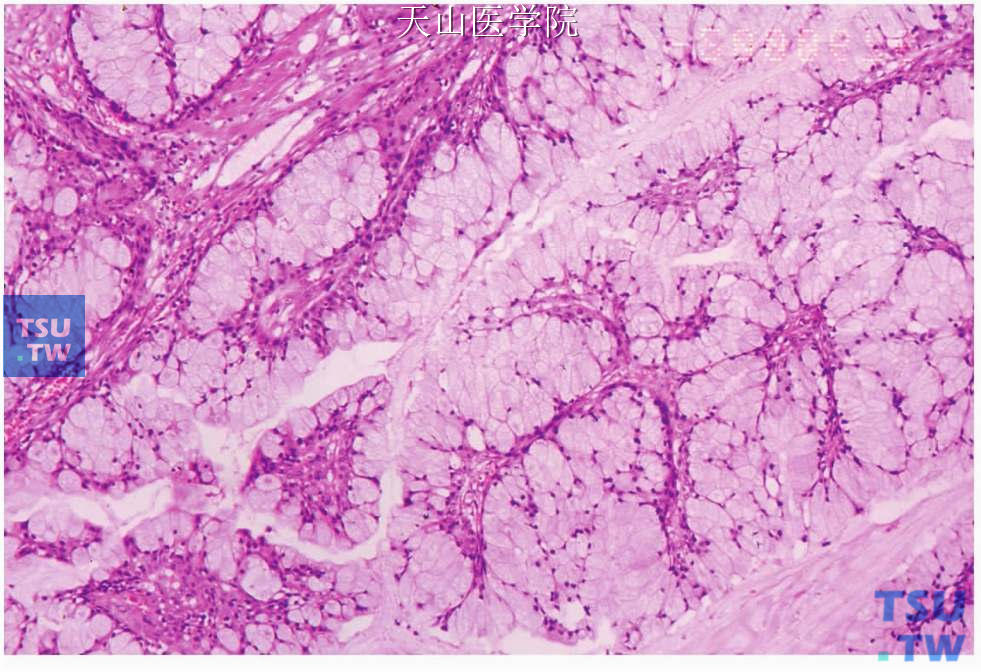
图7-121 高分化黏液表皮样癌:肿瘤以黏液样细胞为主
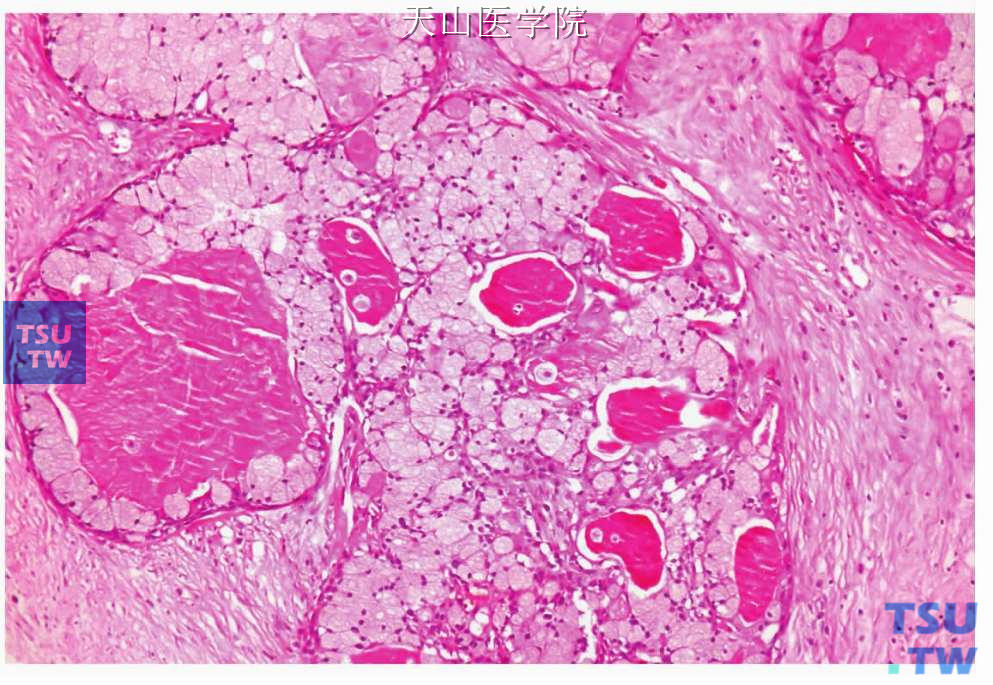
图7-122 高分化黏液表皮样癌:肿瘤形成的囊内含嗜酸性黏液
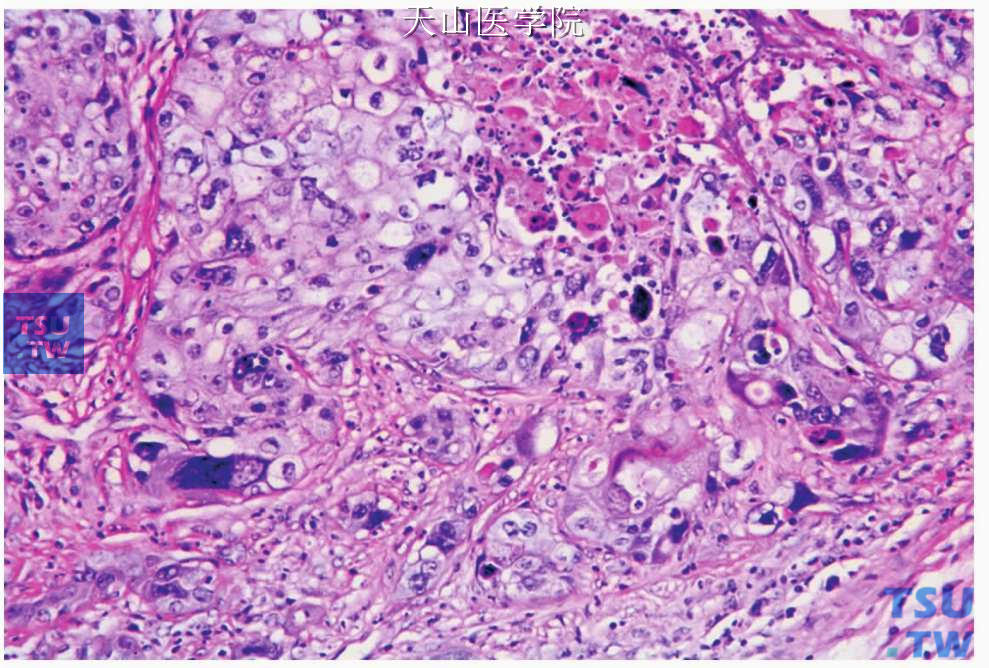
图7-123 低分化黏液表皮样癌:肿瘤细胞的异型性明显,并见坏死
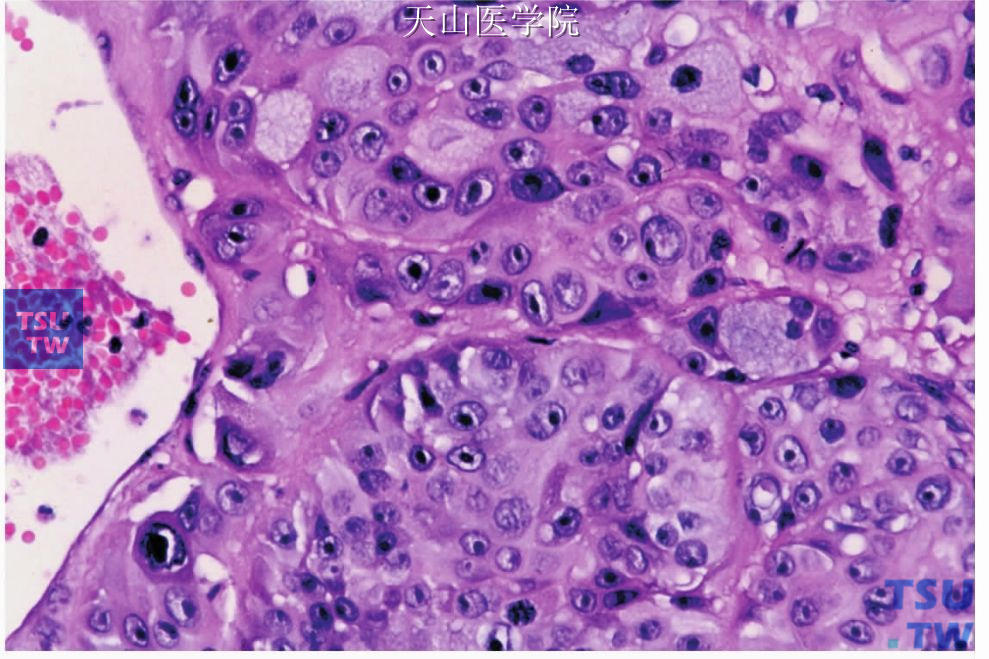
图7-124 低分化黏液表皮样癌:部分肿瘤细胞核深染、核仁明显,围绕血管生长
三、中分化型:介于上述两型之间,黏液细胞多于10%,中间型细胞和表皮样细胞也很显著,常为实性团块,囊性成分少,肿瘤细胞倾向于形成较大的不规则鳞状细胞团或片,偶见细胞异型性及核分裂像(图7-125、7-126),常见浸润性生长区。
黏液表皮样癌的组织变异:除了上述经典的组织学特点外,黏液表皮样癌还可出现一些组织学的变异,多为低级别表现,主要有以下几种:
硬化性黏液表皮样癌伴嗜酸细胞浸润
这是原本发生在Hashimoto甲状腺炎基础上的黏液表皮样癌,临床过程平和。最近有报道发生在大唾液腺,可能是低度恶性。该肿瘤是独立的肿瘤类型还是黏液表皮样癌的变异型还不清楚。肿瘤有浸润性边缘。中心硬化,瘢痕样间质,在硬化性间质中见中度慢性炎症细胞包括嗜酸性细胞浸润,其中有低级别癌岛或梁,多数细胞有鳞状细胞表现,可见局部角化。鳞状细胞岛中混有黏液性上皮细胞和腺体结构,或者腺体结构形成分散的导管。黏液卡红染色见肿瘤细胞内黏液。肿瘤外围可见有滤泡的淋巴组织。
嗜酸细胞型黏液表皮样癌
大小和数量的囊腔,内衬上皮为嗜酸性细胞和杯状黏液细胞。其他的非囊性实性区由嗜酸性表皮样细胞和黏液细胞构成。可见黏液表皮样癌成分构成的囊性区及嗜酸细胞向全部为嗜酸细胞构成的实性区过渡 嗜酸细胞占肿瘤成分75%~95%。镜下:肿瘤成片或巢排列,可见不同(图7-127)。嗜酸细胞有丰富的含嗜酸性颗粒的胞质和位于细胞中央的深染的细胞核,嗜酸细胞也可发生透明细胞变,可误诊为嗜酸细胞腺瘤。
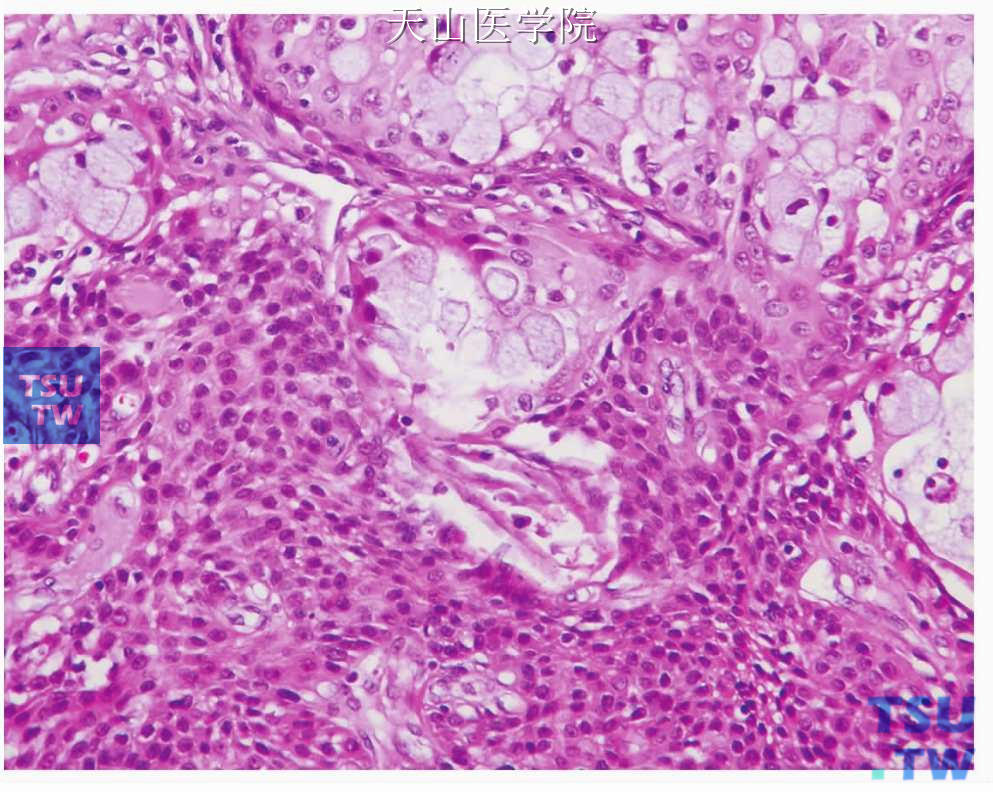
图7-125 中分化黏液表皮样癌:中间细胞较多
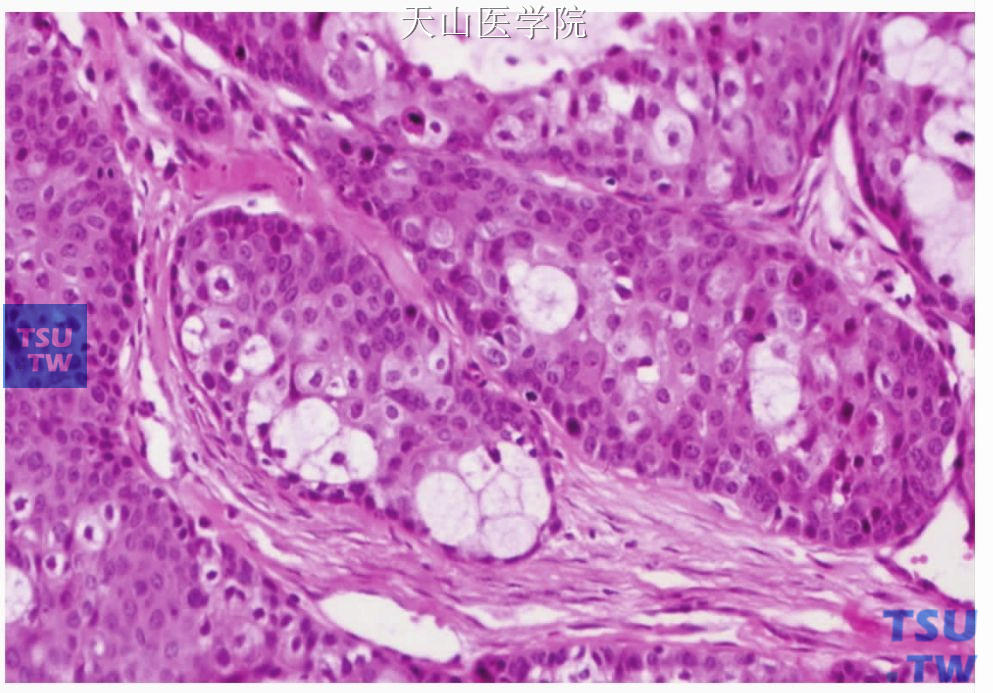
图7-126 中分化黏液表皮样癌:表皮样细胞较多
透明细胞型黏液表皮样癌
黏液表皮样癌中透明细胞常见,当透明细胞占肿瘤大部分时称透明细胞型黏液表皮样癌。透明细胞排列成巢或片,可含腺管样结构和囊性腔隙。表皮样细胞和中间细胞不规则分布于透明细胞之间,它们之间有形态上的过渡。透明细胞大,圆形或多边形,细胞核位于中心或靠边(图7-128)。许多透明细胞含糖原,只是偶尔含黏液或二者均有。导管和微囊结构内可含均质嗜酸性物质,这些物质有时见球状同心圆形钙化(图7-129)。
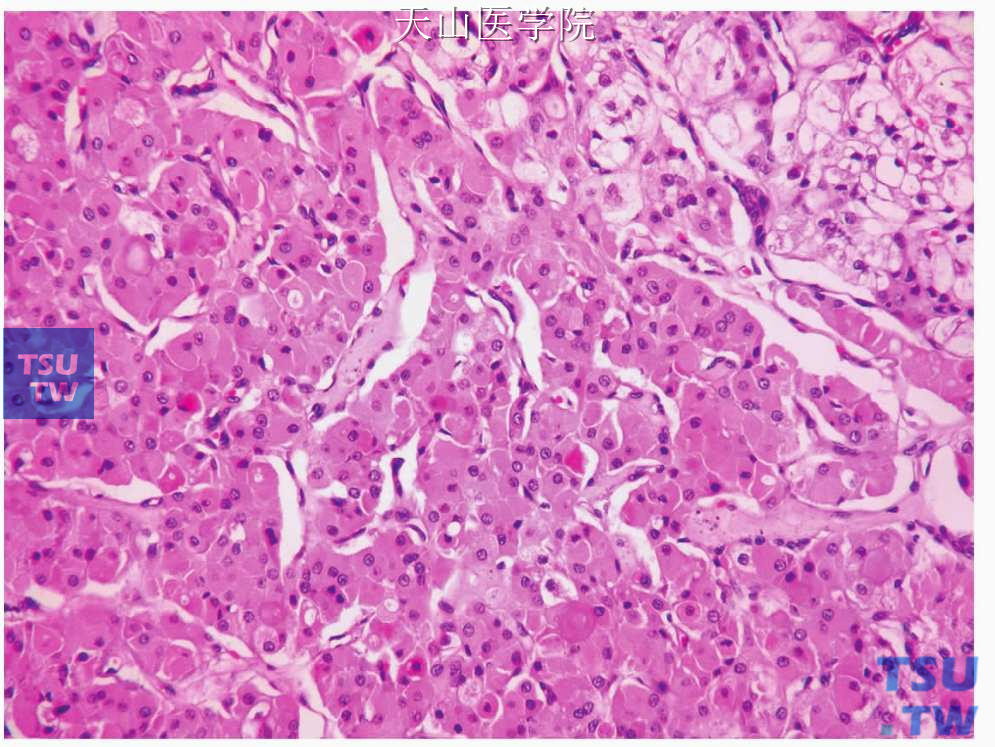
图7-127 嗜酸细胞型黏液表皮样癌:肿瘤细胞类似于嗜酸细胞瘤中的细胞
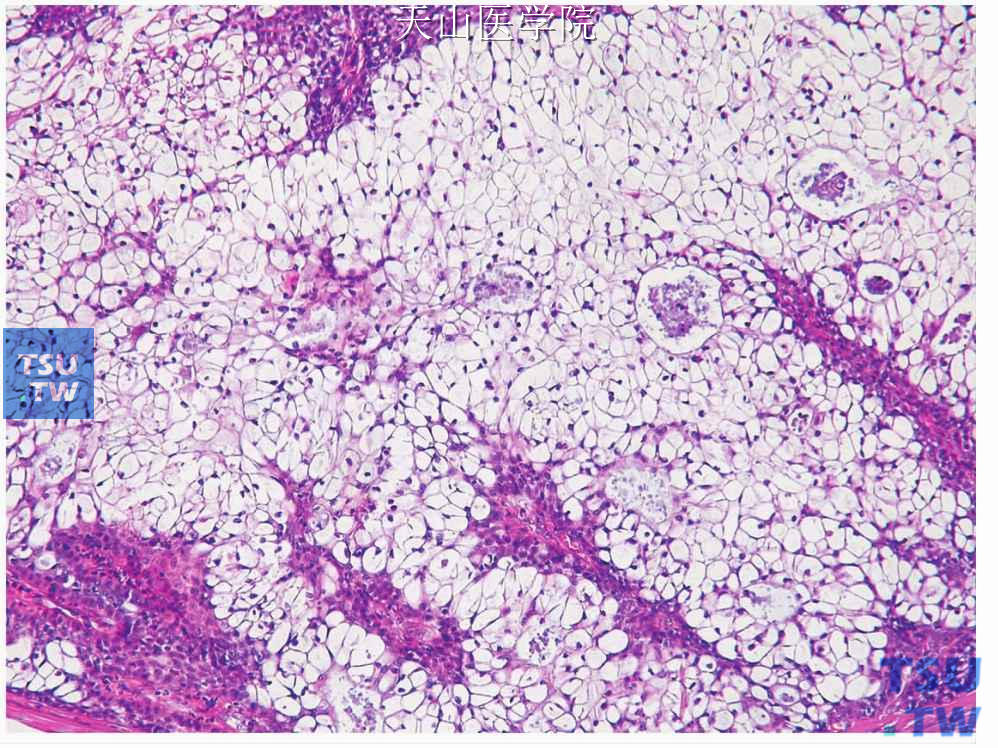
图7-128 透明细胞型黏液表皮样癌:透明细胞构成肿瘤的大部分
梭形细胞黏液表皮样癌
肿瘤界限清楚,有轻微侵袭性。有较典型的微囊区显示黏液表皮样癌的典型细胞和结构特点。而梭形细胞成分占肿瘤体积的70%以上,形态温和的梭形细胞呈束状排列,与典型的黏液表皮样癌区过渡(图7-130)。报道的病例梭形细胞的电镜下、免疫组化特点与普通黏液表皮样癌的中间细胞相似。Ki67表达在典型黏液表皮样癌和梭形细胞区一致,p53和cyclinD1阴性。应注意与肉瘤鉴别。
去分化黏液表皮样癌
目前只有2例报道。转化的高级别成分和低级别成分间有一个过渡带。高级别成分中不含腺样和囊性结构,为实性生长,具有明显的细胞多形性、核分裂多见、坏死广泛。Nagao等报道的1例发生在腮腺,为高级别间变性未分化癌,Ki67表达集中在高级别去分化区。低级别黏液表皮样癌区为2倍体DNA,去分化区为异倍体。诊断后2次复发。
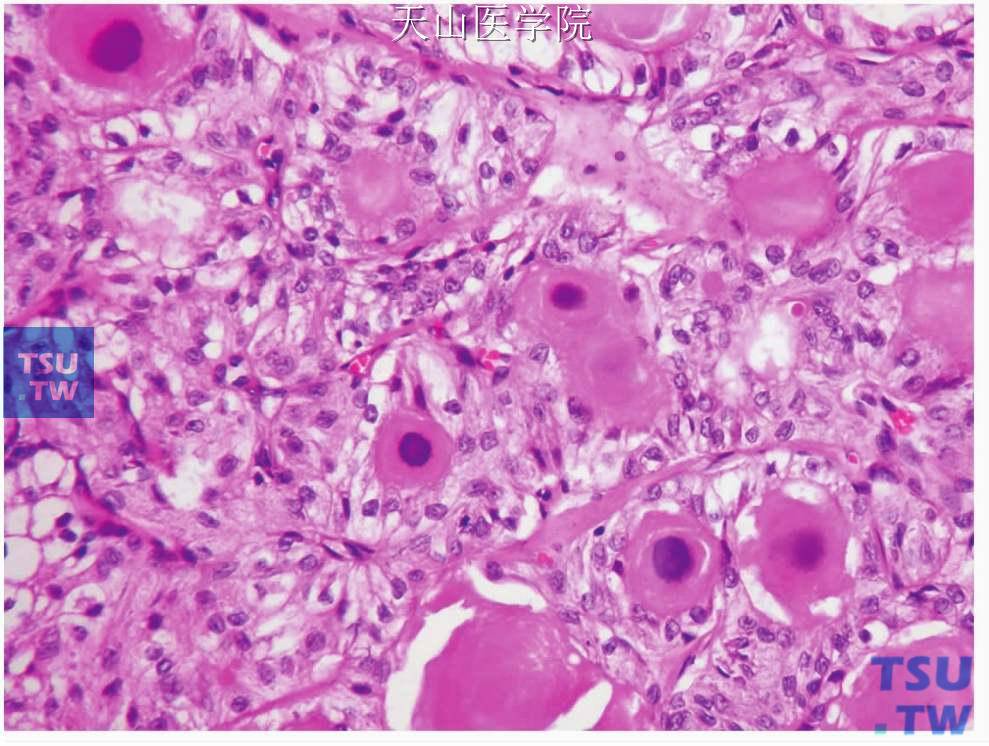
图7-129 透明细胞型黏液表皮样癌:肿瘤形成的同心圆状钙化
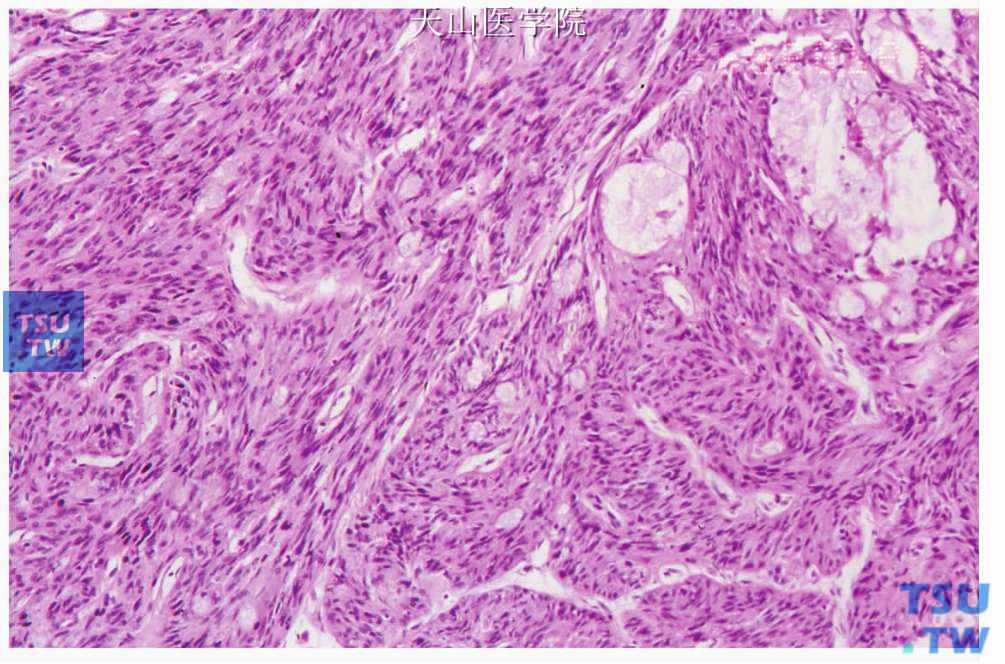
图7-130 梭形细胞黏液表皮样癌:肿瘤细胞呈梭形,成束状排列,间杂以黏液样细胞
此外,在个别病例还可见肿瘤实质中散在黑色素细胞并有黑色素沉着,但并不影响预后。黏液表皮样癌还可和其他肿瘤如腺样囊性癌一起作为杂交瘤出现。
组织化学:黏液细胞及囊腔内黏液显示PAS染色、黏液卡红或奥辛蓝染色阳性反应,透明细胞则显示阴性。在低分化肿瘤中,黏液细胞较少时,组织化学染色可作为鉴别诊断的重要手段。
免疫组化
免疫组化无诊断价值。
细胞角蛋白在黏液细胞表达阳性的有:CK7、CK8,CK18;中间细胞表达CK7,CK8,CK10、CK13、CK14、CK17和CK19,表皮样细胞CK7、CK10、CK13、CK14和CK19阳性。个别病例的中间细胞和表皮样细胞表达Vimentin。肌上皮细胞标志物在黏液表皮样癌一般为阴性。多数肿瘤细胞为EMA阳性。P63在中间细胞和表皮样细胞阳性。表皮样细胞还对EMA显示强阳性反应。癌胚抗原(CEA)阳性者主要分布于黏液样细胞。
细胞增殖标志物很多,Ki67的表达在多数研究中显示与黏液表皮样癌的分级及肿瘤的生物学行为和预后相关。如有研究显示Ki67低于10%者预后良好;高于10%者多发生复发和转移。死亡患者的肿瘤Ki67均高于10%。因此Ki67指数是重要的黏液表皮样癌预后因素,可提高常规组织学分级的准确性。但也有个别研究认为Ki67的表达与预后无关。P27常在低级别黏液表皮样癌呈高表达,在高级别黏液表皮样癌低表达或阴性表达,与肿瘤分级和预后相关。最近有人提出DNA异倍体、PCNA、Ki67和c-Erb-B2高表达及p27低表达预示预后不佳。AgNOR(argyrophillic nuclear organizer region)计数和肿瘤分级正相关。此外,还有研究显示bcl-2在高级别黏液表皮样癌高表达。磷酸化ERK-1/ERK-2阳性者的行为较阴性者更具侵袭性,与预后不良相关。
关于生长因子及其受体在黏液表皮样癌中的表达研究较多,结果不尽相同。一般特点是TGF及其受体在低级别黏液表皮样癌中表达较强,而EGF及其受体倾向于表达在高级别黏液表皮样癌。也有研究显示生长因子的表达与分级和预后无关。
黏液细胞分化相关分子MUC1和MUC4标记腺样结构细胞的顶膜、中间细胞、透明细胞和表皮样细胞全细胞膜,MUC4的表达与肿瘤低级别、低复发率和长生存率相关;相反,MUC1阳性与生存率短、预后不良相关。
超微结构
电镜下见肿瘤细胞为双相分化,既向腺上皮分化,又向鳞状上皮分化。黏液样细胞多为立方或柱状,近腺腔顶端有少量微绒毛突起,侧面为连接复合体,胞质内充满黏液滴,缺乏细胞器,核被挤压于细胞一侧。表皮样细胞为多边形,彼此镶嵌,细胞间以短的桥粒连接,胞质内有张力细丝束,有的可含有黏液滴或分泌颗粒。上述两种细胞内均可见糖原颗粒。中间型细胞表现为腺上皮的特点,胞质内可见少量分泌颗粒、糖原及核糖体。
在光镜水平黏液表皮样癌无肌上皮细胞分化,有的电镜研究见黏液表皮样癌有6种主要细胞:未分化干细胞(立方形)、中间细胞(柱状)、浆黏液样分泌细胞、产黏液杯状细胞、表皮样细胞和肌上皮细胞。低级别和中级别黏液表皮样癌电镜检查发现其与多形性腺瘤在许多结构和细胞方面相似。较明显的是黏液表皮样癌中中间细胞与腔面细胞的关系,与多形性腺瘤中变异肌上皮细胞和腔面细胞的关系相似,提示黏液表皮样癌中中间细胞相当于多形性腺瘤中的变异肌上皮细胞。所以多形性腺瘤和黏液表皮样癌的组织发生关系密切。有研究认为黏液表皮样癌有2种基本细胞:变异腔面上皮细胞和肌上皮细胞。腔面细胞可有不同程度的黏液形成并形成腺腔,这些细胞的变异可形成表皮样细胞。第二种细胞是位于腔面细胞外的具有增生能力的中间细胞(相当于肌上皮细胞),形成中间细胞区。鳞状化生也可发生在中间细胞。认为除排泄管外,腺泡闰管区也具有发生黏液表皮样癌的潜能。
遗传学
黏液表皮样癌较重要的遗传学改变是约30%~70%的病例出现染色体易位t(11;19) (q21;p13),这个易位形成一个位于19p13的黏液表皮样癌T1和位于11q21的MAML2基因融合,形成融合基因MECT1-MAML2,是由CREB(cAMP /cAMP-responsive element binding protein)的共激活子MECT1 (mucoepidermoid carcinoma translocated-1,也称为CRTC1,TORC1 or WAMTP1)的CREB结合域N-端42个残基与Notch信号共激活子MAML2(mastermind-like 2)转录激活域C-端的982个残基融合而成。该融合基因也可见于Warthin瘤和汗腺瘤。融合基因作为Notch和cAMP /CREB通路的转录因子,打破正常细胞周期和细胞分化过程,导致肿瘤发生。存在该基因融合的肿瘤多为低级别黏液表皮样癌,其复发、转移和致死性均较不存在融合者低。患者生存率较高,因此可能作为判断患者预后的标志。但最近在高级别黏液表皮样癌中也发现了融合阳性的病例。在部分融合基因阳性、预后不佳的病例中还发现有CDKN2A的缺失。还有研究发现部分病例出现CRTC3-MAML2融合基因,其预后较好,而且患者年龄较小。研究发现在CRTC1-MAML2融合阴性者多为高级别黏液表皮样癌,干细胞标志之一HMGA2(high-mobility group AT-hook 2 gene) mRNA表达较阳性者强。部分病例有2q,5p,12p和16q等位基因缺失。异倍体与肿瘤高复发率、高颈淋巴结转移机会和低生存率相关。黏液表皮样癌有57. 1%发生6q LOH。位于LCR2区的thrombospondin-2(TSP-2,抑制肿瘤生长和血管形成)表达在肿瘤降低,提示6q LOH缺失在黏液表皮样癌发生中起作用。还有染色体数目异常如X染色体3体等。
表观遗传学研究见部分黏液表皮样癌有p16(INK4a)启动子甲基化、SFRP(secreted frizzled-related proteins)基因甲基化使其蛋白表达下降并与beta-catenin细胞质和细胞核染色及高cyclinD1表达相关。RUNX3(TGF转录因子,发挥抑癌功能)甲基化伴有RUNX3 mRNA量下降,肿瘤抑制基因RASSF1、RARbeta2、DAPK和MGMT甲基化等。
生长因子相关基因的改变包括高级别黏液表皮样癌中具有EGFR高拷贝数,低级别和中级别者EGFR基因拷贝数正常。EGFR基因扩增与生存率相关。EGFR蛋白与组织学分级相关。RUNX3在黏液表皮样癌低表达(20. 6%,7/34)并与预后不良有关。
用PCR方法检查23例黏液表皮样癌,65%有MUC19表达。MUC1和MUC4表达在临床Ⅰ期分别较正常组织高4. 2~21倍。结果提示MUC19表达与黏液表皮样癌相关、MUC1和MUC4过表达与临床早期相关。
有20%左右的黏液表皮样癌有H-ras基因突变,提示H-ras突变在黏液表皮样癌发生和进展中起作用。
低级别黏液表皮样癌的DNA含量大部分为二倍体,异倍体多见于高级别者。
鉴别诊断
鳞状细胞癌:低分化的黏液表皮样癌易与鳞状细胞癌混淆,但后者不存在黏液细胞及黏液,若PAS染色或奥辛蓝染色出现阳性,可诊断为黏液表皮样癌。MUC5AC阳性染色有助于鉴别高级别黏液表皮样癌和鳞状细胞癌。
含透明细胞的肿瘤:如腺泡细胞癌,透明细胞肌上皮癌,皮脂腺癌、转移性肾透明细胞癌:上述肿瘤采用抗淀粉酶、S-100蛋白、肌动蛋白抗体免疫组化染色、脂肪染色等方法有助于鉴别。
坏死性唾液腺化生:有时类似于高级别黏液表皮样癌,但它保留正常腺小叶的轮廓和正常腺泡的外形。鳞状上皮巢外形平滑,没有低级别黏液表皮样癌典型的囊性表现,无中间细胞。
内翻性导管乳头状瘤:有黏液细胞和表皮样细胞,但具有内生性质、广基性推进性边缘,与黏液表皮样癌的多囊性、多灶性及明显的生长不同。
腺泡细胞癌:腺泡细胞癌的空泡性变有时类似于黏液表皮样癌的黏液细胞或透明细胞,但是腺泡细胞癌的细胞单一,无表皮样细胞分化。
囊腺瘤和囊腺癌:通常有典型的乳头状结构,无表皮样成分。一般囊之间的间质较黏液表皮样癌少。
多形性腺瘤伴较明显的黏液和黏液表皮样化生:黏液化生和表皮样化生可同时存在或单独出现,通常为灶性、其范围有限。罕见情况下黏液和表皮样化生成分显著,难以鉴别。多形性腺瘤中的含肌上皮细胞的黏液样间质不出现在黏液表皮样癌,无浸润性生长可区别。
此外,黏液表皮样癌可作为癌在多形性腺瘤中的恶性成分,仔细观察能分辨出2种肿瘤成分。其中的黏液表皮样癌成分更广泛,可能有侵袭周围组织表现。
颌骨内黏液表皮样癌应与腺牙源性囊肿鉴别,腺牙源性囊肿内衬上皮表层细胞为鞋钉样或立方状胞质嗜酸性细胞、内衬上皮内有微囊性腔隙或导管样结构,这些不出现在低级别黏液表皮样癌的囊性区;低级别黏液表皮样癌的表皮样细胞通常见于囊腔的外围,不排列成上皮球或漩涡状向囊腔内突入,而向囊腔内突入的上皮球或漩涡结构是腺牙源性囊肿的特点。
嗜酸性黏液表皮样癌的鉴别诊断包括嗜酸细胞瘤、嗜酸性细胞型囊腺瘤、Warthin瘤、多形性腺瘤嗜酸性化生、嗜酸细胞肌上皮瘤、腺泡细胞癌、唾液腺导管癌和嗜酸细胞性脂肪腺瘤。此外,具有嗜酸细胞特点的转移性肿瘤如肾腺癌、甲状腺癌或肾上腺癌也在应鉴别之列。嗜酸细胞腺瘤和腺癌不含黏液细胞;嗜酸细胞囊腺瘤有多个囊腔,被覆嗜酸细胞,但没有表皮样细胞和中间细胞;Warthin瘤伴黏液化生无黏液;表皮样癌中表皮样细胞有细胞间桥,无中间细胞;多形性腺瘤伴嗜酸细胞化生时仍可见黏液样组织或软骨样组织以及肌上皮细胞,无浸润性生长;嗜酸细胞肌上皮瘤和肌上皮癌显示肌上皮分化特点如梭形细胞和浆样细胞;腺泡细胞癌具有腺泡样结构,含嗜碱性泡沫状胞质和偏中心细胞核;嗜酸细胞型黏液表皮样癌中无成熟脂肪细胞可与脂肪腺瘤鉴别。P63免疫组化染色可帮助鉴别诊断。嗜酸细胞型黏液表皮样癌p63在多数细胞阳性,嗜酸细胞腺瘤和腺癌在肿瘤细胞团外围细胞阳性,腺泡细胞癌p63阴性及线粒体组织化学染色阴性;普通唾液腺导管癌p63阴性而雄性激素受体阳性。
预后
黏液表皮样癌的预后与多种因素相关,与病理分级相关是大家公认的。高分化者为低度恶性,肿瘤生长局限,术后局部复发率仅占6%,很少发生转移,预后较好,5年生存率可达95%;中分化者为中度恶性,局部复发率为20%,少数发生转移,5年生存率为80%~90%;低分化者为高度恶性,肿瘤生长快,侵袭性强,术后有80%复发,常发生远处转移,预后较差,5年生存率仅有25%~30%。下颌下腺黏液表皮样癌的组织学分级与生物学行为的相关性不佳。免疫组织化学指标可能对预后的判断有一定帮助(见免疫组织化学部分)。可能最有前途的黏液表皮样癌预后判断的分子指标是t(11;19) (q21;p13)所导致的融合基因MECT1-MAML2,在研究中出现的频率在38%~82%,多见于低、中级别肿瘤而且预后较好。但是该融合基因在高级别黏液表皮样癌中出现的情况差别巨大。早期研究认为高级别中无该种染色体易位,而最近的研究发现在高级别中也时常发生,可能在某种程度上与所应用的分级有关(如Brandwein分级的高级别在美国陆军病理研究所分级中被认为是中级别)。
与预后相关的临床指标有临床分期、手术切除是否彻底(切缘是否阳性)等,其他相关的因素还有患者的年龄如儿童的黏液表皮样癌预后较成人者好,女性较男性预后好,咽部的黏液表皮样癌预后较差等。远处转移的部位主要为肺、骨、脑,也见于肝、卵巢、腹膜、皮肤。
